异基因造血干细胞移植是治疗恶性血液病、遗传性疾病及骨髓衰竭性疾病等的重要方法[1]。人类白细胞抗原(human leukocyte antigen, HLA)全相合的同胞造血干细胞移植是异基因造血干细胞移植的重要方式,但随着移植技术的进展,近年来HLA不匹配的造血干细胞移植及单倍体造血干细胞移植(haploidentical hematopoietic stem cell transplantation,haplo-HSCT)已经成为异基因造血干细胞移植的重要方式[2]。然而,haplo-HSCT存在较高的移植物抗宿主病(graft versus host disease,GVHD)、感染和移植后复发等问题,其中较高的植入失败(graft failure,GF)发生率是严重威胁患者生存的重要因素[3]。
HLA是具有高度多态性的同种异体抗原,也是人类主要组织相容性复合物抗原,与同种异体移植中的排斥反应密切相关。在HLA不匹配的器官移植中,患者血清中预先存在的抗HLA抗体,靶向针对不匹配供者的HLA抗原时,这些抗体被称为供者特异性HLA抗体(anti-HLA donor-specific antibodies,DSA)[4]。DSA的产生与多种因素相关,如女性、多次妊娠、反复输血以及罹患骨髓增生异常综合征(myelodysplastic syndrome, MDS)等[5]。在HLA不匹配的器官移植中,DSA的发生率达30%,对器官移植排斥或GF发生产生重要影响[6]。近年来,DSA在造血干细胞移植领域中的作用也愈发受到医疗工作者的关注[7]。多项研究表明,患者体内存在的DSA是导致造血干细胞移植物GF、粒系重建时间延迟和长期生存低下的重要因素之一[8-9]。欧洲血液及骨髓移植协作组(EBMT)共识强烈建议,接受haplo-HSCT的患者应进行HLA抗体检测,以避免DSA所致的GF和不良生存事件的发生[10-11]。尽管患者可能有多个潜在的供者,但仍然面临着可能选择患者与适当的供者有DSA的情况,如果没有替代供者,建议在移植前采取对DSA阳性患者进行去敏治疗。针对DSA阳性的去敏治疗措施较多,但主要运用于实体器官移植中,近期已有多种DSA阳性去敏治疗开始应用于造血干细胞移植,包括血浆置换、利妥昔单抗、硼替佐米、大剂量人免疫球蛋白、供者血小板输注等[7],然而其在造血干细胞移植中,去敏治疗的效果仍存在争议。本研究总结并分析了本中心haplo-HSCT中DSA阳性及DSA阳性患者去敏治疗对造血干细胞移植植入效果的影响。
1 资料与方法 1.1 资料来源筛选2017年3月至2023年7月重庆医科大学附属第二医院住院的160例血液系统疾病患者,纳入70例haplo-HSCT患者。纳入标准:移植前进行HLA配型及抗体分析检测,ECOG评分 < 2分,左心室射血分数>50%,血清肌酐 < 130 mmol/L,血清胆红素 < 35 mmol/L,转氨酶 < 2倍正常值的上限,肺功能测试值>50%预测,供者和患者均签署知情同意书,完成haplo-HSCT。排除标准:无HLA检测或配型分析报告,全相合移植,无关供者移植,人类免疫防御病毒阳性、重大精神疾病和妊娠等。本研究已通过本院伦理委员会审批[2023年科伦审第(142)号]。
1.2 HLA分型及抗体的检测HLA分型及抗体检测外送至公共平台检测,采用以测序为基础的SBT法及IMGT/HLA数据库,使用美国Invitrogen公司HLA基因分型试剂盒,对供患者进行HLA高分辨检测,包括HLA-A、B、C、DRB1、DQB1、DPB1共12个位点。采用Luminex流式液相芯片法筛选患者的血清中是否存在抗HLA抗体,LABScreen试剂(美国One Lambda公司)检测患者血浆/血清是否存在Ⅰ类和Ⅱ类抗HLA抗体。HLA抗体阳性者根据制造商的说明(在Luminex平台上使用LanogaPark,CA,美国)使用单抗原珠Ⅰ类(HLA-A、-B和-C)和Ⅱ类(HLA-DR、-DQ和-DP)HLA抗体检测,以确定是否为针对供者位点的DSA阳性。根据实验室检测敏感性及相关研究报道[11-12],DSA水平高于500平均荧光强度(mean fluorescence intensity, MFI)被认为是DSA阳性,MFI < 500为阴性,500~5 000为弱阳性,5 000 < MFI < 10 000为中度阳性,MFI≥10 000为强阳性。
1.3 DSA中度及强阳性患者的去敏治疗清除DSA抗体:治疗性血浆置换(therapeutic plasma exchange, TPE)血浆1 500~2 000 mL/次,2~3次;中和DSA抗体:静注人免疫球蛋白(intravenous injection immunoglobulin, IVIG)0.4 g/(kg·d)×4 d。
抑制抗体生成:利妥昔单抗100 mg/次×1次; 硼替佐米1.3 mg/m2×1次。
1.4 移植预处理方案针对急性白血病、MDS、淋巴瘤、慢性髓系白血病(chronic myeloid leukemia, CML)患者采用下述BUCY方案:白消安(busulfan, BU)3.2 mg/(kg·d)×3 d; 环磷酰胺(cyclophosphamide, CY)50 mg/(kg·d)×2 d; 氟达拉滨30 mg/(m2·d)×5 d; 兔抗人胸腺细胞免疫球蛋白(rabbit anti-human thymocyte immunoglobulin, ATG)2.5 mg/(kg·d)×(3~4)d(若联合CD25单抗,ATG减少至2~3 d);针对复发或难治患者,联合阿糖胞苷2 g/(m2·d)×3 d;伴中枢神经系统受累患者,加用噻替哌;针对再生障碍性贫血(aplastic anemia, AA)、阵发性睡眠性血红蛋白尿患者,BU减量至3.2 mg/(kg·d)×1 d。
PTCY方案:苯达莫司汀200 mg/(m2·d)×1 d;BU 3.2 mg/(kg·d)×3 d;CY 12.5 mg/(kg·d)×2 d,后置CY 50 mg/(kg·d)×2 d。
GVHD的预防采用环孢素A+霉酚酸酯+短程MTX的方案,部分加用间充质干细胞。
1.5 供者干细胞植入标准粒系植入定义为移植后连续3 d绝对中性粒细胞计数(ANC)>0.5×109/L的第1天记为粒系重建时间。血小板植入的定义为:在不需要输注血小板情况下,连续3 d血小板计数维持在20×109/L以上的第1天记为血小板重建时间。GF包括:原发植入失败定义为在移植后28 d连续3 d未能达到ANC >0.5×109/L;继发植入失败被定义为植入成功后续出现的持久ANC < 0.5×109/L,或供体嵌合率低下。
1.6 其他定义单核细胞计数和CD34计数为每公斤受者体质量单核细胞或CD34细胞的总数量。急性GVHD(aGVHD)和慢性GVHD(cGVHD)根据标准进行定义。从移植时间到因任何原因死亡,计算总体生存率(overall survival, OS)。
1.7 统计学分析采用SPSS22.0进行数据处理。对供患者基本信息和造血干细胞移植基本特征相关变量统计进行描述性数据分析。抗体阳性组和阴性组之间,计数资料以例(%)表示,组间比较采用卡方检验,数值小于5时采用Fisher’s精确概率法;正态分布的计量资料以x±s表示,组间比较采用两独立样本t检验,非正态分布的计量资料以中位数M(范围)表示,组间比较采用非参数统计。对影响供体细胞植入的相关因素进行Logistic回归分析,用Kaplan-Meier计算OS。生存曲线的比较采用log-rank检验,P < 0.05为有统计学意义。
2 结果 2.1 患者临床资料共纳入70例haplo-HSCT患者,中位年龄39岁(范围12~59岁),其中男性43例(61.4%),女性27例(38.6%);供者中位年龄30岁(范围13~58岁)。32例(45.7%)为急性髓系白血病(acute myeloid leukemia,AML),13例(18.6%)为AA,9例(12.8%)为急性淋巴细胞白血病(acute lymphocyte leukemia,ALL),7例(10.0%)为MDS,其他疾病患者9例。患者均接受外周血干细胞移植,患者的临床资料见表 1。在受者-供者关系方面,父母供子女20例(28.6%),同胞供者16例(22.8%),子女供父母34例(48.6%)。
| 指标 | haplo-HSCT患者(n=70) | DSA阳性(n=15) | DSA阴性(n=55) | P值 |
| 年龄/岁 | 39(12~59) | 48(15~59) | 39(12~59) | 0.109 |
| 性别(男/女) | 27/43 | 14/1 | 26/29 | 0.006 |
| 疾病类型 | 0.165 | |||
| AA | 13(18.6) | 6(40.0) | 7(12.7) | |
| AML | 32(45.7) | 4(26.7) | 28(50.9) | |
| MDS | 7(10.0) | 2(13.3) | 5(9.1) | |
| ALL | 9(12.8) | 1(6.7) | 8(14.5) | |
| 其他 | 9(12.8) | 2(13.3) | 7(12.7) | |
| 供者年龄[中位数(范围)]/岁 | 30(13~58) | 34(16~52) | 29(13~58) | 0.647 |
| 血型不合 | 28(40.0) | 5(33.3) | 23(41.8) | 0.013 |
| 主要不合/主次均不合 | 15(21.4) | 0(0.0) | 15(27.3) | |
| 次要不合 | 13(18.6) | 5(33.3) | 8(14.5) | |
| 配型位点相合(GVH方向,12位点) | 0.609 | |||
| 6位点 | 12(17.1) | 2(13.3) | 10(18.2) | |
| 7位点 | 18(25.7) | 4(26.7) | 14(25.5) | |
| 8位点 | 16(22.8) | 2(13.3) | 14(25.5) | |
| 8位点以上 | 24(34.3) | 7(46.7) | 17(30.9) | |
| 移植预处理方案 | 0.095 | |||
| Bu+CY | 55(78.6) | 14(93.3) | 39(70.9) | |
| PTCY | 15(21.4) | 1(6.7) | 16(29.1) | |
| CD34总量 | 7.5(1.9~19.7) | 7.3(3.0~19.7) | 7.6(1.9~17.8) | 0.864 |
| 单个核总量 | 7.0(3.8~17.4) | 6.9(4.7~12.0) | 7.1(3.8~17.4) | 0.932 |
| 植入失败 | 6(8.6) | 4(26.7) | 2(3.6) | 0.025 |
| 早期死亡 | 5(7.14) | 0(0.0) | 5(9.1) | |
| 粒系重建时间 | 14(8~35) | 15(10~35) | 14(8~20) | 0.027 |
| 血小板重建时间 | 15(9~210) | 16(11~66) | 15(9~210) | 0.447 |
| aGVHD分级 | 0.259 | |||
| 0~Ⅰ级 | 45(64.3) | 12(80.0) | 33(60.0) | |
| Ⅱ~Ⅳ级 | 25(35.7) | 3(20.0) | 22(40.0) | |
| cGVHD分级 | 29(47.5) | 7(46.7) | 22(47.8) | 0.938 |
| AA:再生障碍性贫血;AML:急性髓系白血病;MDS: 骨髓增生异常综合征;ALL: 急性淋巴细胞白血病;BU:白消安;CY:环磷酰胺;aGVHD:急性移植物抗宿主病;cGVHD:慢性移植物抗宿主病 | ||||
2.2 DSA阳性患者情况分析
15例DSA阳性患者临床特征见表 2,其中7例(46.7%)强阳性,3例(20.0%)中度阳性,5例(33.3%) 弱阳性。患者中位年龄为48岁(范围15~59岁),其中女性14例,男性1例。7例(46.6%)患者DSA针对Ⅰ类HLA抗原,4例(26.7%)针对Ⅱ类HLA抗原,4例(26.7%)是Ⅰ类和Ⅰ类抗原都有,HLA-Ⅰ类抗体强阳性6例,HLA-Ⅱ类抗体强阳性7例。
| 编号 | 性别 | 年龄/岁 | 诊断 | 配型位点相合数 | 供受者关系 | 供者年龄/岁 | 供受者血型 | HLA类型 | DSA去敏治疗 | CD34计数/(×106/kg) | 单个核计数/(×108/kg) | 是否植入成功 |
| 1 | 女 | 24 | ALL | 7 | 父供女 | 48 | B-B | Ⅰ类 | 无 | 4.3 | 9.5 | 是 |
| 2 | 女 | 56 | AA | 9 | 子供母 | 32 | O-O | Ⅱ类 | 有 | 6.1 | 11.7 | 是 |
| 3 | 女 | 55 | MDS | 8 | 子供母 | 26 | O-O | Ⅱ类 | 有 | 8.7 | 7.0 | 是 |
| 4 | 男 | 33 | AA | 9 | 同胞兄弟 | 34 | A-A | Ⅰ类 | 无 | 7.0 | 6.7 | 是 |
| 5 | 女 | 15 | AML | 10 | 父供女 | 50 | A-O | Ⅰ类+Ⅱ类 | 有 | 12.0 | 8.7 | 是 |
| 6 | 女 | 18 | AA | 7 | 父供女 | 49 | O-A | Ⅱ类 | 有 | 14.0 | 6.0 | 是 |
| 7 | 女 | 48 | AML | 7 | 女供母 | 24 | A-A | Ⅰ类+Ⅱ类 | 有 | 7.3 | 8.0 | 是 |
| 8 | 女 | 39 | AML | 6 | 女供母 | 20 | A-A | Ⅰ类+Ⅱ类 | 有 | 3.0 | 6.2 | 否 |
| 9 | 女 | 54 | AA | 9 | 同胞兄弟 | 49 | B-B | Ⅰ类 | 有 | 4.5 | 6.1 | 是 |
| 10 | 女 | 45 | AML | 6 | 同胞兄弟 | 42 | O-O | Ⅰ类 | 有 | 10.9 | 5.7 | 否 |
| 11 | 女 | 49 | AA | 9 | 子供母 | 24 | B-B | Ⅰ类+Ⅱ类 | 无 | 8.0 | 8.3 | 是 |
| 12 | 女 | 51 | AML | 7 | 同胞兄弟 | 50 | A-AB | Ⅰ类 | 无 | 5.3 | 4.7 | 是 |
| 13 | 女 | 51 | CML | 8 | 子供母 | 29 | O-A | Ⅰ类 | 有 | 5.3 | 6.4 | 否 |
| 14 | 女 | 36 | AA | 10 | 子供母 | 16 | A-A | Ⅱ类 | 无 | 11.0 | 12.0 | 是 |
| 15 | 女 | 59 | MDS | 12 | 子供母 | 36 | O-A | Ⅰ类 | 有 | 19.7 | 6.9 | 否 |
| ALL:急性淋巴细胞白血病;AA:再生障碍性贫血;MDS:骨髓增生异常综合征;AML:急性髓系白血病;CML:慢性髓系白血病 | ||||||||||||
2.3 干细胞植入及生存情况
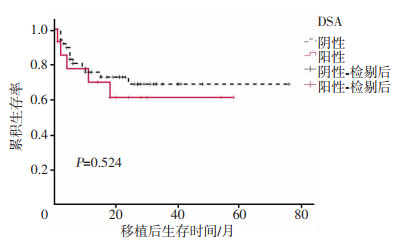
55例DSA阴性患者中,53例(96.4%)获得粒细胞植入; 早期死亡5例,其中2例在粒系植入前,3例在粒系植入后。15例DSA阳性患者,11例(73.3%)粒系植入,无早期死亡。DSA阳性患者粒系植入中位时间较DSA阴性患者明显延迟(P=0.027)。植入失败患者6例,其中DSA阳性患者GF的4例(26.7%),明显高于DSA阴性患者(χ2=5.039,P=0.025)。多因素分析结果显示(表 3),DSA是GF的独立影响因素(HR=9.273,95% CI=1.505~57.124,P=0.016),与患者性别、患者年龄、供者年龄、血型相合程度、HLA相合程度、配型情况、累积MFI值、移植预处理方案、DSA阳性去敏治疗及回输干细胞数量因素无显著相关。aGVHD和cGVHD在DSA阳性和阴性的患者之间均无显著差异。移植成功患者1年和2年的OS分别为86.8%、74.0%。DSA阳性患者1年和2年OS均为60.9%,有低于DSA阴性患者趋势,但差异无统计学意义(P=0.524,图 1)。通过多因素回归分析OS影响因素,发现只有GF是OS的独立影响因素(HR=26.780,95%CI=6.386~112.298,P < 0.01)。
| 影响因素 | GF | OS | |||
| P值 | HR(95%CI) | P值 | HR(95%CI) | ||
| 患者性别 | 0.254 | 0.277(0.031~2.513) | 0.607 | 1.275(0.506~3.213) | |
| 患者年龄 | 0.121 | 1.069(0.983~1.162) | 0.452 | 1.013(0.980~1.047) | |
| 供者年龄 | 0.247 | 0.955(0.884~1.032) | 0.270 | 0.978(0.940~1.017) | |
| 血型不合 | 0.176 | 0.662 | |||
| 主要及主次均不合 | 0.809 | 1.357(0.114~16.164) | 0.787 | 0.838(0.233~3.011) | |
| 次要不合 | 0.076 | 5.700(0.636~38.800) | 0.438 | 1.577(0.499~4.983) | |
| 配型情况(GVH) | 0.626 | 0.705 | |||
| 配型情况(GVH 6个位点相合) | 0.350 | 2.750(0.330~33.921) | 0.593 | 0.651(0.135~3.141) | |
| 配型情况(GVH 7个位点相合) | 0.731 | 0.647(0.054~7.746) | 0.317 | 0.501(0.129~1.940) | |
| 配型情况(GVH 8个位点及以上相合) | 0.807 | 0.733(0.061~8.832) | 0.944 | 1.040(0.349~3.095) | |
| DSA阳性 | 0.016 | 9.273(1.505~57.124) | 0.530 | 1.393(0.496~3.912) | |
| 累积MFI值>10 000 | 0.698 | 1.571(0.160~15.465) | 0.376 | 0.402(0.053~3.026) | |
| 移植预处理方案 | 0.680 | 1.596(0.173~14.756) | 0.521 | 0.712(0.253~2.005) | |
| DSA阳性去敏治疗 | 0.178 | 3.600(0.558~23.244) | 0.849 | 1.131(0.318~4.021) | |
| 干细胞CD34计数 | 0.966 | 0.995(0.796~1.244) | 0.880 | 0.989(0.861~1.137) | |
| 干细胞单个核计数 | 0.127 | 0.640(0.362~1.134) | 0.169 | 0.852(0.679~1.070) | |
| 植入失败 | - | - | < 0.001 | 26.780(6.386~112.298) | |
| 粒系植入时间 | - | - | 0.430 | 1.038(0.946~1.140) | |
| 血小板植入时间 | - | - | 0.912 | 0.999(0.981~1.018) | |
|
| 图 1 DSA阳性和DSA阴性患者的OS比较 |
2.4 DSA阳性患者的去敏治疗
15例DSA阳性患者,针对10例中度阳性和强阳性的患者进行去敏治疗(表 4),联合去敏治疗组患者4例(3例强阳性,1例中度阳性,累及MFI中位值27 675),采用清除或中和抗体(TPE、IVIG)+抑制抗体生成(硼替佐米、利妥昔单抗)的方法;单一去敏治疗组患者6例(累及MFI中位值15 898),包括4例强阳性,2例中度阳性,仅采用中和抗体或者抑制抗体产生的措施;5例患者DSA弱阳性(累及MFI中位值1 127),未采取去敏治疗。3个治疗组在性别、年龄、粒系重建时间及血小板重建时间无显著差异,联合去敏治疗组和单一去敏治疗组患者累积MFI值明显高于无去敏治疗组(P=0.032),累及MFI值>10 000患者比例更高(P=0.014)。而单一去敏治疗组患者GF发生率明显高于联合去敏治疗组(P=0.008)。治疗后有3例患者监测抗体水平,其中2例患者复查DSA位点水平明显下降,干细胞成功植入,而1例患者的抗体滴度,经治疗后无明显降低,最终发生GF。
| DSA去敏治疗措施 | 联合去敏治疗组(n=4) | 单一去敏治疗组(n=6) | 无去敏治疗组(n=5) | P值 |
| 性别(女) | 4(100.0) | 6(100.0) | 1(0.2) | 0.310 |
| 年龄/岁 | 36(15~56) | 49(39~59) | 39(24~51) | 0.466 |
| 累积MFI值 | 27 675(9 711~55 495) | 15 898(5 084~93 741) | 1 127(973~1 436) | 0.032 |
| 累积MFI>10 000 | 3(75.0) | 4(66.7) | 0(0.0) | 0.014 |
| 粒系重建时间/d | 16(15~35) | 15(14~16) | 15(15~16) | 0.398 |
| 血小板重建时间/d | 19(15~66) | 16(15~18) | 16(15~18) | 0.721 |
| 植入失败 | 0(0.0) | 4(66.7) | 0(0.0) | 0.008 |
3 讨论
既往研究表明,在halo-HSCT、脐带血移植、无关供者全相合移植中,DSA均与植入延迟及GF密切相关[13-14]。一项关于89例接受haplo-HSCT患者的研究结果显示,DSA阳性患者的GF为30%、植入延迟率40%、治疗相关死亡率75%,均显著升高(P < 0.05)[15]。而一项针对126例HLA不匹配的造血干细胞移植患者中,DSA阳性率仅为3.97%,中性粒细胞植入延迟主要与女性、干细胞来源和高HSCT特异性共病指数相关,采取DSA去敏治疗后,发现DSA阳性对干细胞植入无显著影响[16]。西班牙的一项多中心回顾性分析包括1 454例haplo-HSCT患者,在69例(4.7%)DSA阳性患者中8例(12%)发生原发性GF,明显高于DSA阴性患者,DSA强度与更差的OS相关[17]。本研究显示,DSA阳性患者在halpo-HSCT占21.4%,均以女性为主,DSA阳性患者粒系植入时间明显延迟,GF率达26.7%,明显高于DSA阴性患者(P=0.025)。DSA对GVHD、OS均无显著影响,可能与样本量较小及采取了DSA阳性的去敏治疗影响有关。
为降低GF的风险,实体器官移植中,采用TPE、IVIG、利妥昔单抗和硼替佐米来逆转DSA介导的移植排斥反应和减少抗体负荷[6, 11]。MISRA等[18]发现血浆置换可以降低DSA,但如果MFI值很高(超过18 000),则需高达20次以上的置换频率才能达到预期疗效。利妥昔单抗和硼替佐米,则是通过抑制B细胞/浆细胞,阻断DSA的产生。对83例haplo-HSCT患者前瞻性分析,采用利妥昔单抗单药对DSA阳性患者进行去敏治疗,但高水平的DSA(MFI≥5 000)阳性患者仍发生较高的植入不良[19]。而在14例DSA阳性的haplo-HSCT患者中,接受硼替佐米联合IVIG的去敏治疗,仅2例患者抗体滴度明显下降;需要通过再次增加IVIG剂量、利妥昔单抗、TPE等联合治疗手段,才能使抗体滴度下降,保证患者成功植入[20]。因此,单一去敏治疗不能达到理想的效果,而联合的去敏治疗可能带来较好的效果。
对于DSA高滴度患者,采用联合去敏治疗临床效果也存在差异。一项多中心回顾性分析,对64例DSA阳性患者,采用TPE、利妥昔单抗、硼替佐米及供者血小板输注等组成的联合去敏治疗,监测治疗后的抗体水平,仍有7%的患者持续MFI>5 000,5%的患者MFI持续>10 000,2例患者出现植入失败[17]。而一项126例HLA不匹配的造血干细胞移植的前瞻性临床研究显示,5例DSA阳性患者,其中3例(1 000 < MFI<5 000)采取包括TPE、IVIG、利妥昔单抗和供者血小板输注的联合去敏治疗后干细胞成功植入,无GF发生,对移植未产生不良影响[16]。本中心采用TPE、IVIG、利妥昔单抗、硼替佐米等多药组合方式,对DSA中度及强阳性患者进行去敏治疗,联合去敏治疗效果优于单一去敏治疗,GF发生率更低。
总之,在拟行haplo-HSCT患者,检测HLA抗体,对于DSA阳性患者,DSA抗体水平滴度过高,可能导致粒系植入延迟或植入失败的发生,需采取联合的DSA去敏治疗,并在处理后动态监测抗体滴度水平,保证干细胞的成功植入,降低GF发生。因本研究为单中心回顾性研究分析,样本量有限,存在一定的局限性,需要前瞻性的多中心临床研究更好地定义和验证haplo-HSCT中DSA管理的共识策略。
致谢 感谢上海荻硕贝肯医学检验所有限公司提供抗体的检测报告| [1] |
SNOWDEN J A, SÁNCHEZ-ORTEGA I, CORBACIOGLU S, et al. Indications for haematopoietic cell transplantation for haematological diseases, solid tumours and immune disorders: current practice in Europe, 2022[J]. Bone Marrow Transplant, 2022, 57(8): 1217-1239. |
| [2] |
TIMOFEEVA O A, PHILOGENE M C, ZHANG Q J. Current donor selection strategies for allogeneic hematopoietic cell transplantation[J]. Hum Immunol, 2022, 83(10): 674-686. |
| [3] |
AULETTA J J, KOU J Q, CHEN M, et al. Real-world data showing trends and outcomes by race and ethnicity in allogeneic hematopoietic cell transplantation: a report from the center for international blood and marrow transplant research[J]. Transplant Cell Ther, 2023, 29(6): 346. |
| [4] |
CIUREA S O, THALL P F, WANG X M, et al. Donor-specific anti-HLA Abs and graft failure in matched unrelated donor hematopoietic stem cell transplantation[J]. Blood, 2011, 118(22): 5957-5964. |
| [5] |
CIUREA S O, THALL P F, MILTON D R, et al. Complement-binding donor-specific anti-HLA antibodies and risk of primary graft failure in hematopoietic stem cell transplantation[J]. Biol Blood Marrow Transplant, 2015, 21(8): 1392-1398. |
| [6] |
AKHTAR W, PETERZAN M A, BANYA W, et al. Donor specific antibodies association with survival and adverse events after heart transplantation: a single center retrospective study between 2006 and 2021[J]. Clin Transplant, 2023, 37(4): e14914. |
| [7] |
ROCCA U L, PERRONE M P, PICIOCCHI A, et al. Anti-HLA donor-specific antibodies in allogeneic stem cell transplantation: management and desensitization protocol[J]. Bone Marrow Transplant, 2019, 54(10): 1717-1720. |
| [8] |
LIMA A C M, GETZ J, DO AMARAL G B, et al. Donor-specific HLA antibodies are associated with graft failure and delayed hematologic recovery after unrelated donor hematopoietic cell transplantation[J]. Transplant Cell Ther, 2023, 29(8): 493. |
| [9] |
HUANG Y R, LUO C X, WU G X, et al. Effects of donor-specific antibodies on engraftment and long-term survival after allogeneic hematopoietic stem cell transplantation-a systematic review and meta-analysis[J]. Bone Marrow Transplant, 2023, 58(5): 544-551. |
| [10] |
APPERLEY J, NIEDERWIESER D, HUANG X J, et al. Haploidentical hematopoietic stem cell transplantation: a global overview comparing Asia, the European union, and the United States[J]. Biol Blood Marrow Transplant, 2016, 22(1): 23-26. |
| [11] |
CIUREA S O, CAO K, FERNANDEZ-VINA M, et al. The European society for blood and marrow transplantation (EBMT) consensus guidelines for the detection and treatment of donor-specific anti-HLA antibodies (DSA) in haploidentical hematopoietic cell transplantation[J]. Bone Marrow Transplant, 2018, 53(5): 521-534. |
| [12] |
ALTAREB M, AL-AWWAMI M, ALFRAIH F, et al. Incidence and significance of donor-specific antibodies in haploidentical stem cell transplantation[J]. Bone Marrow Transplant, 2023, 58(6): 680-686. |
| [13] |
JO T, ARAI Y, HATANAKA K, et al. Adverse effect of donor-specific anti-human leukocyte antigen (HLA) antibodies directed at HLA-DP /-DQ on engraftment in cord blood transplantation[J]. Cytotherapy, 2023, 25(4): 407-414. |
| [14] |
KRUMMEY S M, GAREAU A J. Donor specific HLA antibody in hematopoietic stem cell transplantation: implications for donor selection[J]. Front Immunol, 2022, 13: 916200. |
| [15] |
ZOU J, ROMEE R, SLADE M, et al. Untreated donor specific antibodies against HLA are associated with poor outcomes in peripheral blood haploidentical hematopoietic cell transplantation[J]. Bone Marrow Transplant, 2017, 52(6): 898-901. |
| [16] |
LA ROCCA U, PERRONE M P, PICIOCCHI A, et al. Donor specific anti-HLA antibodies in hematopoietic stem cell transplantation. Single center prospective evaluation and desensitization strategies employed[J]. Blood Transfus, 2023, Epub ahead of print. |
| [17] |
BAILÉN R, ALENDA R, HERRUZO-DELGADO B, et al. Results of haploidentical transplant in patients with donor-specific antibodies: a survey on behalf of the Spanish Group of Hematopoietic Transplant and Cell Therapy[J]. Front Immunol, 2023, 14: 1165759. |
| [18] |
MISRA M K, XIN J J, BROWN N K, et al. Effective desensitization for a strong donor-specific HLA antibody in a case of HLA-mismatched allogeneic hematopoietic cell transplantation[J]. HLA, 2019, 94(3): 307-311. |
| [19] |
王志东, 孙于谦, 闫晨华, 等. 单倍型相合造血干细胞移植前血液病患者体内供者特异性抗人类白细胞抗原抗体水平对利妥昔单抗去敏治疗后造血重建不良的影响分析[J]. 中华内科杂志, 2021, 60(7): 644-649. WANG Z D, SUN Y Q, YAN C H, et al. Negative effects of donor specific anti-HLA antibody on poor hematopoietic recovery in patients with hematological diseases receiving haploidentical stem cell transplantation and rituximab for desensitization[J]. Chin J Intern Med, 2021, 60(7): 644-649. |
| [20] |
CHOE H, GERGIS U, HSU J, et al. Bortezomib and immune globulin have limited effects on donor-specific HLA antibodies in haploidentical cord blood stem cell transplantation: detrimental effect of persistent haploidentical donor-specific HLA antibodies[J]. Biol Blood Marrow Transplant, 2019, 25(2): e60-e64. |




