2. 400038 重庆,陆军军医大学(第三军医大学)基础医学院:组织胚胎学教研室
2. Department of Histoembryology, College of Basic Medical Sciences, Army Medical University (Third Military Medical University), Chongqing, 400038, China
齿状回(dentate gyrus,DG)是哺乳动物海马结构中经典“三突触传递”的第一站[1]。在觉醒状态下,DG可起到对输入海马信息进行模式分离[2]、过滤输入海马的信息[3]、联系输入海马的不同刺激信息[4]以及检测环境新奇性等的作用[5]。研究发现:睡眠期DG神经元的活动也可能具有重要功能。例如,快速眼动(rapid eye movement,REM)睡眠期间,DG区新生神经元放电活动较活跃,参与对场景恐惧记忆的巩固过程[6]。下丘脑乳头体上核-DG神经通路在REM睡眠期激活,参与对社交记忆的巩固[7]。而睡眠剥夺则被发现会损害DG神经活动,并损害记忆能力[8]。综上表明,DG区在睡眠期的活动具有重要的记忆巩固功能。目前尚不清楚DG神经元在睡眠期间与觉醒状态的活动的区别。理解其在睡眠期间的活动特征,是解析DG参与离线状态记忆巩固神经机制的基础。为此,本研究拟利用在体多通道记录技术,比较小鼠DG区不同类型神经元在睡眠-觉醒状态下的放电活动差异,并进一步探讨DG区神经元在睡眠期间记忆巩固相关神经振荡发生时的放电活动特征。
1 材料与方法 1.1 实验动物采用3月龄SPF级雄性C57BL/6野生型小鼠,共6只,体质量22~25 g(由成都集萃药康生物科技有限公司提供)。在手术前的适应期、术后的恢复期以及记录实验期,小鼠均饲养在12 h光照和12 h黑暗、温度21~25 ℃的单笼中。所有实验操作符合陆军军医大学动物福利伦理审查指南要求(AMUWEC20210443)。
1.2 手术方法使用浓度为1%的异氟烷持续麻醉小鼠。麻醉小鼠的头部固定于脑立体定位仪上。调整颅骨位置,使其顶部呈水平位(颅顶部左、右对称位置的高度差不超过0.1 mm,前、后囟高度差不超过0.2 mm)。在双侧小脑上方对称位置各钻1个小孔,分别植入1颗不锈钢螺丝,作为地线与参考电极连接位点。在小鼠左侧海马上方植入1个由4组Tetrode电极所组成的微电极阵列,坐标如下:前囟后1.9 mm、中线旁开1.6 mm、植入深度0.7 mm。在右侧齿状回上方也植入1个由4组Tetrode电极所组成的微电极阵列,坐标:前囟后1.9 mm、中线旁开1.15 mm、植入深度1.4或1.8 mm。微电极阵列的制作参考文献[9]的方法,手术后恢复5 d。在此期间,小鼠体质量和进食逐渐恢复至术前水平。之后再进行实验环境和实验操作的习服,并开始电生理记录。
1.3 电生理信号记录手术恢复5 d后,对小鼠进行操作流程和记录环境的习服训练3~4 d。在此期间,推进器以75 μm/d的速度,将微电极阵列分别向小鼠背侧海马CA1区和DG区推进,直到可以稳定记录到目标区域神经元的峰电位发放活动。使用RHD2000(美国Intan Technologies公司)神经数据采集器、以20 000 Hz采样频率对小鼠背侧海马CA1区和DG区神经元单位放电信号、局部场电位信号进行同步采样。记录均在每天8:30~12:00开展,每次记录时间至少3 h,每只小鼠记录2~3 d,每次记录结束后,DG区微电极阵列需推进50 μm,以便在下一记录日能够记录到新的DG神经元。
1.4 大脑觉醒-睡眠状态判定参照文献[10-11]的方法,用背侧海马的局部场电位活动和头颈部三维加速度反映小鼠的大脑觉醒-睡眠状态。定义标准如下:①觉醒(wakefulness):背侧海马呈现明显θ频带(5~10 Hz)振荡,并且小鼠头颈部三维加速度明显增加,持续时间>10 s。②非快速眼动(non-rapid eye movement,NREM)睡眠:背侧海马呈现出高振幅、低频(1~4 Hz)振荡活动,并且小鼠头颈部无明显三维加速现象,状态持续时间>10 s。③REM睡眠:背侧海马呈现明显θ频带(5~10 Hz)振荡,但小鼠无头颈部三维加速现象,且持续时间>10 s。
1.5 峰电位甄选在离线条件下对记录的局部场电位数据进行带通滤波(800~6 000 Hz)处理。使用KlustaKwik软件对每组电极上采集的单位放电信号进行自动甄选、并归为不同的峰电位集群。再通过Klusters软件,进行手动判别和甄选,获得高信度的DG区神经元峰电位信号。
1.6 神经元类型电生理区分在获取DG区神经元峰电位信号后,参照文献[12]的标准,对所记录神经元的类型进行电生理区分,具体标准如下。
1.6.1 颗粒细胞觉醒状态下平均放电频率<0.5 Hz;峰电位爆发式发放指数>10。峰电位爆发式发放指数通过神经元峰电位发放自相关分布来确定,将3~5 ms区间发放概率与200~300 ms区间发放概率的比值定义为爆发式发放指数。
1.6.2 苔藓细胞觉醒状态下平均放电频率>0.5 Hz,但<5 Hz;峰电位爆发式发放指数>10。
1.6.3 中间神经元觉醒状态下平均放电频率>5 Hz;峰电位爆发式发放指数<5。
1.7 尖波涟漪波离线检测尖波涟漪波(sharp wave ripple,SWR)振荡的检测在NREM睡眠期间进行。参照文献[10-13]的方法,在多道的海马区记录信号中,以SWR幅度最大的通道作为检测通道,以没有SWR的通道作为参考通道。先对2个通道的信号进行差分处理,再对差分信号进行100~250 Hz带通滤波处理。SWR被定义为振幅超过基线均值+4倍基线标准差的事件。
1.8 记录位点鉴定在实验完成后,利用30 μA直流电(10 s)损毁记录电极尖端周围小鼠脑组织。损毁48 h后,腹腔注射致死剂量的戊巴比妥钠(浓度3%)。经心脏灌注生理盐水和4%多聚甲醛溶液各100 mL。将剥离后的脑组织置于4%多聚甲醛溶液中固定12 h,再转移至30%蔗糖溶液中脱水24 h。使用冰冻切片机将脱水后的脑组织制成40~50 μm厚的冠状切片。经DAPI染色后,在荧光显微镜(日本Olympus公司)下观察代表电极尖端位置的损毁区域。只有损毁位点明确在CA1和DG区小鼠的电生理信号数据才可被纳入数据的分析和统计。
1.9 统计学分析数据以 x±s表示,使用SPSS 20.0软件进行统计分析。DG区和CA1区神经元的平均放电频率、峰电位谷-峰宽度的比较采用独立样本t检验。同一神经元在不同大脑活动状态下的平均放电频率比较采用配对样本t检验。P<0.05为差异具有统计学意义。
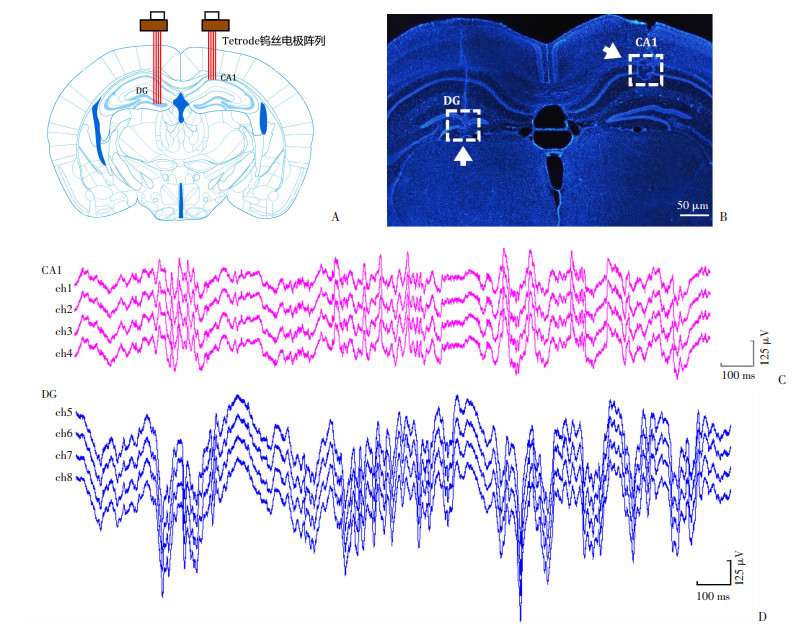
2 结果 2.1 小鼠海马DG神经元的在体电生理记录与分类为确定DG神经元在睡眠以及海马特定振荡发生期间的放电活动特征,将微电极阵列分别植入到小鼠海马DG区(左侧)和CA1区(右侧)。电生理记录之后的组织学鉴定结果显示,微电极阵列分别准确植入到海马DG和CA1区(图 1A、B)。同步记录海马DG和CA1区局部场电位信号(图 1C),且在体多通道记录均在日间时相开展。
|
| A:记录位置示意图;B:代表性DAPI染色 箭头:示阵列电极尖端位置;C:CA1区局部场电位;D:DG区局部场电位 图 1 海马DG区和CA1区局部场电位信号的同步记录 |
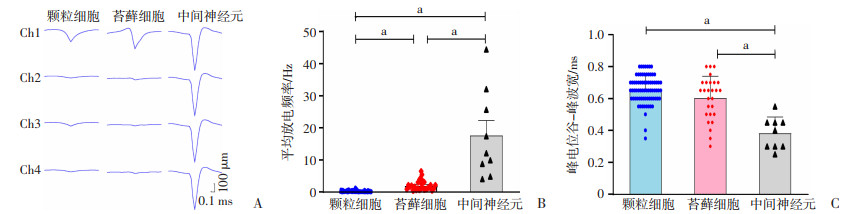
在6只小鼠中记录和甄选出111个DG神经元单位放电活动。将这些神经元分为颗粒细胞、苔藓细胞和中间神经元3类(图 2A)。结果显示:颗粒细胞(n=75)、苔藓细胞(n=27)和中间神经元(n=9)的平均放电频率分别为(0.33±0.03)、(2.09±0.30)、(17.72± 4.85)Hz。统计学分析表明,颗粒细胞的平均峰电位发放频率显著低于苔藓细胞和中间神经元(P<0.001,图 2B)。而比较3类神经元峰电位波宽则显示,颗粒细胞峰电位的谷-峰波宽与苔藓细胞相当(P>0.05),且二者均较中间神经元更宽(P<0.001,图 2C)。结果表明,海马DG区颗粒细胞、苔藓细胞和中间神经元3类细胞具有不同的在体电生理学特性。
|
| A:发放的峰电位;B:平均放电频率;C:峰电位谷-峰波宽;a:P<0.001 图 2 Tetrode电极记录的代表性海马DG区3类神经元电生理学特征 |
2.2 海马DG神经元在不同脑功能状态下的活动特征区别
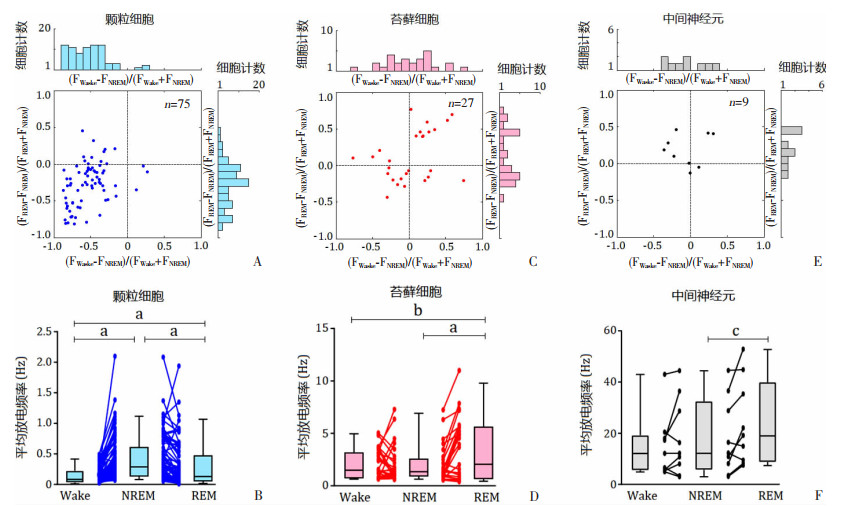
根据大脑皮层脑电振荡活动的频率及动物头颈部三维加速情况,可对小鼠觉醒、NREM睡眠、REM睡眠3种状态进行区分。本研究对3类海马DG区神经元在觉醒、NREM睡眠和REM睡眠状态下的峰电位发放活动进行分析。对Wake-NREM调制指数(FWake-FNREM)/(FWake+FNREM)和REM-NREM调制指数(FREM-FNREM)/(FREM+FNREM)(F是神经元在某状态下的平均峰电位发放频率)的分析显示:颗粒细胞的Wake-NREM调制指数和REM-NREM调制指数分别呈现以-0.52和-0.27为平均重心的偏正态单峰分布,表明其在NREM睡眠期最为活跃(图 3A)。统计学分析证实:颗粒细胞在NREM睡眠期的峰电位发放频率[(0.41±0.04)Hz]显著高于觉醒期[(0.13± 0.02)Hz,t=8.15,P<0.001]和REM睡眠期[(0.30± 0.04)Hz,t=5.04,P<0.001,图 3A]。此外,颗粒细胞在REM睡眠期的峰电位发放频率显著高于觉醒期(t=4.06,P<0.001,图 3B)。以上结果表明,海马DG区颗粒细胞在NREM睡眠期的发放频率最高,REM睡眠期发放频率其次,而在觉醒状态下的发放频率最低。
|
| A:DG区颗粒细胞的Wake-NREM调制指数和REM-NREM调制指数分布;B:3种脑状态下DG区颗粒细胞的放电频率的比较 a:P<0.001;C:DG区苔藓细胞的Wake-NREM调制指数和REM-NREM调制指数分布;D:3种脑状态下DG区苔藓细胞的放电频率的比较 a:P<0.001,b:P<0.01;E:DG区中间神经元的Wake-NREM调制指数和REM-NREM调制指数分布;F:3种脑状态下DG区中间神经元的放电频率的比较 c:P<0.05 图 3 海马DG区不同类型神经元在觉醒、NREM睡眠和REM睡眠状态下放电的不同特征 |
与颗粒细胞不同的是,苔藓细胞的Wake-NREM调制指数和REM-NREM调制指数均呈现以0.02和0.12为平均值的无重心的散在分布(图 3C)。统计分析表明:苔藓细胞在NREM睡眠期的峰电位发放频率[(1.91±0.34)Hz]与觉醒期[(1.96±0.27)Hz,t=0.15,P>0.05]相当,但二者均低于REM睡眠期发放频率[(3.27±0.58)Hz,t=3.73和2.95,Ps<0.01,图 3D]。以上结果表明:海马DG区苔藓细胞在REM睡眠期发放频率最高,而在觉醒期和NREM睡眠期则发放频率相对较低。
此外,中间神经元的Wake-NREM调制指数和REM-NREM调制指数的结果显示,海马DG区中间神经元REM-NREM调制指数呈现以0.15为平均重心的单峰分布,而Wake-NREM调制指数以-0.04位平均值为无重心的散在分布。该结果表明,中间神经元在REM睡眠期最为活跃(图 3E)。统计学分析进一步证实:DG区中间神经元在NREM睡眠期的峰电位发放频率[(18.24±5.28)Hz]与觉醒期[(14.93±4.32)Hz,t=1.33,P>0.05]相当,但低于REM睡眠期[(23.81±5.92)Hz,t=-2.54,P<0.05],见图 3F。以上结果表明,海马DG区中间神经元在REM睡眠期间的发放频率相对较强。
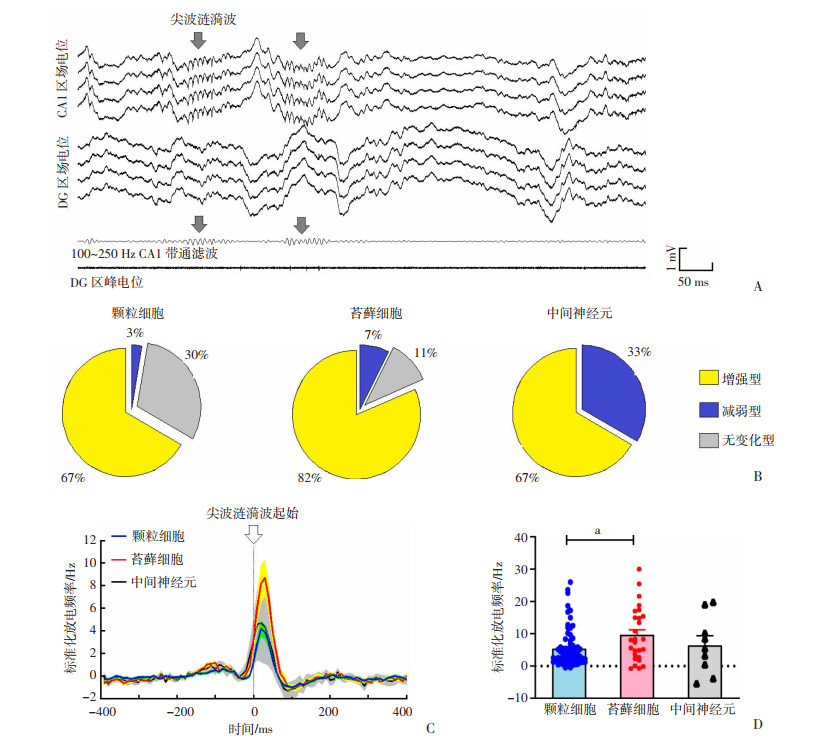
2.3 DG神经元在NREM睡眠海马SWR振荡期间的放电活动特征在NREM睡眠期间,海马内会发生SWR振荡。本研究量化分析了DG区神经元在SWR振荡发生时的发放活动变化。如图 4A所示,DG区神经元在SWR振荡发生后峰电位发放活动增强。67%(50/75)颗粒细胞、82%(22/27)苔藓细胞、67%(6/9)中间神经元在SWR振荡发生时发放增强(图 4B)。统计学分析进一步显示,在3类DG神经元中,苔藓细胞在SWR振荡发生时发放频率的增加程度最大(9.65±1.64),显著高于颗粒细胞[(5.33±0.67),t=2.95,P<0.01,图 4C、D]。
|
| A:DG神经元在尖波涟漪波振荡期间的发放;B:神经元类型及比例;C:放电频率随时间变化曲线;D:不同细胞的放电频率比较 a:P<0.001 图 4 DG区神经元在NREM睡眠海马SWR振荡期间的发放活动变化 |
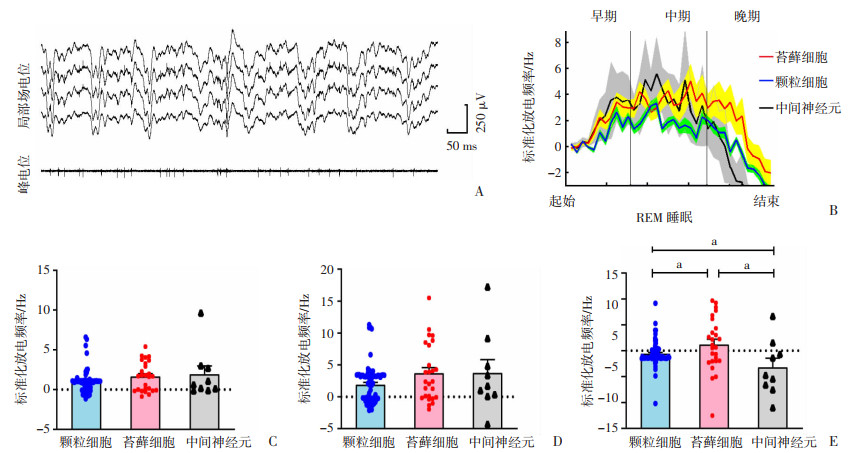
由于REM睡眠期θ震荡参与情绪记忆巩固等重要活动,本研究还量化分析了DG区神经元在θ振荡发生过程中的发放活动变化。如图 5A所示,DG区神经元在θ振荡发生时峰电位发放活动增强。进一步分析和比较了3类DG区神经元在REM睡眠θ振荡早期(前1/3)、中期(中1/3) 以及后期(后1/3)的峰电位发放活动变化(图 5B)。结果显示:在REM睡眠θ振荡早期和中期,3类DG区神经元放电频率均增强但强度差异无统计学意义(图 5C、D)。在REM睡眠θ振荡后期,颗粒细胞[(-0.59±0.28),t=-1.91,P<0.05]和中间神经元[(-3.19±1.89),t=-2.13,P<0.05]的发放频率降低,均低于苔藓细胞(1.22±1.03)。此外,中间神经的发放频率的降低程度也大于颗粒细胞(P<0.05, 图 5E)。
|
| A:DG神经元在θ振荡期间的代表性峰电位发放活动; B:REM睡眠不同阶段发放活动变化; C~E: REM睡眠早期(C)、中期(D)、后期(E)神经元发放比较 a:P<0.05 图 5 DG区神经元在REM睡眠海马θ振荡期间的发放活动变化 |
3 讨论
本研究比较海马DG区颗粒细胞、苔藓细胞和中间神经元在睡眠-觉醒周期中的放电活动差异,并进一步分析它们在睡眠期海马SWR和θ振荡发生时放电活动变化。结果显示:相对于觉醒期,DG区颗粒细胞和苔藓细胞在睡眠期间的放电频率更高,但不同类型细胞放电频率最高的睡眠时相不同。颗粒细胞在NREM睡眠期放电频率最高,而苔藓细胞在REM睡眠期放电频率最高。特别是,DG区3类神经元在睡眠期海马SWR和θ振荡发生时的放电频率会进一步增高。其中,苔藓细胞在SWR振荡发生时放电频率的增加程度最大,在θ振荡放电增强活动持续的时间最长。综上表明DG区3类神经元具有不同睡眠-觉醒状态的放电动力学特征。
3.1 颗粒细胞和苔藓细胞在NREM睡眠期间的放电活动特征齿状回中颗粒细胞数量最多,放电频率低,参与对海马输入信息的模式分离[14]。本研究根据在体电生理学特性的不同,区分出一类峰电位低频发放、峰电位谷-峰波宽较宽的神经元,约占所记录细胞总数的67.6%,这些特性与既往研究报道的颗粒细胞特性相一致[12]。本研究电生理区分出的颗粒细胞在NREM睡眠期放电活动是觉醒状态活动的3倍。此外,颗粒细胞在NREM睡眠期SWR振荡发生时放电活动进一步增强。研究发现,颗粒细胞的放电活动能够促进DG区成年期神经发生[15]。由于睡眠剥夺会显著抑制成年期神经发生及相关的记忆巩固[16]。鉴于此,本研究认为:睡眠剥夺可能会通过使动物长时间处于觉醒状态,从而降低颗粒细胞兴奋活动、并抑制DG区成年期神经发生。
苔藓细胞是分布在DG门区的另一类兴奋性神经元。它可以接受颗粒细胞的兴奋输入,同时还可回返支配DG区颗粒细胞和中间神经元系,调控这2类神经元的放电活动[17]。既往膜片钳记录研究报道,离体条件下可在苔藓细胞上记录到SWR相关发放[18]。本研究进一步证实:在体条件下,苔藓细胞也可展现出SWR振荡相关的放电活动。特别是其放电增加的强度高于颗粒细胞和中间神经元,且表现出放电增强细胞的比例更大。上述结果表明,苔藓细胞放电活动受到SWR振荡的影响更强。这可能是由于苔藓细胞接受海马CA3区锥体细胞的回返投射输入所致[19]。在NREM睡眠期,CA3区锥体细胞的兴奋活动是SWR振荡启动的信号来源[20]。
3.2 颗粒细胞和苔藓细胞在REM睡眠期间的放电活动特征本研究还发现,颗粒细胞和苔藓细胞均展现出REM睡眠期θ振荡相关的放电活动。由于2类细胞均接受来自内侧隔核的乙酰胆碱能和Y-氨基丁酸能纤维输入[21-22]。因此,有理由推测2类细胞在θ振荡发生时的放电活动有可能是受到REM睡眠期内侧隔核信号调控所引起的。此外,本研究中还记录了少量高频率发放的中间神经元,但它们受睡眠状态调控的总体效应相对于颗粒细胞和苔藓细胞较弱。一种可能的原因是,中间神经元主要发挥了调控邻近颗粒细胞的兴奋活动和DG局部振荡状态的作用,故不易受到睡眠-觉醒状态的调控。另一种可能的原因是,本研究记录的中间神经元细胞数量较少。相对较小的样本量可能掩盖相关的统计学差异。因此,DG区中间神经元是否以及如何受睡眠状态调控还需要更多实验的证实。
综上所述,本研究的结果表明DG区颗粒细胞、苔藓细胞和中间神经元在睡眠-觉醒周期中的放电活动存在显著差异。它们在睡眠期海马SWR和θ振荡发生时放电活动会有显著的放电动力学特征变化。
| [1] |
AINMUELLER T, BARTOS M. Dentate gyrus circuits for encoding, retrieval and discrimination of episodic memories[J]. Nat Rev Neurosci, 2020, 21(3): 153-168. |
| [2] |
WANG H S, ROSENBAUM R S, BAKER S, et al. Dentate gyrus integrity is necessary for behavioral pattern separation but not statistical learning[J]. J Cogn Neurosci, 2023, 35(5): 900-917. |
| [3] |
FERNÁNDEZ-RUIZ A, OLIVA A, SOULA M, et al. Gamma rhythm communication between entorhinal cortex and dentate gyrus neuronal assemblies[J]. Science, 2021, 372(6537): eabf3119. |
| [4] |
MILLER L N, WEISS C, DISTERHOFT J F. Learning-related changes in cellular activity within mouse dentate gyrus during trace eyeblink conditioning[J]. Hippocampus, 2022, 32(10): 776-794. |
| [5] |
BORZELLO M, RAMIREZ S, TREVES A, et al. Assessments of dentate gyrus function: discoveries and debates[J]. Nat Rev Neurosci, 2023, 24(8): 502-517. |
| [6] |
KUMAR D, KOYANAGI I, CARRIER-RUIZ A, et al. Sparse activity of hippocampal adult-born neurons during REM sleep is necessary for memory consolidation[J]. Neuron, 2020, 107(3): 552-565.e10. |
| [7] |
QIN H, FU L, JIAN T L, et al. REM sleep-active hypothalamic neurons may contribute to hippocampal social-memory consolidation[J]. Neuron, 2022, 110(23): 4000-4014.e6. |
| [8] |
VERGARA P, SAKAGUCHI M. Mechanisms underlying memory consolidation by adult-born neurons during sleep[J]. Front Cell Neurosci, 2020, 14: 594401. |
| [9] |
ZHANG J, ZHANG K Y, ZHANG L B, et al. A method for combining multiple-units readout of optogenetic control with natural stimulation-evoked eyeblink conditioning in freely-moving mice[J]. Sci Rep, 2019, 9: 1857. |
| [10] |
LI RR, YAN J, CHEN H, et al. Sleep deprivation impairs learning-induced increase in hippocampal sharp wave ripples and associated spike dynamics during recovery sleep[J]. Cereb Cortex, 2022, 32(4): 824-838. |
| [11] |
王斌, 胡昱博, 童柳霞, 等. 腹内侧丘脑神经元在小鼠觉醒-睡眠周期中的放电特征及变化[J]. 陆军军医大学学报, 2022, 44(16): 1585-1591. WANG B, HU Y B, TONG L X, et al. Characteristics of ventromedial thalamic neuronal activity during sleep-wake cycle in mice[J]. J Amry Med Univ, 2022, 44(16): 1585-1591. |
| [12] |
SENZAI Y, BUZSAKI G. Physiological properties and behavioral correlates of hippocampal granule cells and mossy cells[J]. Neuron, 2017, 93(3): 691-704.e5. |
| [13] |
LIU A A, HENIN S, ABBASPOOR S, et al. A consensus statement on detection of hippocampal sharp wave ripples and differentiation from other fast oscillations[J]. Nat Commun, 2022, 13: 6000. |
| [14] |
GOODSMITH D, LEE H, NEUNUEBEL J P, et al. Dentate gyrus mossy cells share a role in pattern separation with dentate granule cells and proximal CA3 pyramidal cells[J]. J Neurosci, 2019, 39(48): 9570-9584. |
| [15] |
LI Y D, LUO Y J, CHEN Z K, et al. Hypothalamic modulation of adult hippocampal neurogenesis in mice confers activity-dependent regulation of memory and anxiety-like behavior[J]. Nat Neurosci, 2022, 25(5): 630-645. |
| [16] |
TERRANOVA J I, OGAWA S K, KITAMURA T. Adult hippocampal neurogenesis for systems consolidation of memory[J]. Behav Brain Res, 2019, 372: 112035. |
| [17] |
SCHARFMAN H E. The enigmatic mossy cell of the dentate gyrus[J]. Nat Rev Neurosci, 2016, 17(9): 562-575. |
| [18] |
SWAMINATHAN A, WICHERT I, SCHMITZ D, et al. Involvement of mossy cells in sharp wave-ripple activity in vitro[J]. Cell Rep, 2018, 23(9): 2541-2549. |
| [19] |
NÚÑEZ-OCHOA M A, CHIPRÉS-TINAJERO G A, GONZÁLEZ-DOMÍNGUEZ N P, et al. Causal relationship of CA3 back-projection to the dentate gyrus and its role in CA1 fast ripple generation[J]. BMC Neurosci, 2021, 22(1): 1-15. |
| [20] |
XIE B, ZHEN Z, GUO O, et al. Progress on the hippocampal circuits and functions based on sharp wave ripples[J]. Brain Res Bull, 2023, 200: 110695. |
| [21] |
LÉRÁNTH C, FROTSCHER M. Cholinergic innervation of hippocampal GAD and somatostatin-immunoreactive commissural neurons[J]. J Comp Neurol, 1987, 261(1): 33-47. |
| [22] |
LERANTH C, HAJSZAN T. Extrinsic afferent systems to the dentate gyrus[J]. Prog Brain Res, 2007, 163: 63-799. |




