1944年Kenneth Watson报道了保留幽门的胰十二指肠切除术(pylorus preserving pancreaticoduodenec-tomy, PPPD)[1],该方法不仅可改善远期胃肠道功能,简化了手术,缩短了手术时间和术中失血量,与传统胰十二指肠切除术(Pancreaticoduodenectomy, PD)对于壶腹周围肿瘤的远期效果也相同[2-5]。近年来,随着科技进步与器械设备的更新,腹腔镜技术已广泛应用于绝大多数腹部手术。
腹腔镜保留幽门胰十二指肠切除术(laparoscopic pylorus preserving pancreaticoduodenectomy, LPPPD)优势在于可行微创操作、保留幽门功能和减少吻合口溃疡等并发症发生。于1994年第一次被报道[6]以来,经过不断的探索与研究发现,该手术方式相较于传统开腹保留幽门胰十二指肠切除术(open pylorus preserving pancreaticoduodenectomy, OPD)是安全可行的,同时在术中失血量和住院时间等方面具有一定的优势[7-10]。圆形吻合器和直线切割吻合器的出现,使得腔镜下消化道重建更加方便,但也存在圆形吻合器置入不便及角度控制受限等问题,导致吻合口出血、漏及狭窄的情况发生,因此许多学者还是建议进行手工重建[11-13]。本中心LPPPD胃肠重建方式主要有两种方式:一是在腔镜下完成胰肠和胆肠重建后,将所保留幽门部十二指肠及需重建的空肠沿标本切口牵出体外,在直视下行十二指肠和空肠的端-侧手工缝合重建后再回纳入腹腔;二是在腔镜下完成胰肠和胆肠重建后,于腔内完成腹腔镜下十二指肠与空肠的端-侧吻合重建,仔细检查无出血、消化道漏等,最后再将标本取出。
LPPPD的难点在于消化道重建,熟练掌握是需要一个较长的培训过程。LPPPD胃肠道重建需在腔镜下行十二指肠和空肠吻合重建,腔镜下吻合存在着输入袢长度、角度测量误差及缝合所需的针距、边距精准度低等问题,尤其在学习曲线阶段。腔外胃肠道重建可通过标本口进行直视下重建,将十二指肠残端和空肠由标本口牵出体外,进行直视下手工吻合重建,理论上可准确控制针距与边距、减少手术时间、提高吻合精准度等。因此,本研究将分析在LPPPD中不同学习曲线阶段行腔外和腔内胃肠道重建围手术期结果,为LPPPD胃-空肠吻合方式的选择提供循证医学证据。
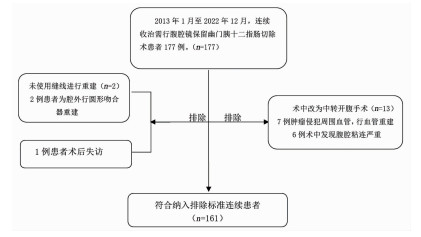
1 资料与方法 1.1 研究对象及标准应用病例对照研究方法,回顾分析了2013年1月至2022年12月,由陆军军医大学第一附属医院肝胆外科连续收治177例接受腹腔镜保留幽门胰十二指肠切除术患者,如图 1所示符合纳入、排除标准共有161例患者,根据手术方式,分为腔外胃-空肠重建组和腔内胃-空肠重建组。其中进行腔外胃-空肠重建62例,腔内胃-空肠重建99例。所有患者术前完成计算机断层扫描血管造影、磁共振胰胆管造影、血液生化学、肿瘤标志物等常规检查,部分患者于超声内镜引导下细针穿刺活检术(EUS-FNA)明确病理诊断。纳入标准同常规微创腹腔镜手术标准:①BMI < 28.0 kg/m2; ②美国麻醉师协会(ASA)评分:Ⅰ~Ⅲ级;③壶腹周围良性肿瘤、胆总管下部肿瘤、胰腺勾突部肿瘤及局限于胰头内部肿瘤; ④慢性胰腺炎伴胰头肿块,保守治疗后反应差; ⑤经多学科会诊讨论和全面评估后,确定可保留幽门情况下切除。排除标准:①既往上腹部手术史并存在腹腔广泛粘连,难以暴露和分离胰腺或建立气腹;②肿瘤存在远处转移,肿瘤位于十二指肠第2部周围,病变超过180°的肠系膜上动脉包裹以及不可重建的肠系膜上静脉/门静脉闭塞或主动脉浸润、包裹等患者不适合行该手术[14];③为控制影响因素,排除使用圆形吻合器及直线切割闭合器进行胃-空肠重建患者;④发现无法继续行腹腔镜治疗,需中转开腹。
|
| 图 1 参与研究的纳入和排除标准 |
所有LPPPD手术由一支外科医疗团队完成,该团队之前有多例开放胰十二指肠切除术(OPD)经验及腹腔镜技术基础。所有手术术前告知患者LPPPD相关风险及存在的优势,并由患者决定手术方式,签署书面知情同意。本研究得到了陆军军医大学第一附属医院伦理委员会批准(批件号:KY2023071)。
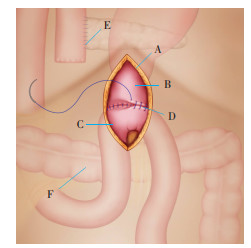
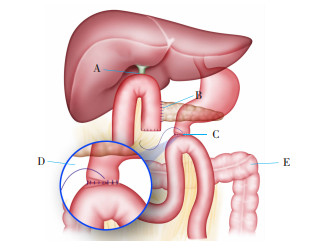
1.2 手术流程患者全身麻醉取分腿仰卧位。控制腹腔充气压力于12~14 mmHg,于脐下经腹壁将10 mm腹腔镜套管(Trocar)穿刺入腹腔,作为腔镜观察孔。于腹直肌外侧插入2个12 mm的主操作孔套管,距离脐部3~4 cm。2个副操作孔用5 mm套管分别置入肋骨边缘与左、右锁骨中线交点处。手术开始时,对腹腔进行了全面探查,以再次确认患者无转移或腹膜播散。术中Kocher切口的切开;胃、胰腺、空肠等的离断;肝十二指肠韧带、肠系膜上静脉-门静脉系统和肠系膜上动脉-腹腔干系统的解剖和必要时的淋巴结清扫步骤基本符合《腹腔镜胰十二指肠切除手术专家共识》[15]提出的相关操作程序及技术标准。完成切除,探查无出血后, 清理腹腔。按胰肠、胆肠和胃肠的顺序进行消化道重建。完成胆肠吻合后,于胆肠吻合口下游45~50 cm处用缝线进行标记。如图 2所示,于剑突下沿上腹正中线做长度约5 cm切口,将标本从切口取出,并将所保留十二指肠残端及缝线标记处空肠牵出腹腔,直视下用4-0 PDS进行端侧手工全层连续缝合及浆肌层连续或间断包埋,吻合完成后还纳入腹腔。如图 3所示,腔内胃肠重建直接于胆肠吻合口下游45~50 cm处,腔镜下用4-0 PDS进行端-侧全层连续缝合及浆肌层连续或间断包埋。确认腹腔无出血,吻合口无渗漏,于胆-空肠吻合口、胰-空肠和十二指肠-空肠吻合口后方放置引流管及腹腔冲洗管,沿套管孔引出腹腔外,移除所有套管,用缝线缝合套管部位。
|
| A: 剑突下标本取出口; B: 十二指肠残端; C: 胆肠吻合口远端45~50 cm处空肠; D: 十二指肠残端与空肠端-侧吻合(全层缝合+浆肌层包埋); E: 胰肠吻合; F: 横结肠 图 2 腔外胃-空肠重建 |
|
| A: 胆管-空肠吻合; B: 胰腺-空肠吻合; C: 十二指肠残端-空肠吻合(全层缝合+浆肌层包埋); D: 倍数放大后的十二指肠残端-空肠吻合(全层缝合+浆肌层包埋); E: 横结肠 图 3 腔内胃-空肠重建 |
1.3 数据收集
所有基数资料包含术前、术中及术后资料。术前资料:性别、年龄、BMI、美国麻醉协会(ASA)评分、总胆红素(TBIL)水平,既往是否患高血压、糖尿病、急慢性胰腺炎、是否行上腹部手术、是否行术前引流。术中资料:胰腺质地[16]、手术时间、胃肠重建时间、术中预估出血量、术后胃管留置时间、是否术中输血。术后资料:术后住院时间、术后并发症(切口感染、术后胃排空延迟、术后胰瘘及胰瘘分级、术后腹腔积液合并感染、术后切口疝)、Clavien-Dindo分级、住院期间是否行二次手术或死亡、术后随访患者生存情况。所有资料在获得后纳入本研究中心数据库进行统计分析。
资料中胰管直径情况根据影像学结果(CTA/MRCP)决定。术中预估出血量为腹腔液体回收系统结合术中吸收血液所用无影纱评估所得。术后胰瘘、胰瘘分级及胃排空延迟等按照国际胰腺疾病研究小组(ISGPS)共识[17]所定义,并根据Clavien-Dindo分级系统[18]进行分级。术后患者生存情况为术后90 d内再手术及死亡情况。
1.4 统计学分析连续基线资料以x±s或M(P25,P75)表示,并通过Student’s t检验进行比较。分类变量以病例数(%)表示,通过χ2检验或Fisher精确检验进行比较。两组患者按照1 ∶1进行倾向评分匹配(propensity score matching,PSM),通过逻辑回归模型进行PSM分析。在建立倾向评分模型后,使用等于倾向评分绝对差值(卡钳值)0.02。使用标准化平均差(SMD)评估匹配数据中的组平衡,并使用组间值< 0.1被认为不显著。基于手术时间利用累计和(cumulative sum, CUSUM)分析方法,使用MATLAB 9.12.0(The MathWorks Inc)软件进行学习曲线图绘制,并根据学习曲线绘制拟合曲线,从拟合曲线拐点制定出学习曲线阶段,并使用SPSS 26.0(SPSS Inc)软件进行统计分析,P<0.05定义为具有统计学意义。
2 结果 2.1 患者基线特征本次研究共纳入161名接受LPPPD患者,其中行腔内胃-空肠重建99名,行腔外胃-空肠重建62名。两种重建方式患者基线资料如表 1所示。161例纳入患者的年龄为(57.5±12.6)岁,接受两种重建方式患者年龄及性别均无统计学差异(P=0.564, P=0.317),术前ASA评分大部分集中于Ⅰ~Ⅱ阶段(P=0.011), 既往有过上腹部手术史患者主要集中于腔内胃-空肠重建组(P=0.014)。围手术结果和病理结果如表 2所示。腔外胃-腔肠重建组的平均手术时间和胃空肠重建时间显著缩短(P<0.001), 在术后留置胃管时间、术中输血、术中出血量及住院时间未发现明显差异,术后并发症(术后90 d内再次手术、死亡、术后胰瘘、胃排空延迟、腹腔积液等)的发生率在组间无统计学差异。
| 变量 | 手术重建方式 | P | ||
| 总病例数(n=161) | 腔内胃-空肠重建(n=99) | 腔外胃-空肠重建(n=62) | ||
| 年龄/岁 | 57.5±12.6 | 57.1±12.9 | 58.2±12.2 | 0.564 |
| 性别 | ||||
| 男性 | 96(59.6) | 56(56.6) | 40(64.5) | 0.317 |
| 女性 | 65(40.4) | 43(43.4) | 22(35.5) | |
| BMI/(kg/m2) | 22.30±2.79 | 22.14±2.81 | 22.58±2.76 | 0.329 |
| ASA评分 | 0.011 | |||
| Ⅰ~Ⅱ | 156(96.9) | 97(98.0) | 59(95.2) | |
| ≥Ⅲ | 5(3.1) | 2(2.0) | 3(4.8) | |
| 既往病史 | ||||
| 糖尿病 | 21(13.0) | 13(13.1) | 8(12.9) | 0.967 |
| 高血压 | 29(18.0) | 15(15.2) | 14(22.6) | 0.233 |
| 胰腺炎 | 5(3.1) | 2(2.0) | 3(4.8) | 0.316 |
| 既往上腹部手术 | 21(13.0) | 18(18.2) | 3(4.8) | 0.014 |
| 总胆红素/(μmol/L) | 106.2(17.6, 229.8) | 96.8(15.2, 220.1) | 119.2(27.7, 232.9) | 0.298 |
| 术前引流 | 49(30.4) | 28(28.3) | 21(33.9) | 0.453 |
| 胰腺质地 | 0.427 | |||
| 柔软的 | 160(99.4) | 98(99.0) | 62(100.0) | |
| 质硬的 | 1(0.6) | 1(1.0) | 0 | |
| 变量 | 手术重建方式 | P | ||
| 总病例数(n=161) | 腔内胃-空肠重建(n=99) | 腔外胃-空肠重建(n=62) | ||
| 手术时间/min | 417.0±84.7 | 436.6±85.2 | 385.8±74.6 | <0.001 |
| 胃空肠重建/min | 30.8±15.3 | 37.2±19.5 | 23.6±13.5 | <0.001 |
| 术中输血 | 26(16.1) | 19(19.2) | 7(11.3) | 0.185 |
| 住院时间/d | 15(12, 20) | 15(13.20) | 14(11.17) | 0.108 |
| 术中出血/mL | 200.0(200.0, 300.0) | 200.0(200.0, 300.0) | 200.0(172.5, 300.0) | 0.432 |
| 术后胃管留置时间/d | 5.4±3.2 | 5.4±2.0 | 4.9±3.4 | 0.225 |
| 术后90 d内 | ||||
| 再次手术 | 7(4.3) | 5(5.1) | 2(3.2) | 0.581 |
| 死亡 | 1(0.6) | 1(1.0) | 0 | 0.427 |
| Clavien-Dindo分级 | ||||
| Ⅰ~Ⅱ | 31(19.3) | 20(20.2) | 11(17.7) | 0.480 |
| ≥Ⅲa | 2(1.2) | 2(2.0) | 0 | |
| 术后胰瘘(≥B级) | 15(9.3) | 10(10.1) | 5(8.1) | 0.665 |
| 胃排空延迟 | 11(6.8) | 8(8.1) | 3(4.8) | 0.428 |
| 术后腹腔积液、感染 | 28(17.4) | 19(19.2) | 9(14.5) | 0.446 |
| 术后切口感染 | 1(0.6) | 1(1.0) | 0 | 0.427 |
2.2 基于手术时间学习曲线制定
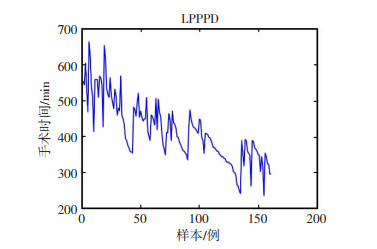
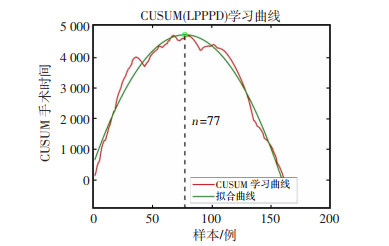
基于手术时间的术中资料,利用CUSUM法进行学习曲线的绘制,并根据学习曲线进行拟合,如图 4、图 5所示。根据公式y=-0.704 868+ 108.744 418*x+551.736 980*x2所绘制拟合曲线拐点发现学习曲线拐点发生于第77例,可认为学习曲线阶段为第1~77例,第77例以后为度过学习曲线阶段。
|
| 图 4 LPPPD原始手术时间图 |
|
| 图 5 LPPPD基于手术时间学习曲线图 |
2.3 学习曲线内两种重建方式的比较
学习曲线阶段内总病例数为77例,其中腔内胃-空肠重建组54例,腔外胃-空肠重建组23例。进一步行1 ∶1的PSM后,排除组间差异如表 3所示,两组各有17例患者。如表 4所示,腔外胃-空肠重建组在手术时间(P=0.006)、胃空肠重建时间(P < 0.001)和术后胃管留置时间(P=0.028)相较于腔内胃-空肠重建组缩短,结果存在统计学差异。在术后胰瘘(P=1.000)、胃排空延迟(P=0.545)、术后90 d内再手术(P=1.000)和死亡(P=0.310)上无明显统计学差异。
| PSM前两种重建方式 | PSM后两种重建方式 | ||||||
| 腔内胃-空肠重建(n=54) | 腔外胃-空肠重建(n=23) | SMD | 腔内胃-空肠重建(n=17) | 腔外胃-空肠重建(n=17) | SMD | ||
| 年龄/岁 | 56.43±13.64 | 59.35±11.16 | 0.234 | 60.71±11.08 | 59.65±10.49 | 0.098 | |
| 女性 | 43(43.4) | 22(35.5) | 0.162 | 8(47.1) | 8(47.1) | 0 | |
| BMI/(kg/m2) | 21.70±2.69 | 21.30±2.92 | 0.142 | 21.29±2.99 | 20.86±2.72 | 0.050 | |
| ASA评分(Ⅰ~Ⅱ) | 53(98.2) | 22(95.6) | 0.150 | 17(100.0) | 16(94.1) | 0.054 | |
| 糖尿病 | 7(13.0) | 3(13.0) | 0 | 3(17.6) | 3(17.6) | 0 | |
| 高血压 | 7(13.0) | 1(4.3) | 0.313 | 1(5.9) | 1(5.9) | 0 | |
| 胰腺炎 | 1(1.9) | 1(4.3) | 0.139 | 0 | 0 | 0 | |
| 既往上腹部手术 | 9(16.7) | 1(4.3) | 0.413 | 3(17.6) | 1(5.9) | 0.369 | |
| 术前引流 | 14(25.9) | 9(39.1) | 0.284 | 7(41.2) | 8(47.1) | 0.119 | |
| PSM后两种重建方式 | P | ||
| 腔内胃-空肠重建(n=17) | 腔外胃-空肠重建(n=17) | ||
| 手术时间/min | 501.47±47.89 | 451.29±51.16 | 0.006 |
| 胃空肠重建时间/min | 45.2±18.5 | 15.5±11.6 | <0.001 |
| 术中输血 | 4(23.5) | 4(23.5) | 1.000 |
| 住院时间/d | 17(13, 20) | 14(11.17) | 0.406 |
| 术中出血/mL | 200.0(172.5, 300.0) | 200.0(200.0, 300.0) | 0.710 |
| 术后胃管留置时间/d | 5.6±3.2 | 4.0±3.0 | 0.028 |
| 术后90 d内再手术 | 1(5.9) | 1(5.9) | 1.000 |
| 术后90 d内死亡 | 1(5.9) | 0 | 0.310 |
| Clavien-Dindo分级(Ⅰ-Ⅱ) | 3(17.6) | 4(23.5) | 0.191 |
| 术后胰瘘(≥B级) | 1(5.9) | 1(5.9) | 1.000 |
| 胃排空延迟 | 2(11.8) | 1(5.9) | 0.545 |
| 术后腹腔积液、感染 | 5(29.4) | 1(5.9) | 0.072 |
| 术后切口感染 | 0 | 0 | - |
2.4 度过学习曲线后两种重建方式的比较
度过学习曲线后病例数为84例,其中腔内胃-空肠重建组45例,腔外胃-空肠重建组39例。进行PSM按照1 ∶1匹配,如表 5所示,腔内和腔外胃-空肠重建组均为25例。进一步行围术期资料比较(表 6)发现两组资料在手术时间(P=0.059)、胃空肠重建时间(P=0.053)、术后胃管留置时间(P=0.521)上无明显统计学差异。主要并发症和术后90 d内生存情况无明显统计学差异。
| PSM前两种重建方式 | PSM后两种重建方式 | ||||||
| 腔内胃-空肠重建(n=45) | 腔外胃-空肠重建(n=39) | SMD | 腔内胃-空肠重建(n=25) | 腔外胃-空肠重建(n=25) | SMD | ||
| 年龄/岁 | 57.84±12.19 | 57.62±12.88 | 0.018 | 56.40±13.08 | 57.28±12.96 | 0.070 | |
| 女性 | 17(37.8) | 14(35.9) | 0.167 | 10(40.0) | 8(32.0) | 0.039 | |
| BMI/(kg/m2) | 22.67±2.90 | 23.34±2.38 | 0.252 | 23.29±2.51 | 22.78±2.46 | 0.205 | |
| ASA评分(Ⅰ~Ⅱ) | 44(97.8) | 37(94.9) | 0.288 | 25(100) | 24(96.0) | 0.155 | |
| 糖尿病 | 6(13.3) | 5(12.8) | 0.015 | 2(8.0) | 3(12.0) | 0.133 | |
| 高血压 | 8(17.8) | 13(33.3) | 0.361 | 6(24.0) | 6(24.0) | 0 | |
| 胰腺炎 | 1(2.2) | 2(5.1) | 0.155 | 1(4.0) | 1(4.0) | 0 | |
| 既往上腹部手术 | 9(20.0) | 2(5.1) | 0.462 | 2(8.0) | 2(8.0) | 0 | |
| 术前引流 | 14(31.1) | 12(30.8) | 0.006 | 6(24.0) | 7(28.0) | 0.091 | |
| PSM后两种重建方式 | P | ||
| 腔内胃-空肠重建(n=25) | 腔外胃-空肠重建(n=25) | ||
| 手术时间/min | 378.12±47.03 | 358.00±27.65 | 0.059 |
| 胃空肠重建/min | 23.5±10.5 | 15.6±12.3 | 0.053 |
| 术中输血 | 5(20.0) | 2(8.0) | 0.221 |
| 住院时间/d | 16.0(11.0, 22.5) | 15.0(12.5, 21.0) | 0.307 |
| 术中出血/mL | 200(150, 300) | 200(125,40) | 0.099 |
| 术后胃管留置时间/d | 4.0±2.5 | 3.8±2.2 | 0.521 |
| 术后90 d内再手术 | 2(4.0) | 0 | 0.149 |
| 术后90 d内死亡 | 0(0) | 0 | - |
| Clavien-Dindo分级(Ⅰ-Ⅱ) | 6(24.0) | 4(16.0) | 0.297 |
| 术后胰瘘(≥B级) | 3(12.0) | 2(8.0) | 0.637 |
| 胃排空延迟 | 0 | 1(4.0) | 0.312 |
| 术后腹腔积液、感染 | 5(20.0) | 3(12.0) | 0.440 |
| 术后切口感染 | 0 | 0 | - |
3 讨论
在过去的一些研究中证实了对于胰腺肿瘤和壶腹部周围肿瘤,保留幽门胰十二指肠(OPPPD)切除术相较于传统胰十二指肠切除术(OPD)的总体长期生存和无病生存是相当的 [4-5, 19]。该术式主要在于改变了传统胃-空肠重建方式,更好的保留了胃肠道功能。在SONG等[9]近几年一项比较LPPPD与OPPPD的大样本量研究分析中表明,LPPPD具有微创腹部手术的典型优点,例如疼痛少,住院时间短,恢复更快,并且在技术上是安全和可行的。既往多数研究主要围绕对于整体术式、相关围手术期及肿瘤结局等影响来进行报道[10, 13]。同样手术方式在不同学习曲线阶段采用腔内和腔外胃-空肠重建对手术操作和围术期结局的影响未见报道。
为进一步去探讨腔内外胃-空肠重建两种方法获益情况,我们纳入了LPPPD患者161例,其中腔内胃-空肠重建患者99例,腔外胃-空肠重建患者62例。根据研究结果,腔内和腔外胃-空肠重建方法在LPPPD患者手术中的应用存在一定差异,在对患者的筛选过程中,除了需满足肿瘤的位置及侵犯情况允许进行LPPPD之外,对行腔外胃-空肠重建患者中,尽可能满足既往无上腹部手术史患者。因为在将残胃及空肠牵出腹腔外重建的过程中,若腹腔粘连较重则无法顺利完成这一步骤。对于腔内重建使用圆形闭合器难度高,无法通过腹腔镜套管,需另行切口,因此均使用缝线进行缝合重建。为平衡影响因素,我们排除了腔外重建使用圆形和直线切割吻合器患者。两种重建方式患者的基线数据比较类似。在本研究中,从总体资料比较可以发现腔外胃-空肠重建组吻合时间和总体手术时间较腔内组缩短,存在统计学差异。经过分析,我们认为,腔外胃-空肠重建更加简便快捷可能是整体手术时间缩短的主要原因。此外,腔内胃-空肠重建组既往上腹部手术史患者占比高于腔外胃-空肠重建组(P=0.014),术中需额外进行粘连松解及组织结构辨认等操作,也是腔内胃-空肠重建组整体手术时间延长的重要原因。但在术中输血、术中出血量、住院时间及术后并发症发生率等方面,两组间没有显著差异。两种重建方式均是安全可行的。
LPPPD是复杂的手术操作,需要一定的时间进行手术过程的熟悉与掌握。所以我们认为,最主要的影响因素可能还是在LPPPD整体术式的熟练程度上,也就是腹腔镜手术本身所存在的一个学习曲线。为进一步证明这一观点,本研究基于手术时间进行了LPPPD学习曲线的研究,并利用拟合曲线拐点客观的对学习曲线阶段进行了制定,发现LPPPD需进行77例手术才能度过学习曲线阶段。我们分别进行了学习曲线阶段和度过学习曲线阶段两种不同重建方式临床获益情况的比较,为排除组间差异及选择偏倚的情况,我们又将两组患者分别进行了1 ∶1倾向评分匹配。发现在学习曲线内,腔外胃-空肠重建组的胃空肠吻合时间、整体手术时间和术后胃管留置时间较腔内胃-空肠重建组明显缩短,差异具有统计学意义。然而,当度过学习曲线后,两组在胃空肠重建时间、整体手术时间和术后胃管留置时间上均无显著性差异。表明在LPPPD学习曲线阶段,相比于腔内胃-空肠重建,腔外胃-空肠重建方式具有简便快捷、更有利于术后胃肠功能恢复的优势。这可能是因为在腔外胃-空肠重建在不增加手术切口创伤的前提下,降低了初期学习阶段的手术操作的复杂性,并提高了胃肠吻合精准度及质量。但在度过学习曲线后这些差异逐渐消失,可能是因为外科医生腹腔镜技术逐渐成熟优化,腔内胃-空肠重建操作更加快捷精确。这也印证了两种重建方式的差异主要体现在不同的学习曲线阶段上。有学者认为,微创胰十二指肠切除手术要达到技术稳定期至少需要60~70例手术经历[20],本研究在学习曲线阶段制定上与其基本一致。笔者认为,腔外重建方式显著降低了胃肠重建难度、加快了手术进程且不会对患者增加额外创伤,即使是度过了LPPPD的学习曲线,仍然是一种值得推荐和选择的胃肠重建方式。
本研究表明,在LPPPD学习曲线阶段内,对于选择性患者,相对于腔内胃-空肠重建,行腔外胃-空肠重建具有简便、快捷优势,更有利于胃肠功能恢复,是该阶段值得推荐的胃肠重建方式。尽管如此,在决定使用哪种重建方法时,还需要充分考虑患者的具体情况和医生的操作经验。
本研究为LPPPD学习曲线阶段内胃肠道重建手术方法的选择提供了有价值的参考,但仍存在一定局限性,如研究的患者数量有限、研究设计的单中心性等。需要进一步开展大样本、多中心的研究探讨这两种重建方法的优劣,结合更多患者的临床资料,确定最适合的重建策略。
| [1] |
WATSON K. Carcinoma of ampulla of vater successful radical resection[J]. Br J Surg, 1944, 31: 368-373. |
| [2] |
LW T, WP L. Preservation of the pylorus in pancreaticoduo-denectomy[J]. Surg Gynecol Obstet, 1978, 146: 959. |
| [3] |
TRAVERSO L W, JR LONGMIRE W P. Preservation of the pylorus in pancreaticoduodenectomy a follow-upevaluation[J]. Ann Surg, 1980, 192(3): 306-310. |
| [4] |
TRAN K T, SMEENK H G, VAN EIJCK C H, et al. Pylorus preserving pancreaticoduodenectomy versus standard Whipple procedure: a prospective, randomized, multicenter analysis of 170 patients with pancreatic and periampullary tumors[J]. Ann Surg, 2004, 240(5): 738-745. |
| [5] |
DIENER M K, KNAEBEL H P, HEUKAUFER C, et al. A systematic review and meta-analysis of pylorus-preserving versus classical pancreaticoduodenectomy for surgical treatment of periampullary and pancreatic carcinoma[J]. Ann Surg, 2007, 245(2): 187-200. |
| [6] |
GAGNER M, POMP A. Laparoscopic pylorus-preserving pancreatoduodenectomy[J]. Surg Endosc, 1994, 8(5): 408-410. |
| [7] |
CHO A, YAMAMOTO H, NAGATA M, et al. Comparison of laparoscopy-assisted and open pylorus-preserving pancreaticoduodenectomy for periampullary disease[J]. Am J Surg, 2009, 198(3): 445-449. |
| [8] |
WELLNER U F, KVSTERS S, SICK O, et al. Hybrid laparoscopic versus open pylorus-preserving pancreatoduo-denectomy: retrospective matched case comparison in 80 patients[J]. Langenbecks Arch Surg, 2014, 399(7): 849-856. |
| [9] |
SONG K B, KIM S C, HWANG D W, et al. Matched case-control analysis comparing laparoscopic and open pylorus-preserving pancreaticoduodenectomy in patients with periampullary tumors[J]. Ann Surg, 2015, 262(1): 146-155. |
| [10] |
PANG L W, KONG J, WANG Y W, et al. Laparoscopic versus open pylorus-preserving pancreatoduodenectomy. The first meta-analyse of retrospective matched cases[J]. Acta Cir Bras, 2018, 33(1): 40-48. |
| [11] |
JIANG H P, LIN L L, JIANG X, et al. Meta-analysis of hand-sewn versus mechanical gastrojejunal anastomosis during laparoscopic Roux-en-Y gastric bypass for morbid obesity[J]. Int J Surg, 2016, 32: 150-157. |
| [12] |
CARRODEGUAS L, SZOMSTEIN S, ZUNDEL N, et al. Gastrojejunal anastomotic strictures following laparoscopic Roux-en-Y gastric bypass surgery: analysis of 1291 patients[J]. Surg Obes Relat Dis, 2006, 2(2): 92-97. |
| [13] |
VAN HILST J, ROOIJ T D, BOSSCHA K, et al. Laparoscopic versus open pancreatoduodenectomy for pancreatic or periampullary tumours (LEOPARD-2): a multicentre, patient-blinded, randomised controlled phase 2/3 trial[J]. Lancet Gastroenterol Hepatol, 2019, 4(3): 199-207. |
| [14] |
BASSI C, MARCHEGIANI G, DERVENIS C, et al. The 2016 update of the International Study Group (ISGPS) definition and grading of postoperative pancreatic fistula: 11 Years After[J]. Surgery, 2017, 161(3): 584-591. |
| [15] |
中华医学会外科学分会胰腺外科学组, 中国医疗保健国际交流促进会胰腺病分会胰腺微创治疗学组, 中国研究型医院学会胰腺疾病专业委员会胰腺微创学组, 等. 腹腔镜胰十二指肠切除手术专家共识[J]. 中华外科杂志, 2017, 55(5): 335-339. Study Group of Pancreatic Surgery in Chinese Society of Surgery of Chinese Medical Association, Pancreas Minimally Invasive Treatment Group in Pancreatic Disease Branch of China International Exchange and Promotion Association for Medical and Healthcare, Pancreas Minimally Invasive Group in Pancreatic Diseases Committee of Chinese Research Hospital Association, et al. Expert consensus of laparoscopic pancreaticoduodenectomy (posts cript of operation process and main steps)[J]. Chin J Surg, 2017, 55(5): 335-339. |
| [16] |
WANG M J, MENG L W, CAI Y Q, et al. Learning curve for laparoscopic pancreaticoduodenectomy: a CUSUM analysis[J]. J Gastrointest Surg, 2016, 20(5): 924-935. |
| [17] |
WENTE M N, VEIT J A, BASSI C, et al. Postpancreatectomy hemorrhage (PPH)—An International Study Group of Pancreatic Surgery (ISGPS) definition[J]. Surgery, 2007, 142(1): 20-25. |
| [18] |
CLAVIEN P A, BARKUN J, DE OLIVEIRA M L, et al. The Clavien-Dindo classification of surgical complications: five-year experience[J]. Ann Surg, 2009, 250(2): 187-196. |
| [19] |
KLINKENBIJL J H, VAN DER SCHELLING G P, HOP W C, et al. The advantages of pylorus-preserving pancreatoduo-denectomy in malignant disease of the pancreas and periampullary region[J]. Ann Surg, 1992, 216(2): 142-145. |
| [20] |
中国抗癌协会胰腺癌专业委员会微创诊治学组, 中华医学会外科学分会胰腺外科学组. 腹腔镜或机器人辅助胰腺癌根治术中国专家共识(2022年版)[J]. 中华外科杂志, 2023, 61(03): 187-195. Study Group of Minimally Invasive Treatment for Pancreatic Cancer in China Anti-Cancer Association, Chinese Pancreatic Surgery Association of Chinese Society of Surgery of Chinese Medical Association. Chinese expert consensus on minimally invasive radical surgery for pancreatic ductal adenocarcinoma (version 2022)[J]. Chin J Surg, 2023, 61(3): 187-195. |




