2. 400038 重庆,陆军军医大学(第三军医大学)创伤与化学中毒全国重点实验室
2. State Key Laboratory of Trauma and Chemical Poisoning, Army Medical University (Third Military Medical University), Chongqing, 400038, China
铜是人体必需微量金属元素之一,是各种伴侣蛋白和酶的重要辅助因子,广泛存在于各组织和器官中,参与酶促反应、伤口愈合和血管生成等各种基本生理过程,对维持人体(如骨骼系统、脑神经系统)的完整性和稳态至关重要[1]。大量研究表明,铜离子(Cu2+)在阿尔茨海默病、帕金森病、普粒子疾病等脑部疾病进程中也发挥着重要作用[2]。近年来由于其在临床医学和环境化学中的潜在应用,用于检测Cu2+的敏感性比色/荧光化学探针的开发受到了广泛的关注[3-7]。它们主要通过以下三种识别机制工作,包括电子转移、质子转移和能量转移,通常分别称为光诱导电子转移、激发态分子内质子转移和Förster共振能量转移。然而目前的探针检测大部分都要借助仪器且存在相关金属离子低灵敏度和高阶干扰等缺点[8-9]。因此,本研究基于氟硼二吡咯化合物(4, 4-difluoro-boradiazaindacene, BODIPY) 荧光染料构建制备了一种可用于肉眼检测水溶液中Cu2+的高选择性、高灵敏度的比色探针BBSCP(BODIPY based specific copper probe),在可见光区消光系数大,光稳定性好,具有较长的吸收和荧光光谱波长,为肉眼确定水溶液中Cu2+含量提供更加简便高效的检测技术。
1 材料与方法 1.1 主要试剂对二甲氨基苯甲醛、2, 4-二甲基吡咯、CH2Cl2、CF3COOH、甲苯、2, 3-二氯-5, 6-二氰基苯醌、三乙胺、三氟化硼乙醚,以上试剂均为分析纯,购于上海阿拉丁生化科技股份有限公司。AgNO3、CuCl2、HgCl2、Cd(NO3)2、NiCl2·6H2O、Pb(OAc)2·3H2O、Fe(NO3)3、ZnCl2,以上试剂均为化学纯,购于西格玛奥德里奇(上海)贸易有限公司。HEPES缓冲液(1 mol/L,Free Acid,无菌)购于上海源叶生物有限公司。
1.2 中间产物BMA的合成参照LI等[10]的方法,对二甲氨基苯甲醛755.6 mg (5 mmol)和2, 4-二甲基吡咯475.7 mg(5 mmol)溶解于干燥的CH2Cl2(50 mL)中,室温。用N2清洗溶液30 min。加入几滴CF3COOH以启动冷凝。2 h后,TLC(二氧化硅,CH2Cl2)显示醛已被全部消耗。反应混合物用饱和NaHCO3水溶液和水洗涤,用Na2SO4干燥、过滤,旋转蒸发仪旋转蒸发。产品溶于干燥的甲苯(50 mL)中,加入2, 3-二氯-5, 6-二氰基苯醌(DDQ, 1.0 g)。20 min后,加入三乙胺(6 mL),随后立即加入三氟化硼乙醚(BFE,6 mL)。室温搅拌3 h后,用水冲洗,Na2SO4烘干,过滤后旋转蒸发。粗产物经硅胶柱层析纯化,得到中间产物BMA。
1.3 比色探针BBSCP的合成93 mg BMA和115 mg N, N-二甲基吡啶苯甲醛(DMPB)被溶解在10 mL干燥的甲苯中。然后在混合物中加入干燥的哌啶(0.1 mL)。反应混合物用适量分子筛加热回流36 h。溶剂蒸发后,以丙酮/二氯甲烷(5 ∶1体积分数)为洗脱液,硅胶柱层析纯化混合物,得到10 mg(收率6%)的深紫色粉末即为化合物BBSCP。
1.4 材料表征鉴定中间产物以及最终比色探针材料的相关表征采用核磁与质谱联合鉴定,使用核磁共振光谱仪(600 MHz,DD2,Agilent)获得1H NMR与13C NMR光谱,利用高分辨质谱仪(LTQ Orbitrap Velos Pro,Thermo Scientific)得到材料质谱图谱。
中间产物BMA:1H NMR(CDCl3, 300 MHz) 1.49(s, 6H), 2.55(s, 6H), 3.02(s, 6H) 5.97(s, 2H), 6.78(d, 2H, J=9 Hz), 7.06(d, 2H, J=9 Hz); 13C NMR (CDCl3, 75 MHz) 14.5, 14.7, 40.3, 112.2, 120.7, 121.9, 128.6, 143.2, 150.5, 154.6。
1.5 BBSCP的化学比色效率检测将8种待测金属离子[AgNO3、CuCl2、HgCl2、Cd(NO3)2、NiCl2·6H2O、Fe(NO3)3、Pb(OAc)2·3H2O、ZnCl2]分别溶解于2 mL混合溶剂中(乙醇∶水=1 ∶6,利用HEPES和NaOH调节其pH值为7.0),终浓度均为10 μmol/L。向以上各溶剂中加入1 mL BBSCP溶液(5 μmol/L)后通过紫外-可见分光光度计(TU-1901,北京普析)测定紫外吸收扫描光谱,扫描波长范围450~750 nm。
探针BBSCP的检测限(limits of detection, LOD)采用滴定法进行计算。测量探针BBSCP(5 μmol/L)的紫外吸收光谱强度20次,得到空白测量的标准偏差,而后通过以下方程计算得到LOD。
LOD =3σ/k
其中,σ是空白测量的标准偏差,k是Cu2+探针滴定时吸光度A560/A612比率和浓度之间的线性斜率[11]。
1.6 Cu2+浓度对BBSCP的化学比色效率的影响配制5 μmol/L BBSCP溶液(溶剂为乙醇∶水=1 ∶6的混合溶剂,pH值调节至7.0),分别滴加不同浓度的Cu2+,终浓度分别为0、1、2、3、4、5、6、7、8、9、10 μmol/L,利用紫外-可见分光光度计测定其在450~750 nm波长范围内的吸收光谱。
1.7 常见金属离子对探针BBSCP检测的干扰配制5 μmol/L BBSCP溶液(溶剂为乙醇∶水=1 ∶6的混合溶剂,pH值调节至7.0),加入10 μmol/L Cu2+后测定其在450~750 nm波长范围内的吸收光谱,而后再分别加入不同的金属离子[AgNO3、CuCl2、HgCl2、Cd(NO3)2、NiCl2·6H2O、Fe(NO3)3、Pb(OAc)2·3H2O、ZnCl2],终浓度均为10 μmol/L,再次扫描检测吸收光谱。
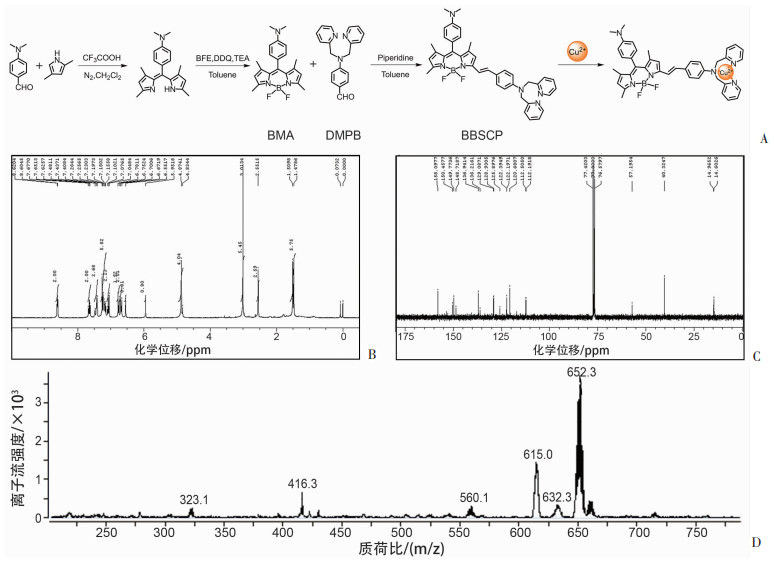
2 结果 2.1 特异性Cu2+探针BBSCP的结构表征根据合成路线(图 1A)成功合成了铜离子响应比色探针BBSCP,并采用1H NMR、13C NMR和HRMS对该探针的化学结构进行了确证,结果见图 1B~D。具体数据如下: 1H NMR (CDCl3, 300 MHz) 1.48 (s, 3H), 1.50 (s, 3H), 2.55 (s, 3H), 3.01 (s, 6H) 4.87 (s, 4H) 5.95 (s, 1H), 6.55 (s, 1H), 6.68 (d, 2H, J=9 Hz), 6.76 (d, 2H, J=9 Hz), 7.05 (d, 2H, J=9 Hz), 7.15-7.25 (m, 5H), 7.42 (d, 3H, J=9 Hz), 7.65 (t, 2H, J=6 Hz), 8.61 (d, 2H, J=6 Hz); 13C NMR (CDCl3, 75 MHz) 14.6, 15.0, 40.3, 57.1, 112.2, 112.5, 120.7, 122.2, 122.4, 125.9, 128.9, 129.1, 136.9, 148.7, 149.8, 150.5, 158.1。高分辨质谱数据计算值为C40H39BF2N6: 652.329 7 (m+), 测试值为652.330 4(正离子模式)。以上核磁氢谱、碳谱数据以及高分辨质谱数据均确证了该探针的化学结构。
|
| A:比色探针的合成及Cu2+检测;B:比色探针的1H NMR表征;C:比色探针的13C NMR表征;D:比色探针的HRMS表征 图 1 比色探针BBSCP的合成及表征 |
2.2 探针BBSCP对Cu2+的选择特异性
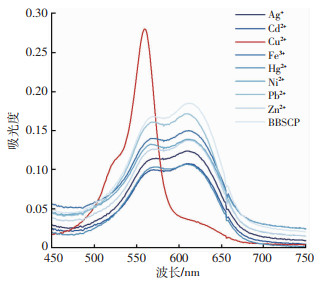
使用HEPES和NaOH调节水溶液的pH值为7.0,用紫外-可见光谱法检测BBSCP在EtOH ∶H2O=1 ∶6 (2 mL)中的阳离子结合性能。如图 2所示,BBSCP在485~670 nm范围内表现出较宽的吸收带。加入Cu2+后,在465~600 nm区间出现蓝移,波段变尖。而其他金属离子没有引起变化。在微摩尔水平Cu2+的存在下,5 μmol/L的溶液可以显示明显的紫色,而常见的其他重金属离子几乎没有干扰(图 3)。这些结果表明,BBSCP可以作为中性缓冲水溶液中Cu2+的“裸眼”特异性显色探针。
|
| 图 2 比色探针BBSCP在乙醇∶水=1 ∶6(2 mL),pH=7.0 (HEPES)溶液中不同金属离子存在下的紫外光谱图 |

|
| 图 3 BBSCP溶液(5 μmol/L)与不同金属离子的颜色变化 |
2.3 Cu2+比色探针的浓度线性关系
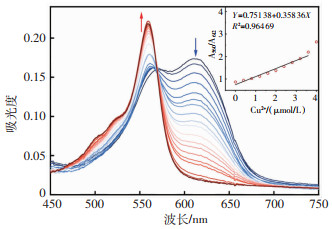
此外,通过紫外-可见滴定法研究了BBSCP对Cu2+的结合能力。在BBSCP溶液中加入越来越多的Cu2+(0~10 μmol/L),在612 nm处的吸收峰减少,而在560 nm处出现蓝移峰(图 4)。在BBSCP溶液中加入Cu2+后,在560 nm处形成新的吸收带。这是由于加入Cu2+后,二吡啶胺上的电子密度发生了变化。因此,与Cu2+配位后,BBSCP的紫外-可见光谱表现出比值行为,使用计算公式3σ/K(图 4内嵌图)得到Cu2+比色探针的LOD为0.19 μmol/L。
|
| 蓝色到红色表示溶液中Cu2+浓度从0逐渐增加至10 μmol/L 图 4 BBSCP (5 μmol/L)溶液加入不同浓度Cu2+的紫外光谱图 |
2.4 Cu2+比色探针的抗干扰能力评价
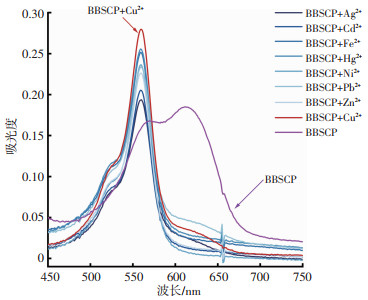
为了评价BBSCP对铜离子的选择性,进行了竞争性实验。图 5显示5 μmol/L的BBSCP溶液对各种重金属离子存在下吸收光谱行为的变化。结果表明混合金属离子存在时,吸光度差异不大。说明BBSCP在其他重金属离子存在的情况下对Cu2+仍然具有良好的选择性。
|
| 图 5 常见金属离子对BBSCP(5 μmol/L)的Cu2+探测效率的影响 |
3 讨论
铜是生物系统中必需的微量元素,广泛分布于生物组织中,在肝脏中浓度最高。大多存在于有机化合物中,其中很多是金属蛋白。在氧化还原化学中起催化辅助因子的作用,参与调节各种酶的活性,例如细胞色素C氧化酶、抗氧化剂SOD等。因此,铜缺乏可导致生物系统功能障碍,导致人类疾病,如心血管疾病、贫血、骨质疏松症等。然而,铜离子浓度过高时同样能造成铜稳态紊乱,过载的铜离子通过诱导调节性细胞死亡(如凋亡、类凋亡、焦亡、铁死亡和铜死亡)表现出更高的毒性。自由铜离子参与Fenton反应,产生有害的自由基,如活性氧(reactive oxygen species, ROS),其确切性质仍在研究中。这些自由基的产生与许多疾病有关,被认为是铜超载疾病细胞损伤的主要来源[12]。
由于工业技术的发展,日益严重的铜污染给水生生物、土壤、农作物乃至人体带来了极大的危害[13]。因此,建立和发展环境样品和人体中Cu2+的定性定量检测新方法具有重要意义。
目前,利用有机比色/荧光化学探针进行新型检测技术的研究已成为热点。与新兴纳米材料相比,有机探针具有生物相容性好、结构可改性强、毒性相对较低等优点。与传统的高效液相色谱法、表面等离子体共振、电感耦合等离子体质谱法、气相色谱法和原子吸收光谱法相比,该探针具有制备简单、灵敏度高、成本低等优点[14-16]。虽然上述传统方法在有效性和精密度方面各有优势,但需要复杂的样品预处理以及昂贵的设备和训练有素的操作人员。
总之,本文设计并合成了一种基于分子内电荷转移(intramolecular charge transfer, ICT)的新型铜离子探针BBSCP,以荧光染料BODIPY为主体结构,具有较大的斯托克斯位移、较高的光稳定性和对Cu2+良好的可逆传感能力。BODIPY连接的配体中的氮与Cu2+具有很强的亲和力,铜离子与配体络合后将电荷转移到另一端的吸电子基团,导致其吸收光谱发生蓝移(图 1A)。通过在其α-位上修饰了4-氨基苯乙烯基,促进了ICT效应。在许多过渡金属离子中,只有Cu2+引起了从612 nm到560 nm的吸收光谱蓝移,颜色由蓝色变为紫色。在EtOH /H2O(1 ∶6体积分数,pH=7.0)中随着加入Cu2+的浓度不断增加至2倍当量,612 nm波长处的吸光度从0.174不断降至0.015。通过计算,本研究制备的Cu2+比色探针的检测限为0.19 μmol/L,这大约是世界卫生组织饮用水中指南(31.5 μmol/L)的160倍[17]。此外,考察了其他常见金属离子对BBSCP比色探针的干扰效应,证实了探针对Cu2+的高度敏感性和选择稳定性,显示了其在生物诊断、食品、环境等多领域的应用前景。
| [1] |
LIU Y M, ZHU J L, XU L L, et al. Copper regulation of immune response and potential implications for treating orthopedic disorders[J]. Front Mol Biosci, 2022, 9: 1065265. |
| [2] |
VERWILST P, SUNWOO K, KIM J S. The role of copper ions in pathophysiology and fluorescent sensors for the detection thereof[J]. Chem Commun, 2015, 51(26): 5556-5571. |
| [3] |
ALI M, MEMON N, MALLAH M A, et al. Recent development in fluorescent probes for copper ion detection[J]. Curr Top Med Chem, 2022, 22(10): 835-854. |
| [4] |
SHARMA S, GHOSH K S. Recent advances (2017-20) in the detection of copper ion by using fluorescence sensors working through transfer of photo-induced electron (PET), excited-state intramolecular proton (ESIPT) and Förster resonance energy (FRET)[J]. Spectrochimica Acta A Mol Biomol Spectrosc, 2021, 254: 119610. |
| [5] |
TANG Y, LI Y Y, HAN J, et al. A coumarin based fluorescent probe for rapidly distinguishing of hypochlorite and copper (Ⅱ) ion in organisms[J]. Spectrochim Acta A Mol Biomol Spectrosc, 2019, 208: 299-308. |
| [6] |
YIN J, WANG Z L, ZHAO F, et al. A novel dual functional pyrene-based turn-on fluorescent probe for hypochlorite and copper (Ⅱ) ion detection and bioimaging applications[J]. Spectrochim Acta A Mol Biomol Spectrosc, 2020, 239: 118470. |
| [7] |
MENG Z Y, ZHAO F, WANG Z L, et al. An efficient tetrahydroquinazolin-2-amine derivative-grafted cellulose fluorescent probe for detection of Cu2+ and Zn2[J]. Carbohydr Polym, 2023, 303: 120445. |
| [8] |
SUN H, XU Q Y, XU C, et al. Construction of a water-soluble fluorescent probe for copper (Ⅱ) ion detection in live cells and food products[J]. Food Chem, 2023, 418: 135994. |
| [9] |
KIRAN S, KHATIK R, SCHIRHAGL R. Smart probe for simultaneous detection of copper ion, pyrophosphate, and alkaline phosphatase in vitro and in clinical samples[J]. Anal Bioanal Chem, 2019, 411(24): 6475-6485. |
| [10] |
LI M L, WANG H, ZHANG X, et al. Development of a new fluorescent probe: 1, 3, 5, 7-tetramethyl-8-(4'-aminophenyl)-4, 4-difluoro-4-bora-3a, 4a-diaza-s-indacence for the determination of trace nitrite[J]. Spectrochim Acta A Mol Biomol Spectrosc, 2004, 60(4): 987-993. |
| [11] |
LONG G L, WINEFORDNER J D. Limit of detection. A closer look at the IUPAC definition[J]. Anal Chem, 1983, 55(7): 712A-724A. |
| [12] |
XUE Q, KANG R, KLIONSKY D J, et al. Copper metabolism in cell death and autophagy[J]. Autophagy, 2023, 19(8): 2175-2195. |
| [13] |
AHMED N, ZAREEN W, YANG X P, et al. Development in fluorescent OFF-ON probes based on Cu2+ promoted hydrolysis reaction of the picolinate moiety[J]. J Fluoresc, 2023, 33(2): 401-411. |
| [14] |
DUAN N, YANG S X, TIAN H Y, et al. The recent advance of organic fluorescent probe rapid detection for common substances in beverages[J]. Food Chem, 2021, 358: 129839. |
| [15] |
PELIN J N B D, EDWARDS-GAYLE C J C, MARTINHO H, et al. Self-assembled gold nanoparticles and amphiphile peptides: a colorimetric probe for copper(Ⅱ) ion detection[J]. Dalton Trans, 2020, 49(45): 16226-16237. |
| [16] |
YIN C X, LI J W, HUO F J. Cu2+ biological imaging probes based on different sensing mechanisms[J]. Curr Med Chem, 2019, 26(21): 3958-4002. |
| [17] |
TONG S M, YANG L S, GONG H Q, et al. Association of selenium, arsenic, and other trace elements in drinking water and urine in residents of the plateau region in China[J]. Environ Sci Pollut Res Int, 2022, 29(18): 26498-26512. |




