随着新型冠状病毒(severe acute respiratory syndrome coronavirus 2, SARS-CoV-2)毒株的不断变异,2022年以来,奥密克戎(Omicron)变异株已取代德尔塔(Delta)变异株,成为全球主要流行株;重庆市本土疫情呈现出传播性强、扩散面广的特点。在临床工作中,胸部放射学检查是新型冠状病毒肺部感染(新冠肺部感染)诊断的重要手段之一,对病变性质、严重程度及疗效评估具有重要意义。为适应川渝两地检查结果互认的政策需求以及重庆市医学影像医疗质量控制中心对胸部影像检查提出的新规范,重庆市医学会放射医学分会胸心学组联合重庆市医学影像医疗质量控制中心编写了本专家共识。本共识在《新型冠状病毒感染诊疗方案(试行第十版)》基础上,增加了重庆市各级医院收治的新冠肺部感染患者影像学表现及尸检病理表现,内容包括新冠肺部感染病原学及临床特点、肺部病理学表现、放射学检查、放射学表现、报告规范、质量控制共6个部分,并推荐“新型冠状病毒肺部感染CT结构化报告模板”。希望能为重庆地区医疗机构在新冠病毒肺部感染的认识、检查与随访上提供相应的指导。
1 新冠肺部感染病原学及临床特点新型冠状病毒简称新冠病毒,属于RNA病毒,其复制酶因缺少校正功能,在复制及传播过程中容易发生重组及变异,甚至诱发突变株或新毒株出现。继阿尔法(Alpha, B.1.1.7株)、贝塔(Beta, B.1.351株)、伽玛(Gamma,P.1株)及Delta(B.1.617.2株) 变异株之后,奥密克戎变异株成为第5个关切变异株[1-2]。研究[3-5]表明,与Beta变异株和Delta变异株相比,奥密克戎变异株可能是B.1.1.519 (20B) 谱系的后代,更容易逃避既往感染产生的免疫力,且突破性感染比例明显比前两者高。目前在我国流行的奥密克戎毒株主要是BA.5.2和BF.7[6]。近期欧美流行的XBB.1和BQ.1变异毒株或将传入我国。
新冠肺部感染者潜伏期(2~4 d)即有传染性,发病后3 d内传染性最强。人群普遍易感,疫苗接种后可明显降低重症及死亡风险。国内外多项研究显示,奥密克戎对肺组织的感染能力减弱,临床表现已衍变为以上呼吸道感染为主[7],主要表现为肌肉酸痛、发热、乏力、头晕头痛、咽干咽痛等,重症患者多在发病5~7 d后出现呼吸困难和(或)低氧血症,极少数患者还可有中枢神经系统受累等表现,儿童感染后其临床表现与成人相似,极少数患儿可出现危及生命的神经系统并发症或儿童多系统炎症综合征(multisystem inflammatory syndrome in children,MIS-C)。在最新发布的第十版新冠肺部感染诊疗方案中,除了提出新冠病毒核酸检测阳性为确诊的首要标准外,增加了病毒抗原检测阳性支持感染新冠的诊断,但抗原阴性不能排除新冠肺部感染。
第十版新冠肺部感染诊疗方案提到影像学的相关内容较少,而最近研究[8-11]表明,影像学检查在病变检出、严重程度及疗效评估、复杂病例的诊断和鉴别诊断中起着不可或缺的作用。
2 新冠肺部感染病理学表现新冠肺部感染主要表现为弥漫性肺泡损伤。早期和症状较轻患者病变区见肺泡隔毛细血管充血,肺泡腔内见浆液、纤维蛋白渗出,透明膜形成。随着病变进展和加重,出现肺泡Ⅱ型上皮细胞坏死、脱落、肺泡腔内大量单核细胞/巨噬细胞和纤维蛋白渗出,部分区域可见增生的上皮细胞融合形成多核巨细胞,偶见细胞内病毒包涵体。肺内各级支气管部分黏膜上皮脱落,腔内可见渗出物和黏液;小支气管和细支气管易见黏液栓形成。肺组织易见灶性出血、坏死,伴有血管炎、血栓形成(混合血栓、透明血栓)及血栓栓塞;部分患者可见细菌和(或)真菌(曲霉菌为主);病程较长的患者,可见肺泡腔内渗出物肉质变和肺间质纤维化[12-13]。
3 新冠肺部感染放射学检查 3.1 检查方法选择新冠肺部感染初期多无影像学异常发现,且数字化X线摄影(digital radiography,DR)检查由于密度分辨率低、前后重叠等因素导致漏诊率高,故不推荐作为疑似病例的首选方法[14]。但对于重型、危重型患者(特别是气管插管机械通气者),床旁DR可作为评估肺部病变进展情况的复查手段[15]。胸部计算机体层成像(CT)为横断面影像,无重叠,推荐作为筛查与诊断的首选方法[16]。儿童如果下呼吸道感染症状明显或持续,或者肺部有异常体征,需考虑行胸部DR或CT检查[17]。
3.2 检查技术规范 3.2.1 DR检查床旁DR推荐参数:管电压50~85 kVp,管电流0.6~2.0 mAs,焦片距90~100 cm。可选参数:自动曝光控制AEC技术。
3.2.2 胸部CT检查① 推荐参数:螺旋容积采集,管电压120 kVp或自动管电压,管电流100~250 mAs,螺距1.0~1.8,转速0.3~0.5 s/rot。儿童建议低剂量扫描方案:管电压80~100 kVp或自动管电压,管电流80~120 mAs,准直器宽度2~5 mm,螺距0.5~1.0,转速0.27~0.8 s/rot。②增强扫描参数同平扫,成人按碘总量的用量为0.30~0.35 g/kg,注射速率3.0~4.0 mL/s。30~35 s扫描动脉期、50~70 s扫描静脉期。③可选参数:自动管电流调制技术,层厚0.5~1.5 mm,层间距0.5~1.5 mm,迭代重建技术。标准算法及高分辨率算法重建后上传至图像归档和传输系统(picture archiving and communication system,PACS)[18]。
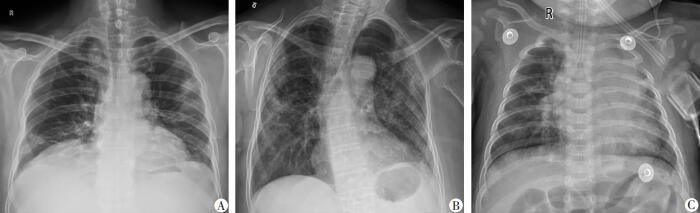
4 新冠肺部感染放射学表现 4.1 DR表现病变早期DR多无异常发现[19],进展后DR常表现为双肺中外带和胸膜下局限性斑片状或多发节段性片状影(图 1A)。重症患者可表现为双肺多发实变,部分可融合成片(图 1B),可伴少量胸腔积液[14]。儿童DR可出现局限性斑片状影,重症与成人类似,可出现双肺多发实变影(图 1C)[17]。
|
| A:68岁男性患者(咳嗽、咳痰10 d,无发热)DR示双肺外带多发斑片影;B:78岁女性患者(咳嗽、咳痰10+ d,无发热)DR示双肺弥漫片絮状影;C:4个月男性患儿(咳嗽2 d,发热1 d)DR示双肺病变,以左肺实变为主 图 1 新冠肺部感染患者胸部DR征象 |
4.2 胸部CT表现
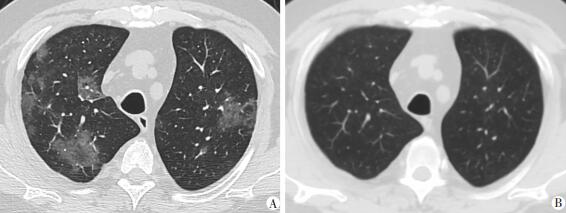
新冠肺部感染患者CT表现主要为两肺多发结节状、斑片状及片状磨玻璃影(ground-glass opacity, GGO)和实变,以中外带和胸膜下多见(图 2A),其内可见小叶间隔增厚形成的网格状影[14](图 3A)。病变可沿支气管血管束分布,相应支气管血管束略增粗[20](图 3B)。少数合并少量胸腔积液和纵隔内淋巴结增大。
|
| A: 双肺多发斑片状GGO, 边界模糊; B: 治疗后第10天双肺GGO明显吸收 图 2 37岁男性新冠肺部感染患者(发热、咳嗽4d)胸部CT表现 |
|
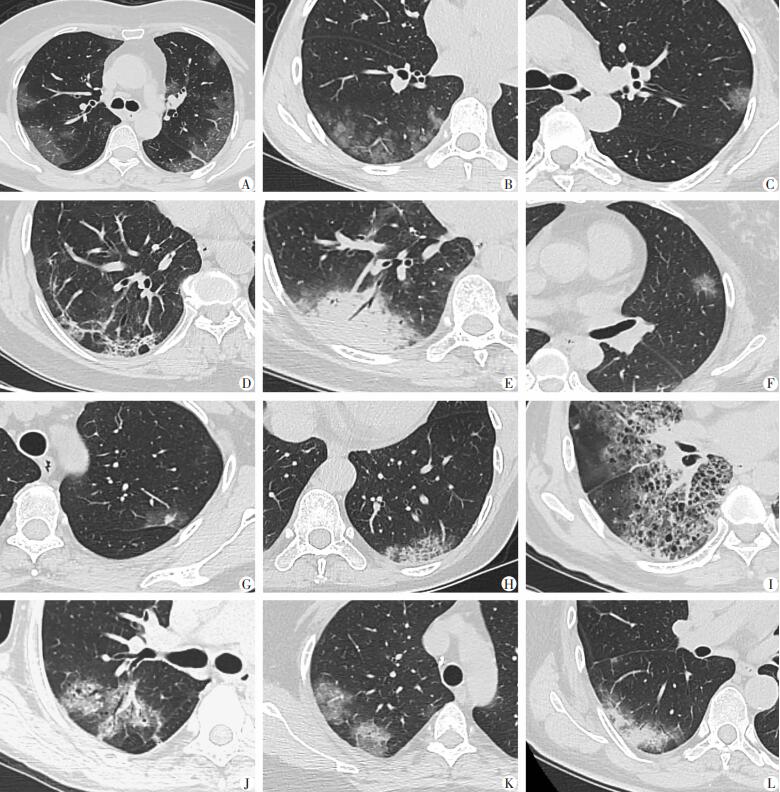
| A: 双肺外带多发GGO, 内见网格影; B: 右肺下叶背段GGO内支气管血管束增粗; C: 左肺上叶尖后段胸膜下小片GGO; D: 右肺下叶后基底段胸膜下纤维条索影; E: 右肺下叶背段实变伴充气支气管征; F: 左肺上叶下舌段浅淡GGO伴支气管血管束增粗; G: 左肺上叶尖后段小片实变伴晕征; H: 左肺下叶后基底段细网格影; I: 右肺中下叶大片GGO伴蜂窝影; J: 右肺上叶后段实变伴充气支气管征及支气管壁稍增厚; K: 右肺上叶后段GGO内见增粗血管影; L: 右肺下叶背段实变伴邻近胸膜局限性增厚 图 3 新冠肺部感染患者的胸部CT征象 |
对重庆市6家三级甲等医院2022年12月检测的2 280例新冠肺部感染患者的影像资料进行分析,包括基本信息、病灶分布、影像征象等。65岁以上感染者有1 452例,占63.7%;男性1 367例(60.0%),多于女性(913例)。①病灶分布:88.0%为双肺多发,右肺略多于左肺,分别占比55.8%和44.2%,以中下肺野受累多见(1 973例,86.5%)。主要分布在外带近胸膜下(2 014例,92.3%)。②病灶类型:以斑片状GGO为主(1 943例,85.2%),表现为胸膜下扇形或楔形GGO(图 3C),可能与病毒微小颗粒累及肺表层小叶的肺泡上皮导致免疫细胞大量聚集有关[21];其次是纤维条索影(1 024例,44.9%;图 3D),与病变吸收或转化为高密度实变伴纤维化有关[22];然后是实变(865例,38.0%;图 3E)与浅淡GGO(774例,34.0%;图 3F)。③其他征象:结节717例,其中伴发晕征415例(图 3G);687例患者可见细网格影(图 3H),其中303例可见“铺路石”征和/或蜂窝影(图 3I);斑片影及实变中可见充气支气管征,297例可见支气管壁增厚,表现为不规则节段性环壁增厚(图 3J);单发病变几乎均为GGO,其内可见增粗血管影(图 3K);188例患者可见胸膜增厚,以邻近病灶的胸膜局限性增厚为主(图 3L),且多见于病程的中晚期;81例患者出现胸腔积液,主要见于合并基础疾病患者,以少量积液为主;支气管扩张(67例),主要见于病程中后期或存在肺部基础疾病患者;43例患者可见纵隔内淋巴结增大。
本组患者中,81例完成3次及以上胸部CT检查,第1次检查一般在临床症状后3~6(4.6±3.4)d,表现为结节、斑片状及浅淡GGO,边界不清,大多在1~2周完全吸收(图 2B)。如果病情进展,自病灶中心出现实变并向周围浸润,病灶密度逐渐增高,一般在第7~9(8.7±4.7)天实变达到峰值。病变转归表现为病灶周围的GGO吸收减少,实变区边界逐渐清晰,病情进展表现为新发GGO或病变范围增大,常表现为多种类型病变共存,该类患者一般表现为临床症状加重或缓解不明显。随着病灶吸收,实变出现向中心收缩的趋势,病灶自外向内逐渐消散、缩小,而中心密度进一步增高,呈条索状改变。因随访时间的限制,多数患者目前肺内仍可见纤维条索存留,有待进一步随访,有报道奥密克戎变异株肺炎的吸收时间为14 d至3个月[23]。
儿童患者胸部CT病变与成人类似,以中外带、胸膜下GGO为主,段或节段性斑片影也比较常见,部分病变可融合成实变,伴或不伴小叶间隔增厚。与成人相比,儿童患者病变分布更局限,弥漫性肺部病变较少,GGO的表现也不如成人典型[24],病变特征不明显,需要结合临床病史和核酸检测结果进行判断。
4.3 胸部CT分期新冠肺部感染患者肺部病变的CT表现具有一定的特征性,在病程中的变化也具有一定规律性,了解其演变规律有助于确定疾病所处阶段、评估病情及与其他潜在并发症进行鉴别。需要注意的是,临床分型与胸部CT的分期和病灶范围没有明确的对应关系。根据新型冠状病毒感染诊疗方案(试行第十版)[3]:临床轻型,以上呼吸道感染为主要临床表现;发现新冠肺部感染特征性的CT征象可以作为诊断临床中型的依据之一;胸部CT显示24~48 h内病灶明显进展>50%,且临床症状进行性加重,则支持临床重型的诊断;危重型以出现脏器衰竭、休克为诊断依据,而影像学有助于临床了解肺内炎症程度,可以根据临床需要采用床旁DR了解病灶变化[14]。另外,胸部CT显示肺部病变明显进展,是成人及儿童重型/危重型早期预警指标之一。
根据病变的CT表现特征大致将其演变过程分为4个阶段:早期、进展期、高峰期和吸收期[14, 25-27],患者入院时可能处于病程中的任何一个阶段。
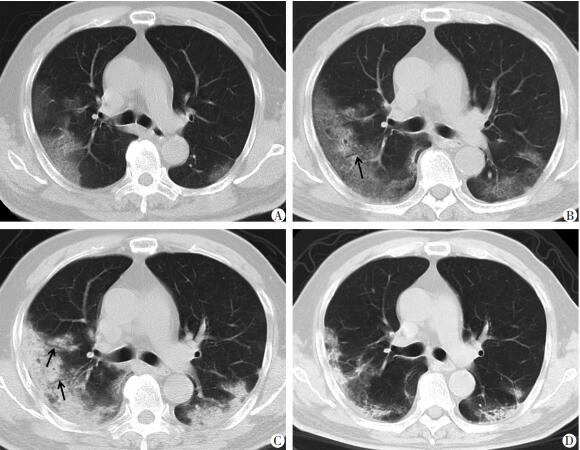
早期(症状出现后0~4 d):单发或散在多发小斑片状或团状GGO、结节影,以中下叶胸膜下分布为主,长轴与胸膜平行,或者沿支气管血管束分布,多数边界不清,部分病灶内可见细支气管充气征、细网格影或“铺路石”征,少数表现为局限性实变伴充气支气管征(图 4A)。部分奥密克戎无症状感染者或轻症患者在病程早期阶段胸部CT表现为阴性,但在短期复查时部分患者可出现肺炎表现[28]。
|
| A: 症状出现后4 d(早期)胸部CT示双肺多发小斑片状GGO及结节影, 以胸膜下分布为主, 长轴与胸膜平行, 边界不清, 部分病灶内可见细网格影或"铺路石"征; B: 症状出现后8 d(进展期), 复查胸部CT示双肺病灶相互融合, 范围扩大, 其内小叶间隔及小叶内间质增厚更明显, 部分病灶内出现局灶性实变, 其内可见充气支气管征(箭头示); C: 症状出现后13 d(高峰期), 复查胸部CT示双肺病变密度进一步增高, 可见多发实变, 部分病灶内可见充气支气管征(箭头示), 实变周围可见少量GGO环绕; D: 症状出现后20 d(吸收期), 复查胸部CT示双肺实变及GGO的密度降低、范围明显缩小, 病变区可见实质条带影, 局部肺结构扭曲 图 4 73岁男性新冠肺部感染患者(4 d前出现发热、乏力)不同病程胸部CT表现 |
进展期(症状出现后5~8 d):以GGO为主的病灶相互融合,范围进一步扩大,累及更多的肺叶,总体分布由外周向中央推进,病灶内小叶间隔及小叶内间质增厚更明显。病灶密度较前显著增高,GGO内出现的大小、程度不等实变,形成“晕征”或“反晕征”,实变内可见充气支气管征(图 4B)。大部分奥密克戎变异株感染的肺炎进展期CT表现仍相对局限,比早期病灶稍增多,少部分与基线CT对比有较大变化[28]。
高峰期(症状出现后9~13 d):肺部病变密度进一步增高,表现为多发实变,周边见少量GGO环绕,双肺大部分受累时呈“白肺”表现,“铺路石”征及GGO的比例显著降低(图 4C)。双侧胸膜增厚常见,并可见少量胸腔积液,呈游离性或包裹性。奥密克戎变异株感染肺炎在高峰期实变的范围较Beta变异株及Delta变异株感染者小[28]。
吸收期(症状出现后14 d及以上):肺部病灶逐渐吸收及机化,表现为实变及GGO的密度逐渐降低、范围逐渐缩小,病变区可见实质条带影、胸膜下线、肺结构扭曲及牵拉性支扩等纤维化样改变(图 4D)。不同个体之间肺部病灶吸收速度存在较大差异,奥密克戎变异株感染肺炎中型患者的GGO可完全吸收。
4.4 随访周期患者入院时可能处于病程中的某个时间段,临床分型、不同的年龄段及有无基础疾病等都会影响病灶的吸收[29-30],可以在不同的病程时间段进行胸部CT检查。但是CT复查的时间窗目前尚无确切依据,根据对已有患者的观察并结合中华医学会放射学分会专家推荐意见(第1版)[14],本共识建议:①患者在诊疗过程中无不适,可不进行CT检查,若出现临床症状或临床症状加重,需随时进行CT检查。②轻型患者,若临床症状持续好转,可不复查CT;若临床症状持续加重,建议CT复查。③中型患者,若临床症状持续好转,出院时复查CT,观察病变吸收情况;若临床症状持续加重,建议CT复查。④重症患者,推荐5~7 d复查胸部CT,观察病变的演变。若病情稳定或临床症状趋于缓解后可适当延长复查时间。⑤危重症患者,可以采用床旁DR摄片观察病情变化,检查次数则根据临床需要进行,整个住院过程中最少检查3次,出院前应复查一次CT[31]。⑥出院患者的随访:部分患者出院时仍有肺部异常改变,非危重型患者出院后随访时间可以在3~6个月内,而危重型患者的随访时间可以长达2年[14, 32-34]。
总之,患者具体的随访时间还应参考患者的年龄、有无基础疾病、临床症状等具体情况进行适当的增减,同时还要注意辐射累积剂量。
4.5 鉴别诊断主要与其他病毒性肺炎、细菌性肺炎、肺部支原体、衣原体感染、肺部非感染性病变等进行鉴别[35]。
4.5.1 与其他病毒性肺炎鉴别流感病毒肺炎CT表现为沿支气管血管束分布的实变,双肺弥漫性GGO与小叶间隔增厚[36-37],其分布特点不同于新冠肺部感染的肺炎,且胸腔积液与支气管扩张更常见。腺病毒肺炎易发生于婴幼儿或免疫功能障碍的人群[38],为双肺多灶性GGO,也可见斑片状实变及大支气管壁增厚[39]。儿童腺病毒肺炎以2岁以下儿童多见,CT特点以向心性的大片实变为主要表现,累及胸膜下少见。儿童甲型流感肺炎临床表现与新冠肺部感染的肺炎类似,以发热、咳嗽为主,CT难以鉴别,需要结合核酸检测结果进行判断。
4.5.2 与细菌性肺炎鉴别细菌感染白细胞数增高,CT多表现为叶、段或亚段的渗出或实变,或沿支气管血管束及中内带分布为主的斑片影。
4.5.3 与支原体、衣原体肺炎鉴别支原体肺炎好发于学龄期儿童,早期肺部体征不明显[40],CT表现以沿支气管分布的模糊小结节、融合的斑片影为主要特征,双肺中内带多见,可合并支气管壁增厚、黏液栓[41-42],可伴发少量胸腔积液和肺门淋巴结肿大[43]。衣原体肺炎常有鸟类或家禽接触史,表现为不同程度的渗出和实变,多为单侧单叶实变,范围与病情严重程度密切相关[44],可伴有淋巴结肿大和胸腔积液。
4.5.4 与肺部非感染性病变鉴别① 过敏性肺炎:是由于吸入各种抗原而引起的变应性肺疾病,表现为弥漫分布的GGO,小叶中心结节,马赛克征、细网格影、纤维条索影及蜂窝影,小叶中心结节和马赛克征是其特点,“铺路石”征及实变少见[45]。②肺泡蛋白沉积症:慢性或亚急性起病,男性多见。病理为肺泡和细支气管腔内积聚过量的过碘酸-希夫染色阳性的类脂蛋白物质。CT典型表现为“铺路石”征,即地图样分布的片状GGO伴网格影[46]。③机化性肺炎:多见于中下肺胸膜下和/或支气管血管束周围的片状实变,可伴有周围GGO,病灶可游走。部分病灶可见中央GGO、边缘环形或新月形实变,即反晕征[47]。
4.6 新技术展望胸部CT检查在新冠肺部感染的肺炎检出方面具有较高的敏感性,但诊断的特异性较低,对其他病原体造成的感染可能造成误诊[48]。人工智能(artificial intelligence,AI)技术可以识别肺部病变并对其进行分类,目前基于机器学习、迁移学习和深度学习的模型在鉴别新冠肺部感染的肺炎与其他肺炎方面具有较高的准确性[49-51],AI技术在医学影像中的应用已日趋成熟,在量化病变方面具有较好的一致性,可以对CT肺炎病灶体积比进行动态精确测量,有助于评价疾病的严重程度和预判疾病的发展趋势[52],有条件的单位可以采用AI辅助评估病灶范围,为临床提供更加客观准确的信息。同时,AI技术还可实现肺炎患者康复时间预测及危险因素分析,为早期诊断和治疗提供线索[53]。尽管AI技术在肺炎诊断和评估中的应用具有广阔前景,但在实际临床工作中还需更多的推广才能全面落地。
5 胸部CT报告规范 5.1 描述规范 5.1.1 阅片与描述顺序按照肺实质、气管与支气管、肺门与纵隔、心脏大血管、胸腔、胸壁、胸外发现的顺序。
5.1.2 病灶描述需要详细描述病灶的范围、分布、类型等要素。①范围:局限性/弥漫性,须定位至肺段。②分布:胸膜下/支气管血管束周围/随机散在。③类型:GGO/实变/网状或索条。④伴随征象:包括有无小叶间隔增厚、“铺路石”征、充气支气管征、血管增粗、肺间质改变、纵隔淋巴结增大、胸腔积液及心包积液等。⑤其他胸部及胸外病变。
5.1.3 AI应用推荐有条件的单位使用AI定量分析肺部病灶,精确判断病变范围和演变情况。
5.2 诊断结论规范放射学诊断结论应包括以下3个层次的内容:①对新冠肺部感染的可能性诊断。包括区分感染性病变与非感染性病变,感染性病变区分病毒性肺炎与非病毒性肺炎,倾向病毒性肺炎时将放射学诊断分为3级,可能性大(诊断信心>80%)、可能(50%≤诊断信心≤80%)、待排(诊断信心<50%)[28];或者参考荷兰放射学协会(the Dutch Radiological Society)的推荐作CO-RADS 0~6的分类[54]。②CT复查的评估。对复查患者需要对比前次检查的CT图像,从病变的范围、密度综合判断,说明病变进展、吸收消散或无变化。③随访及建议。参照本共识“随访周期”,并结合年龄、临床病情等综合考虑,合理建议。
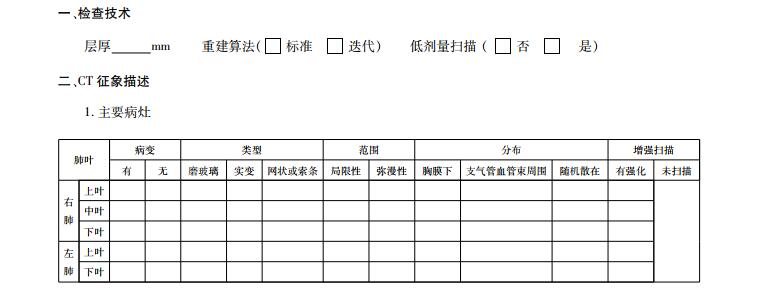
根据上述放射学报告规范,专家共识小组制作了“新型冠状病毒肺部感染CT结构化报告模板”,以供参考,具体见附件1。
6 质量控制 6.1 DR、CT图像质量控制 6.1.1 DR图像质量评价[55](1)图像的信息标识准确完整,不遮挡图像。(2)图像能满足影像诊断的需要:①影像布局合理,无伪影或设备原因的伪影;②两侧肺野显示对称、纹理可辨,纵隔、胸壁及软组织显示良好;③纵隔后方胸椎显示可见,心影后肺及纹理大致可见,肋骨隐约显示;④心脏、纵隔、膈肌及气管分叉边界显示清楚。
6.1.2 CT图像质量评价[55](1)图像的信息标识准确完整,不遮挡图像。(2)图像能满足影像诊断的需要:①上界包括肺尖,下界包括肋膈角,无层面遗漏;②肺窗图像:肺纹理清晰,次级肺小叶结构清晰可辨,距胸膜1 cm以内小血管能够显示;③纵隔窗图像:纵隔内大血管能够清晰显示,且与周围脂肪有锐利界面;④骨窗图像:可清晰显示胸壁诸骨的骨皮质和骨小梁;⑤增强图像血管强化良好,病变组织与正常组织对比明显;⑥图像位于影像中心,大小合适,左右胸廓最外侧缘距影像边缘小于3 cm,图像噪声SD<10。
6.1.3 注意事项[28, 56-57](1)床旁DR常规取胸部前后位的仰卧或半卧,特殊需求可用侧卧位。(2)合理稳妥放置平板探测器,注意防止患者治疗管道的损坏或脱落。(3)CT扫描范围及方向为自肺尖至较低侧肋膈角下1 cm,重型及危重型患者,可采取膈角到肺尖的扫描方向,以减少肺下野因屏气不佳导致的呼吸运动伪影。(4)重型及危重型患者可采取增大螺距、减小球管转速、加大准直宽度等方法缩短扫描时间,以减少呼吸运动伪影。(5)检查时,应积极做好受检者及陪护人员的防护,尤其是儿童性腺等对射线敏感的部位。(6)无法配合吸气、屏气及需镇静后检查的患儿在平静呼吸下完成扫描。
6.2 诊断报告质量控制 6.2.1 质控参考标准参照《放射科管理规范与质控标准(2017版)》[55],危重型患者按照危急值流程处理。
6.2.2 报告内容的完整性放射学诊断报告内容包括受检者姓名、性别、年龄、科别、门诊号(或住院号、床号)、检查号、检查部位和名称、影像学检查技术方法、检查时间、放射学描述、放射学诊断、诊断报告医师/审核医师签名、诊断报告签发时间等。
6.2.3 报告描述的质控报告的描述规范参照本共识第5部分。质控须注意:①主次分明、前后一致、逻辑性强。②对病灶的描述要全面、准确。③采用规范的放射学和医学术语[58]。
6.2.4 报告诊断结论的质控报告的诊断结论规范照本共识第5部分。质控须注意:①诊断结论主次分明,与描述部分前后一致。②包含对新冠肺部感染的可能性诊断、复查评估(有前次CT影像时)和随访建议。③结论要正确和适度,与国家最新的防疫政策和指南要求保持一致。
6.2.5 病例随访的质控每个工作日晨读片针对疑难病例进行集中讨论,及时记录讨论结果。每月进行病例随访工作,利用PACS及医院信息综合管理系统(hospital information system,HIS)查询相关病例资料并统计诊断符合率,每月进行一次随访病例讨论及学习最新版相关防控政策。
本共识由重庆市医学会放射医学分会胸心学组、重庆市医学影像医疗质量控制中心牵头,在王健(陆军军医大学第一附属医院)、郭大静(重庆医科大学附属第二医院)、高万春(重庆大学附属黔江医院)的组织下完成。
执笔专家(按姓氏笔画为序):
方 正 重庆医科大学附属第二医院
江才明 重庆市第九人民医院
刘 凯 重庆大学附属黔江医院
杨 华 重庆市中医院
杨 全 重庆医科大学附属永川医院
陈 伟 陆军军医大学第一附属医院
陈金华 重庆医科大学附属第二医院
陈林丽 重庆医科大学附属第二医院
陈欣重 庆医科大学附属儿童医院
陈维娟 重庆医科大学附属第二医院
姚小红 陆军军医大学第一附属医院
顾 敏 重庆市人民医院
梁红琴 陆军军医大学第一附属医院
褚志刚 重庆医科大学附属第一医院
专家组成员(按姓氏笔画为序):
王舒楠 陆军军医大学第三附属医院
吕发金 重庆医科大学附属第一医院
吕圣秀 重庆市公共卫生医疗救治中心
李 康 重庆市人民医院
李咏梅 重庆医科大学附属第一医院
李传明 重庆大学附属中心医院
刘 波 重庆医科大学附属儿童医院
邹利光 陆军军医大学第二附属医院
何 玲 重庆医科大学附属儿童医院
张伟国 陆军军医大学第三附属医院
张 冬 陆军军医大学第二附属医院
张久权 重庆大学附属肿瘤医院
张志伟 重庆医科大学附属第一医院
罗天友 重庆医科大学附属第一医院
唐茁月 重庆市人民医院
桂 爽 重庆大学附属黔江医院
黄卫春 陆军军医大学第一附属医院
曾 燕 重庆医科大学附属第三医院
曾文兵 重庆大学附属三峡医院
曾国飞 重庆市中医院
温 云 重庆大学附属三峡医院
蔡金华 重庆医科大学附属儿童医院
附件1:新型冠状病毒肺部感染CT结构化报告模板
Structured chest CT report template of SARS-CoV-2 infection