急性颅内出血(intracranial hemorrhage,ICH)起病急骤、病情凶险,具有致残率、病死率高等特点,出血部位及出血量等与治疗方案的制定密切相关[1-3]。平扫CT(conventional non-contrast CT,NCCT)扫描速度快、检查时间短,是急性颅内出血的首选方法,亦是颅内出血诊断的“金标准”[4]。CT血管成像(CT angiography,CTA) 是排除颅内出血患者血管源性病变的主要方法[5],2019版指南[6]提出临床怀疑急性颅内出血的患者,应首选NCCT+CTA的扫描方案,然而,临床工作中实施该方案存在流程不够简洁、放射性辐射剂量偏高等弊端[7]。双源CT双能量扫描可实现一次扫描,同时获得虚拟平扫CT(virtual non-contrast CT,VNCT)和CTA图像,相较于NCCT+CTA的检查方案少一次平扫CT,检查时间短,辐射剂量低,近年来已被应用于颅内出血诊断[5, 7-8]。
目前,颅内出血定性和定量分析通常由放射医师手动测量完成[9]。但处理方法过程繁琐、耗时长、效率低,且完全依靠医师临床经验进行分析,主观因素影响大,可重复性差[10-11];由于不同年资医师的诊断水平有所差异,导致观察者之间的一致性较差[12],存在漏诊和误诊的可能性[13]。为了提高颅内出血的影像诊断效能,利用人工智能(artificial intelligence,AI)技术自动识别颅内出血并分割测量血肿体积逐渐兴起[14-16]。本研究采用双源VNC技术联合人工智能,初步探索该方法在急性颅内出血影像检查流程化及其诊断颅内出血的临床应用价值。
1 材料与方法 1.1 一般资料本研究为横断面研究,纳入2022年1-7月于本院门诊部行急诊头部CT平扫和CTA检查的67例疑似颅内出血患者的影像学资料。其中男性32例,女性35例,年龄35~89(56.2±12.5)岁。纳入标准:①术前行CT扫描检查,包括头部平扫及双能量CTA检查;②AI软件能识别图像。排除标准:①运动或金属伪影干扰,图像质量差;②双能量CTA序列不全。本研究方案经本院医学伦理委员会批准「2019年科伦审第(19)号」。所有患者检查前签署CT增强扫描知情同意书。
1.2 仪器与方法CT检查采用西门子第三代双源CT(SOMATOM Definition Force,Germany)。NCCT扫描参数为:管电压120 kV,CAREDose 4D管电流自动调制技术,参考管电流为300 mAs,螺距0.5,层厚1.0 mm,层间距0.7 mm。平扫完成后,行双能CTA检查,经右侧肘正中静脉预埋18G留置针,采用双筒高压注射器(Ulrich medical)注入非离子型造影剂碘普罗胺注射液(优维显,370 mgI/mL)40~50 mL,注射流率4.5~5.0 mL/s,注射完成后以相同流率注入30 mL生理盐水。使用对比剂智能追踪技术触发扫描,监测点置于主动脉弓层面,触发阈值100 HU,达到阈值后延迟4 s自动触发扫描。扫描参数:管电压90/Sn150 kV,CAREDose 4D管电流自动调制技术,A管和B管参考管电流分别为250 mAs和190 mAs,螺距0.7,层厚1.0 mm,层间距0.7 mm,重建模式为DE Iodine+VNC。
1.3 辐射剂量评估记录患者每个序列的容积CT剂量指数(volume CT dose index,CTDIvol)及剂量长度乘积(dose length product,DLP),按照公式计算有效剂量(effective dose,ED)=DLP×K,其中换算因子K=0.002 1[7]。由于VNCT图像是利用双能CTA数据重建而来,因此以CTA辐射剂量参数作为VNCT的辐射剂量指标。
1.4 图像处理与分析客观评价:将NCCT和VNCT图像上传至Syngo Via工作站,由1名5年以上神经放射学工作经验的医师使用复制、粘贴功能将大小为15~20 mm2的圆形ROI分别置于2组图像病灶最大层面的出血区和基底节区层面的正常脑实质,避开假牙伪影、骨质、钙化等影响结果的部位,分别测量CT值(HU)及标准差SD值,为避免测量误差,重复测量3次,取平均值为最终结果。用基底节区层面的标准差SD表示图像噪声。图像信噪比(signal-to-noise ratio,SNR)和对比噪声比(contrast-to-noise ratio,CNR)的计算公式为:SNR=出血区CT值/出血区SD值,CNR=(出血区CT值-脑实质CT值)/脑实质SD值。
专家评价:由2名具有10年以上的神经放射学工作经验的影像诊断医师在后处理工作站上根据NCCT图像判断是否存在颅内出血及出血部位、类型和颅脑中线是否偏移,意见不一致时经协商达成共识。然后手动测量中线结构偏移程度、出血最大层面的长径和短径、勾画血肿边缘并计算血肿体积,取其平均值。记录医师读片开始至测量结束所用时间,取2名医师的平均值为最终结果。
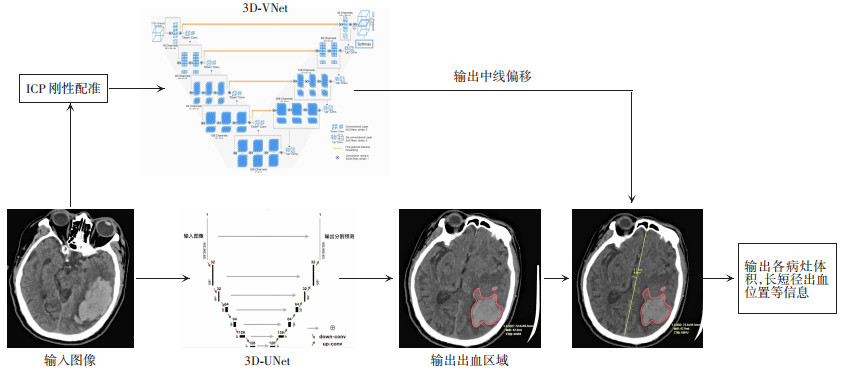
AI评价:将NCCT和VNCT图像上传至Stroke Doc软件(出血性脑卒中智能诊断系统V1.11.9,数坤科技,北京),利用三维卷积神经网络(3D-UNet)自动识别CT图像中的出血区域,并经过归一化处理、配准、建模、分割、分类、区域处理以及信息统计与测量等流程最终输出上述指标相关诊断结果,详细流程见图 1。记录导入图像、检出病灶及定量分析所需时间。
|
| 图 1 急性颅内出血智能诊断系统自动化处理流程图 |
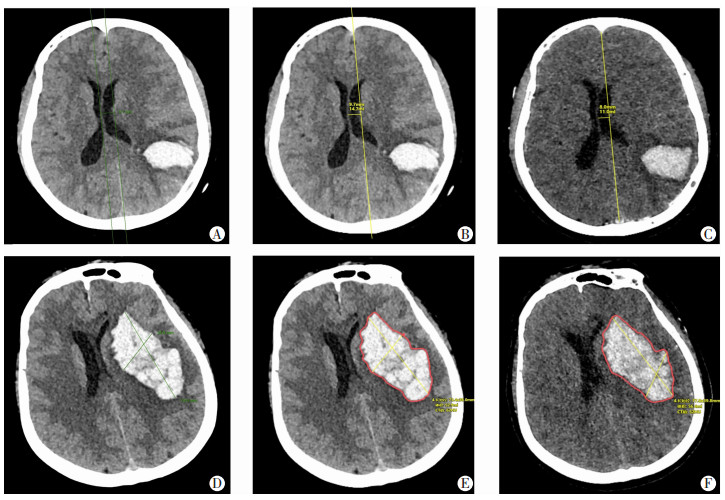
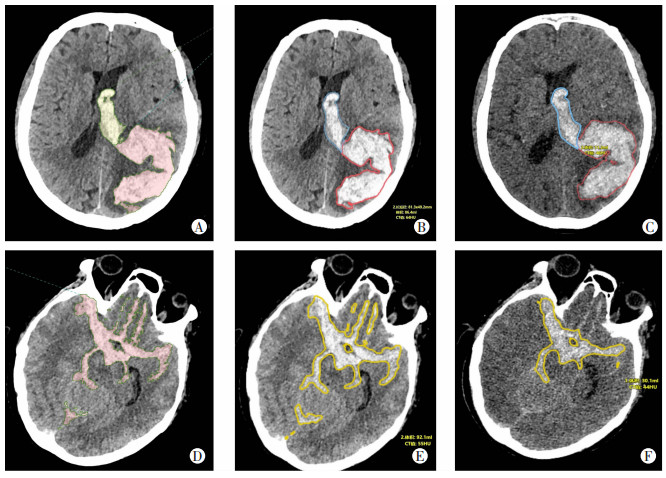
评价标准:按照不同的出血部位,出血类型分为脑实质出血(cerebral parenchymal hemorrhage,CPH)、脑室出血(intraventricular hemorrhage,IVH)、硬膜下出血(subdural hemorrhage,SDH)、硬膜外出血(epidural hemorrhage,EDH)和蛛网膜下腔出血(subarachnoid hemorrhage,SAH);中线结构偏移程度的手动测量平面与AI识别的测量平面一致,并测量偏移的最大距离(图 2);出血最大层面为专家判定的颅内出血最大面积层面,并测量长径和短径(图 2);血肿体积由专家手动逐层勾画并渲染血肿边缘,最后由系统计算出总体积(图 3)。
|
| A~C:依次为中线结构偏移程度专家手动测量、NCCT+AI自动测量和VNCT+AI自动测量;D~F:依次为出血最大层面长径和短径专家手动测量、NCCT+AI自动测量和VNCT+AI自动测量 图 2 典型病例的颅内出血定量分析 |
|
| A~C:依次为CPH和IVH血肿体积专家手动勾画、NCCT+AI自动勾画和VNCT+AI 自动勾画;D~F:依次为SAH血肿体积专家 手动勾画NCCT+AI自动勾画和VNCT+AI自动勾画 图 3 典型病例的颅内出血血肿体积测量 |
1.5 统计学分析
采用SPSS 25.0统计软件进行分析。计量资料用x±s表示,计数资料用例数(百分比)表示。NCCT和VNCT图像的平均CT值、噪声值、SNR、CNR和辐射剂量采用Wilcoxon秩和检验进行统计分析。以专家诊断结果为参考标准,AI软件联合NCCT及VNCT对颅内出血诊断效能的比较采用配对χ2检验。AI测量与手动测量的结果中二分类变量资料采用Cohen’s kappa系数、连续变量资料采用组内相关系数(intraclass correlation coefficient,ICC)进行一致性检验:0.75~1.00为诊断一致性好,0.40~ < 0.75为诊断一致性较好,0~ < 0.40为一致性差。以P < 0.05为差异有统计学意义。
2 结果 2.1 NCCT和VNCT图像质量的客观评价和辐射剂量客观评价方面,VNCT图像出血区和正常脑实质的CT值、SNR和CNR均低于NCCT图像(P均 < 0.001);VNCT图像的噪声大于NCCT图像(P < 0.001),详见表 1。
| 图像类型 | CT值/HU | 噪声/HU | SNR | CNR | |
| 出血区 | 正常脑实质 | ||||
| NCCT | 72.4±6.8 | 40.7±3.6 | 4.7±1.0 | 15.3±4.1 | 6.9±1.9 |
| VNCT | 61.0±6.9 | 29.2±4.3 | 5.8±1.3 | 9.9±2.2 | 5.7±1.8 |
| Z | -6.632 | -6.572 | -4.901 | -6.388 | -4.621 |
| P | < 0.001 | < 0.001 | < 0.001 | < 0.001 | < 0.001 |
NCCT、VNCT以及NCCT+CTA的CTDIvol分别为(32.3±3.2)、(18.3±1.3)、(50.7±3.5)mGy(F=102.000,P < 0.001);DLP分别为(601.2±92.9)、(197.1±40.7)、(798.3±108.4)mGy×cm(F=102.000,P < 0.001);ED分别为(1.3±0.2)、(0.4±0.1)、(1.7±0.2)mSv(F=102.000,P < 0.001)。结果显示:VNCT的辐射剂量明显低于NCCT及NCCT+CTA的辐射剂量。相较于NCCT+CTA检查,患者在单次双能量CTA检查(VNCT)中接受的ED可减少75.6%(1-0.4/1.7)。
2.2 颅内出血定性分析67例患者的颅内出血NCCT、VNCT联合AI与专家的诊断结果见表 2,最终64例经专家确诊为颅内出血,共134处出血,其中44例患者出血累计多部位,余3例为脑肿瘤。NCCT+AI提示62例颅内出血,共138处出血,与专家相比,误诊1例,漏诊3例。VNCT+AI提示59例颅内出血,共120处出血,误诊1例,漏诊6例。以专家诊断结果为参考标准,VNCT+AI和NCCT+AI诊断准确率分别为89.6%和94.0%,两者在患者水平诊断颅内出血的差异无统计学意义(P=0.559)。
| 特征 | 专家 | NCCT+AI | VNCT+AI | 专家vs NCCT+AI | 专家vs VNCT+AI | NCCT+AI vs VNCT+AI | |||||
| 准确率(%) | P | 准确率(%) | P | χ2 | P | ||||||
| 患者/例 | 64 | 62 | 59 | 94.0 | 0.625 | 89.6 | 0.125 | 0.767 | 0.559 | ||
| 出血类型/例 | |||||||||||
| IPH | 51 | 55 | 47 | 90.2 | 0.219 | 83.6 | 0.344 | 3.089 | 0.124 | ||
| IVH | 36 | 36 | 30 | 95.2 | 1.000 | 86.0 | 0.202 | 2.045 | 0.233 | ||
| SAH | 40 | 37 | 32 | 93.3 | 0.250 | 83.0 | 0.087 | 1.449 | 0.336 | ||
| SDH | 7 | 10 | 11 | 55.8 | 0.453 | 60.0 | 0.289 | 0.091 | 1.000 | ||
以出血类型为单位,专家确诊IPH 51处、IVH 36处、SAH 40处和SDH 7处。VNCT+AI对4种出血的诊断准确率分别为83.6%、86.0%、83.0%和60.0%,NCCT+AI的诊断准确率分别为90.2%、95.2%、93.3%和55.8%,VNCT+AI与NCCT+AI的诊断结果之间差异均无统计学意义(P=0.124,P=0.233,P=0.336,P=1.000)。
2.3 颅内出血定量分析定量分析方面,其中VNCT+AI、NCCT+AI诊断中线偏移分别为19、23例,二者的结果一致性好(Kappa=0.862,P<0.001),与专家诊断(23例)的一致性均较好(Kappa=0.655,Kappa=0.669,P均 <0.001);两组对中线偏移程度测量结果分别为(9.0±3.0)、(8.6±3.5)mm,二者结果一致性好(ICC=0.807,P<0.001),与专家测量结果[(8.9±2.6)mm]均一致性好(ICC=0.820,ICC=0.820,P均 <0.001)。
VNCT+AI、NCCT+AI对最大面积长径测量结果分别为(46.6±21.4)、(45.0±19.8) mm,二者结果一致性好(ICC=0.966,P<0.001),与专家测量结果[(44.3±19.8)mm]均一致性好(ICC=0.942,ICC=0.942,P均 <0.001);两组对最大面积短径测量结果分别为(30.9±12.3)、(30.6±12.6) mm,二者结果一致性好(ICC=0.973,P<0.001),与专家测量结果[(27.6±12.7)mm]均一致性好(ICC=0.920,ICC=0.902,P均 <0.001);两组对血肿体积测量结果分别为(41.3±34.1)、(46.9±37.7) mL,二者结果一致性好(ICC=0.949,P<0.001),与专家测量结果[(46.3±36.5)mL]均一致性好(ICC=0.959,ICC=0.985,P均 <0.001)。
手动测量、NCCT+AI和VNCT+AI测量耗时分别为(113.5±66.5)、(58.5±24.9)、(50.6±15.9)s。VNCT+AI和NCCT+AI耗时均显著低于手动测量(P均 <0.001),且VNCT+AI耗时显著低于NCCT+AI(P<0.001)。
3 讨论急性颅内出血患者的定性诊断和定量分析对于临床治疗方案的抉择至关重要,测量不准确、不及时将影响临床决策准确性,错过最佳治疗时机;快速诊断、精准测量具有重要临床意义[17]。然而对于出血部位、类型、大小及体积等关键定量信息仅依据传统CT诊断难以充分描述,且需要花费大量的时间和精力[16]。因此,亟待寻找一种扫描流程快、自动化识别并测量出血量的检查方案以改善工作效率和提高诊断效率,为患者的临床治疗提供可靠的影像依据。
以往关于颅内出血的AI方面的研究,多聚焦于算法的开发和对出血区域的分割识别[18-20],对于SAH、IVH及SDH等特殊类型出血的准确率有限[15]。近期,INKEAW等[21]采用3D CNN网络结构能以0.54的平均Dice系数识别不同颅内出血类型;ALIS等[22]构建的CNN-RNN联合模型对颅内出血的检出准确率达到96.0%,对5种亚型的准确率从86.7%~99.9%。目前涉及AI颅内出血定量分析和临床应用环境实践的研究甚少,本研究将AI应用于临床实践场景中,结果显示基于3D-UNet的Stroke Doc软件诊断颅内出血在患者水平的准确率高,并能以较高的的准确率检出IPH、IVH和SAH,与ALIS等[22]研究结论基本一致。然而,本研究中AI对SDH的检出准确率较低,这可能与AI软件的标注数据集不同和算法不一致有关。此外,本研究发现该AI软件对颅脑中线结构偏移程度、出血最大面积长径和短径、血肿体积的自动化分析与专家手动分析结果的一致性好,且耗费时间较放射专家大幅缩短。
临床实践中针对疑似急性颅内出血患者往往采用平扫加血管成像的扫描方案,配合人工诊断及手动测量,以确定出血特征和责任血管,将耗费大量时间在影像检查和结果分析上,且整个检查流程的工作效率及准确率会受出血特点、设备条件、医师经验等因素的影响[10, 17, 23]。AI的应用为颅内出血的诊疗提供了新的契机,其快速、精准的优势在ICH患者病情的评估、指导治疗等方面均表现出巨大的潜力,对临床诊疗的影响也日益增大。目前国内外对颅内出血AI的研究均以NCCT图像为对象,基于探索更快的急性颅内出血检查及诊断流程,本研究创新性地探讨了VNCT图像和NCCT图像对AI软件诊断准确率的影响情况,结果表明虽然VNCT图像的CT值、SNR和CNR均低于NCCT,噪声比NCCT高,这与以往研究[5, 7-8]一致,但与专家结果相较,VNCT联合AI在患者水平和不同出血类型的颅内出血诊断结果与NCCT具有相似的检出效能且准确率均较高。除此之外,VNCT+AI的定性分析相较于NCCT+AI耗时短,笔者认为这可能与病变特点和AI分割识别有关。另一方面,采用VNCT检查,可以精简急诊患者的检查流程,且患者接受的辐射剂量减少75.6%,这更符合国际放射防护委员会(International Commission on Radiological Protection,ICRP)提出的合理使用低剂量(as low as reasonably achievable,ALARA)原则[24-25]。
本研究的不足在于:①为单中心的横断面研究,未纳入硬膜外出血的病例,存在一定的采样偏倚;②未对颅内出血部位、形态和脑室受压情况进行评价;③未讨论VNCT图像质量对医师诊断的影响,但文献[5, 7-8]均已证实VNCT的图像质量能够满足临床诊断要求。
综上所述,双源CT虚拟平扫技术能减少辐射剂量,优化检查流程,联合基于卷积神经网络的出血性脑卒中智能诊断系统能缩短急性颅内出血诊断时间;对不同类型的急性颅内出血进行精准的定性分析和定量分析,将扩大急诊患者的治疗时间窗,具有良好的临床应用前景。
| [1] |
IRONSIDE N, CHEN C J, MUTASA S, et al. Fully automated segmentation algorithm for hematoma volumetric analysis in spontaneous intracerebral hemorrhage[J]. Stroke, 2019, 50(12): 3416-3423. |
| [2] |
WANG T, SONG N, LIU L L, et al. Efficiency of a deep learning-based artificial intelligence diagnostic system in spontaneous intracerebral hemorrhage volume measurement[J]. BMC medical imaging, 2021, Aug 13;21(1): 125. |
| [3] |
王星辰, 杨文松, 李瑞, 等. 急性脑出血早期神经功能恶化与预后相关性研究[J]. 第三军医大学学报, 2018, 40(12): 1120-1124. WANG X C, YANG W S, LI R, et al. Correlation between early neurological deterioration and poor functional outcomes in patients with acute intracerebral hemorrhage[J]. J Third Mil Med Univ, 2018, 40(12): 1120-1124. |
| [4] |
徐运, 黄丽丽, 武文博. 脑血管病的神经影像学检查[J]. 中华神经科杂志, 2020, 53(7): 531-539. XU Y, HUANG LL, WU W B. Neuroimaging of cerebrovascular disease[J]. Chin J Neurol, 2020, 53(7): 531-539. |
| [5] |
柴学, 张龙江, 盛会雪, 等. 单次对比增强双源双能量CT血管成像评估颅内出血及其原因[J]. 医学研究生学报, 2012, 25(11): 1176-1181. CHAI X, ZHANG L J, SHENG H X, et al. Evaluation of intracranial hemorrhage and its causes by single-contrast-enhanced dual-source dual-energy CT angiography[J]. J Med Postgrad, 2012, 25(11): 1176-1181. |
| [6] |
国家卫生健康委员会脑卒中防治工程委员会神经影像专业委员会, 中华医学会放射学分会神经学组. 脑血管病影像规范化应用中国指南[J]. 中华放射学杂志, 2019, 53(11): 916-926, 927-940. Stroke Prevention Expert Commission Neuroimaging Committee of National Health Commission, Radiology Society Neuroimaging Group of Chinese Medical Association. Chinese guideline for standard utilization of imaging for cerebrovascular diseases[J]. Chin J Radiol, 2019, 53(11): 916-926, 927-940. |
| [7] |
郭兴, 丁伟, 秦慧娟. 双能CT血管成像虚拟平扫对评价蛛网膜下腔出血的应用价值[J]. 中国医学科学院学报, 2010, 32(6): 695-698. GUO X, DING W, QIN H J. Application of virtual non-enhanced images in evaluating subarachnoid hemorrhage by dual-energy computed tomographyangiography[J]. Acta Acad Med Sin, 2010, 32(6): 695-698. |
| [8] |
黄伟, 徐益明, 邵瑾, 等. 双源CT虚拟平扫在头部检查的初步应用[J]. 中华放射学杂志, 2011, 45(3): 229-234. HUANG W, XU Y M, SHAO J, et al. Dual-source virtual non-contrast CT of the head: a preliminary study[J]. Chin J Radiol, 2011, 45(3): 229-234. |
| [9] |
常健博, 姜燊种, 陈显金, 等. 基于卷积神经网络的自发性脑出血血肿分割方法的一致性评价[J]. 中国现代神经疾病杂志, 2020, 20(7): 585-590. CHANG J B, JIANG S Z, CHEN X J, et al. Consistency evaluation of an automatic segmentation for quantification of intracerebral hemorrhage using convolution neural network[J]. Chin J Contemp Neurol Neurosurg, 2020, 20(7): 585-590. |
| [10] |
HEIT JJ, COELHO H, LIMA F O, et al. Automated cerebral hemorrhage detection using RAPID[J]. Am J Neuroradiol, 2021, 42(2): 273-278. |
| [11] |
韦鑫, 陈维娟, 邓昊, 等. VMI+联合人工智能辅助诊断系统对颅内动脉瘤诊断价值的研究[J]. 中国医疗设备, 2021, 36(10): 100-103, 107. WEI X, CHEN W J, DENG H, et al. Research of dual energy CT VMI+ technology combined with artificial intelligence-assisted diagnosis system in the diagnosis of intracranial aneurysm[J]. China Med Devices, 2021, 36(10): 100-103, 107. |
| [12] |
YE H, GAO F, YIN Y B, et al. Precise diagnosis of intracranial hemorrhage and subtypes using a three-dimensional joint convolutional and recurrent neural network[J]. Eur Radiol, 2019, 29(11): 6191-6201. |
| [13] |
张天麒, 康波, 孟祥飞, 等. 基于U-Net的颅内出血识别算法[J]. 北京邮电大学学报, 2020, 43(3): 92-98. ZHANG T Q, KANG B, MENG X F, et al. U-net based intracranial hemorrhage recognition[J]. J Beijing Univ Posts Telecommun, 2020, 43(3): 92-98. |
| [14] |
常健博, 王任直, 冯铭. 人工智能在颅内出血诊断与治疗中的应用[J]. 中国现代神经疾病杂志, 2019, 19(9): 622-626. CHANG J B, WANG R Z, FENG M. The application of artificial intelligence in clinical diagnosis and treatment of intracranial hemorrhage[J]. Chin J Contemp Neurol Neurosurg, 2019, 19(9): 622-626. |
| [15] |
张康微, 魏来, 孟瑾茜, 等. 基于CT影像组学和机器学习脑出血研究进展[J]. 中国医学影像技术, 2022, 38(4): 604-606. ZHANG K W, WEI L, MENG J Q, et al. Research progresses of radiomics and machine learning based on CT for cerebral hemorrhage[J]. Chin J Med Imaging Technol, 2022, 38(4): 604-606. |
| [16] |
MATSOUKAS S, SCAGGIANTE J, SCHULDT B R, et al. Accuracy of artificial intelligence for the detection of intracranial hemorrhage and chronic cerebral microbleeds: a systematic review and pooled analysis[J]. Radiol Med, 2022, 127(10): 1106-1123. |
| [17] |
赖建东, 王宁, 罗坤, 等. 基于深度学习计算机辅助诊断系统测量脑出血量[J]. 中国医学影像技术, 2020, 36(12): 1781-1785. LAI J D, WANG N, LUO K, et al. Measuring volume of cerebral hemorrhage based on deep learning computer aided diagnostic system[J]. Chin J Med Imaging Technol, 2020, 36(12): 1781-1785. |
| [18] |
王霁雯, 林雨, 熊建华, 等. 基于深度学习的自发性脑出血CT影像分割算法精准计算病灶体积的应用探讨[J]. 中华放射学杂志, 2019, 53(11): 941-945. WANG J W, LIN Y, XIONG J H, et al. Evaluation of spontaneous intracerebral hemorrhage by using CT image segmentation and volume assessment based on deep learning[J]. Chin J Radiol, 2019, 53(11): 941-945. |
| [19] |
JUNGHWAN C, KI-SU P, MANOHAR K, et al. Improving sensitivity on identification and delineation of intracranial hemorrhage lesion using cascaded deep learning models[J]. J Digit Imaging, 2019, 32(3): 450-461. |
| [20] |
WANG X Y, SHEN T, YANG S, et al. A deep learning algorithm for automatic detection and classification of acute intracranial hemorrhages in head CT scans[J]. Neuroimage Clin, 2021, 32: 102785. |
| [21] |
INKEAW P, ANGKURAWARANON S, KHUMRIN P, et al. Automatic hemorrhage segmentation on head CT scan for traumatic brain injury using 3D deep learning model[J]. Comput Biol Med, 2022, 146: 105530. |
| [22] |
ALIS D, ALIS C, YERGIN M, et al. A joint convolutional-recurrent neural network with an attention mechanism for detecting intracranial hemorrhage on noncontrast head CT[J]. Sci Rep, 2022, 12(1): 2084. |
| [23] |
赵杰祎, 周正松, 王晓宇, 等. 基于分水岭及区域增长算法建立一种测量自发性脑出血血肿体积的分割方法[J]. 四川大学学报(医学版), 2022, 53(3): 511-516. ZHAO J Y, ZHOU Z S, WANG X Y, et al. Hematoma segmentation of spontaneous intracerebral hemorrhage based on watershed and region-growing algorithm[J]. J Sichuan Univ Med Sci, 2022, 53(3): 511-516. |
| [24] |
林禹, 张潇潇, 张有彬, 等. 双层探测器光谱CT虚拟平扫应用于肝脏三期增强扫描[J]. 中国医学影像技术, 2020, 36(S1): 29-33. LIN Y, ZHANG X X, ZHANG Y B, et al. Application of dual-layer spectral detector CT virtual non-contrast images in hepatic triple-phase enhanced scan[J]. Chin J Med Imaging Technol, 2020, 36(S1): 29-33. |
| [25] |
张进, 李小虎, 余玲, 等. 能谱CT虚拟平扫成像在尿路造影中替代常规平扫的可行性研究[J]. 安徽医科大学学报, 2018, 53(4): 595-599. ZHANG J, LI X H, YU L, et al. Virtual non-contrast CT imaging replaces the conventional non-contrast CT imaging in urography: a feasibility study[J]. Acta Univ Med Anhui, 2018, 53(4): 595-599. |




