2. 400050 重庆,重庆医科大学附属康复医院神经科;
3. 400038 重庆,陆军军医大学(第三军医大学)基础医学院生理学教研室;
4. 400042 重庆,陆军特色医学中心医学心理科
2. Department of Neurology, the Affiliated Rehabilitation Hospital of Chongqing Medical University, Chongqing, 400050;
3. Department of Physiology, College of Basic Medical Sciences, Army Medical University (Third Military Medical University), Chongqing, 400038;
4. Department of Medical Psychology, Army Medical Center of PLA, Chongqing, 400042, China
中线丘脑(midline thalamus)是觉醒上行网状激活系统的关键区域,位于动物丘脑复合体的中间,主要包括丘脑室旁核(paraventricular thalamic nucleus,PVT)、丘脑中央内侧核(central medial thalamic nucleus,CM)、菱形核(rhomboid thalamic nucleus,Rh)与连接核(reuniens thalamic nucleus,Re)[1-3]。PVT位于中线丘脑背侧,紧邻背侧第三脑室[3]。PVT神经元活动在睡眠向觉醒转换前升高,诱导觉醒发生[4],并且在觉醒期表现出高放电活动[5]。在饥饿状态下,PVT神经元放电频率进一步增加,介导饥饿诱导的觉醒[6]。CM位于PVT下方,CM神经元在觉醒期活跃,光遗传学技术激活CM诱发快速的睡眠向觉醒转换。此外,CM神经元自发放电有助于诱导NREM睡眠期皮层慢波振荡的上升相及其全脑同步化[7]。Rh/Re靠近下丘脑及腹侧第三脑室,SALAY等[8]发现Rh/Re可被视觉相关危险信号强烈激活,明显提高觉醒水平,以帮助动物逃避危险。因此,中线丘脑神经元在觉醒期活跃的活动模式为其调控觉醒及其依赖的相关行为提供了重要电生理基础。中线丘脑向前脑发出广泛投射,如前额叶皮层(medial prefrontal cortex,mPFC)、伏隔核(nucleus accumbens,NAc)、杏仁核[Amygdala,包括中央杏仁核(central amygdala,CeA)和基底外侧杏仁核(basolateral amygdala,BLA)]和终纹床核(bed nucleus of the stria terminalis,BNST等[9-11]。中线丘脑与上述脑区形成的通路参与觉醒及相关行为的调控。杏仁核作为中线丘脑的重要下游靶区之一,是情绪信息处理的关键神经核团[12]。中线丘脑-杏仁核通路参与调节觉醒依赖的一系列行为,如恐惧应激[13-14]、焦虑[15]、抑郁[16]、神经性疼痛信号传导[17]和防御行为[8, 18]等。例如,PVT-CeA通路在恐惧条件反射中联系增强,促进恐惧记忆的形成和表达[13]。Rh/Re-BLA通路激活诱导小鼠冻结行为增加以避免被捕食者发现[8]。但是,中线丘脑各核团-中央杏仁核通路在自然觉醒/睡眠周期中的神经元活动模式尚未明确。因此,揭示中线丘脑-杏仁核通路在觉醒/睡眠周期中的活动模式有助于更好的理解这些通路参与觉醒依赖行为调节的方式和规律。
为此,本研究首先通过逆行神经示踪技术,系统探索中线丘脑不同神经核团与杏仁核的联系特征,为中线丘脑-杏仁核通路研究提供形态学基础;进而利用光纤钙信号记录和脑电图(electroencephalogram,EEG)-肌电图(electromyogram,EMG)记录技术结合观察中线丘脑-中央杏仁核通路在觉醒/睡眠中的活动模式,为中线丘脑-杏仁核通路调控觉醒的作用机制研究提供依据。
1 材料与方法 1.1 实验动物实验所用小鼠均为8~12周龄,体质量20~25 g的SPF级雄性C57BL/6J小鼠,购自陆军军医大学动物实验中心。小鼠饲养于12 h光照/12 h黑暗交替(6:00-18:00照明)的昼夜节律控制箱中,可自由饮食和活动,环境温度控制在(22±1)℃。所有实验操作和小鼠伦理严格遵守相关实验动物福利和伦理规范,并尽量减少实验动物的痛苦和使用量。
1.2 方法 1.2.1 逆行神经示踪实验在逆行神经示踪实验中将同一批10只小鼠按随机数字表法分为2组,每组5只,分别在杏仁核的两个亚区CeA和BLA注射100 nL逆行示踪荧光微粒RetroBeads(R180-1000, Lumaflouor, USA),感染3~7 d后,观察形态。
立体定位注射操作流程参考课题组已发表的工作[5]。小鼠在麻醉诱导盒中以浓度2.0%,流速0.6 mL/min科研用异氟烷(瑞沃德公司,中国)气体诱导麻醉5 min,随后将小鼠头部固定于单臂数显脑立体定位仪(瑞沃德公司,中国)上,将麻醉浓度调整为1.0%,流速调整为0.5 mL/min,且手术过程中维持此浓度。用红霉素眼膏保护小鼠眼睛,防止灯光长时间直接照射致盲。剃除小鼠头顶毛发后,用碘伏棉球消毒小鼠头皮,用眼科剪沿中线剪开小鼠头皮,暴露颅骨。在显微镜下以前囟点为原点调整小鼠头部,使小鼠颅骨与水平面平行。参照Franklin & Paxinos小鼠脑图谱以及相关文献,确定各脑区病毒注射的位置坐标,分别对CeA(前囟后1.20 mm,中线旁开2.80 mm,脑膜下深度4.00 mm)、BLA(前囟后1.20 mm,中线旁开3.35 mm,脑膜下深度3.65 mm)进行立体定位。使用玻璃微电极(3-000-203-G/X,Drummond Scientific公司,美国)抽取100 nL RetroBeads。按照坐标将玻璃微电极缓慢下降至相应位置并停针5 min后,以20 nL/min的速度推注病毒,注射完成后停留10 min,等待病毒或示踪剂扩散,随后缓慢升起玻璃电极。消毒伤口,缝合头皮,将小鼠放置在保温垫上,待其恢复清醒后放入水粮充足的饲养笼中。
1.2.2 脑肌电记录与分析将麻醉的小鼠固定在立体定位仪上,剪开头皮,暴露颅骨,并调平(过程同病毒注射);在小鼠颅骨表面开4个直径0.80 mm的骨窗,坐标分别为前囟点前1.50 mm,左右旁开1.50 mm与前囟点后3.00 mm,左右旁开2.00 mm;将EEG-EMG电极的螺钉按顺时针方向旋进骨窗内,螺钉刚好接触到脑组织表面即可,以接收小鼠脑电信号,将额外一颗螺钉旋进第4个骨窗内;用精细镊将焊有锡球的3根导线穿进小鼠颈部肌肉内,并保证一定的距离,使其互不形成串联电路,以接受小鼠肌电信号。牙科水和牙科粉混合,将EEG-EMG电极固定在小鼠颅骨上,完全覆盖电极的导线,并避免金属暴露部分互相接触。待牙科水泥干透后,将小鼠放置到加热垫上保温并等待其恢复,小鼠完全清醒后放回水粮充足的饲养笼中,做好标记。
小鼠手术7 d后,将小鼠通过脑肌电电极接入恒温恒湿并控制昼夜节律(ZT0=6:00, ZT12=18:00)的隔音睡眠觉醒记录箱中,用日本Kissei Comtec公司的Vital Recorder软件记录脑电/肌电信号(EEG: 0.3~30.0 Hz, EMG: 10~1 000 Hz,采样频率: 512 Hz)并保存。将数据导出后,通过SleepSign for Animals睡眠分析软件将小鼠的睡眠/觉醒状态自动评分,并根据小鼠睡眠觉醒状态的定义手工修正。根据脑电/肌电图的频谱特征,将小鼠状态分为清醒期(Wake)、非快速眼动(non-rapid eye movement,NREM)睡眠期和快速眼动(rapid eye movement,REM)睡眠期。Wake被定义为不同步、低振幅的脑电图节律和伴有相位爆发的肌电活动升高。NREM睡眠被定义为同步、高振幅和低频率(0.5~4.0 Hz, delta)的脑电图活动和较低的肌电活动,与觉醒相比没有相位爆发。REM睡眠被定义为包含明显的Theta (4~10 Hz)节律,几乎没有肌电活动。利用快速傅里叶变换对0~25 Hz频率范围内连续4 s的原始脑肌电数据进行计算,分析脑电活动的增量功率。
1.2.3 光纤记录实验为了观察特异性投射到中央杏仁核的中线丘脑神经元在觉醒/睡眠中的活动模式,将同一批15只小鼠随机分为3组,每组5只,在CeA注射逆行标记病毒AAV2/retro-Syn-Cre 100 nL,并分别在PVT、CM、Rh/Re注射AAV-EF1α-DIO-GCaMp7b 100 nL,病毒注射及手术方法与过程同前。病毒感染3~4周后分别在PVT上方(前囟后1.20 mm,中线旁开0 mm,脑膜下深度2.35 mm)、CM上方(前囟后1.20 mm,中线旁开0 mm,脑膜下深度3.00mm)、Rh/Re上方(前囟后1.20 mm,中线旁开0 mm,脑膜下深度3.80 mm)埋置光纤,同时埋置EEG-EMG电极。手术恢复7 d后,在光照期记录神经元钙信号活动的变化,并同步记录小鼠脑肌电信号。使用Inper Technology提供的脚本以40 Hz记录光纤钙信号,光纤钙信号的变化由ΔF/F=(F-F0)/F0公式计算,使用最小二乘回归法从488 nm信号中扣除410 nm信号,使用多项式拟合校正来减小长期记录造成的漂白效应。
1.2.4 灌注与取材将病毒感染时间充分后的小鼠和记录结束的小鼠用37℃的磷酸盐缓冲溶液(phosphate buffered solution,PBS)(ZLI-9061, 中杉金桥公司,中国)和4 ℃的4%多聚甲醛(158127,Sigma公司,美国)溶液进行心脏灌流,随后取出完整的脑组织,于4 ℃的4%多聚甲醛溶液中固定4~6 h后转移至30%的蔗糖(生工公司,中国)溶液中脱水。
1.2.5 脑片制备与形态分析脱水完成后的脑组织沉至管底,将脑组织取出,用滤纸吸去水分,沿冠状切面修整脑组织块。用冰冻切片机(CM1900,Leica公司,美国)在-20 ℃下连续切片,切片厚度为30 μm。将切下的脑片每120 μm取1张,在载玻片上连续贴片,待其自然风干后,用含DAPI的防荧光淬灭封片剂(F6057,Sigma公司,美国)进行封片。将制作好的脑片标本放入标本盒中并保存在4 ℃冰箱中。脑片标本用数字切片工作站—OlympusVS120显微镜扫描并保存图片,在OLYVIA软件中进行可视化调整及图像的保存和输出。利用激光共聚焦显微镜Zeiss LSM880拍摄高分辨率图像,并在Zen 2012成像系统软件中调整图像对比度,完成逆行示踪中线丘脑中RetroBeads阳性神经元计数。通过形态学验证发现光纤记录实验中2只PVT-CeA组小鼠病毒感染状况不良,数据被剔除;CM-CeA组1只小鼠病毒感染状况不良,数据被剔除。
1.3 统计学分析用SPSS 21.0软件对数据进行差异性统计分析;用GraphPad Prism 8.0或SigmaPlot 12.5绘制统计图。以平均值±标准误(x±s)mean±SEM表示实验结果。两组间比较使用配对/非配对t检验,不满足正态分布使用Wilcoxon符号秩检验;三组数据比较时使用单因素方差分析,若方差不齐,则使用Kruskal-Wallis单因素秩方差分析。P < 0.05差异存在统计学意义。
2 结果 2.1 逆行示踪鉴定投射至杏仁核的中线丘脑神经元分布特征为了比较中线丘脑神经核团与杏仁核联系的密切程度,本研究分别在杏仁核的两个亚区CeA和BLA注射逆行示踪荧光微粒RetroBeads(图 1A),发现中线丘脑的3个脑区PVT、CM、Rh/Re内RetroBeads标记的神经元数量和分布情况差别较大(图 1B~D左)。统计CeA、BLA逆行追踪到中线丘脑的神经元总数量,发现投射至CeA的PVT神经元显著多于投射至BLA的PVT神经元(P < 0.01),PVT投射至CeA和BLA的神经元总数量分别为(848±144)个和(376±34)个(图 1B右);投射至CeA的CM神经元与投射至BLA的CM神经元总数量相似(P=0.588),分别为(186±86)个和(114±56)个(图 1C右);投射至CeA的Rh/Re神经元较投射至BLA的Rh/Re神经元总数量多,神经元总数量分别为(258±24)个和(92±34)个(图 1D)。其中,在中线丘脑投射到CeA的神经元中PVT神经元占73.81%,CM神经元占8.51%,Rh/Re神经元占17.68%;在中线丘脑投射到BLA的神经元中PVT神经元占66.34%,CM神经元占23.55%,Rh/Re神经元占10.11%(图 1E)。进一步对投射至CeA和BLA的中线丘脑3个神经核团内RetroBeads阳性神经元数量进行比较(图 1F、G),发现投射至CeA和BLA的中线丘脑神经元主要分布在PVT(P < 0.001);投射至BLA的中线丘脑神经元在CM分布也较多(P < 0.05)。以上结果表明中线丘脑神经核团中的PVT与杏仁核联系较紧密,其中PVT与CeA的联系最为紧密。

|
| A:杏仁核内注射逆行示踪荧光微粒RetroBeads示意图以及注射位点CeA、BLA内RetroBeads表达情况;B:投射至CeA和BLA的PVT RetroBeads阳性神经元数量比较(n=5) 非配对t检验,b: P < 0.01,与CeA组比较;C:投射至CeA和BLA的CM RetroBeads阳性神经元数量比较(n=5) 非配对t检验;D:投射至CeA和BLA的Rh/Re RetroBeads阳性神经元数量比较(n=5) 非配对t检验,b: P < 0.01,与CeA组比较;E:上图为投射至CeA的中线丘脑神经元分布情况,下图为投射至BLA的中线丘脑神经元分布情况;F、G:投射至CeA、BLA的PVT、CM、Rh/Re RetroBeads阳性神经元总数量对比(n=5)单因素方差分析,a: P < 0.05,c: P < 0.001,3组间两两比较 图 1 投射至杏仁核的中线丘脑神经元分布情况 |
2.2 PVT-CeA通路在觉醒/睡眠周期中的活动模式
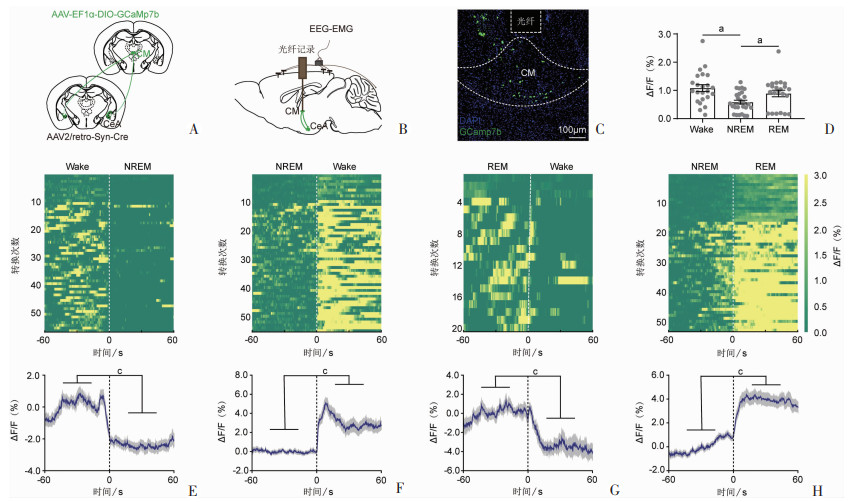
为了监测PVT-CeA通路在觉醒/睡眠周期中的神经元活动特征,首先在CeA注射逆行标记病毒AAV2/retro-Syn-Cre,同时在PVT注射Cre依赖的病毒AAV-EF1α-DIO-GCaMp7b(图 2A),标记特异性投射至CeA的PVT神经元。3~4周后在PVT上方埋置光纤,同时在颅骨表面埋置EEG-EMG电极(图 2B)。手术恢复1周后,记录脑肌电信号和神经元钙信号活动。分析特异性投射至CeA的PVT神经元在Wake期、NREM睡眠期、REM睡眠期的钙信号活动,发现该群神经元在Wake期的ΔF/F为(0.91±0.09)%,在NREM期的ΔF/F为(0.46±0.08)%,在REM期的ΔF/F为(0.27±0.05)%(图 2D)。说明在Wake期该群神经元明显活跃,NREM期和REM期神经元活动水平较低(P < 0.05)。随后分析觉醒/睡眠状态转换时钙信号的变化,发现在Wake期向NREM期转换时,神经元活动降低(图 2E);NREM期向Wake期转换时,神经元活动明显升高(图 2F);REM期向Wake期转换时,神经元活动升高(图 2G);在NREM期向REM期转换时,神经元活动呈下降趋势(图 2H)。以上结果说明PVT-CeA通路在觉醒期活跃。

|
| A:PVT和CeA病毒注射示意图;B: 光纤及脑肌电电极埋置示意图;C:PVT内感染GCamp7b及光纤记录典型代表图;D:特异性投射至CeA的PVT神经元在觉醒/睡眠各状态下钙信号活动平均值Kruskal-Wallis单因素秩方差分析,a:P < 0.05, 3组之间两两比较;E:Wake期向NREM期转换时投射至CeA的PVT神经元钙信号活动变化Wilcoxon符号秩检验,c:P < 0.001,状态转换前后60 s比较;F:NREM期向Wake期转换时投射至CeA的PVT神经元钙信号活动变化Wilcoxon符号秩检验,c:P < 0.001,状态转换前后60 s比较;G: REM期向Wake期转换时投射至CeA的PVT神经元钙信号活动变化Wilcoxon符号秩检验,c:P < 0.001,状态转换前后60 s比较;H:NREM期向REM期转换时投射至CeA的PVT神经元钙信号活动变化配对t检验,c:P < 0.001,状态转换前后60 s比较 图 2 PVT-CeA通路在觉醒/睡眠周期中的活动模式 |
2.3 CM-CeA通路在觉醒/睡眠周期中的活动模式
为了观察CM-CeA通路在觉醒/睡眠周期中的神经元活动特征,在CeA注射逆行标记病毒AAV2/retro-Syn-Cre,同时在CM注射Cre依赖的病毒AAV-EF1α-DIO-GCaMp7b(图 3A),标记特异性投射至CeA的CM神经元,并在病毒感染3~4周后在CM上方埋置光纤插芯用来记录神经元钙信号活动,在颅骨表面埋置EEG-EMG电极记录脑肌电信号(图 3B)。发现投射至CeA的CM神经元在Wake期ΔF/F为(1.08±0.12)%,在NREM期ΔF/F为(0.58±0.07)%,在REM期ΔF/F为(0.89±0.12)%(图 3D)。表明该群神经元在Wake期和REM期活跃,在NREM期活动水平较低(P < 0.05)。分析觉醒/睡眠转换期间的神经元活动变化,发现在Wake期向NREM期转换时,神经元活动降低(图 3E);NREM期向Wake期转换时,神经元活动明显升高(图 3F);REM期向Wake期转换时,神经元活动降低(图 3G);在NREM期向REM期转换时,神经元活动上升(图 3H)。以上结果表明CM-CeA通路在觉醒期和快速眼动睡眠期活跃。
|
| A:CM和CeA病毒注射示意图;B: 光纤及脑肌电电极埋置示意图;C:CM内感染GCamp7b及光纤记录典型代表图;D:特异性投射至CeA的CM神经元在觉醒/睡眠各状态下钙信号活动平均值Kruskal-Wallis单因素秩方差分析,a: P < 0.05,3组之间两两比较;E:Wake期向NREM期转换时投射至CeA的CM神经元钙信号活动变化Wilcoxon符号秩检验,c:P < 0.001,状态转换前后60 s比较;F:NREM期向Wake期转换时投射至CeA的CM神经元钙信号活动变化Wilcoxon符号秩检验,c:P < 0.001,状态转换前后60 s比较;G: REM期向Wake期转换时投射至CeA的CM神经元钙信号活动变化配对t检验,c:P < 0.001,状态转换前后60s比较;H:NREM期向REM期转换时投射至CeA的CM神经元钙信号活动变化Wilcoxon符号秩检验,c:P < 0.001,状态转换前后60 s比较 图 3 CM-CeA通路在觉醒/睡眠周期中的活动模式 |
2.4 Rh/Re-CeA通路在觉醒/睡眠周期中的活动模式
为了探索Rh/Re -CeA通路在觉醒/睡眠周期中的神经元活动特征,在CeA注射逆行标记病毒AAV2/retro-Syn-Cre,同时在菱形核与连接核(Rh/Re)注射Cre依赖的病毒AAV-EF1α-DIO-GCaMp7b(图 4A),标记特异性投射至CeA的Rh/Re神经元,并在病毒感染3~4周后在Rh/Re上方埋置光纤插芯用来记录神经元钙活动(图 4B)。在记录脑肌电的同时记录神经元钙信号活动,发现投射至CeA的Rh/Re神经元在Wake期ΔF/F为(0.29±0.02)%,在NREM期ΔF/F为(0.12±0.01)%,在REM期ΔF/F为(0.24±0.01)%(图 4D)。证明该群神经元在Wake期和REM期活跃,在NREM期活动水平较低(P < 0.05)。分析觉醒/睡眠转换期间的神经元活动变化,发现在Wake期向NREM期转换时,神经元活动降低(图 4E);NREM期向Wake期转换时,神经元活动明显升高(图 4F);REM期向Wake期转换时,神经元活动降低(图 4G);在NREM期向REM期转换时,神经元活动上升(图 4H)。以上结果表明Rh/Re -CeA通路在觉醒期和快速眼动睡眠期活跃。

|
| A:Rh/Re和CeA病毒注射示意图;B: 光纤及脑肌电电极埋置示意图;C:Rh/Re内感染GCamp7b及光纤记录典型代表图;D:特异性投射至CeA的Rh/Re神经元在觉醒/睡眠各状态下钙信号活动平均值Kruskal-Wallis单因素秩方差分析,a: P < 0.05,3组之间两两比较;E:Wake期向NREM期转换时投射至CeA的Rh/Re神经元钙信号活动变化Wilcoxon符号秩检验,c:P < 0.001,状态转换前后60s比较;F:NREM期向Wake期转换时投射至CeA的Rh/Re神经元钙信号活动变化Wilcoxon符号秩检验,c:P < 0.001,状态转换前后60 s比较;G: REM期向Wake期转换时投射至CeA的Rh/Re神经元钙信号活动变化Wilcoxon符号秩检验,c:P < 0.001,状态转换前后60 s比较;H:NREM期向REM期转换时投射至CeA的Rh/Re神经元钙信号活动变化配对t检验,c:P < 0.001,状态转换前后60 s比较 图 4 Rh/Re-CeA通路在觉醒/睡眠周期中的活动模式 |
2.5 不同中线丘脑-CeA通路在觉醒/睡眠周期中活动模式差异性的比较
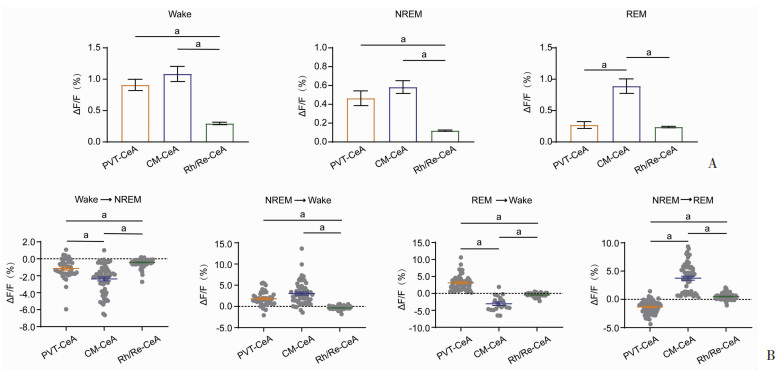
在对投射至CeA的中线丘脑各群神经元的光纤记录数据分析中发现不同神经元在觉醒/睡眠周期中的活动模式不同。在Wake期,投射至CeA的PVT和CM神经元活动水平较高;在NREM期投射至CeA的PVT和CM神经元活动水平比投射至CeA的Rh/Re神经元活动水平高;在REM期投射至CeA的CM神经元活动水平明显高于PVT和Rh/Re神经元活动水平(图 5A)。以上结果表明在Wake期PVT-CeA通路和CM-CeA通路比较活跃,在REM期CM-CeA通路更加活跃。与投射至CeA的PVT神经元和CM神经元相比,投射至CeA的Rh/Re神经元总体活动水平较低,可能是由于投射至CeA的Rh/Re神经元数量较少。
|
| A:在觉醒/睡眠周期不同状态下投射至CeA的中线丘脑各核团神经元钙信号活动模式对比;B:在觉醒/睡眠不同状态转换时投射至CeA的中线丘脑各核团神经元钙信号活动变化特征对比 a: P < 0.05 图 5 中线丘脑-中央杏仁核不同通路在觉醒/睡眠周期中活动特征 |
进一步对3条通路在觉醒/睡眠转换时神经元的钙信号变化模式进行对比,发现在Wake期向NREM期转换时,各群神经元活动均下降;在NREM期向Wake期转换时,投射至CeA的PVT神经元和CM神经元活动升高;在REM期向Wake期转换时,投射至CeA的PVT神经元活动升高,投射至CeA的CM神经元和Rh/Re神经元活动均下降,说明PVT神经元在Wake期比REM期的活动更高,而CM和Rh/Re神经元在REM期的活动水平比Wake期更高;在NREM期向REM期转换时,投射至CeA的PVT神经元活动下降,投射至CeA的CM神经元和Rh/Re神经元活动均上升,且CM神经元活动升高更明显(图 5B)。以上结果可以提示PVT-CeA通路在觉醒期更活跃;CM-CeA通路在觉醒期和快速眼动睡眠期都活跃,且在快速眼动睡眠期更活跃;Rh/Re-CeA通路整体活动水平较低,但在快速眼动睡眠期较活跃。
3 讨论觉醒作为人与其他动物进化上高度保守的行为,为其他活动提供基础支撑。觉醒由弥散分布于全脑的觉醒调控系统活动控制[19-20],其中中线丘脑在维持觉醒中起着至关重要的作用[7]。情绪活动是影响觉醒/睡眠状态的重要因素之一。如恐惧、焦虑[22]、抑郁[16]等觉醒依赖情绪信息可在REM睡眠期得以巩固,进而影响正常觉醒/睡眠周期。临床研究表明,负性情绪与睡眠障碍存在恶性循环关系[23],直接导致日间觉醒不良。杏仁核作为情绪整合的关键核团[24-26],是中线丘脑的重要输出靶区之一[27]。本研究首先利用逆行神经示踪技术,探究中线丘脑各神经核团和杏仁核各亚区之间形态学联系特征,并进一步记录了投射到CeA的中线丘脑不同神经元在觉醒/睡眠周期中的活动模式,为中线丘脑-杏仁核通路在觉醒/睡眠周期中的作用机制研究提供了基础。
杏仁核主要由CeA和BLA组成,其中CeA是恐惧信号生成和传导的中继站和输出站[28]。在本研究中,我们发现投射到CeA的中线丘脑核团(PVT与Rh/Re)神经元数量明显高于投射到BLA的神经元数量,提示中线丘脑与CeA形成了更为紧密的联系。光纤记录研究投射到CeA的中线丘脑神经元在自然觉醒/睡眠周期中活动模式,发现PVT-CeA通路在觉醒期活跃,其觉醒期活动水平显著高于NREM睡眠期与REM睡眠期。PVT-CeA通路与多种生理和病理相关情绪活动密切相关,如恐惧[14]、应激[29]、奖赏[14]、药物成瘾[30]和抑郁[16]等。由于情绪活动通常伴随觉醒水平变化,PVT-CeA通路在觉醒期的选择性高活动水平可能为该通路在调节觉醒依赖行为中发挥作用提供基础。电生理记录结果表明CM神经元在觉醒期和REM睡眠期神经元活动均较强,且REM期更为活跃。CM神经元的REM睡眠高活动驱动背内侧前额叶皮层微环路兴奋/抑制平衡变化,从而巩固REM睡眠相关的情绪记忆(Paradoxical somatodendritic decoupling supports cortical plasticity during REM sleep)[7, 31]。我们发现CM-CeA通路除在觉醒期表现出较高水平的活动外,其REM睡眠期活动水平明显高于NREM睡眠期,提示CM-CeA通路可能参与REM睡眠期的情绪记忆巩固。Rh/Re作为腹侧中线丘脑的重要组成部分,参与调节饥饿、应激[32]、焦虑[22]及光照周期相关行为(Importance of the ventral__midline thalamus in driving hippocampal functions)。此外,Rh/Re与认知系统重要结构海马及前额叶皮层形成双向联系,将前额叶皮层的输出信息中继至海马,从而协调前额叶皮层与海马之间的信息流动,完成睡眠期的记忆巩固[31, 33]。Rh/Re-CeA通路在觉醒期与REM睡眠期均表现出较高的活动水平,提示该通路可能同时参与Rh/Re调节的觉醒与睡眠相关行为功能。
本研究主要探讨了中线丘脑-杏仁核通路形态学特征并重点研究了中线丘脑-CeA通路在睡眠/觉醒周期中的活动模式。值得注意的是,中线丘脑同时也投射至BLA并参与调节重要的行为功能。例如,化学遗传学激活Rh/Re-BLA通路增加视觉天敌威胁诱发的本能防御反应,如冻结行为等[8]。然而,中线丘脑-BLA通路在睡眠/觉醒周期中的活动模式有待阐明。此外,本研究的逆行示踪实验结果表明投射至CeA的Rh/Re与CM神经元数量相似,但是CM-CeA通路钙信号活动水平明显高于Rh/Re-CeA通路活动水平。这可能是由于投射至CeA的Rh/Re神经元主要集中于Re近腹侧近第三脑室的位置,而GCaMP7b标记的投射至CeA的Rh/Re神经元集中于Re背侧部,从而导致神经元数量偏少,钙信号活动水平偏低。在未来的研究中,需进一步标记全部投射至CeA的Rh/Re神经元并记录其活动模式。
综上所述,本研究利用逆行神经示踪技术,观察了中线丘脑各神经核团与杏仁核各亚区之间的形态学联系特征,以及投射至CeA的中线丘脑各核团神经元在觉醒/睡眠中的活动模式。研究结果为中线丘脑在觉醒调控中的地位提供了形态学基础,为情绪调节异常导致的觉醒/睡眠障碍提供了新的环路方向。
| [1] |
BENTIVOGLIO M, BALERCIA G, KRUGER L. The specificity of the nonspecific thalamus: the midline nuclei[J]. Prog Brain Res, 1991, 87: 53-80. |
| [2] |
SU H S, BENTIVOGLIO M. Thalamic midline cell populations projecting to the nucleus accumbens, amygdala, and hippocampus in the rat[J]. J Comp Neurol, 1990, 297(4): 582-93. |
| [3] |
VERTES R P, LINLEY S B, HOOVER W B. Limbic circuitry of the midline thalamus[J]. Neurosci Biobehav Rev, 2015, 54. |
| [4] |
MÁTYÁS F, KOMLÓSI G, BABICZKY Á, et al. A highly collateralized thalamic cell type with arousal-predicting activity serves as a key hub for graded state transitions in the forebrain[J]. Nat Neurosci, 2018, 21(11): 1551-62. |
| [5] |
REN S, WANG Y, YUE F, et al. The paraventricular thalamus is a critical thalamic area for wakefulness[J]. Science, 2018, 362(6413): 429-34. |
| [6] |
HUA R, WANG X, CHEN X, et al. Calretinin neurons in the midline thalamus modulate starvation-induced arousal[J]. Curr Biol, 2018, 28(24): 3948-59. |
| [7] |
GENT T C, BANDARABADI M, HERRERA C G, et al. Thalamic dual control of sleep and wakefulness[J]. Nat Neurosci, 2018, 21(7): 974-84. |
| [8] |
SALAY L D, ISHIKO N, HUBERMAN A D. A midline thalamic circuit determines reactions to visual threat[J]. Nature, 2018, 557(7704): 183-9. |
| [9] |
VAN DER WERF Y D, WITTER M P, GROENEWEGEN H J. The intralaminar and midline nuclei of the thalamus. Anatomical and functional evidence for participation in processes of arousal and awareness[J]. Brain Res Brain Res Rev, 2002, 39(2-3): 107-40. |
| [10] |
VERTES R P, HOOVER W B, RODRIGUEZ J J. Projections of the central medial nucleus of the thalamus in the rat: node in cortical, striatal and limbic forebrain circuitry[J]. Neuroscience, 2012, 219: 120-36. |
| [11] |
KIROUAC G J. Placing the paraventricular nucleus of the thalamus within the brain circuits that control behavior[J]. Neurosci Biobehav Rev, 2015, 56: 315-29. |
| [12] |
KRABBE S, GRÜNDEMANN J, LVTHI A. Amygdala inhibitory circuits regulate associative fear conditioning[J]. Biological Psychiatry, 2018, 83(10): 800-9. |
| [13] |
PENZO M A, ROBERT V, TUCCIARONE J, et al. The paraventricular thalamus controls a central amygdala fear circuit[J]. Nature, 2015, 519(7544): 455-9. |
| [14] |
DO-MONTE F H, QUINONES-LARACUENTE K, QUIRK G J. A temporal shift in the circuits mediating retrieval of fear memory[J]. Nature, 2015, 519(7544): 460-3. |
| [15] |
HSU D T, KIROUAC G J, ZUBIETA J-K, et al. Contributions of the paraventricular thalamic nucleus in the regulation of stress, motivation, and mood[J]. Front Behav Neurosci, 2014, 8: 73. |
| [16] |
ZHAO D, LIU C, CUI M, et al. The paraventricular thalamus input to central amygdala controls depression-related behaviors[J]. Exp Neurol, 2021, 342: 113744. |
| [17] |
LIANG S H, ZHAO W J, YIN J B, et al. A neural circuit from thalamic paraventricular nucleus to central amygdala for the facilitation of neuropathic pain[J]. J Neurosci, 2020, 40(41): 7837-54. |
| [18] |
MCNALLY G P. Motivational competition and the paraventricular thalamus[J]. Neurosci Biobehav Rev, 2021, 125: 193-207. |
| [19] |
SCAMMELL T E, ARRIGONI E, LIPTON J O. Neural circuitry of wakefulness and sleep[J]. Neuron, 2017, 93(4): 747-65. |
| [20] |
BROWN R E, BASHEER R, MCKENNA J T, et al. Control of sleep and wakefulness[J]. Physiol Rev, 2012, 92(3): 1087-187. |
| [21] |
PACE-SCHOTT E F, GERMAIN A, MILAD M R. Effects of sleep on memory for conditioned fear and fear extinction[J]. Psychol Bull, 2015, 141(4): 835-57. |
| [22] |
LINLEY S B, ATHANASON A C, ROJAS A K P, et al. Role of the reuniens and rhomboid thalamic nuclei in anxiety-like avoidance behavior in the rat[J]. Hippocampus, 2021, 31(7): 756-69. |
| [23] |
BAUDUCCO S V, FLINK I K, JANSSON-FRöJMARK M, et al. Sleep duration and patterns in adolescents: correlates and the role of daily stressors[J]. Sleep Health, 2016, 2(3): 211-8. |
| [24] |
JANAK P H, TYE K M. From circuits to behaviour in the amygdala[J]. Nature, 2015, 517(7534): 284-92. |
| [25] |
GALLAGHER M, CHIBA A A. The amygdala and emotion[J]. Curr Opin Neurobiol, 1996, 6(2): 221-7. |
| [26] |
SMITH D M, TORREGROSSA M M. Valence encoding in the amygdala influences motivated behavior[J]. Behav Brain Res, 2021, 411: 113370. |
| [27] |
MA C, ZHONG P, LIU D, et al. Sleep regulation by neurotensinergic neurons in a thalamo-amygdala circuit[J]. Neuron, 2019, 103(2). |
| [28] |
FADOK J P, MARKOVIC M, TOVOTE P, et al. New perspectives on central amygdala function[J]. Curr Opin Neurobiol, 2018, 49: 141-7. |
| [29] |
PLIOTA P, BÖHM V, GRÖSSL F, et al. Stress peptides sensitize fear circuitry to promote passive coping[J]. Mol Psychiatry, 2020, 25(2): 428-41. |
| [30] |
KEYES P C, ADAMS E L, CHEN Z, et al. Orchestrating opiate-associated memories in thalamic circuits[J]. Neuron, 2020, 107(6). |
| [31] |
VYAZOVSKIY V V, OLCESE U, LAZIMY Y M, et al. Cortical firing and sleep homeostasis[J]. Neuron, 2009, 63(6): 865-78. |
| [32] |
QUET E, MAJCHRZAK M, COSQUER B, et al. The reuniens and rhomboid nuclei are necessary for contextual fear memory persistence in rats[J]. Brain Struct Funct, 2020, 225(3): 955-68. |
| [33] |
CASSEL J-C, PEREIRA DE VASCONCELOS A. Importance of the ventral midline thalamus in driving hippocampal functions[J]. Prog Brain Res, 2015, 219: 145-61. |




