我国临床用血的需求量以每年10%~15%的速度增长,但人口献血率仅为0.84%,临床用血量的增加超过人群献血量的增加,导致用血紧张[1]。而控制性降压作为围术期血液保护措施中的常见方法之一,现已广泛应用于颅脑肿瘤、脊柱外科、髋关节等较易出血手术以及鼻内镜、关节镜等术野要求较高的手术[2]以减少出血、改善手术视野。然而,术中低血压麻醉可能导致脑低灌注和随后的脑缺血性损伤,如苏醒延迟、脑卒中、术后谵妄和术后认知功能障碍[3]。而脑卒中是一种严重的并发症,其在非心血管手术患者的发生率为0.1%~0.8%,且其风险与低血压以及低血压持续时间相关[4],可导致手术后死亡率增加8倍[5]。因此术中有效监测防止脑缺血缺氧对患者预后至关重要。
硝普钠作为控制性降压最常见的药物之一,起效快、时效短(半衰期约3~4 min)[6-7],对动静脉平滑肌均有直接扩张作用,不影响心肌收缩,以往文献报道,使用硝普钠行控制性降压可以增加脑血流量或保持其不变[8],但这些研究主要是通过经颅多普勒超声进行评估的,其通过测量大脑中动脉血流速度来反应脑血流量且需要假定血管直径不变[8],但研究表明,单纯使用脑血流速度评估脑血流量是不准确的,因为大脑中动脉也具有血管舒缩活性,血管直径对脑血流量也会产生很大的作用[9]且其反应的是大脑大动脉的灌注而无法反应微循环灌注情况。而氧立见(oxygen to see, O2C)作为反应微循环灌注和氧合的监测仪器已用于各种人体手术, 如外周动脉闭塞性疾病、胃肠道、心肌和移植手术,且该项技术在检测脑外科术中局部脑血流(regional cerebral blood flow, rCBF)、局部脑组织氧饱和度(regional cerebral oxygen saturation,rSO2)和血红蛋白浓度(regional cerebral haemoglobin,rHb)已得到有效验证[10]。与传统仅能监测脑血流量或脑氧合的大脑监测仪器如经颅多普勒超声[8]、近红外光谱脑氧监测[11]相比,其监测更精确更全面。由于猪生理功能与人较为相似[12],为控制性降压模型提供了良好的选择。本研究拟在硝普钠降压下采用O2C仪器监测不同降压幅度下猪大脑rCBF与rSO2的变化情况。
1 材料和方法 1.1 实验动物健康雌性长白猪6头,4~6月龄,体重23.5±0.6 (22~25) kg,由陆军军医大学动物实验中心提供。所有实验猪在单独的通风笼内饲养,在笼内适应一周;在麻醉前禁食12 h, 禁饮4 h。该实验方案通过了陆军军医大学伦理委员会动物实验伦理(AMUWEC20212142) 审核。
1.2 麻醉与管理实验前用盐酸赛拉嗪注射液(2~3 mg/kg)(批号070031777, 敦化市圣达动物药品有限公司)肌注镇静并吸入七氟醚(批号:9Y071,Maruishi Pharmaceutical Co. ltd, 日本)麻醉诱导,行心电监护以及外周氧饱和度(peripheral capillary oxygen saturation, SpO2)监测(深圳理邦,elite V8)。随后插入气管导管(如图 1A)并连接呼吸机,调整呼吸参数(潮气量8~10 mg/kg,通气频率16~20次/min,FiO2调整为25%~30%),呼吸回路与气管导管之间连接气体采样管监测呼气末气体浓度(深圳迈瑞WATOEX-65麻醉机)。通过超声(华声Naviu深圳市沃霖电子有限公司)引导下行股动静脉穿刺置管用于连续监测有创动脉血压以及中心静脉压指导补液和用药(如图 1B)。整个实验过程中使用加温毯并监测体温保持猪体温在38~39 ℃。术中全凭吸入麻醉药七氟醚维持麻醉(1~1.5 MAC),辅以适量的肌肉松弛剂苯磺酸顺阿曲库铵(批号H20203700,南京健友生化制药股份有限公司),整个实验由同一名临床经验丰富的麻醉医师实施麻醉以确保足够的麻醉深度。准备完毕后将实验猪取俯卧位固定于试验架上。

|
| A: 猪人工气道建立; B: 超声引导下血管穿刺 图 1 气管插管和血管穿刺 |
1.3 大脑微循环和脑氧合测量方法
本研究采用O2C仪器(德国MedizinTechnik)对脑微循环和氧合进行评估,其可以向组织发射830 nm的连续激光和500~800 nm的白光,在组织表面通过探针中的光纤采集信号来测量rCBF、rSO2和rHb[13]。与近红外光谱相比,O2C光谱不能穿透颅骨,必须与相应部位的脑组织近距离接触才能反应脑组织微循环的情况,因此本研究需要凿开颅骨至硬脑膜,并放入探针(探测深度约1.5 mm)才能准确反应脑组织微循环状况(如图 2)。为了消除环境光的干扰,实验在暗室中进行。

|
| 图 2 探针固定 |
1.4 数据采集
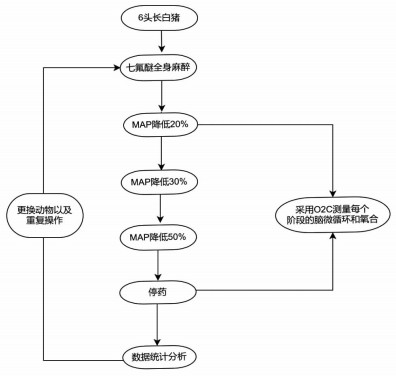
在七氟醚全麻维持下,固定探针并进行校准,随后记录血压平稳后的rCBF、rSO2、rHb、平均动脉压(mean arterial pressure, MAP)、心率(heart rate, HR)、SpO2作为基础值,然后通过股静脉持续泵入硝普钠进行控制性降压,从高到低依次降压,记录3个降压幅度(较基础MAP下降20%、30%、50%,分别对应轻、中、重度降压)下每一个降压幅度血压稳定后5、10、15 min相关指标以及药物泵注速度,然后记录停药后5、10、15 min的相关指标、血压恢复时间以及整个降压过程中脑缺氧事件的发生情况(rSO2较基线值下降20%或绝对值降低至50%[14])。降压过程中MAP保持在目标血压的±5 mmHg范围内。流程如图 3。
|
| 图 3 实验流程图 |
1.5 统计分析
本研究采用SPSS 24.0统计软件进行数据分析,计量资料以x±s表示,各降压幅度下的rCBF、rSO2、HR、SpO2等指标与自身基线进行配对t检验以分析各降压幅度下的变化情况,若不满足正态分布,则使用Wilcoxon符号秩和检验。两变量间的相关关系采用Pearson相关性分析, 若不满足正态分布,则使用Spearman相关性分析。并采用多元线性回归分析不同因素对rSO2的影响,以P < 0.05表示差异具有统计学意义。
2 结果 2.1 不同低血压所需硝普钠维持剂量硝普钠诱导20%、30%、50%的降压幅度时,需持续输注的平均速率分别为2.2±0.7 μg·kg-1·min-1、5.2±1.3 μg·kg-1·min-1、10.7±2.9 μg·kg-1·min-1。
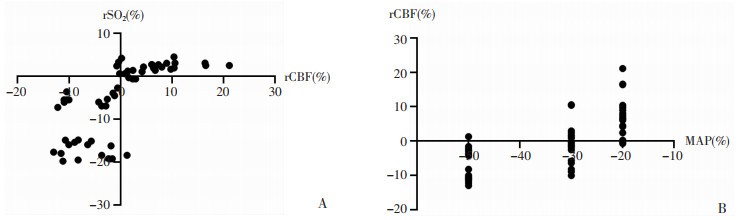
2.2 rCBF与rSO2、MAP的相关性分析整个降压过程中rCBF与rSO2的相关性较好(r=0.843),且MAP与rCBF的相关性也较好(r=0.793),图 4。
|
| A: rSO2与rCBF变化百分比的相关性;B: MAP与rCBF变化百分比的相关性 图 4 rCBF与rSO2、MAP的相关性分析 |
2.3 不同因素与rSO2的线性回归分析
本次分析纳入了rCBF、MAP、降压时间、心率、rHb等变量,经逐步回归分析,仅MAP、rHb和rCBF 3个因素有统计学意义,即rSO2与MAP、rHb和rCBF呈线性相关(R2=0.853,P < 0.05)(表 1),且与rSO2的线性相关程度依次为rHb>MAP>rCBF。
| 指标 | 未标准化系数 | 标准化系数 | P值 | |||
| B | 标准误差 | Beta | t值 | |||
| (常量) | 0.027 | 0.018 | 1.506 | 0.138 | ||
| rHb | 2.044 | 0.207 | 0.670 | 9.877 | 0.000 | |
| MAP | 0.137 | 0.054 | 0.209 | 2.518 | 0.015 | |
| rCBF | 0.170 | 0.084 | 0.168 | 2.023 | 0.048 | |
| a. 因变量:rSO2;b. 回归模型Y=0.027+2.044X1+0.137X2+0.170X3(Y表示rSO2,X1、X2、X3分别为rHb、MAP、rCBF); c.R2=0.853 | ||||||
2.4 不同血压下rCBF与rSO2的变化以及脑缺氧发生情况
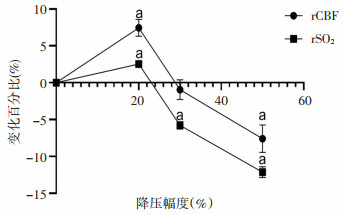
与基线值相比,在降压20%时,rCBF和rSO2明显增加(P < 0.05),平均分别增加约7.4%和2.5%,图 5;降压30%时,rCBF相较于基线值下降不显著(约0.9%) (P>0.05),而rSO2较基线值下降5.8%(P < 0.05);降压50%时,rCBF和rSO2较基线值分别下降约7.6%(P < 0.05)和12.1%(P < 0.05)。在整个降压过程中未出现脑缺氧事件。
|
| a: P < 0.05, 与基线值相比 图 5 不同降压幅度下的rCBF和rSO2的百分比变化 |
2.5 不同血压下HR、SpO2变化
在降压幅度为20%时,与基线值相比,SpO2差异无统计学意义(P>0.05)(表 2);在降压30%、50%时,SpO2相较于基线值下降(P < 0.05)。而HR除了在降压50%的10 min、15 min差异无统计学意义外,其余降压幅度HR较基线值下降(P < 0.05)。
| 变量 | 时间/min | MAP/mmhg | HR | SpO2 |
| 基线值 | 73.9±7.5 | 81.0±14.5 | 99.0±0.8 | |
| 降压20% | 5 | 57.2±7.1a | 80.3±14.8a | 99.1±1.0 |
| 10 | 57.6±6.3a | 80.1±14.6a | 99.0±1.1 | |
| 15 | 57.6±7.0a | 80.0±14.7a | 99.1±1.0 | |
| 降压30% | 5 | 48.4±5.6a | 79.1±14.6a | 98.0±1.7a |
| 10 | 48.9±5.8a | 78.8±14.2a | 98.0±1.7a | |
| 15 | 49.2±6.1a | 78.8±14.2a | 98.0±1.7a | |
| 降压50% | 5 | 39.5±2.9a | 79.8±17.0a | 98.4±1.4a |
| 10 | 39.6±3.4a | 80.0±16.9 | 98.4±1.3a | |
| 15 | 39.8±3.8a | 80.3±17.6 | 98.6±1.4a | |
| a: P < 0.05,与各自基线值相比 | ||||
2.6 停药后rCBF与rSO2、HR、SpO2变化
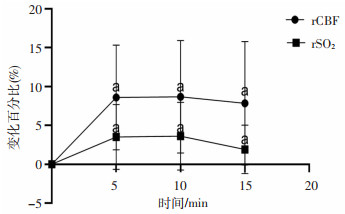
停药后rCBF与rSO2不同时间相较于基线值均增加(P < 0.05)(如图 6)。停药后至血压恢复时的SpO2较基线值差异无统计学意义(P>0.05)(表 3);停药后不同时间HR较基线值轻微下降(P < 0.05)。血压恢复基线时间为(5.8±1.3)min。
|
| a: P < 0.05, 与基线值相比 图 6 停药后rCBF与rSO2变化情况 |
| 变量 | 时间/min | MAP /mmhg |
HR | SpO2 |
| 基线值 | 73.9±7.5 | 81.0±14.5 | 99±0.8 | |
| 停药后 | 5 | 79.9±10.9a | 79.4±14.4a | 99.3±0.7 |
| 10 | 83.2±11.3a | 79.6±14.6a | 99±1.4 | |
| 15 | 84.7±11.8a | 79.2±14.5a | 99±1.4 | |
| 血压恢复 | 76.0±10.0a | 79.7±15.0a | 99.3±0.7 | |
| a: P < 0.05,与基线值相比 | ||||
3 讨论
控制性降压过程中,不合理的降压可能会导致脑灌注不足,引发脑缺血缺氧,而传统上根据MAP来反映脑灌注并不准确,因为在一定范围内降压,大脑自主调节(cerebral autoregulation,CA)可以维持脑血流的相对稳定,且有研究表明血压本身并不是一个可靠的组织灌注指标,即使MAP降低,脑组织并不一定会缺血缺氧[15]。本研究结果显示,血压可能并不是反应脑灌注的可靠指标,因为在轻度降压时rCBF和rSO2与MAP呈负相关,即随着血压的下降,rCBF和rSO2反而增加;中度降压时rCBF下降无统计学意义但rSO2明显下降;重度降压时,rCBF和rSO2与MAP变化较一致,均下降。在整个降压过程中,即使是重度降压也未出现脑缺氧事件。此外,我们观察到硝普钠降压过程中HR先下降后上升但变化幅度较小无临床意义,而SpO2在中度降压时才开始下降,下降幅度较小且未出现缺氧。停药后MAP、SpO2迅速恢复基线附近,而rCBF和rSO2增加。
目前评估脑灌注主要有经颅多普勒超声、激光多普勒血流测量、正电子发射断层扫描、功能磁共振成像等现代技术[16]以及基于近红外光谱的rSO2测量[11]。OLESEN等[8]采用经颅多普勒超声评估大脑中动脉血流平均速度,结果表明MAP下降20%~30%,CBF保持不变,这与本研究中降压30%结果较为一致,但本研究中所使用的技术反映的是大脑微循环的血流量,与经颅多普勒超声反应大脑大动脉血流量有所不同。一项前瞻性观察性队列研究采用经颅多普勒超声评估血流量,其建议为减少脑缺血的风险术中MAP应不低于60 mmhg(较基础降低约40%)[17],这与本研究的MAP降至50%也较安全有所不同。此外,SCHUMANN-BARD P等[18]在狒狒上进行控制性降压(MAP较基线值降低50%),通过正电子发射断层扫描评估局部脑血流量,结果表明硝普钠导致rCBF增加,这与本研究降压20%时的结果一致,而降压50%时,rCBF明显下降。有文献报道,MAP和rSO2之间存在中度的互相关,MAP降低至55~60 mmHg(相当于较基线MAP降低29%~42%), 手术中脑氧合下降不显著[19],而本研究也显示MAP与rSO2中度相关,但在降压30%,rSO2便开始下降,但下降幅度较小(约5.8%),且尚未达到脑缺氧标准。
在轻度降压时,rCBF和rSO2增加。rCBF的增加除了与使用硝普钠引起心输出量的增加有关[8]外,还可能与硝普钠释放的NO的直接扩血管作用有关[8]。虽然CO2对rCBF的影响较大,但是本研究中的PaCO2维持在35~45 mmHg的正常范围内,同时所使用的麻醉药七氟醚并不影响CO2反应性[13],对rCBF和rSO2也没有明显的影响[13, 20],且七氟醚的MAC维持在0.3和1.5之间不影响健康个体的脑血管反应性[21], 本研究便控制在1~1.5 MAC之间。此外,硝普钠诱导的低血压可以降低大脑CO2反应性[22],这些因素均最大限度的减少了对rCBF和rSO2的影响。但第一次降压实验时出现rCBF增加而rSO2反而下降的情况,这可能与硝普钠扩张肺血管导致肺动脉压下降使肺组织灌注减少而降低动脉氧合[23]等有关,此外,还可能与输液过多导致的血液稀释有关[24],而中度降压时rCBF下降不明显而rSO2明显下降,可能也与上述原因有关。在中度降压时,rCBF下降不显著呈现出CA,但整个控制性降压过程中,除了降压30%时可能存在CA外,其他降压幅度下均未观察到经典的CA,这可能与硝普钠削弱CA有关,但有文献报道硝普钠本身并不影响CA[25]。有研究显示CA主要涉及大脑中动脉以及颈内动脉等大血管[26],但本研究表明微血管可能也参与CA,这与以往的研究结果不同[20]。重度降压时,rCBF与rSO2均下降,这可能是因为硝普钠对脑血管的扩张作用不足以抵消脑灌注的减少所致。rSO2通常可接受范围是55%~80%,但对于脑缺氧并没有明确的界定,通常认为是rSO2较基线值下降20%或绝对值降低至50%[14],但CETIN等[27]建议将rSO2低于基线值15%~20%时作为预测脑缺血的最佳阈值,本研究中,即使降压50%,rSO2降低也不到15%,这说明使用硝普钠降压是较安全的。但一项大型回顾性队列研究表明MAP < 60 mmHg(约较基线MAP降低约42%)超过20分钟与急性缺血性脑卒中的风险增加独立相关[4],本研究为防止重度低血压(降压50%)以及低血压持续时间对脑组织带来的损伤而影响特定低血压下对脑微循环和氧合测量的干扰,我们在三个降压幅度下均选择在20 min内的三个时间点(5、10、15 min)采集脑微循环和氧合数据。因此,术中应用重度降压时应严格控制使用时间以免造成脑组织损伤。
但本研究中存在着一定的缺陷,PaCO2控制的范围较大,因为即使是CO2的微小变化也会对CBF产生很大的影响[28]。有研究表明,七氟醚麻醉下,rCBF随着CO2升高而升高[13],且有研究显示PaCO2从35 mmHg变化至45 mmHg(即10 mmHg)使rCBF增加了30%至45%[10]。此外,该研究的控制性降压是在全凭吸入麻醉的情况下进行的,与临床上常用的全凭静脉和静吸复合麻醉有所不同,未能探索在此类情况下控制性降压对脑微循环的影响。
术中使用硝普钠进行控制性降压时,即使降压50%时,rSO2下降幅度仍维持在15%以内,不易导致术中脑组织缺血缺氧,对维持大脑灌注和氧合具有一定的作用。但降压20%时,rCBF增加,可能不利于颅内压增高的患者。
| [1] |
周素. 临床用血的影响因素及需求量预测研究进展[J]. 华夏医学, 2014, 27(5): 144-148. ZHOU S. Research advance on the influence factors and demand prediction in clinical blooduse[J]. Acta Med Sin, 2014, 27(5): 144-148. |
| [2] |
DROVER D R, HAMMER G B, BARRETT J S, et al. Evaluation of sodiumnitroprusside for controlled hypotension in children during surgery[J]. Front Pharmacol, 2015, 6: 136. |
| [3] |
ZHANG L, YU Y, XUE J, et al. Effect of deliberate hypotension on regional cerebral oxygen saturation during functional endoscopic sinus surgery: a randomized controlledtrial[J]. Front Surg, 2021, 8: 681471. |
| [4] |
MAZZEFFI M, CHOW J H, ANDERS M, et al. Intraoperative hypotension and perioperative acute ischemic stroke in patients having major elective non-cardiovascular non-neurological surgery[J]. J Anesth, 2021, 35(2): 246-253. |
| [5] |
MASHOUR G A, SHANKS A M, KHETERPAL S. Perioperative stroke and associated mortality after noncardiac, nonneurologic surgery[J]. Anesthesiology, 2011, 114(6): 1289-1296. |
| [6] |
ZHANG D, LI R, CHEN MM, et al. Photoacoustic imaging of in vivo hemodynamic responses to sodium nitroprusside[J]. J Biophotonics, 2021, 14(7): e202000478. |
| [7] |
COBB A, THORNTON L. Sodiumnitroprusside as a hyperinflation drug and therapeutic alternatives[J]. J Pharm Pract, 2018, 31(4): 374-381. |
| [8] |
OLESEN N D, FISCHER M, SECHER N H. Sodiumnitroprusside dilates cerebral vessels and enhances internal carotid artery flow in young men[J]. J Physiol, 2018, 596(17): 3967-3976. |
| [9] |
JARRETT C L, SHIELDS K L, BROXTERMAN R M, et al. Imaging transcranial Doppler ultrasound to measure middle cerebral artery blood flow: the importance of measuring vessel diameter[J]. Am J Physiol Regul Integr Comp Physiol, 2020, 319(1): R33-R42. |
| [10] |
KLEIN K U, SCHRAMM P, GLASER M, et al. Intraoperative monitoring of cerebral microcirculation and oxygenation: a feasibility study using a novel photo-spectrometric laser-Doppler flowmetry[J]. J Neurosurg Anesthesiol, 2010, 22(1): 38-45. |
| [11] |
VANPETEGHEM C M, BRUNEEL B Y, LECOUTERE I M, et al. Ephedrine and phenylephrine induce opposite changes in cerebral andparaspinal tissue oxygen saturation, measured with near-infrared spectroscopy: a randomized controlled trial[J]. J Clin Monit Comput, 2020, 34(2): 253-259. |
| [12] |
GASTHUYS E, VANDECASTEELE T, DE BRUYNE P, et al. The potential use of piglets as human pediatric surrogate for preclinical pharmacokinetic and pharmacodynamic drug testing[J]. Curr Pharm Des, 2016, 22(26): 4069-4085. |
| [13] |
KLEIN K U, GLASER M, REISCH R, et al. The effects of arterial carbon dioxide partial pressure and sevoflurane on capillary venous cerebral blood flow and oxygen saturation during craniotomy[J]. Anesth Analg, 2009, 109(1): 199-204. |
| [14] |
NATARAJAN P, GUHABISWAS R, SAHA A, et al. Persistent cerebral desaturation on near-infrared spectroscopy without neurological insult[J]. Indian J Anaesth, 2018, 62(8): 643-645. |
| [15] |
VAN NOORD B A, STALKER C L, ROFFEY P, et al. The use of regional cerebraloximetry monitoring during controlled hypotension: a case series[J]. J Clin Monit Comput, 2014, 28(3): 319-323. |
| [16] |
MIKKELSEN M L G, AMBRUS R, MILES J E, et al. Effect of propofol and remifentanil on cerebral perfusion and oxygenation in pigs: a systematic review[J]. Acta Vet Scand, 2016, 58(1): 42. |
| [17] |
HA T N, VAN RENEN R G, LUDBROOK G L, et al. The relationship between hypotension, cerebral flow, and the surgical field during endoscopic sinussurgery[J]. Laryngoscope, 2014, 124(10): 2224-2230. |
| [18] |
SCHUMANN-BARD P, TOUZANI O, YOUNG A R, et al. Cerebrovascular effects of sodium nitroprusside in the anaesthetized baboon: a positron emission tomographic study[J]. J Cereb Blood Flow Metab, 2005, 25(4): 535-544. |
| [19] |
FARZANEGAN B, ERAGHI M G, ABDOLLAHI S, et al. Evaluation of cerebral oxygen saturation during hypotensive anesthesia in functional endoscopic sinus surgery[J]. JAnaesthesiol Clin Pharmacol, 2018, 34(4): 503-506. |
| [20] |
KIMME P, LEDIN T, SJÖBERG F. Dose effect of sevoflurane and isoflurane anesthetics on cortical blood flow during controlled hypotension in the pig[J]. Acta Anaesthesiol Scand, 2007, 51(5): 607-613. |
| [21] |
GOETTEL N, PATET C, ROSSI A, et al. Monitoring of cerebral blood flow autoregulation in adults undergoing sevoflurane anesthesia: a prospective cohort study of two age groups[J]. J Clin Monit Comput, 2016, 30(3): 255-264. |
| [22] |
MATTA B F, LAM A M, MAYBERG T S, et al. Cerebrovascular response to carbon dioxide during sodiumnitroprusside- and isoflurane-induced hypotension[J]. Br J Anaesth, 1995, 74(3): 296-300. |
| [23] |
BUTTERWORTH J F, MACKEY D C, WASNICK J D. Morgan & Mikhail's clinical anesthesiology[M]. 6th ed. New York: McGraw-Hill Education LLC, 2018: 438-444.
|
| [24] |
CHOI S H, LEE S J, JUNG Y S, et al. Nitroglycerin- andnicardipine-induced hypotension does not affect cerebral oxygen saturation and postoperative cognitive function in patients undergoing orthognathic surgery[J]. J Oral Maxillofac Surg, 2008, 66(10): 2104-2109. |
| [25] |
LAVI S, EGBARYA R, LAVI R, et al. Role of nitric oxide in the regulation of cerebral blood flow inhumans[J]. Circulation, 2003, 107(14): 1901-1905. |
| [26] |
LIU J, ZHU Y S, HILL C, et al. Cerebral autoregulation of blood velocity and volumetric flow during steady-state changes in arterial pressure[J]. Hypertension, 2013, 62(5): 973-979. |
| [27] |
CETIN M, BIRBICER H, HALLIOGLU O, et al. Comparative study between the effects of dexmedetomidine and propofol on cerebral oxygenation during sedation at pediatric cardiac catheterization[J]. Ann Card Anaesth, 2016, 19(1): 20-24. |
| [28] |
DE JONG D L K, TARUMI T, LIU J, et al. Lack of linear correlation between dynamic and steady-state cerebralautoregulation[J]. J Physiol, 2017, 595(16): 5623-5636. |




