2. 400016 重庆,重庆医科大学医学数据研究院
2. Institute of Medical Data Sciences, Chongqing Medical University, Chongqing, 400016, China
胼胝体(corpus callosum,CC)是大脑半球中最大的连合纤维,它联系两侧大脑半球从而使大脑成为一个功能整体,在大脑半球的连接中起着至关重要的作用。过去很多临床工作者认为大脑灰质及其深部的核团才是认知活动的基础,而CC仅仅是一个连接的结构,直到1940年外科医生通过胼胝体切开术控制了癫痫的发作证实CC可能是两侧大脑半球间的主要通路[1],CC才引起了临床医生更多的关注。胼胝体体积或厚度的改变可能是发育或者多种疾病过程的结果,如巨脑回畸形、多小脑回畸形、缺氧缺血性脑病、急性创伤、多发性硬化[2-3]等,而且儿童胼胝体发育不全的转归并不固定[4],因此胼胝体在核磁共振(magnetic resonance imaging,MRI)上的结构的改变可能是儿科中枢神经系统疾病的一个特征性的表现[5]。
由于儿童生长发育的特殊性,大脑结构随着年龄的增长有所变化。目前缺乏儿童胼胝体结构的参考范围,临床影像诊断中经常存在无法判断儿童胼胝体是否存在形态异常、异常主要是存在于哪一个亚区、是偏厚抑或偏薄等困惑;影像诊断医师凭临床经验大致判断,缺乏确切、客观的理论依据。此外,既往的研究主要是测量正中矢状位层面的CC面积[6-7]并非体积,而单一的面积测量其临床意义相对比较局限。因此,建立不同年龄/性别的儿童胼胝体参考范围的需求尤为亟迫。本研究通过招募正常学龄前儿童行脑部MRI的3DT1序列扫描,利用FreeSurfer软件自动提取正常学龄前儿童的CC数据并计算其体积,在初步构建学龄前各年龄段、不同性别儿童CC体积的参考范围的基础上,探讨其CC体积变化的特征。
1 资料与方法 1.1 研究对象本研究由重庆医科大学附属儿童医院放射科于2018年3月至2019年3月在重庆市公开共招募100名2~6岁的正常志愿者儿童,监护人签署知情同意书,并先后完成一般调查问卷、体格检查、Gesell发育量表(Gesell Developmental Scale,GDS)测试及头颅MRI检查,依据纳入标准和排除标准最终共纳入89名儿童研究,对不同性别、不同年龄段学龄前儿童的胼胝体体积参考范围进行描述性研究。
本研究得到重庆医科大学附属儿童医院医学伦理委员会的批准[(2018)年伦审(研)第(82)号],所有入组志愿者在监护人在知晓本研究目的与具体操作流程后,签署了知情同意书。
1.1.1 纳入标准① 所有监护人知情同意并签署知情同意书;②监护人完成一般问卷调查;③志愿者完成一般体格检查,包括身高、体质量、BMI、脑部MRI扫描和GDS测试。
1.1.2 排除标准① 一般问卷调查显示有认知障碍表现、癫痫及其他神经系统疾病史,有明确的颅脑外伤史,近3个月有急性或慢性感染疾病;②MRI图像质量较差或发现有明显器质性疾病;③GDS测试任一能区得分<75分。
1.1.3 退出和终止标准① 有明显MRI检查禁忌证(如幽闭恐惧症、体内含有不能取出的金属物植入等)。②检查过程中出现任何不适,导致检查不能继续进行的。
1.2 研究方法 1.2.1 一般情况问卷采用自编量表了解被试者的一般人口学资料(性别、年龄、民族)、既往史等。
1.2.2 一般体格检查评估指标及评估标准均在MRI检查当天由完成统一培训的医师对正常儿童进行体格测量,采用电子秤测量:体质量测值精确到0.1 kg,身高测值精确到0.1 cm,参照2006年WHO儿童生长发育评价标准,数据以x±s表示。
1.2.3 GDS智力测试及评估标准由经过专门培训的5名医师在患儿检查当天且未镇静情况下完成测试,评估环境1人1室,测试时间50~60 min。
1.2.4 镇静方式被试者经过6~8 h的睡眠剥夺,口服10% 水合氯醛0.5 mL/kg,最大剂量≤10 mL。
1.2.5 影像学数据的采集使用荷兰Phillps公司的Achieva 3.0T超导磁共振(PhillpsAchieva 3.0T MR),8通道头颅正交线圈。常规序列包括轴位T1W1、T2W1、T2FLAIR及矢状位T2WI,排除明显的神经系统器质性疾病。解剖结构像:矢状位三维扰相梯度回波序列(three-dimensional spoiled gradient echo,3D-SPGR),具体参数如下:重复时间(TR)=7.7 ms;回波时间(TE)=3.8 ms;翻转角8°;视野(FOV):256 mm×256 mm;矩阵250×250;体素=1 mm×1 mm×1 mm;层厚=1 mm;扫描时间共2 min 35 s,共156幅。
1.2.6 MRI图像分析常规序列图像分析由1位中级职称医师及1位高级职称医师共同完成。3DT1序列使用FREESURFER v6.0(http://surfer.nmr.mgh.harvard.edu/)软件进行分析。FreeSurfer是基于MRI的3DT1薄层图像利用一系列的算法来量化大脑的结构以及功能,自动提取并计算大脑皮层的结构指标。Fischl(2012)[8-9]的出版物和参考文献中详细描述了该程序的使用细节和说明[8]。按照Freesurfer的步骤处理每个受试者的3D-SPGR MRI数据,包括体积处理和表面处理两部分。
1.2.6.1 体积处理步骤包括:运动校正→Talairach转换→非均匀变形→强度归一化→颅骨剥离→注册→CA强度归一化→CA非线性体积注册→体积标签→强度归一化→白质分割→白质ASeg编辑→填充和切割等,共13步。
1.2.6.2 表面处理步骤包括:镶嵌→平滑→膨胀→自动拓扑结构校正→欧拉数→平滑→膨胀→最后冲浪→皮质带状面具→球形变形→球形注册→将平均曲率映射到主体→皮层取消(标记)→皮层注销统计等,共17步。
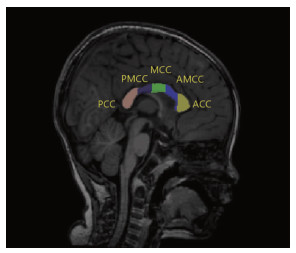
以上各步均由软件自动完成。每位受试者的胼胝体沿长轴方向被自动等分为5个解剖学亚区:胼胝体前部(anterior corpus callosum,ACC)、胼胝体前中部(anterior-middle corpus callosum,AMCC)、胼胝体中部(middle corpus callosum,MCC)、胼胝体中后部(mid-posterior corpus callosum,PMCC)、胼胝体后部(posterior corpus callosum,PCC),见图 1。CC总体积(total corpus callosum,TCC)的体积是这五个亚区的体积之和。脑总体积(total brain volume,TBV)由Freesurfer估算得出,包括除小脑和脑干以外的一切组织。
|
| 利用FreeSurferV6.0软件将胼胝体沿长轴方向等分为5个解剖学亚区:胼胝体前部(anterior corpus callosum,ACC)、胼胝体前中部(anterior-middle corpus callosum,AMCC)、胼胝体中部(middle corpus callosum,MCC)、胼胝体中后部(mid-posterior corpus callosum,PMCC)、胼胝体后部(posterior corpus callosum,PCC) 图 1 胼胝体在MRI正中矢状位层面的分区 |
1.3 统计学分析
利用Excel 2007软件对收集的数据进行双人核对录入,采用IBM SPSS 22.0统计软件进行数据分析。首先对计量资料进行正态性分布分析(K-S检验),符合正态分布数据以x±s表示,组间比较采取t检验或方差分析;非正态分布数据以M(P25~P75)表示,组间比较采用Mann-Whitney U或Kruskal-Wallis检验。计数资料采用频次(%)表示,多组间差异比较先进行总体crosstable分析,以确定整体水平多组间是否存在显著性差异,若存在显著性差异则用χ2分割检验进行两两比较以确定具体的组间差异。相关性检验采用Pearson(正态资料)或Spearman(非正态或等级资料)检验。参考值范围取95%CI,以P < 0.05认为差异具有统计学意义。
2 结果 2.1 纳入研究儿童的基本资料本研究实际共计招募研究对象100例,1例GDS测试5个能区DQ均<75分、4例未能满意镇静而未完成MR检查、3例MR图像存在运动伪影、1例常规MRI序列发现髓鞘化障碍、1例后遗软化改变及1例透明隔囊肿而剔除,最终纳入89例。其中男性49例(55.1%),女性40例(44.9%);24~72(51.18±20.09)月龄,各年龄段男性及女性所占比例的差异无统计学意义(χ2= 5.726,P=0.126)见表 1。
| 年龄段 | 男性(n=49) | 女性(n=40) | 合计 |
| 24~36个月 | 14(28.6) | 8(20.0) | 22(24.7) |
| 36~48个月 | 5(10.2) | 12(30.0) | 17(19.1) |
| 48~60个月 | 10(20.4) | 6(15.0) | 16(18.0) |
| 60~72个月 | 20(40.8) | 14(35.0) | 34(38.2) |
| χ2 | 5.726 | ||
| P | 0.126 | ||
2.2 CC及各亚区体积与年龄、性别的关系 2.2.1 CC及各亚区体积与年龄的相关性分析
为排除性别对年龄与CC各亚区体积相关性的交叉影响,研究首先比较男性和女性的年龄分布发现差异无统计学意义(P=0.632)。将CC各亚区的体积与年龄进行相关性分析发现:PCC(r=0.250)、PMCC(r=0.450)、MCC(r=0.344)、AMCC(r=0.257)及TCC(r=0.373)与年龄呈正相关性(P < 0.05),而ACC体积与年龄则未显示相关性(r= 0.155,P=0.148)。
2.2.2 不同性别间CC各亚区体积的差异分析不同性别间CC各亚区体积的差异分析结果见表 2,结果显示不同性别间的CC各亚区体积的差异无统计学意义(P>0.05)。
| 性别 | n | PCC | PMCC | MCC | AMCC | ACC | TCC |
| 男性 | 49 | 693.08±146.98 | 390.65±108.31 | 472.59±124.56 | 464.13±129.57 | 752.80±148.03 | 2773.26±516.17 |
| 女性 | 40 | 721.03±114.85 | 395.08±84.56 | 481.80±123.18 | 483.87±108.69 | 746.08±109.24 | 2827.87±364.54 |
| t | -0.982 | -0.211 | -0.349 | -0.768 | 0.239 | -0.654 | |
| P | 0.329 | 0.833 | 0.728 | 0.445 | 0.812 | 0.574 | |
| PCC:胼胝体后部;PMCC:胼胝体中后部;MCC:胼胝体中部;AMCC:胼胝体前中部;AMCC:胼胝体前部;TCC:总胼胝体 | |||||||
2.2.3 依据年龄段对比分析不同性别间CC及各亚区体积的差异
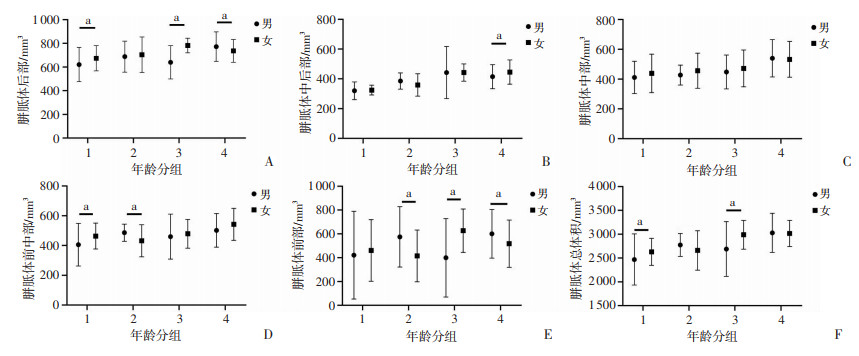
为明确CC各亚区体积是否存在性别差异,依据年龄段对比分析不同性别间CC各亚区体积的差异,见图 2。
|
|
a:P < 0.05 A:胼胝体后部;B:胼胝体中后部;C:胼胝体中部;D:胼胝体前中部;E:胼胝体前部;F:胼胝体总体积 1:24~36个月(n=22);2:36~48个月(n=17);3:48~60个月(n=16);4:60~72月(n=34) 图 2 各年龄组儿童不同性别的CC各亚区体积差异(x±s) |
2.2.3.1 PCC的体积
24~36、48~60个月组中女性的体积显著大于男性,60~72个月组女性显著低于男性;差异存在统计学意义(P < 0.05)。而36~48个月组男、女性差异无统计学意义(P>0.05)。
2.2.3.2 PMCC的体积60~72个月女性较男性显著增高,差异具有统计学意义(P < 0.05);而24~36、48~60及36~48个月组男、女性之间的差异无统计学意义(P>0.05)。
2.2.3.3 MCC的体积各年龄段,男、女性之间MCC的体积差异均无统计学意义(P>0.05)。
2.2.3.4 AMCC的体积24~36个月组女性较男性显著增高,36~48个月组女性较男性显著降低,差异存在统计学意义(P < 0.05)。而48~60、60~72个月组男、女性之间的差异无统计学意义(P>0.05)。
2.2.3.5 ACC的体积36~48、60~72个月组女性较男性显著降低,48~60个月组女性较男性显著增高,差异存在统计学意义(P < 0.05)。而24~36个月组男、女性之间差异无统计学意义(P>0.05)。
2.2.3.6 TCC的体积24~36、48~60个月女性较男性显著增高,差异存在统计学意义(P < 0.05)。36~ 48、60~72个月组男、女性之间差异无统计学意义(P>0.05)。
2.3 各年龄段不同性别儿童CC各亚区参考范围CC各亚区体积参考值范围取各年龄段相对应性别95%CI,具体见表 3~8,可知在24~72个月正常儿童中,男性和女性在CC各部分体积的差异均无统计学意义(P>0.05)。
| 年龄段 | 男性(n=49) | 女性(n=40) | |||
| 均值 | 95%CI | 均值 | 95%CI | ||
| 24~36个月 | 674.06 | 537.22~704.36 | 674.06 | 585.36~762.76 | |
| 36~48个月 | 687.58 | 525.52~849.64 | 703.89 | 608.32~799.46 | |
| 48~60个月 | 639.52 | 538.85~740.19 | 782.22 | 717.60~846.84 | |
| 60~72个月 | 771.85 | 713.81~829.88 | 736.36 | 680.68~792.04 | |
| 年龄段 | 男性(n=49) | 女性(n=40) | |||
| 均值 | 95%CI | 均值 | 95%CI | ||
| 24~36个月 | 320.41 | 286.23~354.59 | 324.44 | 296.92~351.96 | |
| 36~48个月 | 385.82 | 317.84~453.80 | 359.10 | 311.02~407.18 | |
| 48~60个月 | 442.61 | 317.99~567.23 | 407.18 | 382.32~503.42 | |
| 60~72个月 | 415.05 | 377.19~452.91 | 445.81 | 398.72~492.90 | |
| 年龄段 | 男性(n=49) | 女性(n=40) | |||
| 均值 | 95%CI | 均值 | 95%CI | ||
| 24~36个月 | 411.06 | 348.53~473.60 | 438.46 | 330.66~546.27 | |
| 36~48个月 | 426.74 | 343.39~510.09 | 456.58 | 381.99~531.16 | |
| 48~60个月 | 447.61 | 366.35~528.87 | 471.45 | 341.93~600.97 | |
| 60~72个月 | 539.61 | 480.94~598.27 | 532.63 | 463.16~602.09 | |
| 年龄段 | 男性(n=49) | 女性(n=40) | |||
| 均值 | 95%CI | 均值 | 95%CI | ||
| 24~36个月 | 405.75 | 323.06~488.44 | 463.19 | 390.44~535.94 | |
| 36~48个月 | 486.12 | 414.55~557.69 | 432.01 | 363.77~500.24 | |
| 48~60个月 | 459.75 | 351.73~567.77 | 478.67 | 377.27~580.07 | |
| 60~72个月 | 501.70 | 448.87~554.53 | 542.37 | 480.27~604.47 | |
| 年龄段 | 男性(n=49) | 女性(n=40) | |||
| 均值 | 95%CI | 均值 | 95%CI | ||
| 24~36个月 | 710.66 | 604.32~817.01 | 730.46 | 622.51~838.41 | |
| 36~48个月 | 787.42 | 630.40~944.44 | 707.82 | 638.66~776.97 | |
| 48~60个月 | 699.71 | 581.79~817.63 | 813.37 | 717.99~908.74 | |
| 60~72个月 | 800.19 | 752.38~847.99 | 758.96 | 701.65~816.28 | |
| 年龄段 | 男性(n=49) | 女性(n=40) | |||
| 均值 | 95%CI | 均值 | 95%CI | ||
| 24~36个月 | 2 468.68 | 2 159.33~2 778.03 | 2 630.61 | 2 393.46~2 867.77 | |
| 36~48个月 | 2 773.68 | 2 475.69~3 071.67 | 2 659.39 | 2 397.30~2 921.48 | |
| 48~60个月 | 2 689.20 | 2 277.75~3 100.65 | 2 988.57 | 2 670.65~3 306.49 | |
| 60~72个月 | 3 028.39 | 2 836.97~3 219.80 | 3 016.13 | 2 857.13~3 175.13 | |
3 讨论 3.1 构建学龄前儿童胼胝体参考范围的价值
CC是由神经纤维组成的白质纤维束,主要起将大脑半球连接的作用。目前关于CC的研究几乎存在于神经系统相关的各个领域。在神经退行性疾病或炎症性疾病,如阿尔茨海默病[10-12]和多发性硬化[13-14]中均发现有CC体积的变化。有研究发现具有精神病症状和局限性精神病的CC面积和厚度均显著减小[15],此外也有多项研究发现CC可能与精神分裂症[16-17]、阅读障碍[18]、癫痫[19]、抑郁症[20]等相关,常见的临床症状如吸烟、酒精中毒[16]等也可能伴随CC面积的变化。上述关于CC的研究主要是来自于成人,而儿童CC的相关研究比较有限。有研究[21]报道胼胝体发育不全的儿童生活质量低下和睡眠问题均为较为普遍存在的,YOUNG等[22]研究发现儿童在遭受虐待后CC的体积会减小。GIULIANO等[23]也提到在现有的数据资料中,6岁以下正常儿童的CC数据极其缺乏,尤其是缺乏正常儿童的资料。本研究首次在招募的正常儿童脑部MRI数据基础上制订学龄前各年龄段、不同性别儿童CC体积的参考范围,为儿科影像的临床工作提供一定的参照,为后续神经发育障碍疾病的临床和基础研究提供参照依据。
3.2 学龄前儿童胼胝体各个亚区的发育本研究结果显示:2~6岁正常儿童的CC总体积以及CC的4个亚区包括PCC、PMCC、MCC、AMCC的体积均与年龄呈正相关,而ACC体积与年龄则未显示相关性。这可能跟CC的发育方向有一定的关系,CC的发育方向是由前向后发育(不同于大脑由后向前发育),提示可能在2岁时ACC已经完成发育,体积相对比较恒定。而PCC、PMCC、MCC、AMCC的体积在2~6岁的阶段内仍随年龄的增长而逐步发育。因此我们认为在2岁时虽然90%的大脑白质髓鞘化进程已经完成,但是在2~6岁的阶段内CC的发育仍在进行,体积仍有变化,而且各个亚区的发育进程不一致,这就意味着我们对学龄前儿童CC的研究,尤其是发育进程、发育类疾病相关的CC的研究,更应该细化CC的分区来研究。DTI的分析研究认为CC各个亚区的投射纤维和连接的功能并不一致,腹侧和背侧前额叶等高级别认知的皮层主要通过膝部投射纤维,顶叶和枕叶纤维主要通过CC的压部投射,比如视觉中枢等,而来自感觉运动皮层的纤维主要通过体部投射[24],因此我们认为胼胝体分区研究和分析也非常有必要。
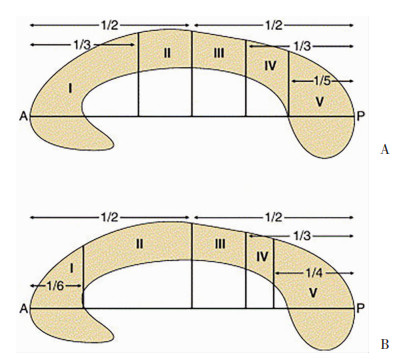
3.3 胼胝体的脑部MRI分区目前关于CC的分区没有统一的方法。临床上常将CC由前到后大致分为嘴、膝、体和压部[25-26],各区域间并没有明确的解剖界定。文献中提到了以下几种常用的分区方法。HOFER法[26]是将CC分为5个不等分的亚区,首先划出CC的最长横径(即CC的最前端与最后端之间的距离),沿最长横径,前1/6为CC-1区,CC前1/2部去除CC-1为CC-2区,后1/2部去除后1/3部为CC-3区,后1/3部去除后1/4为CC-4区,后1/4部为CC-5区。WITELSON[27]基于神经组学研究提出了与Hofer类似的胼胝体分区方法,是目前应用较广泛的胼胝体细分方案之一(图 3)。还有学者在不同文献中提出依照CC的前后径将其不等分为5分区、7分区和9分区,也有以扇形分割CC的方法。VACHET等[28]提出测量CC的长度及厚度并依照长度分区,并且还提出了胼胝体各部的连接范围:1区连接前额叶;2区连接前/辅助运动皮层;3区连接运动皮层;4区连接感觉皮层;5区连接顶/颞/枕叶的皮层。本次研究我们根据FreeSurfer软件将胼胝体等分为5个亚区进行分析,期望对其所连接相应脑区的疾病的分析和判断能有相对精确的依据。
3.4 学龄前儿童胼胝体各亚区体积的性别差异
本研究结果显示:24~36、36~48、48~60、60~72个月等4个年龄段,不同性别、CC各个亚区的体积差异不一致。比如,在MCC,男、女性在各个年龄段均无明显差异。但是在AMCC,24~36、36~48个月组男、女性有差异,48~60、60~72个月组男、女性无明显差异。而在ACC的分析中,24~36个月各年龄段、性别间无明显差异,而36~48、48~60、60~72个月年龄段却存在较明显的性别差异,等等。因此我们认为在2~6岁儿童中,不同年龄段性别对CC的某些亚区的体积有影响,但是也有某些亚区性别对其体积没有影响,这可能跟我们的样本量有关系,但这也提示在学龄前儿童CC的体积研究中,我们很有必要根据年龄及性别来进行分析和参考。
本次研究仍具有一定的局限性,招募的志愿者数量有限,后续我们还将继续扩大样本量,并基于大样本人群的CC图像,利用人工智能构造正常儿童CC的模型,并推广应用于临床,期望能为儿科影像的临床工作提供一定的参照。
| [1] |
VAN WAGENEN W P. Surgical division of commissural pathways in the corpus callosum[J]. Arch NeurPsych, 1940, 44(4): 740. |
| [2] |
HENGST M, TVCKE J, ZERRES K, et al. Megalencephaly, mega corpus callosum, and complete lack of motor development: Delineation of a rare syndrome[J]. Am J Med Genet A, 2010, 152A(9): 2360-2364. |
| [3] |
BINDU P S, TALY A B, SINHA S, et al. Mega-corpus callosum, polymicrogyria, and psychomotor retardation syndrome[J]. Pediatr Neurol, 2010, 42(2): 129-132. |
| [4] |
RAILE V, HERZ N A, PROMNITZ G, et al. Clinical outcome of children with corpus callosum agenesis[J]. Pediatr Neurol, 2020, 112: 47-52. |
| [5] |
ANDRONIKOU S, PILLAY T, GABUZA L, et al. Corpus callosum thickness in children: an MR pattern-recognition approach on the midsagittal image[J]. Pediatr Radiol, 2015, 45(2): 258-272. |
| [6] |
ZHAO Y Q, WANG F, WANG C J, et al. MRI in differential diagnosis and prognostic evaluation of reversible splenial lesion syndrome and ischemic cerebral infarction in adults[J]. J Hebei Med Univ, 2021, 42(02): 209-213. |
| [7] |
周陶成, 童光磊, 李旭, 等. 孤独症谱系障碍患儿胼胝体面积与神经行为障碍的相关性研究[J]. 中国基层医药, 2020, 27(22): 2708-2712. ZHOU T C, TONG G L, LI X, et al. Research on the correlation between corpus callosum area and neurobehavioral disorders in children with autism spectrum disorders[J]. Chin J Prim Med Pharm, 2020, 27(22): 2708-2712. |
| [8] |
FISCHL B. FreeSurfer[J]. NeuroImage, 2012, 62(2): 774-781. |
| [9] |
FUJIHARA K, TAKEI Y. FreeSurfer as a platform for associating brain structure with function[J]. Brain Nerve, 2018, 70(7): 841-848. |
| [10] |
GOLD B T, JOHNSON N F, POWELL D K, et al. White matter integrity and vulnerability to Alzheimer's disease: preliminary findings and future directions[J]. Biochim Biophys Acta, 2012, 1822(3): 416-422. |
| [11] |
RADANOVIC M, PEREIRA F R S, STELLA F, et al. White matter abnormalities associated with Alzheimer's disease and mild cognitive impairment: a critical review of MRI studies[J]. Expert Rev Neurother, 2013, 13(5): 483-493. |
| [12] |
RASGON N, ANANTH J, MENA I, et al. Agenesis of corpus callosum and dementia of the Alzheimer'S type: a review and case report[J]. Can J Psychiatry, 1994, 39(7): 429-432. |
| [13] |
GARG N, REDDEL S W, MILLER D H, et al. The corpus callosum in the diagnosis of multiple sclerosis and other CNS demyelinating and inflammatory diseases[J]. J Neurol Neurosurg Psychiatry, 2015, 86(12): 1374-1382. |
| [14] |
DE KOUCHKOVSKY I, FIEREMANS E, FLEYSHER L, et al. Quantification of normal-appearing white matter tract integrity in multiple sclerosis: a diffusion kurtosis imaging study[J]. J Neurol, 2016, 263(6): 1146-1155. |
| [15] |
PRENDERGAST D M, KARLSGODT K H, FALES C L, et al. Corpus callosum shape and morphology in youth across the psychosis Spectrum[J]. Schizophr Res, 2018, 199: 266-273. |
| [16] |
BACHMANN S, PANTEL J, FLENDER A, et al. Corpus callosum in first-episode patients with schizophrenia: a magnetic resonance imaging study[J]. Psychol Med, 2003, 33(6): 1019-1027. |
| [17] |
MONNIG M A, THAYER R E, CAPRIHAN A, et al. White matter integrity is associated with alcohol cue reactivity in heavy drinkers[J]. Brain Behav, 2014, 4(2): 158-170. |
| [18] |
ELNAKIB A, SOLIMAN A, NITZKEN M, et al. Magnetic resonance imaging findings for dyslexia: a review[J]. J Biomed Nanotechnol, 2014, 10(10): 2778-2805. |
| [19] |
UNTERBERGER I, BAUER R, WALSER G, et al. Corpus callosum and epilepsies[J]. Seizure, 2016, 37: 55-60. |
| [20] |
WALTERFANG M, YVCEL M, BARTON S, et al. Corpus callosum size and shape in individuals with current and past depression[J]. J Affect Disord, 2009, 115(3): 411-420. |
| [21] |
INGRAM D G, CHURCHILL S S. Sleep problems in children with agenesis of the corpus callosum[J]. Pediatr Neurol, 2017, 67: 85-90. |
| [22] |
YOUNG D A, NEYLAN T C, CHAO L L, et al. Child abuse interacts with hippocampal and corpus callosum volume on psychophysiological response to startling auditory stimuli in a sample of veterans[J]. J Psychiatr Res, 2019, 111: 16-23. |
| [23] |
GIULIANO A, SAVIOZZI I, BRAMBILLA P, et al. The effect of age, sex and clinical features on the volume of Corpus Callosum in pre-schoolers with Autism Spectrum Disorder: a case-control study[J]. Eur J Neurosci, 2018, 47(6): 568-578. |
| [24] |
PARK H J, KIM J J, LEE S K, et al. Corpus callosal connection mapping using cortical gray matter parcellation and DT-MRI[J]. Hum Brain Mapp, 2008, 29(5): 503-516. |
| [25] |
BLAAUW J, MEINERS L C. The splenium of the corpus callosum: embryology, anatomy, function and imaging with pathophysiological hypothesis[J]. Neuroradiology, 2020, 62(5): 563-585. |
| [26] |
HOFER S, FRAHM J. Topography of the human corpus callosum revisited-Comprehensive fiber tractography using diffusion tensor magnetic resonance imaging[J]. NeuroImage, 2006, 32(3): 989-994. |
| [27] |
WITELSON S F. Hand and sex differences in the isthmus and genu of the human corpus callosum. A postmortem morphological study[J]. Brain, 1989, 112(Pt 3): 799-835. |
| [28] |
VACHET C, YVERNAULT B, BHATT K, et al. Automatic corpus callosum segmentation using a deformable active Fourier contour model[C]//SPIE Medical Imaging. Proc SPIE 8317, Medical Imaging 2012: Biomedical applications in molecular, structural, and functional imaging, San Diego, California, USA. 2012, 8317: 79-85. DOI: 10.1117/12.911504.
|