2. 400042 重庆,陆军特色医学中心:病理科
2. Department of Pathology, Army Medical Center of PLA, Chongqing, 400042, China
上尿路尿路上皮癌(upper tract urothelial carcinoma,UTUC)是发生于肾盂或输尿管尿路上皮的恶性肿瘤中最常见的一种病理类型,在欧美人群中其发病率占所有尿路上皮癌的5%~10%[1-2];而在国人中占9.3%~29.9%[3]。虽然UTUC比膀胱癌发病率低,但由于其发生于肾盂或输尿管的狭小腔道内,加之部分病例又缺乏典型临床表现,增加了UTUC发病早期的隐匿性,容易被忽视或漏诊,导致在初次诊断时的临床分期比膀胱癌晚,54.0%~65.9%已发展为肌层浸润阶段,手术治疗后复发、转移风险高,影响患者长期生存[2, 4-6]。因此,早期发现与诊断对于UTUC的治疗及预后至关重要。
目前UTUC的诊断主要是基于输尿管镜检+活检、影像学、尿液基细胞学。输尿管镜检+活检是治疗前明确诊断的重要方式,不仅能在镜下观察上尿路的具体情况,还能取样获得组织病理学依据;但该方式存在以下问题:①有创,对于非癌患者术后可能导致粘连狭窄;②对于上尿路存在解剖变异或尿路重建史时镜检困难;③可能因活检样本较小而出现假阴性结果[7];④有增加根治性肾输尿管切除术后膀胱内复发的风险[8]。因此,目前输尿管镜检+活检在UTUC诊断中的应用有一定争议。影像学主要包括CTU及MRU,尽管敏感性较高[9],但容易遗漏微小及扁平肿瘤,并且对于软组织病变的定性诊断存在一定局限,也缺乏病理学依据。尿液基细胞学是基于细胞形态学的病理诊断,最大优势为相对简单、无创,同时诊断特异性高(80%~100%),但是其诊断敏感性受病理医师主观经验等因素影响,在各个中心间存在差异,为21%~80%[10];因此,相当一部分尿液基细胞学阴性患者存在漏诊风险。
DNA倍体分析是通过测定细胞DNA含量或倍体来评估是否为肿瘤;既往已有较多研究将DNA倍体分析应用于宫颈癌、肺癌、膀胱癌等肿瘤的诊断中[11-13],但DNA倍体应用于UTUC检测中研究较少,国内3项小样本研究[14-16]报道的敏感性为60.0%~77.1%,特异性为95.5%~100.0%。荧光原位杂交(fluorescence in situ hybridization,FISH)作为另外一种无创的检查手段,是根据细胞染色体变异来判断是否为肿瘤;在临床应用中表现出了可观的敏感性(52%~100%)与特异性(33%~96%)[10];多数研究指出其敏感性优于液基细胞学,特异性与液基细胞学相当,国内指南也将FISH列为在有条件单位可选择的UTUC的辅助诊断手段。基于以上问题,本研究采用本单中心UTUC患者数据,分析基于尿液无创的液基细胞学、DNA倍体及FISH在UTUC患者中单独及联合诊断的价值。
1 资料与方法 1.1 临床资料连续纳入本中心2013年1月至2021年6月影像学可疑UTUC的患者,排除合并膀胱癌、术前3个月内无尿液基细胞学、无组织病理检测结果者。共纳入246例患者,其中组织病理证实为UTUC 190例、非肿瘤病变43例、其他类型肿瘤13例;246例均有自然排尿标本的液基细胞学结果,其中178例有DNA倍体分析结果、167例有FISH结果,11例同时有肾盂输尿管冲洗尿的液基细胞学结果;纳入患者均行CT、MRI或膀胱镜排除膀胱癌。本研究经本单位伦理委员会审核通过[医研伦审(2018)第96号]。
1.2 诊断方法及结果判定 1.2.1 标本制作收集患者清晨清洁中段尿液约100 mL, 将尿液倒入离心管内,将尿样离心后弃上清液,在沉淀内加入适量缓冲液后得到细胞悬液;取部分细胞悬液,采用沉降式液基薄层技术制成1张薄层细胞片,用于HE染色进行细胞学检查;另取部分细胞悬液采用涂片离心机制成1张薄层细胞片,用于DNA染色程序(Feulgen染色法),然后用细胞DNA定量自动分析系统(武汉兰丁医学高科技有限公司)对玻片进行扫描。收集患者清晨清洁中段尿约200 mL,经反复离心、冲洗及固定液固定后,采用北京金普嘉医疗科技有限公司提供的FISH DNA探针和DAPI复染剂进行原位杂交及复染后在荧光显微镜下进行观察。
1.2.2 液基细胞学诊断[15]结果分为4类,Ⅰ类:未见肿瘤细胞,Ⅱ类:查见少量异型细胞,Ⅲ类:查见可疑癌细胞,Ⅳ类:查见癌细胞,其中以Ⅳ类为阳性,Ⅰ类、Ⅱ类和Ⅲ类为阴性。
1.2.3 DNA倍体分析[15]所有Feulgen染色片用DNA定量自动分析系统进行扫描处理,系统可对每张玻片上6 000个以上细胞核进行扫描测定,经扫描后的每个细胞核均有123个特征值,系统根据不同细胞成分所具有的不同特征来完成自动细胞分类和计数。以正常尿路上皮细胞为对照,所测出的平均光密度为2C的参考值,计算各个细胞的DNA含量,并以DNA指数(DI)表示,DI=DNA含量/2。正常细胞DI值多为1左右,增生细胞或疑似癌变细胞1<DI<2.5,DI≥2.5提示细胞癌变,并称之为异倍体细胞。系统所做的分析结果分为3级,Ⅰ级:以正常二倍体细胞为主,未见异倍体细胞以及异倍体细胞峰;Ⅱ级:可见少量DNA倍体异常细胞(1~2个细胞,DI≥2.5);Ⅲ级:可见大量DNA倍体异常细胞(3个及以上细胞,DI≥2.5)以及异倍体细胞峰。其中DI≥2.5以上的标本玻片需经细胞诊断医师在显微镜下进行核实,以排除系统将垃圾和重叠的细胞核误认为癌细胞或异常细胞。将Ⅰ级视为阴性,Ⅱ级和Ⅲ级视为阳性。
1.2.4 FISH[17]计数信号包括CSP3(绿色)、CSP7(红色)、CSP17(绿色)、GLP16(红色),计数100个细胞,正常细胞各个探针均可见2个信号,异常信号在3号、7号、17号染色体主要表现为多体(CSP3、CSP7及CSP17信号≥3个),在GLP16主要表现为缺失(GLP16信号≤1个),检测指标大于等于阈值(CSP3、CSP7、CSP17、GLP16≥15%),则认为该单项探针阳性;在CSP3、CSP7及CSP17中出现至少2个探针阳性、或者出现单独GLP16阳性则判定为FISH阳性,否则视为阴性。
1.2.5 组织病理以组织病理结果为金标准,活检或外科切除手术中所获取的组织标本行HE染色观察,以尿路上皮癌为阳性,非肿瘤病变为阴性。UTUC分级参考WHO2004版标准,分期参考UICC2017版标准。
1.3 统计学分析分别计算液基细胞学、DNA倍体及FISH三者单独及联合后的敏感性、特异性、阳性预测值、阴性预测值。敏感性=真阳性/(真阳性+假阴性),是在组织病理诊断为UTUC的患者中,经诊断试验检测为阳性者所占的比例;特异性=真阴性/(真阴性+假阳性),是在组织病理诊断为非肿瘤病变的患者中,经诊断试验检测为阴性者所占的比例;阳性预测值=真阳性/(真阳性+假阳性),是在诊断试验检测为阳性的患者中,经组织病理诊断为UTUC者所占的比例;阴性预测值=真阴性/(真阴性+假阴性),是在诊断试验检测为阴性的患者中,经组织病理诊断为非肿瘤病变者所占的比例。采用χ2检验比较不同检测方法敏感性差异,采用χ2检验比较三者联合(任一阳性)与细胞学单独诊断的特异性差异;采用受试者工作特征曲线(receiver operating characteristic curve,ROC曲线)进行关联分析。使用SPSS23.0统计软件,不符合正态分布的计量资料以中位数M(Q1~Q3)表示,检验水准α=0.05。
2 结果 2.1 246例患者临床特征共纳入246例影像学可疑UTUC患者,包含190例尿路上皮癌、43例非肿瘤和13例其他类型肿瘤;各组患者临床特点见表 1。在43例非肿瘤患者中,以输尿管炎性狭窄最为多见,有26例;在13例其他类型肿瘤中以原发于肾盂的肿瘤多见,有6例;见表 2。
| 临床特征 | 尿路上皮癌 (n=190) |
非肿瘤 (n=43) |
其他类型肿瘤 (n=13) |
| 年龄/岁 | 67(58~75) | 45(38~61) | 63(48~68) |
| 性别 | |||
| 男 | 126(66.3) | 13(30.2) | 9(69.2) |
| 女 | 64(33.7) | 30(69.8) | 4(30.8) |
| 临床症状 | |||
| 无痛肉眼血尿 | 127(66.8) | 8(18.6) | 5(38.5) |
| 血尿伴腰腹部疼痛 | 20(10.6) | 4(9.3) | 0(0.0) |
| 腰腹部疼痛 | 26(13.7) | 24(55.8) | 5(38.5) |
| 无/其他 | 17(8.9) | 7(16.3) | 3(23.0) |
| 肾积水 | |||
| 有 | 127(66.8) | 36(83.7) | 11(84.6) |
| 无 | 63(33.2) | 7(16.3) | 3(15.4) |
| 肿瘤/病变位置 | |||
| 肾盂/肾脏 | 107(56.3) | 7(16.3) | 8(61.5) |
| 肾盂及输尿管 | 15(7.9) | 2(4.7)a | 0(0.0) |
| 输尿管 | 68(35.8) | 34(79.0) | 5(38.5) |
| 病理分级 | |||
| 低级别 | 28(14.7) | ||
| 高级别 | 162(85.3) | ||
| 病理分期 | |||
| Ta | 17(8.9) | ||
| T1 | 57(30.0) | ||
| T2 | 34(17.9) | ||
| T3 | 75(39.5) | ||
| T4 | 7(3.7) | ||
| a: 2例为肾盂输尿管连接部梗阻(ureteropelvic junction obstruction,UPJO) | |||
| 组织病理类型 | 例数 |
| 非肿瘤病例 | 43 |
| 输尿管炎性狭窄 | 26 |
| 输尿管子宫内膜异位症 | 2 |
| 输尿管息肉 | 5 |
| UPJO | 2 |
| 肾囊肿伴出血 | 3 |
| 输尿管结核 | 1 |
| 肾海绵状血管瘤 | 1 |
| 节段性肾埂死 | 1 |
| 肾积脓 | 1 |
| 肾盂黏膜炎性增生 | 1 |
| 其他类型肿瘤病例 | 13 |
| 肾盂鳞癌 | 2 |
| 肾盂/输尿管腺癌 | 2a |
| 肾盂肉瘤化癌 | 1 |
| 肾盂软组织肌上皮癌 | 1 |
| 输尿管平滑肌肉瘤 | 1 |
| 输尿管转移性腺癌 | 3 |
| 肾盂黏膜下平滑肌瘤 | 1 |
| 肾细胞癌 | 2 |
| a: 肾盂及输尿管腺癌各1例 | |
2.2 三种诊断方法单独及联用的准确性评价及比较
自然排尿标本的液基细胞学、DNA倍体及FISH的敏感性分别为:44.7%、82.2%、57.9%,特异性分别为97.7%、82.4%、92.3%,阳性预测值分别为:98.8%、94.9%、97.5%,阴性预测值分别:28.6%、53.9%、30.0%。将液基细胞学与FISH联合诊断(两者任一阳性),敏感性为75.2%;将液基细胞学与DNA倍体联合诊断(两者任一阳性),敏感性为85.9%;将DNA倍体与FISH联合诊断(两者任一阳性),敏感性为92.8%;再将三种方法联合诊断(三者任一阳性),敏感性为93.8%,见表 3。三者联合后的敏感性与单独液基细胞学比较,χ2=65.214,P < 0.001,与单独DNA倍体比较,χ2=6.737,P=0.009,与单独FISH比较,χ2=36.755,P < 0.001,差异均有统计学意义。三种方法对不同病理分级的UTUC的敏感性比较,液基细胞学、DNA倍体及FISH对于高级别UTUC的敏感性分别为:48.1%、87.7%、60.7%,均高于低级别UTUC,对应P值分别为:0.023、P < 0.001、0.078,见表 4。UTUC患者中有7例自然排尿的液基细胞学结果虽为阴性,但通过取肾盂输尿管冲洗尿样,再次行液基细胞学检查,其中2例结果为阳性;在我们非肿瘤病例中有4例自然排尿的液基细胞学结果为阴性,但因结合影像仍怀疑UTUC,也采集了肾盂输尿管冲洗尿样再次行液基细胞学检查,结果均为阴性。
| 检查方法 | 敏感性 | 特异性 | 阳性预测值 | 阴性预测值 |
| 液基细胞学 | 44.7%(85/190)a | 97.7%(42/43)a | 98.8%(85/86) | 28.6%(42/147) |
| FISH | 57.9%(77/133)a | 92.3%(24/26) | 97.5%(77/79) | 30.0%(24/80) |
| DNA倍体 | 82.2%(111/135)a | 82.4%(28/34) | 94.9%(111/117) | 53.9%(28/52) |
| 液基细胞学+FISH | 75.2%(100/133) | 88.5%(23/26) | 97.1%(100/103) | 41.1%(23/56) |
| 液基细胞学+DNA倍体 | 85.9%(116/135) | 79.4%(27/34) | 94.3%(116/123) | 58.7%(27/46) |
| FISH+DNA倍体 | 92.8%(90/97) | 81.0%(17/21) | 95.7%(90/94) | 70.8%(17/24) |
| 液基细胞学+FISH+ DNA倍体 | 93.8%(91/97) | 76.2%(16/21) | 94.8%(91/96) | 72.7%(16/22) |
| a: P < 0.05,与液基细胞学+FISH+DNA倍体比较 | ||||
| 检查方法 | 低级别 | 高级别 | χ2值 | P值 |
| 液基细胞学 | 25.0%(7/28) | 48.1%(78/162) | 5.174 | 0.023 |
| FISH | 37.5%(6/16) | 60.7%(71/117) | 3.103 | 0.078 |
| DNA倍体 | 52.4%(11/21) | 87.7%(100/114) | 12.829 | <0.001 |
尽管三者联合(任一阳性)可提高诊断敏感性,但同时导致其诊断特异性下降至76.2%, 与液基细胞学单独使用时比较,χ2=5.345,P=0.021。我们将任意两者同时阳性作为诊断UTUC的标准(两者均阴性或仅一者阳性视为阴性)时,这种联合诊断方法的阳性预测值及特异性均为100%。详见表 5。
| 检查方法 | 敏感性 | 特异性 | 阳性预测值 | 阴性预测值 |
| 液基细胞学+FISH | 30.8%(41/133) | 100.0%(26/26) | 100.0%(41/41) | 22.0%(26/118) |
| 液基细胞学+DNA倍体 | 48.9%(66/135) | 100.0%(34/34) | 100.0%(66/66) | 33.0%(34/103) |
| FISH+DNA倍体 | 49.5%(48/97) | 100.0%(21/21) | 100.0%(48/48) | 30.0%(21/70) |
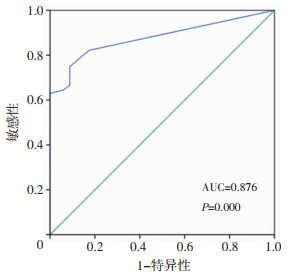
本研究86例液基细胞学检查阳性患者中有1例假阳性,组织病理为输尿管炎性狭窄,DNA倍体及FISH均阴性;79例FISH阳性患者中有2例假阳性,组织病理分别为左肾节段性梗死、右肾海绵状血管瘤,均为单独P16缺失,液基细胞学及DNA倍体均阴性。117例DNA倍体阳性患者中有6例假阳性,组织病理分别为2例输尿管息肉、2例输尿管炎性狭窄、1例肾盂黏膜炎性增生、1例UPJO,异倍体细胞数目均较少(1~8个),6例患者液基细胞学均阴性,2例患者FISH阴性,另外4例缺乏FISH结果。将DNA异倍体细胞数目与是否为UTUC进行关联分析,采用ROC曲线取最佳阈值,曲线下面积(area under the curve,AUC)为0.876,见图 1,最大约登指数(66.0%)对应的阈值≥ 2.5个异倍体细胞,敏感性为74.8%,特异性为91.2%。
|
| 图 1 UTUC患者异倍体细胞数目最佳阈值的ROC分析 |
2.3 其他类型肿瘤的检出情况
在其他类型的上尿路肿瘤中有3例液基细胞学阳性,组织病理证实为2例肾细胞癌和1例输尿管转移性腺癌;有6例DNA倍体阳性,组织病理证实为2例输尿管转移性腺癌、1例肾盂鳞癌、1例肾盂软组织肌上皮癌、1例肾细胞癌及1例肾盂黏膜下平滑肌瘤;有1例FISH阳性,组织病理证实为黏膜下平滑肌瘤。
3 讨论尿液基细胞学作为一种液态活检方式,因无创便捷及特异性高的特点,是诊断UTUC的基石性检查之一,但是其敏感性较低;如何增加UTUC诊断敏感性一直是临床研究热点。本研究采用液基细胞学、DNA倍体及FISH三种方法分别从细胞的形态学、生物学行为和分子学特征等方面多角度综合评估,拟探讨增加诊断UTUC的敏感性。结果发现三种方法对UTUC的特异性均较高,敏感性均较低,对UTUC均有一定诊断价值;将三者联合(任一阳性)后,对UTUC的检测敏感性提升至93.8%,相较于三者单独使用均得到了显著提高,有助于降低漏诊率。此外,将任意两者同时阳性作为诊断UTUC的标准(两者均阴性或仅一者阳性视为阴性)时,其阳性预测值及特异性均为100%。说明采用三者中同时有两者阳性的标准去确诊UTUC有助于降低误诊率。通过三者的联合能提高UTUC诊断的准确性,这对于指导UTUC的临床治疗有重要意义。
UTUC术前获得准确的病理诊断是目前临床面临的难点,虽然输尿管镜活检可为诊断提供帮助,但受限于其敏感性及术后易导致种植转移等问题,其在UTUC诊断中的应用仍受争议。目前国内外各大指南[2, 18]均强烈推荐所有可疑UTUC常规行尿液基细胞学检查,多数研究报道的敏感性较低,为25.9%~59.0%[17, 19-20]。导致敏感性较低的可能原因如下:①诊断时脱离了组织背景,形态学上较难客观判断,敏感性受病理医师的主观经验影响较大。本研究将DNA倍体和FISH与液基细胞学有机整合,减少形态学主观判断影响,发现可明显提高UTUC诊断敏感性。SUN等[17]研究发现将液基细胞学与FISH联合后检测UTUC的敏感性可达85.2%;SASSA等[19]的研究也提示FISH可提高液基细胞学对UTUC的诊断敏感性,提升至65.9%。此外,苏杰等[15]、赵雪等[14]研究指出:DNA倍体分析在诊断UTUC时的敏感性高于液基细胞学,两者任一阳性的联合方式能提高液基细胞学对UTUC诊断的敏感性,但并不明显优于DNA倍体单独诊断敏感性。上述研究仅探讨了DNA倍体和FISH分别联合液基细胞学对UTUC诊断敏感性影响,而本研究通过回顾性分析将3项指标联合诊断(任一阳性),评估其在UTUC诊断中意义,其将UTUC诊断敏感性提升至93.8%,明显高于液基细胞学与其中一者联合结果。②低级别肿瘤的粘附性较好不易脱落、分化高异型性较小不易鉴别导致其敏感性较低,与既往研究[20]一致,本研究也发现无论液基细胞学、DNA倍体还是FISH,对高级别UTUC的诊断敏感性均更高。③由UTUC病灶导致的上尿路梗阻可能会限制癌细胞随尿液排出;本研究发现肾盂输尿管冲洗尿行细胞学检查可增加敏感性,其中7例自然排尿样本液基细胞学阴性的UTUC患者采集了肾盂输尿管冲洗尿样行液基细胞学检查后,发现其中2例阳性。研究也证实通过膀胱镜下输尿管插管或者输尿管镜检过程中冲洗取样的方式有利于增加UTUC的检出[21-22]。
虽然三者在诊断UTUC时特异性均较高,但每种方法均存在假阳性发生。首先,本研究发现液基细胞学诊断特异性为97.7%,与叶烈夫等[20]的研究结果相近;本研究中液基细胞学含有1例假阳性,组织病理为输尿管炎性狭窄,该患者术前合并尿脓毒血症,影像学查见右侧输尿管上段管壁明显增厚伴强化,导致管腔明显狭窄,输尿管镜检+活检后行尿液基细胞学发现阳性;导致假阳性原因可能与输尿管镜机械操作或感染相关,BIER等[23]也有相关报道。其次,本研究发现DNA倍体特异性为82.4%,与苏杰等[15]研究结果相比较低。本研究DNA倍体分析存在6例假阳性病例,这些病例异倍体细胞数目均较少,仅1~8个,因而异倍体细胞数目较少可能与DNA倍体假阳性密切相关。本研究对异倍体细胞数目与UTUC诊断敏感性和特异性进行ROC曲线分析,发现在异倍体细胞数目为3个时的约登指数最大,对应的敏感性为74.8%,特异性为91.2%;而佘东立等[24]研究指出将DNA倍体分析阳性阈值设定为DNA指数(DI值)2.3,异倍体细胞比例9‰或10‰时诊断效果最好,敏感性为59%,特异性为95%。最后,本研究发现FISH诊断特异性是92.3%,较SASSA等[19]研究报道的特异性高。本研究中2例FISH假阳性患者均表现为单独P16缺失,与SASSA等[19]研究结论一致,单独P16缺失与FISH假阳性密切相关,主要因为P16缺失也可能出现在正常的尿路上皮细胞中。此外,发病年龄也与假阳性密切相关,在本研究9例假阳性患者中,8例患者较年轻(27~55岁),不在UTUC的高发年龄段内(60岁以上[25-26])。总之,在面对异倍体细胞数目少、FISH为单独P16缺失、患者较年轻等情况时,假阳性的风险相对较大;为避免假阳性发生,本研究也发现将液基细胞学、DNA倍体和FISH中任意两者同时阳性作为诊断UTUC的标准时,阳性预测值及特异性均为100%。与赵雪等[14]、SASSA等[19]结果一致。
除了本研究分析的3个因素外,其他基于尿液的检测方式还包括膀胱肿瘤抗原(BTA)、核基质蛋白22(NMP22)、免疫细胞检查(ImmunoCyt)、DNA甲基化修饰、尿液游离DNA的基因突变等。既往研究也显示这些方法单独或综合检测都能对UTUC的诊断有所帮助[23, 27-29],但确切的临床应用价值尚存争议,这些也值得我们下一步进行探讨。
综上所述,尿液基细胞学、DNA倍体和FISH对UTUC均有一定诊断价值,三者结合可有效提高诊断的敏感性或特异性,但具体临床应用需结合患者临床特点、影像特征等多因素综合评估,从而给出个性化诊治,降低漏诊或误诊风险。因本研究属于回顾性,并且样本量有限,所得结论有待于前瞻性、大样本研究进一步验证。
| [1] |
SIEGEL R L, MILLER K D, JEMAL A. Cancer statistics, 2019[J]. CA Cancer J Clin, 2019, 69(1): 7-34. |
| [2] |
ROUPRET M, BABJUK M, BURGER M, et al. European Association of Urology guidelines on upper urinary tract urothelial carcinoma: 2020 update[J]. Eur Urol, 2021, 79(1): 62-79. |
| [3] |
方冬, 李学松, 周利群. 上尿路尿路上皮癌诊断与治疗中国专家共识[J]. 中华泌尿外科杂志, 2018, 39(7): 485-488. FANG D, LI X S, ZHOU L Q. Chinese expert consensus for diagnosis and treatment of upper urinary tract urinary carcinoma[J]. Chin J Urol, 2018, 39(7): 485-488. |
| [4] |
YUAN Y C, WANG Y Q, ZHANG N, et al. Influence of American society of anesthesiologists score on oncologic outcomes in patients with upper tract urothelial carcinoma after radical nephroureterectomy: a large-sample study in two institutions[J]. Front Oncol, 2021, 11: 723669. |
| [5] |
YAMADA Y, NAKAGAWA T, MIYAKAWA J, et al. Smaller decline of renal function after nephroureterectomy predicts poorer prognosis of upper tract urothelial carcinoma: a multicentre retrospective study[J]. Jpn J Clin Oncol, 2021, 51(10): 1577-1586. |
| [6] |
JIANG Y Z, YAO Z C, ZHU X Q, et al. Risk factors and oncological outcome for intravesical recurrence in organ-confined upper urinary tract urothelial carcinoma patients after radical nephroureterectomy: a propensity score-matched case control study[J]. Int J Surg, 2020, 76: 28-34. |
| [7] |
VASHISTHA V, SHABSIGH A, ZYNGER D L. Utility and diagnostic accuracy of ureteroscopic biopsy in upper tract urothelial carcinoma[J]. Arch Pathol Lab Med, 2013, 137(3): 400-407. |
| [8] |
GUO R Q, HONG P, XIONG G Y, et al. Impact of ureteroscopy before radical nephroureterectomy for upper tract urothelial carcinomas on oncological outcomes: a meta-analysis[J]. BJU Int, 2018, 121(2): 184-193. |
| [9] |
JANISCH F, SHARIAT S F, BALTZER P, et al. Diagnostic performance of multidetector computed tomographic (MDCTU) in upper tract urothelial carcinoma (UTUC): a systematic review and meta-analysis[J]. World J Urol, 2020, 38(5): 1165-1175. |
| [10] |
JIN H Y, LIN T H, HAO J Q, et al. A comprehensive comparison of fluorescence in situ hybridization and cytology for the detection of upper urinary tract urothelial carcinoma: a systematic review and meta-analysis[J]. Medicine, 2018, 97(52): e13859. |
| [11] |
陈学敬, 周立娟, 杜伟丽, 等. 细胞DNA定量分析技术在肺癌诊断中的应用价值[J]. 中华临床医师杂志(电子版), 2021, 15(5): 331-334. CHEN X J, ZHOU L J, DU W L, et al. Value of quantitative analysis of DNA ploidy in diagnosis of lung cancer[J]. Chin J Clin Electron Ed, 2021, 15(5): 331-334. |
| [12] |
COSTA A F, POGERE A, PASINATO A P B F, et al. DNA ploidy measurement and human papillomavirus in abnormal cervical cytology[J]. Cytopathology, 2021, 32(2): 180-186. |
| [13] |
吴康, 满艳茹, 唐文潇, 等. 自动尿液细胞DNA定量分析对泌尿系统炎症与膀胱癌的鉴别诊断价值[J]. 中国临床医学, 2016, 23(5): 629-632. WU K, MAN Y R, TANG W X, et al. The value of automated urine cell DNA quantitative analysis in the differential diagnosis of urinary tract inflammation and bladder cancer[J]. Chin J Clin Med, 2016, 23(5): 629-632. |
| [14] |
赵雪, 杜广, 李东, 等. DNA倍体分析系统在输尿管癌筛查及诊断中的应用[J]. 临床和实验医学杂志, 2019, 18(11): 1215-1217. ZHAO X, DU G, LI D, et al. Application value of DNA ploidy analysis system in screening and diagnosis of ureteral cancer[J]. J Clin Exp Med, 2019, 18(11): 1215-1217. |
| [15] |
苏杰, 陶伟, 张培, 等. 细胞DNA定量分析技术在尿路上皮癌诊断中的应用价值[J]. 实用医学杂志, 2016, 32(5): 750-753. SU J, TAO W, ZHANG P, et al. Application of DNA-image cytometry in the diagnose of urothelial cell carcinomas[J]. J Pract Med, 2016, 32(5): 750-753. |
| [16] |
罗文强. DNA图像分析对尿路上皮癌检出效力的前瞻性研究[D]. 上海: 上海交通大学, 2019. LUO W Q. Detection of urothelial carcinoma by DNA image cytometry[D]. Shanghai: Shanghai Jiaotong University, 2019. |
| [17] |
SUN X Q, LIU X B, XIA M, et al. The combined application of urinary liquid-based cytology with fluorescence in situ hybridization and p16/Ki-67 dual immunostaining is valuable for improving the early diagnosis of upper tract urothelial carcinomas[J]. Diagn Cytopathol, 2017, 45(10): 895-902. |
| [18] |
黄健. 中国泌尿外科和男科疾病诊断治疗指南: 2019版[M]. 北京: 科学出版社, 2020: 191-204. HUANG J. Guidelines for diagnosis and treatment of urological and andrological diseases in China: 2019 update[M]. Bejing: Science Press, 2020: 191-204. |
| [19] |
SASSA N, IWATA H, KATO M, et al. Diagnostic utility of UroVysion combined with conventional urinary cytology for urothelial carcinoma of the upper urinary tract[J]. Am J Clin Pathol, 2019, 151(5): 469-478. |
| [20] |
叶烈夫, 黄水通, 杨泽松, 等. 荧光原位杂交技术在上尿路尿路上皮癌诊断中的应用价值[J]. 福建医药杂志, 2016, 38(3): 5-8, 181. YE L F, HUANG S T, YANG Z S, et al. Application value offluorescence in situ hybridization for the diagnosis of urothelial carcinoma of the upper urinary tract[J]. Fujian Med J, 2016, 38(3): 5-8, 181. |
| [21] |
ZHANG M L, ROSENTHAL D L, VANDENBUSSCHE C J. Upper urinary tract washings outperform voided urine specimens to detect upper tract high-grade urothelial carcinoma[J]. Diagn Cytopathol, 2017, 45(8): 700-704. |
| [22] |
MALM C, GRAHN A, JAREMKO G, et al. Diagnostic accuracy of upper tract urothelial carcinoma: how samples are collected matters[J]. Scand J Urol, 2017, 51(2): 137-145. |
| [23] |
BIER S, HENNENLOTTER J, ESSER M, et al. Performance of urinary markers for detection of upper tract urothelial carcinoma: is upper tract urine more accurate than urine from the bladder?[J]. Dis Markers, 2018, 2018: 5823870. |
| [24] |
佘东立. 自动化DNA图像分析在尿路上皮癌诊断中的应用[D]. 兰州: 兰州大学, 2016. SHE D L. The diagnostic value of automated DNA image cytometry in urothelial carcinoma[D]. Lanzhou: Lanzhou University, 2016. |
| [25] |
COLLÀ RUVOLO C, NOCERA L, STOLZENBACH L F, et al. Incidence and survival rates of contemporary patients with invasive upper tract urothelial carcinoma[J]. Eur Urol Oncol, 2021, 4(5): 792-801. |
| [26] |
方冬, 黄吉炜, 鲍一歌, 等. 中国上尿路尿路上皮癌人群特征和地区差异: 基于CUDA-UTUC协作组的多中心研究[J]. 中华泌尿外科杂志, 2017, 38(12): 885-890. FANG D, HUANG J W, BAO Y G, et al. Characteristics and regional difference of Chinese upper tract urothelial carcinoma patients: a multi-center study by CUDA-UTUC Collaborative Group[J]. Chin J Urol, 2017, 38(12): 885-890. |
| [27] |
王元元, 阴正坤, 邱爱萍, 等. EC、FISH及BTA联合在肾盂癌鉴别诊断中的应用价值[J]. 现代泌尿外科杂志, 2019, 24(4): 287-290. WANG Y Y, YIN Z K, QIU A P, et al. The applicative value of EC, FISH and BTA in the differential diagnosis of renal pelvic carcinoma[J]. J Mod Urol, 2019, 24(4): 287-290. |
| [28] |
GUO R Q, XIONG G Y, YANG K W, et al. Detection of urothelial carcinoma, upper tract urothelial carcinoma, bladdercarcinoma, and urothelial carcinoma with gross hematuria using selected urine-DNA methylation biomarkers: a prospective, single-center study[J]. Urol Oncol, 2018, 36(7): 342. |
| [29] |
HAYASHI Y, FUJITA K, MATSUZAKI K, et al. Diagnostic potential of TERT promoter and FGFR3 mutations in urinary cell-free DNA in upper tract urothelial carcinoma[J]. Cancer Sci, 2019, 110(5): 1771-1779. |




