2. 100091 北京,解放军总医院骨科医学部派驻第八医学中心骨科
2. Orthopedic Department Stationed in the Eighth Medical Center, Orthopedic Department of Chinese PLA General Hospital, Beijing, 100091, China
目前临床主要采用病灶清除结合抗生素骨水泥填充植入的方法治疗慢性胫骨骨髓炎,虽然感染得到了控制,但遗留有大段骨缺损,需要进行修复和功能重建。胫骨大段骨缺损重建方法包括Masquelet技术、同种异体骨移植、Ilizarov牵张成骨技术、骨搬移技术重建骨缺损。而这些重建技术骨愈合需要较长时间,且存在植骨块吸收、感染风险、骨塑形差、即时力学强度不足等弊端,同时易出现患肢肌肉萎缩、功能恢复差。因此胫骨骨髓炎术后骨缺损的修复存在一定的挑战。近年来随着3D打印技术在骨科领域的应用,解剖型钛合金假体形态更加符合解剖要求,能够精准匹配骨缺损形态,弹性模量接近宿主骨,避免应力遮挡,具有较强的支撑力,有利于力学传导、早期下地和功能恢复,减少了关节僵直等并发症的发生[1-2]。2015年1月至2020年12月解放军总医院第八医学中心采用3D打印解剖型钛合金假体治疗慢性胫骨下段骨髓炎病灶清除术后骨缺损5例,取得了初步临床疗效,现报告如下。
1 资料与方法 1.1 病例选择标准纳入标准:①年龄18~80岁,性别不限,诊断均符合胫骨慢性骨髓炎诊断标准[3];②清创后骨缺损长度大于5 cm;③术前行胸部CT检查,全身同位素骨扫描排除其他部位感染;④细菌培养找到致病菌且有敏感抗生素,感染已控制,术前白细胞、血沉、C反应蛋白均在正常范围内;⑤患肢软组织覆盖良好,无肌腱、骨外露,无窦道形成,局部无持续性炎症反应;⑥在本院接受3D打印胫骨假体重建术;⑦患者及其家属均有较好的依从性,并签署知情同意书;⑧随访12个月以上,并且随访资料齐全;⑨身体条件好,无严重心肺肝肾功能异常,能够耐受手术治疗。
排除标准:①感染未得到有效控制,合并有肺部或其他部位感染者;②伴有严重的骨质疏松、重建困难者;③合并手术禁忌或身体基本情况差无法耐受手术者;④精神疾病或术后不能配合者;⑤软组织条件差,皮肤覆盖不好;⑥对金属植入物过敏者;⑦下肢肌力下降者;⑧术前患侧髋、膝关节功能障碍,影响下肢功能康复和评估者。
1.2 一般资料根据以上纳入和排除标准,选取2015年1月至2020年12月在解放军总医院第八医学中心入院接受3D打印解剖型钛合金胫骨假体手术治疗的胫骨下段骨髓炎病灶清除术后骨缺损患者5例,其中男性4例,女性1例;年龄38~61(50.75±10.34)岁;左侧3例,右侧2例;术后骨缺损长度9~22(15.5±5.3)cm;初始损伤为开放性骨折3例,闭合骨折2例,Pilon骨折患者2例,胫骨下段粉碎性骨折患者3例;3例初始骨折手术采用螺丝钉、克氏针内固定,2例初始骨折手术采用螺丝钉钢板内固定。病程为5~16(11.0±4.7)年,患者既往术中均已行细菌培养并做药敏试验,单种细菌感染3例,混合感染2例;其中金黄色葡萄球菌3例,铜绿假单胞菌1例,肺炎克雷伯菌1例,表皮葡萄球菌1例。术前患者感染均已控制,白细胞计数、血沉、C反应蛋白均在正常参考值范围内,伤口无窦道形成,皮肤无红肿,无炎性反应。术后随访12个月,患者资料见表 1。本研究经解放军总医院第八医学中心医学伦理委员会伦理审查(309202205121422)。
| 编号 | 性别 | 年龄/岁 | 病史时间/年 | 致病菌 | 敏感抗生素 | 初始损伤类型 | 既往手术方式 | 既往手术次数/次 | 感染累及部位 | 胫骨缺损长度/cm |
| 1 | 男 | 47 | 16 | 肺炎克雷伯菌 | 亚胺培南+丁胺卡那霉素 | 开放损伤 | 克氏针+螺丝钉 | 4 | 胫骨下段,踝关节 | 16 |
| 2 | 男 | 57 | 13 | 金黄色葡萄球菌 | 万古霉素 | 开放损伤 | 克氏针+螺丝钉 | 4 | 胫骨下段,踝关节 | 15 |
| 3 | 男 | 38 | 10 | 金黄色葡萄球菌+表皮葡萄球菌 | 万古霉素 | 闭合损伤 | 钢板螺丝钉 | 6 | 胫骨下段,踝关节 | 22 |
| 4 | 女 | 61 | 5 | 铜绿假单胞菌 | 头孢他啶 | 闭合损伤 | 钢板螺丝钉 | 3 | 胫骨下段,踝关节 | 9 |
| 5 | 男 | 51 | 6 | 金黄色葡萄球菌 | 万古霉素 | 开放损伤 | 克氏针+螺丝钉 | 3 | 胫骨下段,踝关节 | 12 |
1.3 假体的设计与制备
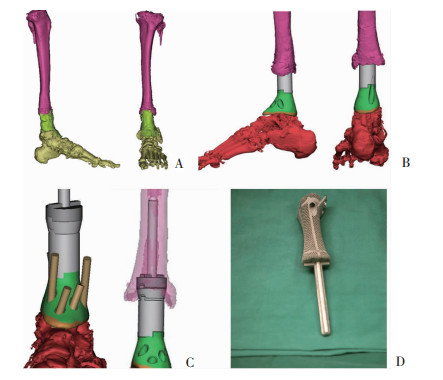
病变部位拍摄X线平片、320排CT扫描、磁共振成像(MRI)和骨扫描(ECT)。采用MRI和同位素骨扫描确定假体边界。320排CT扫描包括患肢和健侧胫骨,层厚0.5 mm。骨缺损部位以健侧肢体为参照,通过Mimics 17.0(Materialise’s interactive medical image control system,Materialize公司,比利时)软件中的镜像功能,恢复患侧胫骨图像作为假体重建的数据参考。将扫描获得的图像数据以Dicom格式存储并导入Mimics 17.0软件中,分别在软件中生成冠状位、矢状位、水平位面CT图像,通过软件功能对患者图像进行阈值分割、提取、模型编辑等操作生成三维模型,以STL格式保存并输出,导入EBM(Q10)3D打印机(Arcam公司,瑞典)中,制备假体(北京春立正达医疗器械公司)。假体根据长度设计为每间隔1 cm为一种型号。假体采用束熔融技术(electronic beam melting,EBM),材料选用钛合金(Ti6Al4V)制备而成。假体包括髓内针部分、胫骨假体主体部分、踝关节部分(图 1)。髓内针部分通过骨水泥固定于胫骨上段,踝关节部分有锁定固定孔,踝关节和骨质的接触界面设计为直径400~450 μm多孔结构,覆盖率70%,厚度1.5 mm[4]。
|
| A:Mimics 17.0软件三维重建骨缺损部分;B:模拟在骨缺损处植入假体情况;C:模拟假体髓内针端和踝关节端固定情况;D:3D打印胫骨解剖型假体 图 1 3D打印胫骨解剖型假体术前计划和假体外观 |
胫骨骨缺损术后重建假体设计的要求:①符合解剖结构的假体,早期活动,有利于患肢功能改善和避免力线不良;②假体与骨接触面能够易于骨长入,避免远期假体松动[5];③假体重量不应过大,弹性模量接近骨组织,避免患肢活动困难和应力遮挡,以减少术后并发骨折的机会;④假体与骨接触面在骨长入前,可提供即刻稳定性。
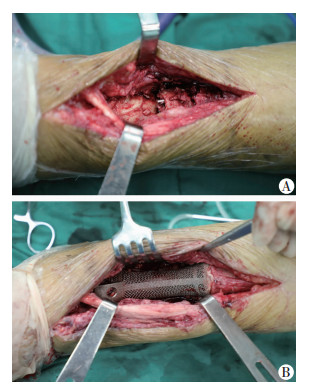
1.4 3D打印假体植入和骨缺损重建腰麻或持续硬膜外麻醉成功后,患者取仰卧位,术中使用止血带。根据病灶情况设计胫骨前正中入路,逐层显露软组织,暴露胫骨,取出骨水泥占位器,术中根据术前MRI、同位素骨扫描结果判断清创边界。用刮勺刮除病变组织,清除感染、坏死组织,依据术前计划截骨平面至正常骨质0.5 cm以上,直至创面新鲜渗血为止。胫骨上段扩髓,踝关节采用导向器进行截骨,使用双氧水以及碘伏浸泡,脉冲冲洗创面。使用常规手术器械,将试模假体植入骨缺损部位,调整试模假体长度,观察试模假体的贴合程度、稳定性、周围软组织张力、双侧下肢长度差异、下肢力线。取出试模假体,根据试模选择假体大小,植入假体后胫骨端用加入盐酸万古霉素的抗生素骨水泥固定髓内针,踝关节端用锁定钉固定,采用负压封闭引流术(vacuum sealing drainage, VSD)进行负压引流,逐层缝合切口。见图 2。
|
| A:术中取出骨水泥临时占位器;B:植入3D打印胫骨解剖型假体 图 2 3D打印胫骨解剖型假体植入 |
1.5 术后管理
术后根据既往细菌培养和药敏结果选择敏感抗生素,6周后采用利福平胶囊0.45 g,口服3~6个月,术后8 h给予低分子肝素钙5 000 U皮下注射抗凝,VSD创面负压吸引5~7 d;术后1 d开始股四头肌、腘绳肌、胫前肌等长收缩训练,每次收缩15 s,放松10 s,每组30次,分5组训练;拔除引流管后,患侧膝关节在CPM机辅助下进行被动伸屈功能锻炼,首次活动范围为0°~30°,每天增加10°~15°(以患者忍受程度为准),一般在2周内达到110°~120°,每次30 min,每天2次;术后14 d拆线,开始纠正步态训练,拄拐患肢部分负重,负重程度从体质量25%开始,行走时全程佩戴护踝,术后3个月完全负重,每次训练10 min,每天训练3次;术后1个月采用弹力带辅助下股四头肌、胫前肌、小腿三头肌渐进式抗阻训练,每次训练30 s,休息15 s,30次为1组,每天3组。
1.6 观察指标和评价标准术中记录手术时间、术中出血量;术后随访患肢的疼痛情况、膝踝关节功能、行走能力、生活质量,监测炎症指标及并发症发生情况,并进行影像学评价。
① 疼痛评价:采用视觉模拟量表(visual analog scale, VAS)评分评估疼痛程度,总分0~10分,0分表示完全无痛,10分表示疼痛无法忍受,分值越高表示疼痛越剧烈。②采用美国特种外科医院(hospital for special surgery, HSS)膝关节评分标准,AOFAS踝-后足(AOFAS Ankle Hindfoot Scale) 评分系统评价膝踝关节功能。③采用6 min步行距离,比较患者术前和术后12个月的负重行走情况,测试在平坦的地面上进行,在患者无支撑的条件下测量6 min最远行走距离(m);采用“起立-行走”计时测试快速定量评定功能性步行能力,记录患者起立(背部离开椅背),行走3 m,到再次坐下所用的时间,以s为单位。④采用36条简明健康状态调查表(36-item Short Form Health Survey, SF-36),以问卷自填的形式分8个维度评价患肢健康生活质量,包括生理健康和心理健康两个方面的内容,即生理功能(physical functioning, PF)、生理职能(role physical, RP)、躯体疼痛(bodily pain,BP)、总体健康状况(general health,GH)、活力(vitality, VT)、社会功能(social functioning, SF)、情感职能(role emotional,RE)、精神健康(mental health,MH),共36条[6-9]。每个维度满分100分,生活质量和分值呈正相关。⑤监测炎症指标,随访期间监测白细胞、血沉、C-反应蛋白。⑥并发症情况:观察伤口情况、下肢力线。⑦影像学评估:X线、CT、MRI、同位素骨扫描观察骨缺损和假体植入情况。
1.7 统计学分析采用SPSS 23.0统计软件对数据进行分析,计量资料以x±s表示,采用配对资料t检验,以P<0.05为差异有统计学意义。
2 结果 2.1 手术一般情况本组5例患者均按照术前计划重建胫骨下段骨缺损,手术时间110~207(156.75±32.40)min,术中出血量400~630(490.00±84.06)mL。
2.2 疼痛情况、膝踝关节功能5例患者随访12个月,VAS疼痛评分、HSS评分、AOFAS踝-后足评分较术前明显改善,差异有统计学意义(P<0.05,表 2)。
| 时间 | VAS评分 | HSS评分 | AOFAS评分 |
| 术前 | 5.25±0.95 | 52.00±9.38 | 40.75±11.78 |
| 术后12个月 | 1.25±1.25 | 72.25±4.57 | 67.25±6.07 |
| t值 | 9.798 | -7.059 | -3.581 |
| P值 | 0.002 | 0.006 | 0.037 |
2.3 行走能力评分对比
所有患者随访12个月,术后“起立-行走”时间和6 min步行最长距离较术前均有明显提高,差异有统计学意义(P<0.01,表 3)。
| 时间 | “起立-行走”计时/s | 6 min步行最长距离/m |
| 术前 | 89.00±10.67 | 80.00±21.60 |
| 术后12个月 | 55.40±8.26 | 230.00±42.42 |
| t值 | 8.806 | -11.619 |
| P值 | 0.000 | 0.001 |
2.4 生活质量评分
患者均获得12个月随访,术后生活质量评分SF-36量表各项得分较术前均有明显提高,差异有统计学意义(P<0.05,表 4)。
| 时间 | 生理功能 | 生理职能 | 躯体疼痛 | 总体健康 | 活力 | 社会功能 | 情感职能 | 精神健康 |
| 术前 | 46.60±9.86 | 45.80±10.25 | 43.80±8.61 | 45.60±7.60 | 50.40±9.78 | 50.00±4.41 | 46.60±6.22 | 48.80±10.32 |
| 术后12个月 | 68.00±5.78 | 70.40±6.58 | 72.60±8.04 | 70.60±7.70 | 68.00±7.90 | 69.60±8.59 | 73.40±6.02 | 73.20±7.69 |
| t值 | -3.276 | -4.703 | -13.824 | -12.5 | -3.016 | -3.884 | -6.492 | -3.449 |
| P值 | 0.031 | 0.009 | 0.000 | 0.000 | 0.039 | 0.018 | 0.003 | 0.026 |
2.5 炎症指标监测
术前所有患者白细胞计数、血沉、C反应蛋白均未见异常,术后持续监测白细胞计数、血沉及C反应蛋白至术后12个月,均在正常范围内,见表 5。
| 时间 | 白细胞/×109·L-1 | 血沉/mm·h-1 | C反应蛋白/mg·L-1 |
| 术前 | 5.85±1.41 | 8.57±1.75 | 4.56±0.81 |
| 术后12个月 | 6.07±0.91 | 9.27±2.11 | 4.85±0.77 |
| t值 | -0.854 | -1.084 | -1.046 |
| P值 | 0.400 | 0.288 | 0.304 |
2.6 术后随访及并发症发生情况
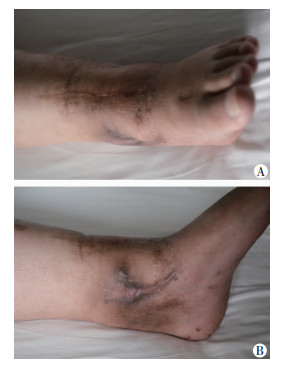
5例患者均获得完整随访,术后随访12个月,伤口愈合良好,无窦道形成,见图 3。
|
| A:术后伤口正面;B:术后伤口侧面 图 3 患者术后伤口正侧面观察 |
2.7 典型病例
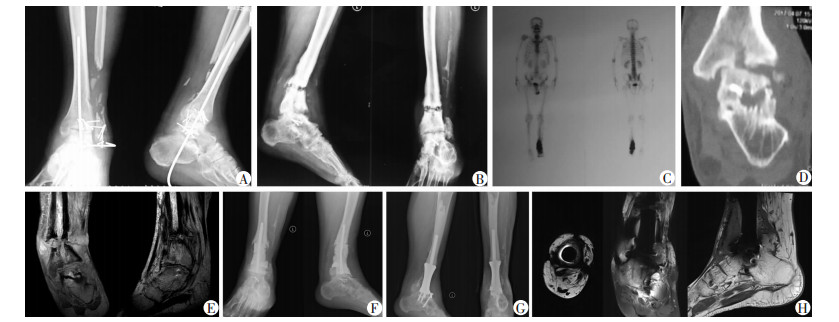
患者男性,47岁,2005年车祸致左胫腓骨开放粉碎性骨折,行清创缝合内固定术,术后3个月出现感染,取出内固定装置,窦道形成,感染迁延不愈。2017年行病灶清除,植入抗生素骨水泥临时占位器。术后12个月复查伤口愈合良好,炎症指标控制在正常范围内,取出骨水泥占位器,骨缺损部位植入3D打印解剖型钛合金假体。患者术前、术后影像学表现见图 4。
|
| A:2005年患者X线表现示左胫腓骨骨折复位内固定术后; B:2009年患者X线表现取出内固定后胫骨、腓骨下端骨折不愈合,慢性骨髓炎;C:同位素骨扫描提示踝关节周围核素浓聚;D:2009年患者内固定装置取出术后踝关节冠状位CT表现示踝关节、距下关节骨质破坏;E:2009年患者踝关节MRI表现示骨折端未愈合,有脓性渗出,窦道形成;F:2017年X线表现示病灶清除、抗生素骨水泥临时占位器植入;G:术中取出骨水泥临时占位器,植入假体术后12个月复查X线表现;H:假体植入术后12个月复查MRI横断位、冠状位和矢状位示假体位置良好,无脓性渗出和窦道形成 图 4 左胫腓骨骨折患者术前、术后影像学表现 |
3 讨论
慢性骨髓炎病灶清除术后骨缺损重建是骨科疑难问题之一。在敏感抗生素的控制下,彻底清除病灶、治疗慢性胫骨骨髓炎取得了良好的疗效[10-11]。然而,广泛病灶清除后造成胫骨大段骨缺损,重建下肢力线和早期有效功能康复成为临床研究热点。临床上重建胫骨缺损最常用的方法包括Ilizarov牵张成骨技术、Masquelet技术、带血管蒂游离腓骨移植技术等。其中Ilizarov牵张成骨术治疗周期长,邻近关节易发生僵硬、下肢力线不良和轴向偏移,牵张成骨延长总长度越长,并发神经、血管损伤的风险越高[12-13];Masquelet技术以自体骨和人工骨混合形式填充骨缺损,存在自体骨来源有限,对供骨区破坏较大,松质骨皮质化时间长,易发生骨吸收、应力性骨折、骨延迟或不愈合等并发症[14-15];带血管蒂游离腓骨移植技术对显微外科操作要求高,手术时间长,从健侧肢体取腓骨,对正常肢体有破坏,受区由于反复感染,血运差,影响植骨块愈合[16]。随着数字化骨科的不断进步,3D打印技术能够提供大小和形状同胫骨下段骨缺损匹配的个性化假体材料,从而避免了传统治疗方法的弊端。
与传统的牵张成骨、Masquelet技术、带血管蒂游离腓骨移植技术相比较,采用3D打印解剖型钛合金胫骨假体重建胫骨下段骨缺损具有以下优势:①匹配性良好。3D打印技术利用镜像原理,通过对侧数据并综合患肢情况设计的假体符合解剖形态,匹配性好,能够保持下肢长度和形态,避免畸形发生,有利于早期下地进行康复训练,改善邻近关节功能[17]。②支撑强度大。假体采用钛合金材质,强度高于骨移植材料,能够保证足够的强度支撑,保持正常生物力学传导,有利于早期负重和功能康复。③骨融合易。假体的接触面结构决定假体和骨融合的能力[18],假体和骨质接触面孔径为400 μm,孔隙率为75%,有利于假体和接触骨面融合,为长期稳定性提供了技术上的保证,减少了不稳定引起的疼痛。④即刻强度好。利用Mimics 17.0软件设计假体远端螺丝钉固定方向为强度最大的区域,近端采用骨水泥固定,既提供稳定的即刻强度,又提高了手术的精准度,奠定了早期康复的基础。
本研究5例患者随访12个月,观察VAS疼痛评分,表明术后患者疼痛症状明显缓解;膝关节HSS评分、AOFAS踝-后足评分较术前明显改善,说明采用3D打印解剖型胫骨假体重建胫骨下段骨缺损能够有效缓解疼痛,改善邻近关节功能;随访“起立-行走”时间和6 min步行最长距离明显提高,说明术后患者的运动功能有提高;比较SF-36量表评分结果,提示重建术后患者生活质量明显较术前改善。
白细胞计数、C反应蛋白、血沉是评价慢性骨髓炎和判断预后的重要指标,敏感性高。当机体发生创伤、感染、炎症反应时,白细胞计数、C反应蛋白、血沉迅速升高,其水平与炎症反应程度呈正相关。本研究结果显示,白细胞计数、C反应蛋白、血沉术前在正常范围内,说明术前慢性骨髓炎得到控制,具备植入假体基本条件。术后12个月,3种炎症因子均在正常范围内,说明假体植入的安全性,无感染复发征象。所有患者术后伤口愈合良好,无窦道形成,下肢力线和假体位置良好,提示该技术是一种安全有效的方法。
本研究设计的假体重建胫骨下段骨缺损,在假体设计和手术操作方面有以下经验:①假体周径尺寸设计应考虑软组织条件。根据患肢皮肤、皮下组织延展性,适当缩小假体周径,保证软组织覆盖假体;②假体和距骨接触面要彻底去除软骨,以利于假体和骨融合;③安装假体时保持下肢力线在机械轴上;④早期下地时部分负重,需佩戴踝关节护具,在重力作用下既可以早期刺激假体接触面的骨长入,又可以早期维持踝关节的稳定,防止假体松动。
本研究尚存在一定的局限性:①由于假体制作成本高,对研究对象的经济能力有一定的要求,同时纳入标准严格,入选病例少,样本量小;②未与其他手术方式进行对照研究;③研究周期短,随访时间不足,中远期并发症尚未暴露;④尚未开展多中心研究。
综上所述,本组病例随访初步结果证实,应用3D打印解剖型胫骨假体重建胫骨下段骨缺损能够缓解患者疼痛状态,改善相邻关节功能、行走能力、生活质量,有效控制感染复发等优势,但存在制作成本高的问题,远期效果仍需大样本及长期随访进一步证实。
| [1] |
VIDAL L, KAMPLEITNER C, BRENNAN M Á, et al. Reconstruction of large skeletal defects: current clinical therapeutic strategies and future directions using 3D printing[J]. Front Bioeng Biotechnol, 2020, 8: 61. |
| [2] |
ZHANG L, YANG G J, JOHNSON B N, et al. Three-dimensional (3D) printed scaffold and material selection for bone repair[J]. Acta Biomater, 2019, 84: 16-33. |
| [3] |
胥少汀, 葛宝丰, 徐印坎. 实用骨科学[M]. 3版. 北京: 人民军医出版社, 2005. XU S T, GE B F, XU Y K. Practical orthopedics[M]. 3rd ed. Beijing: People's Military Medical Publishing House, 2005. |
| [4] |
MARKHOFF J, WIEDING J, WEISSMANN V, et al. Influence of different three-dimensional open porous titanium scaffold designs on human osteoblasts behavior in static and dynamic cell investigations[J]. Materials (Basel), 2015, 8(8): 5490-5507. |
| [5] |
WEI R, GUO W, JI T, et al. One-step reconstruction with a 3D-printed, custom-made prosthesis after total en bloc sacrectomy: a technical note[J]. Eur Spine J, 2017, 26(7): 1902-1909. |
| [6] |
WARE J E Jr, SHERBOURNE C D. The MOS 36-item short-form health survey (SF-36). I. Conceptual framework and item selection[J]. Med Care, 1992, 30(6): 473-483. |
| [7] |
WARE J E Jr. SF-36 health survey update[J]. Spine (Phila Pa 1976), 2000, 25(24): 3130-3139. |
| [8] |
JENKINSON C, STEWART-BROWN S, PETERSEN S, et al. Assessment of the SF-36 version 2 in the united kingdom[J]. J Epidemiol Community Health, 1999, 53(1): 46-50. |
| [9] |
TAFT C, KARLSSON J, SULLIVAN M. Performance of the Swedish SF-36 version 2.0[J]. Qual Life Res, 2004, 13(1): 251-256. |
| [10] |
韩大伟, 张百明, 叶灵超. 抗生素骨水泥治疗创伤性胫骨骨髓炎的创面愈合效果观察[J]. 浙江创伤外科, 2017, 22(4): 673-674. HAN D W, ZHANG B M, YE L C. Observation on wound healing effect of antibiotic bone cement in the treatment of traumatic tibial osteomyelitis[J]. Zhejiang J Trauma Surg, 2017, 22(4): 673-674. |
| [11] |
刘光永. 抗生素骨水泥结合抗生素在外固定治疗创伤性胫骨骨髓炎的疗效体会[J]. 创伤外科杂志, 2017, 19(3): 226-227. LIU G Y. Clinical effect of bone cement combined with antibiotics for the treatment of traumatic tibial osteomyelitis[J]. J Trauma Surg, 2017, 19(3): 226-227. |
| [12] |
张明焕, 毛文, 刘雷, 等. 骨搬移术治疗慢性骨髓炎致下肢长骨骨缺损中的并发症研究[J]. 生物骨科材料与临床研究, 2021, 18(1): 89-90, 94. ZHANG M H, MAO W, LIU L, et al. The treatment of chronic osteomyelitis by bone removal for complications of osteomyelitis[J]. Orthop Biomech Mater Clin Study, 2021, 18(1): 89-90, 94. |
| [13] |
郭乾臣, 张弢. Ilizarov牵张成骨在肢体延长中的临床应用及新进展[J]. 中华保健医学杂志, 2011, 13(4): 349-351. GUO Q C, ZHANG T. Clinical application and new progress of Ilizarov distraction osteogenesis in limb lengthening[J]. Chin J Heal Care Med, 2011, 13(4): 349-351. |
| [14] |
贾乐. Masquelet技术修复骨缺损应用及研究进展[J]. 西南医科大学学报, 2020, 43(4): 421-424. JIA L. Application of Masquelet technique in repairing bone defects and its research progress[J]. J Southwest Med Univ, 2020, 43(4): 421-424. |
| [15] |
纪振钢, 周大鹏, 刘欣伟, 等. Masquelet技术治疗长骨骨缺损并发症分析[J]. 创伤与急危重病医学, 2017, 5(5): 267-270. JI Z G, ZHOU D P, LIU X W, et al. Complications of induced membrane technique for the treatment of long bone segmental defects[J]. Trauma Crit Care Med, 2017, 5(5): 267-270. |
| [16] |
景斗星, 任宏杰, 靳文阔, 等. 带血管蒂游离腓骨复合组织瓣移植一期修复小腿下段骨与组织缺损的临床应用[J]. 中华损伤与修复杂志(电子版), 2021, 16(1): 64-67. JING D X, REN H J, JIN W K, et al. Clinical application of vascularized free fibula composite tissue flap in one-stage repair of bone and tissue defects in the lower leg[J]. Chin J Inj Repair Wound Heal Electron Ed, 2021, 16(1): 64-67. |
| [17] |
宋恺, 赵爽, 田耘, 等. 3D打印假体植入修复四肢大段骨缺损的围手术期管理[J]. 中华骨与关节外科杂志, 2021, 14(8): 712-716. SONG K, ZHAO S, TIAN Y, et al. Perioperative management of 3D printing for repairing large bone defects of limbs[J]. Chin J Bone Joint Surg, 2021, 14(8): 712-716. |
| [18] |
DZIADUSZEWSKA M, ZIELIṄSKI A. Structural and material determinants influencing the behavior of porous Ti and its alloys made by additive manufacturing techniques for biomedical applications[J]. Materials (Basel), 2021, 14(4): 712. |




