2. 050083 石家庄,陆军军医大学士官学校战术卫勤系;
3. 400037 重庆,陆军军医大学(第三军医大学)第二附属医院骨科
2. Department of Tactical Health Service, Noncommissioned Officer School of Army Medical University, Shijiazhuang, 050083, Hebei Province;
3. Department of Orthopedics, Second Affiliated Hospital, Army Medical University(Third Military Medical University), Chongqing, 400037, China
大出血及出血性休克是战场上导致可预防性死亡的最常见原因,占所有创伤性伤亡的40%以上。死亡的主要机制是失血性休克引发心脏骤停,被称为失血引发的创伤性心跳骤停(hemorrhage-induce traumatic cardiac arrest, HiTCA)[1-3]。HiTCA的救治成功率非常低,一度被认为对其进行心肺复苏是徒劳的[4]。后经临床实践和研究表明,使用全血和血液制品及时进行复苏可促进自主循环恢复(return of spontaneous circulation, ROSC),成功率接近内科性心跳骤停(medical cardiac arrest, MCA)[4-6]。创伤和失血后出现的高血糖、高血钾、酸中毒等病理变化,对创伤性心跳骤停(traumatic cardiac arrest, TCA)复律和脏器功能可能有重要的影响。其中,血糖和血钾变化是失血后常见的变化[7-10],对心肌能量代谢和TCA后的复律有明显影响。目前尚末有针对上述病理变化的救治策略的研究。假设通过补充三磷酸腺苷(adenosine triphosphate, ATP)和使用改进的极化液(glucose-insulin-potassium, GIK)方法促进心肌能量代谢,可改善HiTCA后的ROSC和脏器功能恢复,本文针对这一假设进行验证。
1 材料与方法 1.1 实验材料三磷酸腺苷、胰岛素、氯化钾、葡萄糖购自重庆医药公司;酶联免疫吸附测定(enzyme-linked immunosorbent assay,ELISA)试剂盒购自美国Signalway Antibody LLC公司;手持式血气分析仪购自新加坡Flextronics公司;BC-5180 CRP型全自动全血细胞计数仪购自中国深圳迈瑞公司;HB-P01全自动干式生化分析仪购自光宝医疗器械常州有限公司;rac-030自动凝血分析仪购自中国深圳雷诺生命科学有限公司;微孔板光密度仪(MR-96A)购自中国深圳迈瑞公司。
1.2 动物分组和制模20只家兔[实验动物生产许可证号为SCXK(渝)20170002,使用许可证号为(渝)20170002]。本实验已获陆军军医大学校伦理委员会许可(AMUWEC 20192178),雌雄不拘,质量(2.82±0.43) kg,(9.5±0.45)月龄,通过随机数字分组法分为A、B两组(n=10),通过控制性失血法制备HiTCA模型。制模前,1%戊巴比妥钠以5 mL·kg-1的剂量腹腔注射麻醉家兔,然后左侧颈总动脉置管用于持续监测平均动脉压(mean arterial pressure, MAP)、收缩压、舒张压和心率以及采集动脉血做血气分析。右侧颈内静脉置三通管用于采集血样,检测血常规、常规凝血象和血生化以及用于输注复苏液体[11]。左侧股动脉置管,用于控制性抽取血液降压。完成上述工作后,从股动脉置管中以2 mL/(kg·min) 的速度抽取血液,直至收缩压 < 20 mmHg,且持续20 s以上[4-6];此时,判定HiTCA动物模型制备成功。抽取的血液用柠檬酸磷酸葡萄糖储存,室温20 ℃下保存,用于下述的复苏策略。
1.3 复苏策略制模成功后10 min内,2组动物分别接受全血回输和全血回输+三磷酸腺苷+改进GIK治疗。两组均回输抽取的全血,输注速度均为3 mL·kg-1·min-1。上述时间点的选择模拟我军《战伤救治规则》中规定,即战现场急救在伤后10 min内完成。改进的GIK方法为:根据测量的葡萄糖和钾浓度应用GIK疗法,即根据测量的葡萄糖和钾浓度调整胰岛素、葡萄糖与钾离子之间的比例:如果葡萄糖水平>6.0 mml/L,钾离子浓度>5.5 mmol/L,则胰岛素剂量为0.1 U/kg在5 min内泵入,不补充氯化钾;如果葡萄糖水平在3.0~ 6.0 mml/L之间,钾离子浓度在3.5~5.5 mmol/L之间,则使用相同剂量胰岛素的标准GIK方案(200 g/L葡萄糖、50 U/L胰岛素和80 mmol/L氯化钾)。如果钾离子浓度 < 3.5 mmol/L且葡萄糖水平 < 3.0 mml/L(大出血后非常罕见),则使用高糖和适当体积的氯化钾调整GIK;如果只有血糖或钾水平异常,则相应地调整GIK治疗[12-13]。ATP使用方法:每小时每只动物静推0.1 mL。
收缩压恢复至50 mmHg、维持1 min以上且可触及颈总动脉搏动判定为ROSC[5-6]。从复苏结束至恢复ROSC计时,各组间进行比较。ROSC后,持续监测MAP和心率,TCA后1 h内每隔20 min记录1次MAP和心率,1~4 h每隔1 h记录1次MAP和心率,4~8 h每隔2 h记录1次MAP和心率,8~24 h每隔4 h记录1次MAP和心率。
1.4 实验室检测指标和方法麻醉后制模前(0 h)、制模后1、4、8、24 h取血检测各项实验室指标。使用手持式血气分析仪测定动脉血气,记录乳酸和血氧饱和度(SaO2)。使用全自动全血细胞计数仪计数血细胞,记录红细胞和血小板数量。各时相点1.5 mL静脉血低速离心后取血浆使用HB-P01全自动干式生化分析仪检测血糖、钾离子、肌酐、尿素氮、谷丙转氨酶、谷草转氨酶、肌酸激酶同工酶-MB的浓度;使用rac-030自动凝血分析仪检测常规凝血象,记录国际标准化比值(international ratio, INR)。
制模后24 h,所有血液标本收集后,以过量氯化钾溶液静推致死动物。如果在实验终点前动物发生死亡,其各项测量指标统计至其死亡前一时相点。死亡判断标准:收缩压为0 mmHg,无自主呼吸,持续时间>3 min。
1.5 ELISA检测ELISA检测指标包括S100β蛋白, C反应蛋白(C-reaction protein, CRP)和Syndecan-1。1.5 mL血液低速离心后取血浆按照说明书进行ELISA检测,方法简述如下:将100 μL各稀释液(标准、空白和样品)添加到适当的孔中,并用平板密封剂覆盖平板,在37 ℃下培养2 h。然后从每个孔中取出液体,将100 μL检测试剂
A工作溶液添加到每个孔中,然后在37 ℃下将培养皿再培养1 h。孵育后,吸入溶液,并用300 μL洗涤液洗涤孔3次。随后,向每个孔中添加100 μL检测试剂B工作溶液,并在37 ℃下培养1 h。培养后,再次清洗孔,然后向每个孔中添加90 μL底物溶液,并将平板再培养15 min。最后,向每个孔中添加50 μL终止液,并通过轻敲板的侧面进行混合。从平板底部去除所有水滴和指纹,并确认液体表面没有气泡,然后立即用微孔板光密度仪在450 nm处测量吸光度来测量上述标记物的浓度。
1.6 统计学分析各组数值以x±s记录,使用SPSS 17.0软件进行分析。使用Kolmogorov-Smirnov法检测各组内数据的正态分布性后,使用单因素方差分析进行组间比较差异性。置信区间设定为95%,以P < 0.05为差异有统计学意义。
2 结果 2.1 ROSC、生存率和生理指标变化情况各组动物达到HiTCA制模成功时的失血量之间无显著性差异,分别为(67.4±5.87)mL和(62.6±8.06)mL(P>0.05)。2组家兔自主循环恢复率均为100%,从复苏至获得ROSC时间分别为(104±7.52)s和(98±6.03)s,无显著差异(P>0.05)。
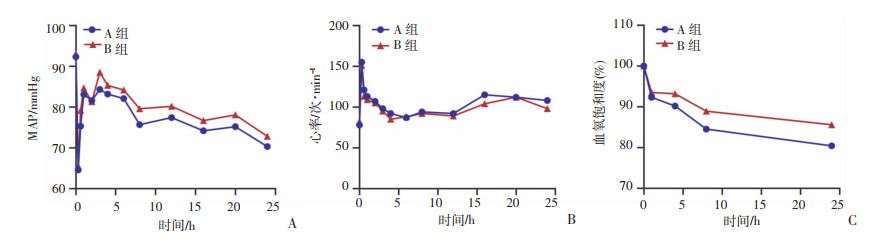
恢复ROSC后,A组和B组动物MAP在1 h输注血液后趋于稳定,波动在(64.6±6.22)~(86.8±7.43)mmHg之间,B组动物稍高于A组,但无显著性差异(P>0.05,图 1A)。心率在HiTCA后处于最高值,约为150~160次/min,然后逐渐降低并趋于平稳,波动在88~115次/min左右,两组之间无显著差异(P>0.05,图 1B)。两组动物SaO2在0 h最高,为100%;HiTCA后各个时相点波动在91.4%~96.7%,B组数值略高于A组,但两组之间无显著差异(P>0.05,图 1C)。
|
| A:两组平均动脉压变化情况;B:两组心率变化情况;C:两组血氧饱和度变化情况 图 1 两组生理指标变化情况 |
A组8~24 h内死亡2只动物,B组动物24 h内无死亡发生。
上述结果可见,全血回输基础上增加ATP和极化液后心率等生理指标稍好于全血输注,并可一定程度减少死亡率。
2.2 实验室检测指标变化与基础值相比,HiTCA后葡萄糖和钾离子浓度显著升高(P < 0.05,表 1);与A组相比,接受GIK治疗的B组的葡萄糖和钾浓度显著降低(P < 0.05,表 1)。A组和B组的红细胞计数、血小板计数显著低于基础值(P < 0.05,表 1),且随着时间延长,和基础值相差越大;2组之间红细胞计数、血小板计数无显著差异(P>0.05,表 1)。
| 组别 | 时相点 | n | 血糖/mmol·L-1 | 乳酸浓度/mmol·L-1 | 血小板计数/×1012·L-1 | 肌酐/μmol·L-1 | 谷草转氨酶/U·L-1 |
| A组 | 0 h | 10 | 5.40±0.39 | 1.39±0.15 | 439.80±28.45 | 45.30±5.21 | 4.20±0.27 |
| 1 h | 10 | 12.50±0.98bd | 2.89±0.23b | 385.80±43.76ac | 67.40±6.74a | 27.80±1.92b | |
| 4 h | 10 | 13.30±1.23bd | 6.45±0.63bc | 357.50±23.67ac | 92.40±9.65bc | 48.90±3.95bc | |
| 8 h | 10 | 16.70±1.54bd | 7.07±0.88bc | 345.80±29.38bc | 127.50±14.12bc | 60.30±5.51bc | |
| 24 h | 8 | 16.20±1.82bd | 7.65±0.93bc | 338.20±28.62bc | 175.80±15.42bc | 72.80±8.12bc | |
| B组 | 0 h | 10 | 5.20±0.46 | 1.41±0.17 | 445.50±37.68 | 43.20±6.48 | 4.30±0.22 |
| 1 h | 10 | 6.70±0.57a | 2.22±0.26a | 417.40±46.25 | 61.90±5.13a | 24.20±1.87b | |
| 4 h | 10 | 7.20±0.59a | 4.58±0.35b | 406.50±35.44a | 78.60±6.68b | 29.60±4.10b | |
| 8 h | 10 | 6.20±0.58a | 5.12±0.43b | 396.90±27.45a | 88.70±7.34b | 42.80±4.32b | |
| 24 h | 10 | 8.40±0.69a | 5.89±0.76b | 394.37±29.72a | 123.60±11.45b | 56.80±5.23b | |
| 组别 | 时相点 | 血钾/mmol·L-1 | 红细胞计数/×1012·L-1 | 尿素氮/mmol·L-1 | 谷丙转氨酶/U·L-1 | 肌酸激酶同工酶-MB/U·L-1 | |
| A组 | 0 h | 3.30±0.27 | 5.64±0.53 | 4.70±0.45 | 7.10±0.47 | 3.50±0.23 | |
| 1 h | 4.30±0.52a | 5.04±0.49 | 5.50±0.62ac | 17.20±0.47bc | 6.90±0.51b | ||
| 4 h | 4.60±0.66ac | 4.49±0.47ac | 7.20±0.59ac | 24.80±2.59bc | 11.60±0.79bc | ||
| 8 h | 5.40±0.47ac | 4.37±0.39ac | 8.90±0.91bc | 47.80±6.32bc | 18.90±0.92bc | ||
| 24 h | 4.90±0.58ac | 4.03±0.41ac | 9.80±0.77bc | 79.90±7.92bc | 21.50±1.04bc | ||
| B组 | 0 h | 3.40±0.35 | 5.85±0.76 | 4.40±0.37 | 7.60±0.59 | 3.60±0.32 | |
| 1 h | 4.10±0.38a | 5.36±0.64 | 5.40±0.45a | 14.60±1.52a | 6.20±0.57b | ||
| 4 h | 3.20±0.33 | 5.33±0.75a | 6.10±0.38a | 19.70±2.53b | 8.70±0.83b | ||
| 8 h | 3.70±0.45 | 4.99±0.62a | 6.70±0.71b | 30.80±5.07b | 12.70±0.93b | ||
| 24 h | 3.90±0.47a | 4.92±0.41a | 7.60±0.62b | 52.90±4.67b | 15.50±1.06b | ||
| a: P < 0.05,b: P < 0.01,与0 h比较;c: P < 0.05,d: P < 0.01,与B组比较 | |||||||
在0 h和1 h的时间点,2组间乳酸、肌酐、尿素氮、谷丙转氨酶、谷草转氨酶和肌酸激酶同工酶-MB的浓度无统计学差异(P>0.05,表 1)。HiTCA后4 h,B组乳酸、肌酐、尿素氮、谷丙转氨酶、谷草转氨酶和肌酸激酶同工酶-MB的浓度显著低于A组(P < 0.05,表 1)。这些数据表明ATP和GIK治疗对心脏、肾脏和肝功能有保护作用。
与基础值相比,2组的INR值显著增加,呈创伤凝血病的表现。在0 h和1 h的时间点,两组间INR无显著差异(P>0.05,图 2),而在4 h后的各个时相点,B组的INR值低于A组(P < 0.05,图 2)。这一结果表明,ATP和GIK治疗可改善HiTCA后的凝血功能障碍。

|
| a: P < 0.05, 与A组比较 图 2 两组家兔不同时相点INR变化情况 |
2.3 ELISA检测结果
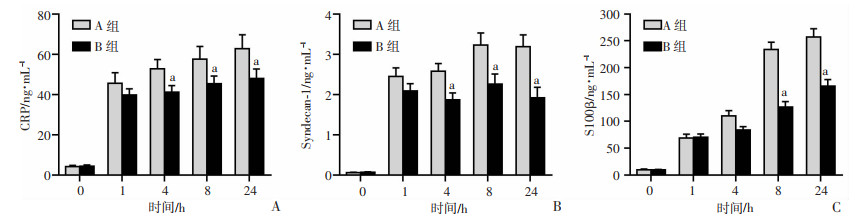
在HiTCA后4 h的各个时相点,B组CRP浓度低于A组(图 3A),这一结果表明ATP和GIK治疗有助于减轻HiTCA后的炎性反应。
|
| a: P < 0.05, 与A组比较 图 3 ELISA检测两组家兔CRP(A)、Syndecan-1(B)和S100β(C)水平变化情况 |
与基线值相比,各组的Syndecan-1浓度均明显升高(图 3B)。从HiTCA后4 h的各个时相点,B组Syndecan-1浓度明显低于A组(P < 0.05)。因为Syndecan-1具有肝素效应的内皮糖萼成分,可能导致凝血病,因而B组中syndecan-1低于A组与B组INR值低于A组有关,表明ATP和GIK治疗有助于减轻HiTCA后凝血病的严重程度。
S100β是脑损伤的有效标志物[14]。在HiTCA后8 h和24 h两个时相点,B组S100β浓度低于A组(P < 0.05)。这表明全血复合ATP、GIK治疗对HiTCA后脑组织有保护作用(图 3C)。
3 讨论HiTCA后会发生高血钾、高血糖等病理生理改变,目前研究结果显示高血钾对创伤修复是负向作用,但高血糖在HiTCA中的作用尚存一定的争议[7-10]。
创伤后的急性高血糖主要是由应激引起的下丘脑-肾上腺低生理应激反应引起的,应激反应受创伤严重程度、休克发生率和年龄的调节。失血性休克是哺乳动物中最强烈的应激源,可引发最高水平的皮质醇和儿茶酚胺,进而诱发显著的高血糖。既往研究显示,高血糖对创伤患者预后既有负面影响[7-9],也有正面的影响[10],TCA患者也是如此。一些研究支持高血糖在心跳骤停期间有益的假设[15-16]。相反,RUSSO等[17]发现,心跳骤停患者入院后96 h内平均血糖水平升高与死亡率增加和严重神经功能障碍相关。由于使用全血复苏本身促进ROSC的概率较高,因而本文研究发现,使用ATP和改进后的GIK治疗没有明显提高ROSC的概率,但这种治疗方法却明显改善了乳酸浓度、血压、凝血等指标,并最终减轻了心脏、肝脏、肾脏和脑的功能损伤。
本研究表明,TCA后结局的关键是心脏能否有效利用葡萄糖,并满足产生力量的能量需求。一方面,基于实际葡萄糖和钾浓度的GIK治疗可能增加心脏和其他脏器的葡萄糖利用率,ATP进一步提供了脏器能量代谢所需物质,这些有助于促进ROSC和维持其他脏器功能;另一方面,它可以减少高血糖的负面影响。结果发现,ATP和GIK治疗后CRP浓度显著降低,表明GIK治疗可减轻HiTCA的炎症反应。此外,发现GIK治疗后凝血各项指标有所改善。研究结果显示,急性高血糖会加剧创伤诱导的内皮细胞和糖萼损伤[18],因此,ATP和GIK疗法对凝血功能的改善可能是由对内皮细胞的保护作用引起的[19]。Syndecan-1是具有肝素效应的内皮糖萼的一种成分,已证明较高水平的Syndecan-1可能导致凝血病[11]。ATP和GIK治疗后血小板活化的降低也可能有助于凝血功能提高,如血小板计数和MA值升高[20]。GIK降低酸中毒水平可进一步改善凝血功能[21]。凝血功能的改善可能会提高ROSC的获得率和关键器官的整体功能[22]。同时,改进后的GIK治疗明显降低了HiTCA后的血钾水平,其可能对维护内皮细胞功能有重要作用,进而可进一步减轻HiTCA后凝血病的严重程度[23],减轻各脏器损伤的严重程度。同时,GIK和ATP治疗后的乳酸水平降低、能量利用增加和血钾浓度降低对心脏、肝脏、肾脏和脑组织等有直接的保护作用[24],进而减轻HiTCA导致的损伤。
本研究尚存在一定的局限性。一是本研究选用家兔作为研究对象,既往研究多以猪或狗作为研究对象,结果的可比性需要进一步验证。选择家兔作为研究对象的主要原因是市场上针对家兔的抗体、ELISA等试剂盒明显多于猪和狗,有利于进行机制研究;次要原因是家兔的凝血系统同人比较接近,而狗或猪与人相比呈现高凝特性[11]。二是本研究和其他研究一样,使用单纯失血制造HiTCA模型(因其操作方便,易于制备标准化动物模型)[6, 25-26],与真实创伤中很少有单纯失血导致HiTCA的情形。在以后的研究中,将验证ATP+GIK治疗对创伤合并大出血所致TCA中的效果。三是本研究未观察心肺复苏对ROSC和脏器功能的效果,主要原因是许多研究证明心肺复苏对HiTCA的结局是有害的[4-6]。
| [1] |
LOCKEY D J, LYON R M, DAVIES G E. Development of a simple algorithm to guide the effective management of traumatic cardiac arrest[J]. Resuscitation, 2013, 84(6): 738-742. |
| [2] |
SMITH J E, RICKARD A, WISE D. Traumatic cardiac arrest[J]. J R Soc Med, 2015, 108(1): 11-16. |
| [3] |
SHERREN P B, REID C, HABIG K, et al. Algorithm for the resuscitation of traumatic cardiac arrest patients in a physician-staffed helicopter emergency medical service[J]. Crit Care, 2013, 17(2): 308. |
| [4] |
BARNARD E B G, HUNT P A F, LEWIS P E H, et al. The outcome of patients in traumatic cardiac arrest presenting to deployed military medical treatment facilities: data from the UK Joint Theatre Trauma Registry[J]. J R Army Med Corps, 2018, 164(3): 150-154. |
| [5] |
RALL J, COX J M, MADDRY J. The use of the abdominal aortic and junctional tourniquet during cardiopulmonary resuscitation following traumatic cardiac arrest in swine[J]. Mil Med, 2017, 182(9): e2001-e2005. |
| [6] |
WATTS S, SMITH J E, GWYTHER R, et al. Closed chest compressions reduce survival in an animal model of haemorrhage-induced traumatic cardiac arrest[J]. Resuscitation, 2019, 140: 37-42. |
| [7] |
MCCOWEN K C, MALHOTRA A, BISTRIAN B R. Stress-induced hyperglycemia[J]. Crit Care Clin, 2001, 17(1): 107-124. |
| [8] |
KERBY J D, GRIFFIN R L, MACLENNAN P, et al. Stress-induced hyperglycemia, not diabetic hyperglycemia, is associated with higher mortality in trauma[J]. Ann Surg, 2012, 256(3): 446-452. |
| [9] |
BOSARGE P L, SHOULTZ T H, GRIFFIN R L, et al. Stress-induced hyperglycemia is associated with higher mortality in severe traumatic brain injury[J]. J Trauma Acute Care Surg, 2015, 79(2): 289-294. |
| [10] |
TSAI Y W, WU S C, HUANG C Y, et al. Impact of stress-induced hyperglycemia on the outcome of children with trauma: a cross-sectional analysis based on propensity score-matched population[J]. Sci Rep, 2019, 9(1): 16311. |
| [11] |
DUAN K P, YU W K, LIN Z L, et al. A time course study of acute traumatic coagulopathy prior to resuscitation: from hypercoagulation to hypocoagulation caused by hypoperfusion?[J]. Transfus Apher Sci, 2014, 50(3): 399-406. |
| [12] |
ZHAO K, ZHANG Y, LI J, et al. Modified glucose-insulinpotassium regimen provides cardio protection with improved tissue perfusion in patients undergoing cardio pulmonary bypass surgery[J]. J Am Heart Assoc, 2020, 9(6): e012376. |
| [13] |
JIN P Y, ZHANG H S, GUO X Y, et al. Glucose-insulinpotassium therapy in patients with acute coronary syndrome: a meta-analysis of randomized controlled trials[J]. BMC Cardiovasc Disord, 2014, 14: 169. |
| [14] |
MOLNAR M, BERGQUIST M, LARSSON A, et al. Hyperglycaemia increases S100β after short experimental cardiac arrest[J]. Acta Anaesthesiol Scand, 2014, 58(1): 106-113. |
| [15] |
NEHME Z, NAIR R, ANDREW E, et al. Effect of diabetes and pre-hospital blood glucose level on survival and recovery after out-of-hospital cardiac arrest[J]. Crit Care Resusc, 2016, 18(2): 69-77. |
| [16] |
MENTZELOPOULOS S D, MALACHIAS S, CHAMOS C, et al. Vasopressin, steroids, and epinephrine and neurologically favorable survival after in-hospital cardiac arrest: a randomized clinical trial[J]. JAMA, 2013, 310(3): 270-279. |
| [17] |
RUSSO J J, JAMES T E, HIBBERT B, et al. Hyperglycaemia in comatose survivors of out-of-hospital cardiac arrest[J]. Eur Heart J Acute Cardiovasc Care, 2018, 7(5): 442-449. |
| [18] |
DIEBEL L N, DIEBEL M E, MARTIN J V, et al. Acute hyperglycemia exacerbates trauma-induced endothelial and glycocalyx injury: an in vitro model[J]. J Trauma Acute Care Surg, 2018, 85(5): 960-967. |
| [19] |
ZHAO X D, QIN Y H, MA J X, et al. Influence of intensive insulin therapy on vascular endothelial growth factor in patients with severe trauma[J]. J Huazhong Univ Sci Technolog Med Sci, 2013, 33(1): 107-110. |
| [20] |
KAHN N N. Platelet-stimulated thrombin and PDGF are normalized by insulin and Ca2+ channel blockers[J]. Am J Physiol, 1999, 276(5): E856-E862. |
| [21] |
MOORE E E, MOORE H B, KORNBLITH L Z, et al. Trauma-induced coagulopathy[J]. Nat Rev Dis Primers, 2021, 7(1): 30. |
| [22] |
KOAMI H, SAKAMOTO Y, SAKURAI R, et al. Thrombo elastometric analysis of the risk factors for return of spontaneous circulation in adult patients with out-of-hospital cardiac arrest[J]. PLoS One, 2017, 12(4): e0175257. |
| [23] |
DOBSON G P, LETSON H L. Adenosine, lidocaine, and Mg2+ (ALM): from cardiac surgery to combat casualty care: teaching old drugs new tricks[J]. J Trauma Acute Care Surg, 2016, 80(1): 135-145. |
| [24] |
HUTCHINGS S D, NAUMANN D N, HOPKINS P, et al. Microcirculatory impairment is associated with multiple organ dysfunction following traumatic hemorrhagic shock: the MICROSHOCK study[J]. Crit Care Med, 2018, 46(9): e889-e896. |
| [25] |
HOOPS H E, MANNING J E, GRAHAM T L, et al. Selective aortic arch perfusion with fresh whole blood or HBOC-201 reverses hemorrhage-induced traumatic cardiac arrest in a lethal model of noncompressible torso hemorrhage[J]. J Trauma Acute Care Surg, 2019, 87(2): 263-273. |
| [26] |
JEFFCOACH D R, GALLEGOS J J, JESTY S A, et al. Use of CPR in hemorrhagic shock, a dog model[J]. J Trauma Acute Care Surg, 2016, 81(1): 27-33. |




