心导管评估小鼠心功能是最准确和有效的手段[1],已成为明确小鼠心脏功能表型的标准方法[2]。麻醉剂的使用可使动物在心导管操作期间保持镇静,易于操作,但麻醉剂可能对心血管功能存在较为显著的影响[3]。目前实验中常用麻醉剂包括腹腔注射氯胺酮(ketamine)和甲苯噻嗪(xylazine)、三溴乙醇(tribromoethanol)、巴比妥类(barbiturates)或吸入性麻醉剂,如异氟烷(isoflurane)。这些药物具有不同的药理学特征,在小鼠麻醉过程中产生不同的心血管效应[4-5]。近年来研究多关注麻醉剂对正常小鼠心功能的影响,但对心脏疾病模型小鼠心功能检测的影响鲜有报道。因此,本研究旨在探讨不同麻醉剂对心衰小鼠心功能检测的影响,研究结果有助于为心衰模型小鼠心功能评估实验中麻醉剂的选择提供参考。
1 材料与方法 1.1 实验动物与试剂实验动物由陆军军医大学(第三军医大学)第二附属医院动物中心提供(AMUWEC20201478),所有操作程序符合陆军军医大学动物伦理委员会关于动物实验的要求及使用指南。选用8周龄、体质量20~25 g的雄性C57/BL6小鼠120只,随机分为2部分,每部分60只,实验小鼠置于聚丙烯笼子中(每只笼子5只小鼠),并提供食物和水,每天保持12 h的暗光周期。根据实际经验总结设置麻醉剂的浓度,戊巴比妥钠:1.0%水溶液;三溴乙醇:1.2%水溶液;异氟烷:4.5%麻醉诱导,2.0%维持麻醉。
1.2 实验方案实验分为2部分。第一部分共60只小鼠,随机分为4组,每组15只小鼠,其中主动脉弓缩窄(transverse aortic constriction,TAC)10只,主动脉弓缩窄假手术组(Sham组)5只。第一组异氟烷吸入麻醉(2.0%体积分数),第二组腹腔注射三溴乙醇(0.2 mL/10 g),第三组腹腔注射戊巴比妥钠(0.05 mL/10 g),第四组氯胺酮(0.016 mL/10 g)。
第二部分共60只小鼠,随机分为9组;第1~3组,每组4只,行主动脉弓缩窄假手术,分别用浓度为2%、4%、6%的异氟烷麻醉;第4~6组,每组8只,行主动脉弓缩窄手术,分别用浓度为0.20 mL/10 g、0.18 mL/10 g、0.15 mL/10 g三溴乙醇麻醉;第7~9组,每组8只,行主动脉弓缩窄手术,分别用浓度为1.0%、1.5%和2.0% (体积分数)的异氟烷进行麻醉。比较不同麻醉剂不同剂量下小鼠心功能的变化。
1.3 实验方法主动脉弓缩窄模型:C57/BL6小鼠(体质量20~25 g;年龄8~10周)异氟烷麻醉诱导后,放置于温度可控的动物恒温毯上。气管插管连接呼吸机(呼吸频率120次/min,潮气量0.2 mL/次)。将小鼠仰卧固定后,胸前正中切开皮肤,上至胸骨上窝,下至第二肋骨水平。用显微镊分离胸腺暴露主动脉弓,并游离出右颈总动脉,以27 G针头直径缩窄主动脉弓,建立主动脉弓缩窄小鼠模型。操作完成后逐层关胸,缝皮,关闭麻醉。术后每只小鼠皮下注射0.5 mL生理盐水补充血容量。待小鼠恢复自主呼吸后脱机拔管。Sham组开胸后不做结扎。所有小鼠饲养8周。观测小鼠心脏体质量比和心脏射血分数(ejection fraction, EF)。
心导管测定心功能:将小鼠置于10倍解剖放大显微镜(德国莱卡体式显微镜M80)下行显微手术操作以监测平均动脉压力。分离并暴露右颈总动脉,5-0丝线结扎近心端和远心端,眼科剪在动脉上剪一小口,Millar导管从开口处进入右颈总动脉,打开近心端结扎线,将导管送入左心室,检测器上显示出压力容积信号,固定导管。观察波形和压力-容积环的形态,记录左心室内压最大上升速率(dp/dt max)、左心室舒张末期压力(left ventricular end-diastolic pressure,LVEDP)和左心室收缩末期压力(left ventricular end-systolic pressure,LVESP)。使用肝素生理盐水,以防止动脉线凝血并维持血容量。
麻醉诱导时间和苏醒时间的定义[6-7]:①当小鼠麻醉给药后即开始计时,为T0;②小鼠麻醉后仰卧体位下心跳及呼吸均匀,肌肉松弛,四肢无活动,胡须无触碰反应,踏板反射消失,即视为达到完全麻醉状态,此时为T1;③小鼠完全麻醉后,若小鼠的前肢开始抖动,即判定为开始复苏,此时为T2。麻醉诱导时间= T1-T0,苏醒时间=T2-T0。
1.4 统计学分析分析采用SPSS 26.0软件,作图使用Graphpad prism 8.0软件。实验数据以x±s表示,计数资料采用百分率表示。多组间比较采用单因素方差分析或χ2检验。P < 0.05为差异有统计学意义。
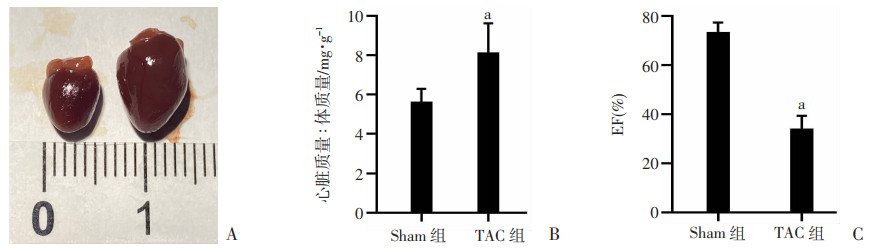
2 结果 2.1 小鼠压力负荷模型构建与鉴定主动脉弓缩窄术构建小鼠压力负荷下心力衰竭模型是一种较为经典的小鼠心衰模型。小鼠TAC术后8周,心脏代偿性肥大(图 1A),心功能显著下降与Sham组相比,TAC术后8周小鼠心脏体质量比显著增加(P < 0.01),见图 1B。心脏射血分数显著降低(P < 0.01),见图 1C。
|
| A:心衰小鼠(右)与正常小鼠(左)心脏大小;B:两组小鼠心脏/身体质量比 a:P < 0.05,与Sham组比较;C:两组小鼠的EF值a:P < 0.05,与Sham组比较 图 1 小鼠压力负荷模型构建与相关参数比较(n=5,x±s) |
2.2 不同麻醉剂对TAC和Sham小鼠麻醉效果的比较
异氟烷吸入性麻醉的诱导时间最短,10~20 s即可进入麻醉状态。Sham组小鼠的异氟烷诱导时间为(18.20±3.11) s,TAC组小鼠的异氟烷诱导时间为(19.10±3.96) s,两组差异无统计学意义,见图 2A。与异氟烷吸入性麻醉相比,其他几种腹腔注射的麻醉药物的诱导时间显著延长,但其在正常小鼠和心衰小鼠中的诱导时间均无显著差异,见图 2A。在进行心导管测量过程中,导管进入右侧颈总动脉后记录颈动脉压力,心衰小鼠麻醉后的压力为(93±10)mmHg(收缩压)、(62±8) mmHg(舒张压)(不同麻醉方式下,颈动脉压力无显著差异)。对心衰小鼠麻醉时,按照既往参考剂量易导致心衰小鼠在麻醉过程中出现死亡:异氟烷组10%(10只小鼠有1只死亡),三溴乙醇组30%(10只小鼠有3只死亡),戊巴比妥钠组40%(10只小鼠有4只死亡),氯胺酮组30%(10只小鼠有3只死亡)。心衰小鼠麻醉后的苏醒时间明显延长。停用异氟烷后,心衰小鼠的清醒时间为(19.70±4.06) min,显著高于Sham组的清醒时间(P < 0.05)。几种腹腔注射的麻醉药物也不同程度延长了心衰小鼠麻醉后清醒时间(P < 0.05),见图 2B。

|
| A:不同麻醉剂诱导时间的比较;B:不同麻醉剂清醒时间的比较 a:P < 0.05,与Sham组比较 图 2 不同麻醉剂对TAC组和Sham组小鼠的麻醉效果的比较(x±s) |
2.3 不同麻醉剂对TAC组小鼠和Sham组小鼠的心率和心功能的影响
Sham组小鼠用异氟烷麻醉后,其心率和心功能均发生不同程度的变化。分别用2%、4%、6%的浓度进行麻醉,随着麻醉剂量的增加,小鼠心功能指标显著下降(图 3)。

|
| 图 3 不同浓度的异氟烷麻醉Sham组小鼠的左心室压力-容积环(n=4,x±s) |
Sham组小鼠麻醉30 min后,其心率和心功能与麻醉早期(10 min)无显著差异(P>0.05,图 4A、B)。但是,在心衰小鼠麻醉中,戊巴比妥钠和氯胺酮显著降低了小鼠麻醉30 min后的心率(P < 0.05,图 4C)。与之相比,异氟烷吸入麻醉和三溴乙醇腹腔注射麻醉的TAC组小鼠,在麻醉过程中心率变化无差异(P>0.05)。戊巴比妥钠和氯胺酮麻醉的心衰小鼠其心脏射血分数在麻醉后期(30 min)显著降低;而异氟烷吸入麻醉和三溴乙醇腹腔注射麻醉的心衰小鼠EF值变化不明显(图 4D)。

|
| A:不同麻醉剂对Sham组小鼠心率影响的比较;B:不同麻醉剂对Sham组小鼠心功能影响的比较;C:不同麻醉剂对TAC组小鼠心率影响的比较 a:P < 0.05,与Sham组比较;D:不同麻醉剂对TAC组小鼠心功能影响的比较a:P < 0.05,与Sham组比较 图 4 不同麻醉剂麻醉对Sham组小鼠和TAC组小鼠心率及心功能的影响(n=5,x±s) |
2.4 评估不同麻醉剂量对小鼠心导管结果的影响
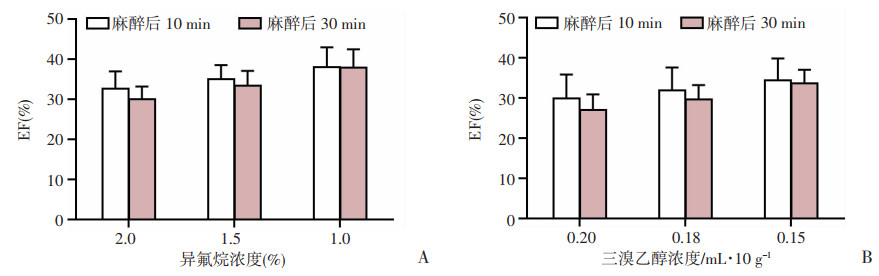
为进一步观察TAC组小鼠在心导管检测时的最佳麻醉方式和麻醉剂量,本实验对异氟烷和三溴乙醇进行了不同剂量的比较。异氟烷麻醉组,2.0%的浓度和1.5%浓度可以降低TAC组小鼠麻醉过程中的EF值,但当异氟烷浓度调整为1.0% 时,心衰小鼠EF值在麻醉过程中无明显变化(P>0.05),见图 5A。腹腔注射三溴乙醇组,0.15 mL/10 g的麻醉剂量可以较好地维持TAC组小鼠麻醉过程中的EF值,见图 5B。
|
| A:不同浓度异氟烷对TAC组小鼠心功能影响的比较;B:不同浓度三溴乙醇剂对TAC组小鼠心功能影响的比较 图 5 不同剂量麻醉剂对TAC组小鼠心功能的影响(n=8, x±s) |
3 讨论
心导管检测是精确评估小鼠心功能的一种有创技术。具有数据精确可靠、重复性好等优点。研究表明麻醉剂剂量与小鼠心功能密切相关[4-5],于心衰小鼠而言,因其心功能下降,更容易受到麻醉剂的影响,相关研究鲜有报导。本文选择4种不同的麻醉剂,观察其对心衰小鼠心功能的影响。研究结果显示,吸入异氟烷是小鼠心导管检测期间较安全稳定的麻醉剂。1.5% v/v剂量的异氟烷在心衰小鼠中可以维持小鼠血压和心率平稳。腹腔注射三溴乙醇麻醉也有较好的麻醉效果,但在心力衰竭小鼠中,腹腔注射三溴乙醇存在安全性问题。既往文献的推荐剂量容易导致心衰小鼠死亡。因此,对于心衰小鼠的麻醉,吸入性异氟烷可能是较好的选择。
3.1 麻醉剂对小鼠心脏功能的影响实验中常用的麻醉剂对小鼠心脏功能都有一定影响,不同程度地抑制心功能,但不同麻醉剂的抑制程度不同。既往研究选用清醒小鼠作为对照,研究麻醉剂对小鼠心功能的抑制[5, 8],但在小鼠清醒状态下直接抓持,其本身会引起小鼠交感神经兴奋,导致小鼠心率过快,检测结果并非小鼠静息心功能[9]。因此,本研究中未设置清醒小鼠作为对照,心衰小鼠的心功能较差,过大的刺激会导致小鼠死亡。同时部分小鼠在清醒状态下,心率和心功能变化较大,稳定性较差。心导管检测心功能也受操作者技术的影响,实验中存在数次因导管放置位置不准确,小鼠出现心率异常现象,需要停止操作,待其恢复平静后继续测量。此外,影响心率的因素众多,选择合理的麻醉药物,实现满意的麻醉镇静镇痛,可以抑制交感神经,减慢心律,减少抓取或手术疼痛导致的交感神经兴奋,一定程度上排除了植物神经对心率的干扰[10]。本研究在保证小鼠完全麻醉的情况下检测心率,发现不同的麻醉药物均会导致小鼠心率有一定程度的减慢,这一现象在心衰小鼠模型中尤为明显。因此,本研究组认为,在麻醉小鼠的过程中,选择对小鼠心率影响越小的麻醉药物,可能更适合应用于心衰模型小鼠心功能检测。
3.2 不同麻醉剂量对小鼠心脏功能的影响本研究组选择参考文献推荐的剂量,不同麻醉剂都有一定的使用剂量范围。既往数据表明,4种麻醉剂的推荐用量为:异氟烷吸入麻醉(2.0%体积分数)或腹腔注射三溴乙醇(1.25%,0.2 mL/10 g)或腹腔注射戊巴比妥钠(1%,0.05 mL/10 g)或氯胺酮(5%,0.016 mL/10 g),在实验中观察到,即使对于同一种麻醉剂,当使用剂量小于推荐剂量时,虽然可以实现足够的镇静作用,但是镇痛效果差。如果增加麻醉剂量虽可以提供足够的镇痛作用,但是与之相关的死亡率风险和血流动力学不稳定性增加。针对同种麻醉剂梯度剂量影响的研究结果显示:对于心功能较差的小鼠而言,适度减低麻醉剂用量,可以保证小鼠麻醉过程中的安全。
3.3 研究的不足之处在评估麻醉药物对小鼠的致死率时,研究所纳入的样本量偏少,这可能导致死亡率的统计分析存在一定程度的偏倚。通过多次重复试验的观察及验证,在本实验所使用的麻醉剂量下,4种麻醉剂导致心衰小鼠死亡率都在可接受范围内。在后续的研究中,将增大样本量进行进一步研究。
本研究发现:异氟烷吸入使用便捷,参数稳定性好,更适于心衰小鼠心功能检测。既往亦有多项研究证实异氟烷吸入麻醉更适于小鼠有创实验[11-12]。由于不同麻醉剂对心功能影响程度不同,对多种参数的影响程度也不同,因此实际操作时,应根据实验需要谨慎选择麻醉剂,并在同一实验中保持前后麻醉剂选择一致,麻醉剂量及条件一致,最大程度避免因麻醉剂而产生的实验误差。
综上所述,对于压力负荷诱导心衰模型小鼠的麻醉,异氟烷吸入的安全性高,对心功能的影响小,明显优于其他麻醉剂。
| [1] |
BURKHOFF D, MIRSKY I, SUGA H. Assessment of systolic and diastolic ventricular properties via pressure-volume analysis: a guide for clinical, translational, and basic researchers[J]. Am J Physiol Heart Circ Physiol, 2005, 289(2): H501-H512. |
| [2] |
PACHER P, NAGAYAMA T, MUKHOPADHYAY P, et al. Measurement of cardiac function using pressure-volume conductance catheter technique in mice and rats[J]. Nat Protoc, 2008, 3(9): 1422-1434. |
| [3] |
CONSTANTINIDES C, MEAN R, JANSSEN B J. Effects of isoflurane anesthesia on the cardiovascular function of the C57BL/6 mouse[J]. ILAR J, 2011, 52(3): e21-e31. |
| [4] |
LI C, DAI J, WU F, et al. Impacts of different anesthetic agents on left ventricular systolic function in mice assessed by echocardiography[J]. Physiol Res, 2019, 68(3): 365-374. |
| [5] |
SABATINI C F, O'SULLIVAN M L, VALCOUR J E, et al. Effects of injectable anesthetic combinations on left ventricular function and cardiac morphology in Sprague-Dawley rats[J]. J Am Assoc Lab Anim Sci, 2013, 52(1): 34-43. |
| [6] |
HOHLBAUM K, BERT B, DIETZE S, et al. Impact of repeated anesthesia with ketamine and xylazine on the well-being of C57BL/6JRj mice[J]. PLoS ONE, 2018, 13(9): e0203559. |
| [7] |
IMAI R, MAKINO H, KATOH T, et al. Desflurane anesthesia shifts the circadian rhythm phase depending on the time of day of anesthesia[J]. Sci Rep, 2020, 10(1): 18273. |
| [8] |
ZIEGLER T, LAUGWITZ K L, KUPATT C. Left ventricular pressure volume loop measurements using conductance catheters to assess myocardial function in mice[M]//Methods in Molecular Biology. New York: Springer US, 2020: 33-41. DOI: 10.1007/978-1-0716-0668-1_3.
|
| [9] |
WEI C L, KAN C D, WANG J N, et al. Does conductance catheter measurement system give consistent and reliable pressure-volume relations in rats?[J]. IEEE Trans Biomed Eng, 2011, 58(6): 1804-1813. |
| [10] |
MACHADO M L, SOARES J H, PYPENDOP B H, et al. Effect of heart rate on the pharmacokinetics of fentanyl in dogs anesthetized with isoflurane and hydromorphone[J]. Vet Anaesth Analg, 2019, 46(6): 736-744. |
| [11] |
ROTH D M, SWANEY J S, DALTON N D, et al. Impact of anesthesia on cardiac function during echocardiography in mice[J]. Am J Physiol Heart Circ Physiol, 2002, 282(6): H2134-H2140. |
| [12] |
TAN T P, GAO X M, KRAWCZYSZYN M, et al. Assessment of cardiac function by echocardiography in conscious and anesthetized mice: importance of the autonomic nervous system and disease state[J]. J Cardiovasc Pharmacol, 2003, 42(2): 182-190. |




