2. 400038 重庆,陆军军医大学(第三军医大学)第一附属医院:放射科
2. Department of Radiology, First Affiliated Hospital, Army Medical University (Third Military Medical University), Chognqing, 400038, China
慢性硬膜下血肿(chronic subdural hematoma,CSDH)多由创伤所致,多见于老年人,并且发病率逐年升高[1]。组织学研究发现CSDH的形成与包膜血管生成及渗漏有关,并认为血肿包膜血供可能来源于脑膜中动脉(middle meningeal artery,MMA)[2-3]。有学者对CSDH患者进行MMA选择性血管造影,发现MMA弥漫性扩张,并见MMA分支末端呈棉絮状染色[4];另有学者对难治性CSDH患者采用栓塞MMA治疗,与传统手术治疗比较,发现栓塞MMA治疗组的复发率远低于传统手术组[5-6]。由此可见MMA在CSDH的发生、发展过程中扮演了重要角色。为此,国外有学者通过磁共振血管成像(MR angiography,MRA)测量MMA管径,发现CSDH患者的MMA管径明显增粗[7]。然而,也有学者认为该研究测量方法欠准确,且没有涉及MMA管径与CSDH术后复发的关系[8]。因此,本研究对测量方法进行改良,采取回顾性匹配对照研究分析本院收治的CSDH患者,在脑动脉三维时间飞越法(3D time of flight,3D TOF)MRA检查上测量CSDH患者的MMA管径并与匹配的健康人进行对比,以明确CSDH患者MMA是否增粗,并对比钻孔引流术后复发侧与非复发侧MMA管径,以明确复发侧MMA是否增粗更明显,从而提供一个判断CSDH患者预后的因素,并为进一步精准治疗提供筛选指标。
1 资料与方法 1.1 一般资料回顾性分析我院2014年5月至2021年5月收入神经外科治疗的CSDH患者病历资料。纳入标准:①结合病史、辅助检测及临床表现被诊断为CSDH患者;②年龄在18~90岁;③患者均在治疗前行头颅(3D TOF) MRA。排除标准:头颅(3D TOF) MRA成像质量较差的患者。本研究获本院伦理委员会批准[(B)KY2021079]。
共纳入CSDH患者41例,30例为创伤所致,其余11例出血原因不明。其中男性36例(87.8%),女性5例(12.2%);年龄20~89(68.56±14.38)岁。CSDH发生在左侧19例,右侧7例,双侧15例;11例双侧出血量明显不同的CSDH患者中右侧血肿居多者3例,左侧居多者8例。对应每个患者,从门诊系统中选择1名年龄(±1岁)和性别匹配的因健康体检行头颅(3D TOF) MRA检查的健康人进行对照,排除患有急性硬膜外血肿、蛛网膜下腔出血、硬膜动静脉瘘、颈动脉闭塞、脑肿瘤、脑外科手术、急性硬膜下血肿或CSDH者。
41例CSDH患者中23例采取钻孔引流术,其中复发9例12侧,非复发14例18侧。对比复发侧与非复发侧MMA管径,以明确CSDH患者行钻孔引流术后复发侧MMA是否增粗更明显。首次钻孔引流术后,头颅CT或MRI提示硬膜下血肿出血量进行性增加,症状加重,需再次手术定义为“术后复发”[9]。
1.2 测量方法采用西门子3.0T磁共振(simens magnetom trio) 进行(3D TOF) MRA检查。具体成像参数为:TR 20 ms, TE 3.69 ms,翻转角度18°,FOV 260 mm× 260 mm,矩阵尺寸384×384,体素尺寸0.7 mm×0.7 mm×0.7 mm。所有MRA图像传输到MRSC磁共振工作站进行定量分析。将1例因疑似伴有颅内动脉瘤术前行脑血管造影的患者的(3D TOF)MRA血管重建图像与脑血管造影图像比对,发现两者MMA的部位及走行基本一致(图 1),从而更确定(3D TOF)MRA源图像上MMA的部位,并最终使用3D MPR在源图像上测量MMA管径。回顾本组头颅(3D TOF) MRA血管重建图像,我们发现MMA在入棘孔到蝶骨棘之间即中颅窝段成像更清晰,更便于测量MMA管径,于是由神经外科医师在(3D TOF)MRA源图像中,选取MMA中颅窝段平眶上裂轴位层面的MMA区域为感兴趣区。因感兴趣区血管的截面不一定是血管长轴的短轴位,因此在所选感兴趣区的斜冠状位及斜矢状位标记垂直血管长轴的坐标后以确定短轴位,以此在轴位层面确定MMA测量截面;再由不知受试者信息及出血情况的神经放射医师在该截面上测量MMA管径(图 2)。
|
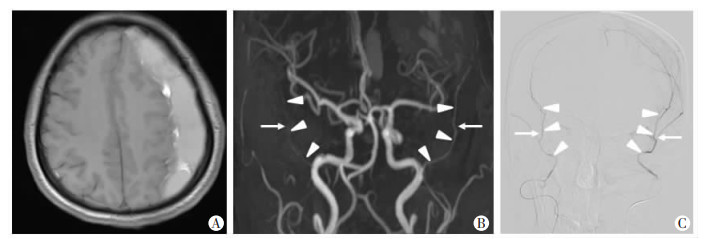
| A:头颅MRI T1 FLAIR像提示左侧额颞顶部CSDH;B:头颅(3D TOF)MRA血管重建图像上MMA的部位及走行(△)、测量部位(↑);C:正位MMA超选造影显示MMA的部位及走行(△)、测量部位(平眶上裂)(↑) 头颅(3D TOF)MRA血管重建图像的MMA与脑血管造影图像比对,部位及走行一致 图 1 左侧CSDH患者(3D TOF)MRA及脑血管造影的MMA特征 |
|
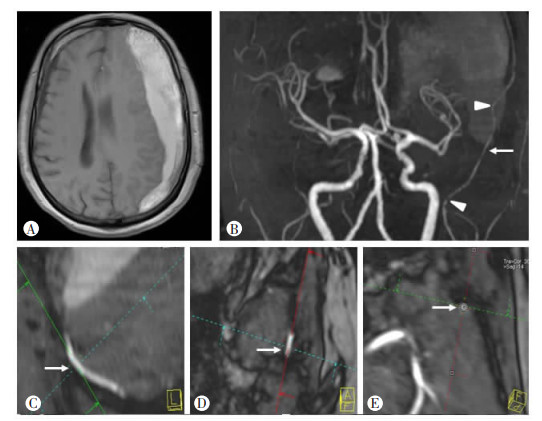
| A:头颅MRI T1 FLAIR像提示左侧额颞顶部CSDH;B:头颅(3D TOF)MRA血管重建图像上MMA过棘孔及蝶骨棘处明显弯折(△),测量部位位于两明显弯折之间中颅窝段的平眶上裂平面(↑);C:(3D TOF)MRA源图像中,在所选感兴趣区的斜冠状位标记垂直血管长轴的坐标(↑);D:在所选感兴趣区的斜矢状位标记垂直血管长轴的坐标(↑);E:确定垂直于血管长轴的短轴位作为MMA测量截面(↑) 图 2 头颅(3D TOF)MRA源图像上MMA管径测量方法 |
1.3 统计学分析
采用SAS 9.4统计软件,P < 0.05认为差异有统计学意义。本研究对比CSDH患者出血侧、非出血侧,以及健康人MMA管径;由于每个研究对象提供了双侧MMA管径数据,为了考虑数据的关联性,采用多变量线性混合模型来做相关比较,患者的年龄和性别被放入模型中。另外,在双侧出血且一侧出血多于另一侧的CSDH患者中,采用Wilcoxon秩检验来评估两侧MMA管径的差异。对比钻孔引流术后复发侧与非复发侧MMA管径,同样采用多变量回归模型进行分析。
2 结果 2.1 一般情况本组测量41例CSDH患者56侧血肿侧MMA管径、26侧非血肿侧MMA管径以及所匹配41例健康人82侧MMA管径。经多变量线性混合模型估算后,CSDH出血侧MMA管径均值大于非出血侧MMA管径均值(2.17 vs 1.70 mm, P < 0.01),CSDH出血侧MMA管径均值大于健康人MMA管径均值(1.50 mm),差异有统计学意义(P < 0.01),CSDH非出血侧MMA管径均值也大于健康人MMA管径均值(P < 0.01)。11例双侧出血量明显不同的CSDH患者出血较多侧MMA管径均值2.23 mm,出血较少侧MMA管径均值2.13 mm,两者比较无明显差异(P=0.18)。经多变量回归模型估算后,23例钻孔引流CSDH患者中复发9例12侧MMA管径均值为2.40 mm,非复发14例18侧MMA管径均值为1.82 mm, 复发患者MMA管径较非复发患者明显增粗,差异有统计学意义(P < 0.01)。
2.2 典型病例患者女性,67岁。入院2个月前因双侧额颞顶部CSDH行双侧额颞顶部硬膜下血肿钻孔引流术(图 3A),术后复查头颅CT示硬膜下血肿较术前明显减少(图 3B)。入院3 d前患者出现右侧肢体乏力伴失语,行头颅MRI示左侧额顶部CSDH复发(图 3C),(3D TOF)MRA显示左侧MMA明显较对侧增粗(图 3D)。拟进行MMA栓塞术,栓塞前正侧位MMA超选造影示左侧MMA明显增粗并见棉絮样染色的异常血管网(图 3E、F),造影后行Dyna-CT示血肿包膜强化(图 3G)。使用聚乙烯醇颗粒100 μm栓塞MMA,栓塞后异常血管网消失(图 3H)。栓塞后3个月复查CSDH几乎完全吸收。

|
| A:头颅CT提示双侧额颞顶部CSDH;B:术后复查头颅CT示硬膜下血肿较术前明显减少; C:头颅MRI示左侧CSDH复发; D:头颅(3D TOF)MRA显示左侧MMA明显增粗(△);E、F:栓塞前正侧位MMA超选造影示左侧MMA明显增粗(Δ)和呈棉絮样染色异常血管网(↑);G:造影后行Dyna-CT示血肿包膜强化(↑);H:栓塞后呈棉絮样染色异常血管网未显影 图 3 双侧额颞顶部CSDH患者钻孔引流术后复发行MMA栓塞影像学表现 |
3 讨论
CSDH的发病率随着人口老年化及抗凝药物的广泛使用而逐年升高,采用传统治疗方式如钻孔引流术治疗,其复发率高达33%[10-11],即便采用新兴的口服阿托他汀治疗,轻型及中型CSDH患者中仍有11%的患者需再次行手术治疗[12],其中的缘由可能与CSDH周围包膜血管生成、未成熟的毛细血管生长从而导致血液长期渗漏这一独特的病理生理过程有关[2-3]。而血肿包膜血供的来源经过脑血管造影及MMA栓塞治疗证实可能为MMA[4],因此,我们推测可以通过MMA管径间接反映包膜的新生血管及血管渗漏情况,从而预测CSDH的预后。本研究回顾了我院7年来CSDH患者的头颅(3D TOF)MRA资料,通过这一无创检查将CSDH出血侧与非出血侧以及匹配对照组MMA管径进行对比,得出CSDH患者出血侧MMA管径明显增粗的结论,从而证实MMA管径与CSDH的发生和发展有明确相关性。
2016年TAKIZAWA等[7]首次通过(3D TOF)MRA研究MMA与CSDH的关系,报道了CSDH出血侧MMA管径为(1.48±0.48) mm,而非出血侧为(0.93±0.21) mm,最终结论与本研究相同,但MMA管径明显低于本研究,考虑是由于该研究是在TOF血管重建图像上进行测量,受动脉信号强度的影响,测量值可能不能反映MMA的确切管径,并且所选取测量部位可能并非垂直于血管长轴。因此, 本研究对测量方法进行改良,首先明确了头颅(3D TOF)MRA血管重建图像上的MMA部位及走形与脑血管造影图像的一致性;其次使用3D MPR在(3D TOF)MRA源图像上测量MMA管径,并选取垂直于血管长轴的测量截面,保证所测量的管径数据更接近真实。另外,本研究发现CSDH非出血侧MMA较健康人MMA粗大,通过对CSDH患者进行的脑血管造影发现部分单侧血肿的包膜血供可能来源于双侧MMA,因此该类患者非出血侧MMA也同样增粗,从而可证实本研究的上述结论。
CSDH钻孔引流术后复发一直以来是困扰临床医师的一大难题,有研究发现双侧硬膜下血肿、使用抗血小板药及抗凝药物是CSDH术后复发的危险因素[13]。近期有研究认为,炎症、血管再生、局部凝血和渗出物等与CSDH术后复发有关[14-15]。结合以上CSDH的病理生理特点,不难推测MMA的管径可能与术后复发相关。而在TAKIZAWA等[7]的研究中并没有涉及MMA管径与术后复发的关系。然而, 本研究发现钻孔引流术后复发侧MMA管径增粗更明显,提示MMA管径可能与CSDH钻孔引流术后复发相关,从而为临床提供了一个判断CSDH患者预后的因素。
结合本研究中的典型病例,可以发现该例双侧CSDH患者钻孔引流术后单侧复发,复发侧MMA明显较非复发侧增粗,也证实了以上MMA管径与术后复发相关的结论。并且在脑血管造影中发现MMA弥漫性扩张,MMA分支末端呈棉絮状染色,以及Dyna-CT所呈现的血肿包膜强化,结合既往研究结果[16],均提示MMA参与了血肿包膜供血。因此,通过治疗前的(3D TOF)MRA筛选出该类MMA明显增粗的患者,给予栓塞MMA进而闭塞血肿包膜新生血管网减少渗出,可作为减少钻孔引流术后复发的预防性治疗,也可作为不需要紧急外科手术治疗的CSDH患者的单独治疗方式。
本研究的局限性在于:①样本量小,且为回顾性研究,存在一定程度偏倚,还需要更大样本量的前瞻性随机对照研究进一步明确MMA管径与CSDH预后的相关性;②通过MRA测量MMA此类小血管管径仍欠准确,目前MMA栓塞开始成为CSDH的新兴治疗方式,可将栓塞前的脑血管造影作为评估MMA管径及血肿包膜血供情况更准确的检查方法,从而更准确、更可靠地评估MMA与CSDH的关系。
综上所述,本研究证实CSDH患者出血侧MMA较非出血侧及健康人增粗,钻孔引流术后复发侧MMA增粗更加明显,提示MMA管径与CSDH的发生及发展有关,并且与患者行钻孔引流术的预后相关,从而为临床提供了一个判断CSDH患者预后的因素,并为进一步精准治疗提供筛选指标。
| [1] |
YANG W Y, HUANG J. Chronic subdural hematoma: epidemiology and natural history[J]. Neurosurg Clin N Am, 2017, 28(2): 205-210. |
| [2] |
LEE K S. History of chronic subdural hematoma[J]. Korean J Neurotrauma, 2015, 11(2): 27-34. |
| [3] |
LEE K S. Natural history of chronic subduralhaematoma[J]. Brain Inj, 2004, 18(4): 351-358. |
| [4] |
HASHIMOTO T, OHASHI T, WATANABE D, et al. Usefulness of embolization of the middle meningeal artery for refractory chronic subdural hematomas[J]. Surg Neurol Int, 2013, 4: 104. |
| [5] |
BAN S P, HWANG G, BYOUN H S, et al. Middle meningeal artery embolization for chronic subdural hematoma[J]. Radiology, 2018, 286(3): 992-999. |
| [6] |
LINK T W, BODDU S, PAINE S M, et al. Middle meningeal artery embolization for chronic subdural hematoma: a series of 60 cases[J]. Neurosurgery, 2019, 85(6): 801-807. |
| [7] |
TAKIZAWA K, SORIMACHI T, ISHIZAKA H, et al. Enlargement of the middle meningeal artery on MR angiography in chronic subdural hematoma[J]. J Neurosurg, 2016, 124(6): 1679-1683. |
| [8] |
DASH C, SINGLA R, GARG K, et al. Letter to the Editor: Enlargement of the middle meningeal artery[J]. J Neurosurg, 2016, 125(6): 1613-1615. |
| [9] |
HIRAI S, YAGI K, HARA K, et al. Postoperative recurrence of chronic subdural hematoma is more frequent in patients with blood type A[J]. J Neurosurg, 2021, 135(4): 1203-1207. |
| [10] |
TOI H, FUJⅡ Y, IWAMA T, et al. Determining if cerebrospinal fluid prevents recurrence of chronic subdural hematoma: a multi-center prospective randomized clinical trial[J]. J Neurotrauma, 2019, 36(4): 559-564. |
| [11] |
KOLIAS A G, CHARI A, SANTARIUS T, et al. Chronic subdural haematoma: modern management and emerging therapies[J]. Nat Rev Neurol, 2014, 10(10): 570-578. |
| [12] |
JIANG R C, ZHAO S G, WANG R Z, et al. Safety and efficacy of atorvastatin for chronic subdural hematoma in Chinese patients: a randomized ClinicalTrial[J]. JAMA Neurol, 2018, 75(11): 1338-1346. |
| [13] |
CHON K H, LEE J M, KOH E J, et al. Independent predictors for recurrence of chronic subdural hematoma[J]. Acta Neurochir (Wien), 2012, 154(9): 1541-1548. |
| [14] |
EDLMANN E, GIORGI-COLL S, WHITFIELD P C, et al. Pathophysiology of chronic subdural haematoma: inflammation, angiogenesis and implications for pharmacotherapy[J]. J Neuroinflammation, 2017, 14(1): 108. |
| [15] |
HOLL D C, VOLOVICI V, DIRVEN C M F, et al. Pathophysiology and nonsurgical treatment of chronic subdural hematoma: from past to present to future[J]. World Neurosurg, 2018, 116: 402-411.e2. |
| [16] |
NAKAGAWA I, PARK H S, KOTSUGI M, et al. Enhanced hematoma membrane on DynaCT images during middle meningeal artery embolization for persistently recurrent chronic subdural hematoma[J]. World Neurosurg, 2019, 126(4): e473-e479. |




