颈椎后纵韧带骨化症(ossification of posterior longitudinal ligament,OPLL)是以颈椎后纵韧带异位骨化并对脊髓产生压迫而引起的一组临床症候群,多发于中老年,在东亚地区发病率为1.9%~4.3%[1-3]。颈椎前路手术可从根本上解除脊髓前方的骨性压迫,同时重建颈椎生理曲度,效果优良[4-5]。颈椎前路手术需切除病变节段的椎体及骨化的后纵韧带,以达到彻底减压的目的。椎体次全切后需要采用自体骨块、钛网等重建材料进行椎体间融合[6-7],使用髂骨块存在吸收、塌陷等并发症,同时取自体髂骨不仅延长了手术时间,也带来了一定的损伤和并发症[6-8]。钛网加自体骨、羟基磷灰石人造骨块等颈椎前路重建材料存在骨-材料界面不能密切接触、假体移位下沉等弊端[9]。近年来随着3D打印技术突飞猛进的发展,3D打印人工椎体不仅具有良好的机械强度、耐腐蚀性和生物相容性,而且通过调整微孔的大小,使人工椎体具有与椎体皮质骨和松质骨相近的弹性模量。研究发现3D打印微孔钛金属材料能够促进成骨细胞在其表面黏附和成骨分化,3D打印人工椎体开始在临床中初步使用[8]。本院2018年1月至2020年1月采用3D打印微孔钛合金人工椎体作为颈前路重建材料治疗颈椎OPLL,并与采用钛网作为颈前路重建材料的术式进行对比,评价使用3D打印人工椎体治疗颈椎后纵韧带骨化症的安全性、疗效及优势。
1 资料与方法 1.1 病例资料回顾性分析本院脊柱科2018年1月至2020年1月行颈前路椎体次全切除减压、3D打印微孔钛合金人工椎体植入或钛网植入、钛板内固定术的颈椎OPLL患者临床资料64例,符合纳入及排除标准者57例。根据内植物的不同分为观察组(内植物为3D打印人工椎体,28例)及对照组(内植物为钛网,29例)。两组患者基线资料见表 1,两组性别、年龄、病变节段、病程、JOA评分对比,差异无统计学意义(P>0.05),具有可比性。本研究获本院伦理委员会批准(2018-LH-KY-001-047),所有患者签署知情同意书。
| 组别 | 性别 | 年龄/岁 | 病变节段/例 | 病程/年 | JOA评分 | ||||
| 男 | 女 | C4 | C5 | C6 | C7 | ||||
| 观察组 | 21 | 7 | 52.67±5.52 | 5 | 10 | 8 | 5 | 3.78±0.69 | 11.61±0.99 |
| 对照组 | 20 | 9 | 51.51±5.24 | 4 | 11 | 9 | 5 | 3.53±0.58 | 11.37±1.08 |
| 检验统计量 | χ2=0.257 | t=0.790 | χ2=0.200 | t=1.482 | t=0.827 | ||||
| P值 | 0.770 | 0.433 | 0.978 | 0.144 | 0.412 | ||||
1.2 纳入及排除标准
纳入标准:①症状、体征及影像学符合国际颈椎后纵韧带骨化症诊断标准[4];②年龄18~70岁;③行颈椎前路单个椎体次全切减压、3D打印人工椎体植入或钛网植入钛板内固定术者。
排除标准:①诊断为骨质疏松症(骨密度T值≤-2.5),未经系统治疗者;②既往有颈椎手术史者;③失去随访者。
1.3 植入材料及内固定器械3D打印微孔钛合金人工椎体,由爱康宜诚医疗器材股份有限公司提供。首先应用64排CT对所有颈椎后纵韧带骨化症患者采集颈椎三维模型数据,将模型数据导入3D打印设备(Arcam AB公司,瑞典),采用比利时Matefialise公司计算机辅助设计软件设计。人工椎体设计为圆柱形(图 1),人工椎体高度为病变节段椎体加上、下椎间盘的高度之和,直径为病变节段椎体的前后径缩小4 mm,人工椎体的上下接触面按照上一椎体的下终板与下一椎体的上终板面反向设计。孔隙率为(68.0±5.3)%,孔径为(800±200)μm,弹性模量为(2.5±0.2)GPa,压缩强度为(63.0±4.7)MPa。

|
| A:3D打印微孔钛合金椎间融合器;B:微孔钛合金融合器微观结构孔径(800±200)μm 图 1 3D打印人工椎体 |
钛网由北京市富乐科技开发有限公司提供,为圆柱状,直径规格为8、10、12 mm,厚度1.0 mm,侧壁上有直径约为3 mm的孔,见图 2。

|
| A:钛网;B:颈前路钛板 图 2 钛网及颈前路钛板 |
颈前路钛钢板系统为北京市富乐科技开发有限公司产品,钛板采用钛合金材料,厚度1.8 mm,长度22.5~120 mm(长度间隔2.5 mm);螺钉为钛合金材料,直径4.0~4.5 mm,长度分别为14、16、18 mm,见图 2。
1.4 手术方法采用气管插管的全身麻醉及肩部垫高使颈部后仰的仰卧位。切口取相应节段水平的右侧横切口,切开颈阔肌,在颈深筋膜浅层分离,切开颈深筋膜,在颈动脉鞘和内脏鞘间隙分离至椎体。在椎体上插入定位针,透视确认切除的椎体后,在病变椎体上下的椎体置入撑开钉,安装Caspar撑开器,切除病变椎体的上下椎间盘,适度撑开椎间隙后,应用超声骨刀沿着颈长肌内缘切除病变节段椎体及后纵韧带骨化块,显露出硬脊膜,充分减压脊髓及神经根,仔细止血。
观察组:在3D打印人工椎体中央的小孔内填入切除椎体制成的微小骨粒,然后在椎间适度撑开的状态下将3D打印人工椎体置入椎间,放松Caspar撑开器。注意3D打印人工椎体上缘为微弧形、下缘为斜坡形,与椎体的上下缘形态完全吻合。放入颈前路钛板,透视确认内置物的位置良好后,拧入钛板的螺钉牢固固定。
对照组:测量椎体次全切后的上下椎体间高度,根据测量高度对钛网进行精准修剪,在钛网内填入切除椎体制成的碎骨粒。将钛网安放于椎间,低于椎体前缘2~3 mm,临时安装钛板,透视检查钛网及钛板位置良好后,拧入钛板的螺钉固定。
放置负压吸引管,逐层关闭切口。术后佩戴颈托制动,术后次日下床活动,进行四肢康复功能锻炼。
1.5 随访及疗效评价标准 1.5.1 一般指标记录手术时间(从切开皮肤到皮肤缝合完毕的时间)、术中出血量(吸引器瓶内血量加上纱布估算量)、术后伤口愈合及并发症情况。
1.5.2 神经功能评价采用日本矫形外科学会(Japanese orthopaedic association,JOA)17分法对患者脊髓功能评分。神经功能改善率=(随访时评分-术前评分)/(17-术前评分)×100%。
1.5.3 椎间融合标准① 植骨块两端与椎体上下接触面之间结合紧密无明显透亮带;②植骨块与椎体接触面间可见骨小梁形成;③通过颈椎过曲或过伸位X线片观察融合节段棘突间无异常活动。符合以上2条即为椎体融合[10]。
1.5.4 影像学指标术前、术后1周及末次随访时,在颈椎侧位片上或CT正中矢状位上测量施术椎节的椎间前高、后高,与术后即刻相比较,不论前高还是后高,椎间高度下降≥3 mm即视为发生假体沉降[11]。
1.6 统计学分析采用SPSS 19.0统计学软件,计量资料以x±s表示,采用t检验或χ2检验进行两组间差异比较,P<0.05认为差异有统计学意义。
2 结果 2.1 一般指标57例患者均顺利完成手术,观察组手术时间为(59.32±12.09)min,术中出血量(102.75±11.25)mL,对照组手术时间为(67.55±4.71)min,术中出血量(102.06±13.83)mL。观察组手术时间显著短于对照组(P=0.001)。术中出血量两组间比较差异无统计学意义。随访12~15(14.3±2.7)个月,1例(对照组)出现伤口感染;术后出现颈部吞咽不适症状7例,其中观察组3例,对照组4例,1~2周后消失。患者均无钢板螺钉断裂、移位发生。末次随访时均骨性愈合。
2.2 神经功能评价末次随访时,观察组JOA评分由术前的(11.61±0.99)分提高至(16.10±0.68)分,改善率为(83.03±12.68)%;对照组JOA评分由术前的(11.37±1.08)分提高至(16.03±0.56)分,改善率为(81.58±12.67)%。两组的JOA评分较术前均有显著提高,两组改善率差异无统计学意义。
2.3 影像学测量假体沉降发生率观察组1例(3.57%),对照组12例(41.38%),两组间对比差异有统计学意义(P=0.001)。
2.4 典型病例观察组患者,男性,57岁,颈椎后纵韧带骨化症(C5~C6),行C6椎体次全切减压、3D打印微孔钛合金人工椎体植入内固定融合术(图 3)。
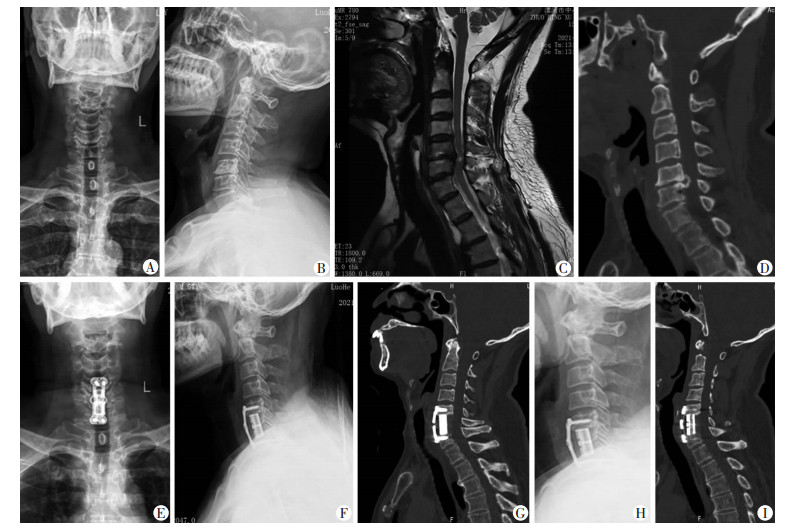
|
| A、B:术前颈椎正、侧位X线片颈5/6椎间隙变窄、唇样增生;C:术前颈椎MRI T2矢状位颈5/6水平脊髓受压,髓内有一高信号影;D:术前颈椎CT矢状位颈6椎体后缘有后纵韧带骨化影;E、F:术后1周颈椎正、侧位X线片3D打印人工椎体位置良好;G:术后1周颈椎CT矢状位人工椎体位置良好;H:术后6个月颈椎侧位片人工椎体位置良好无变化;I:术后6个月颈椎CT矢状位人工椎体位置良好无变化 图 3 3D打印人工椎体治疗颈椎后纵韧带骨化症患者的影像学观察 |
对照组患者,男性,52岁,颈椎后纵韧带骨化症(C5~C6),行C6椎体次全切减压、钛网植入内固定融合术(图 4)。
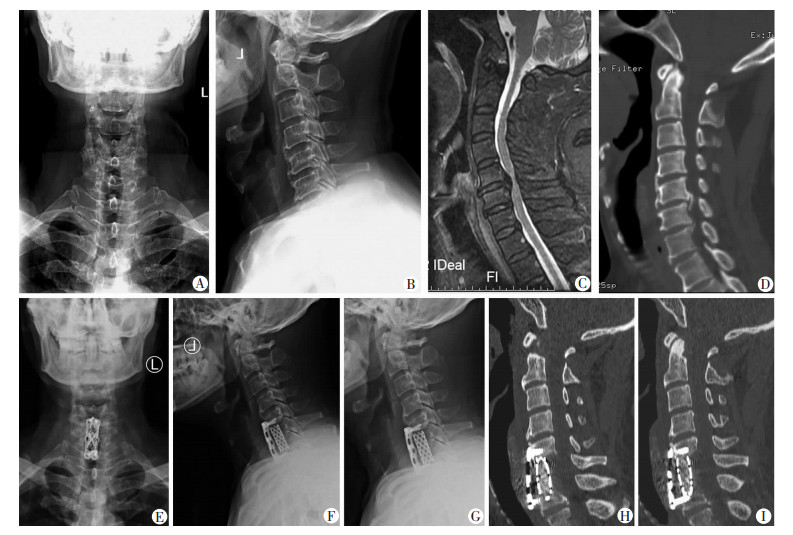
|
| A、B:术前颈椎正、侧位X线片颈5/6和颈6/7椎体前后缘唇样增生;C:术前颈椎MRI T2矢状位颈5/6水平脊髓受压;D:术前颈椎CT矢状位颈5/6椎体后缘有后纵韧带骨化影;E、F:术后1周颈椎正、侧位X线片钛网位置良好;G:术后6个月颈椎侧位X线片见钛网下沉,与螺丝钉触碰;H:术后1周颈椎CT矢状位钛网位置良好;I:术后6个月颈椎CT矢状位钛网下缘下沉,与螺丝钉触碰 图 4 钛网治疗颈椎后纵韧带骨化症患者的影像学观察 |
3 讨论 3.1 应用3D打印微孔钛合金人工椎体治疗颈椎OPLL的优缺点
颈椎OPLL的骨化块位于脊髓的前方,前路手术可直接去除致压物,达到脊髓减压彻底的目的[12-14]。颈椎前路手术为了切除骨化块,需首先切除病变节段的椎体,颈前路椎体次切除后能否重建颈椎稳定性,主要决定因素之一是重建材料的选择[10, 12]。目前常用的重建材料为钛网,钛网克服了自体三面皮质骨块容易吸收移位、需要取自体骨的缺点,但是钛网为厚度只有1 mm的中空笼状结构,与终板的接触面为点状接触,且材料是实体的钛合金,实体钛合金的弹性模量高达110 GPa,远高于椎体区域骨组织的弹性模量,高的弹性模量会在骨-材料界面形成应力遮挡,易导致钛网下沉,造成颈椎前路手术纠正度的丢失,部分患者可引起神经症状[15-18]。3D打印人工椎体是采用逐层堆积的增量化加工方式生产的钛合金微孔结构,通过调整微孔的大小,使其具有与椎体皮质骨和松质骨接近的弹性模量(弹性模量为0.05~30 GPa),克服了实体钛合金高弹性模量的缺点,同时3D打印人工椎体的上下接触面是根据CT扫描数据建模,与上下终板的解剖形态完全一致,从而在术中使人工椎体与椎体的上下终板密切咬合,安装方便快捷,节省了放置融合器的手术时间。本组结果显示两组均能重建颈椎的稳定性,但3D打印人工椎体沉降率明显低于钛网,而且观察组手术时间低于对照组。研究发现,微孔钛合金具有诱导骨长入的生物活性,促进成骨细胞在钛合金表面的黏附[19-20],可为成骨细胞的黏附及分化提供有利环境,本组患者均获得良好的骨性融合。
本研究57例患者中13例达到沉降标准,沉降率22.81%。结合文献[9, 18]分析,重建材料沉降的因素包括:①患者自身情况,如存在骨质疏松等。②处理终板时损伤了终板的皮质骨结构,使重建材料陷入松质骨内形成塌陷。③重建材料与邻近椎体终板的接触面积。接触面积越小,导致终板界面应力越集中,越容易出现假体沉降。④重建材料与终板的结合紧密程度。假体与终板形态越符合,终板的受力越均匀,越不容易出现终板塌陷。⑤过度撑开。随着椎体间撑开距离的增大,造成假体与椎体间的压缩负荷增加,超过终板的承受能力时,假体就可能发生沉降。
3D打印定制或通用人工椎体优点[21]:①3D打印微孔钛合金人工椎体的上下面与椎体上下终板的弧形、斜面形状吻合,能够无限接近解剖形态,从而达到骨-材料界面的密切咬合,减少了支撑体和终板间的压强。观察组只有1例出现假体沉降,为老年患者。②术前通过三维立体重建,完全模拟了去除后纵韧带骨化的椎体高度和形态,高度误差不超过2 mm。术中减压后在撑开器撑开的状态下直接置入3D打印人工椎体,放松撑开器后即刻达到稳定,从而省去了修剪、选择假体的时间。③3D打印微孔钛合金人工椎体具有良好的生物相容性、支撑强度和类似于椎体皮质骨、松质骨的弹性模量,同时骨细胞可长入其中,最终实现骨融合。④不需要取自体骨,易于被医患双方接受。缺点为个体化定制需要2~3 d,延长了术前准备时间,但通用的3D打印人工椎体(每2毫米递增)可克服此缺点。
3.2 切除颈椎后纵韧带骨化块的技巧及注意事项颈椎OPLL前路减压的方法有骨化块彻底切除法和漂浮法[22]。本组采用骨化块彻底切除法,切除骨化块应注意:①根据颈椎后纵韧带骨化的具体部位、范围、椎管矢状面狭窄率选择减压范围,减压范围需超过骨化块的长度和宽度,建立纵向、矢向、横向三维空间减压思路。②切骨先从骨化上下端的未骨化部位进行,从脊髓侧方磨骨切骨。③切除上下椎间盘后,应用超声骨刀的磨头,均匀平行硬膜囊磨骨,直至呈现为菲薄的骨片,先将椎体后壁-骨化物四周磨透,切开上下端黄韧带,小钩探子钩开骨化窗口,硬膜囊逐渐膨胀,骨化物随之漂浮,脊髓压迫即得到初步解除,然后将骨化块逐步分离后整块切除。应用超声骨刀具有振动小和减少出血等优势。④为预防内植物的下沉,术中注意避免损伤骨性终板,同时避免过度撑开。⑤内植物放置在椎体的正中间,位于弧形的中部。
3.3 本研究的局限性和不足本研究属回顾性研究,未能前瞻性地开展对比研究,证据可信度有待提升;颈椎前路支撑物为钛合金材料,术后影像学上存在伪影和遮挡。病例数较少,需要多中心、大样本的远期研究验证。
综上所述,采用3D打印人工椎体或钛网的两种手术方式均能重建OPLL患者颈椎稳定性,取得良好的手术疗效;与钛网相对比,3D打印人工椎体具有更好的骨-材料结合界面,安装快捷,不易出现假体下沉,具有良好的临床应用前景。
| [1] |
MOON B J, CHOI S K, SHIN D A, et al. Prevalence, incidence, comorbidity, and mortality rates of ossification of posterior longitudinal ligament in the cervical spine: a nested case-control cohort study[J]. World Neurosurg, 2018, 117: e323-e328. |
| [2] |
KAWAGUCHI Y, NAKANO M, YASUDA T, et al. Characteristics of ossification of the spinal ligament; incidence of ossification of the ligamentum flavum in patients with cervical ossification of the posterior longitudinal ligament—Analysis of the whole spine using multidetector CT[J]. J Orthop Sci, 2016, 21(4): 439-445. |
| [3] |
HEAD J, RYMARCZUK G, STRICSEK G, et al. Ossification of the posterior longitudinal ligament: surgical approaches and associated complications[J]. Neurospine, 2019, 16(3): 517-529. |
| [4] |
GLINSKI A V, TAKAYANAGI A, ELIA C, et al. Surgical treatment of ossifications of the cervical anterior longitudinal ligament: a retrospective cohort study[J]. Global Spine J, 2021, 11(5): 709-715. |
| [5] |
BADHIWALA J H, LEUNG S N, ELLENBOGEN Y, et al. A comparison of the perioperative outcomes of anterior surgical techniques for the treatment of multilevel degenerative cervical myelopathy[J]. J Neurosurg Spine, 2020, 33(6): 1-8. |
| [6] |
代锦岳, 姜亮, 吴云霞. 颈椎后纵韧带骨化症前路手术并发症及相关因素的研究进展[J]. 中国脊柱脊髓杂志, 2021, 31(6): 566-571. DAI J Y, JIANG L, WU Y X, et al. Research progress of surgical complications and related factors in anterior cervical approach for ossification of the posterior longitudinal ligament[J]. Chin J Spine Spinal Cord, 2021, 31(6): 566-571. |
| [7] |
YU F B, MIAO J H, LIAO X Y, et al. Evaluation of a new type of titanium mesh cage versus the traditional titanium mesh cage for single-level, anterior cervical corpectomy and fusion[J]. Eur Spine J, 2013, 22(12): 2891-2896. |
| [8] |
王志强, 冯皓宇, 马迅, 等. 3D打印人工椎体及椎间融合器在颈椎前路手术中应用的临床效果[J]. 中国修复重建外科杂志, 2021, 35(9): 1147-1154. WANG Z Q, FENG H Y, MA X, et al. Effectiveness of three-dimensional printing artificial vertebral body and interbody fusion cage in anterior cervical surgery[J]. Chin J Reparative Reconstr Surg, 2021, 35(9): 1147-1154. |
| [9] |
潘孟骁, 陈德玉, 陈宇. 颈椎前路椎体次全切除后钛网下沉原因及对颈神经功能的影响[J]. 中国组织工程研究, 2017, 21(15): 2355-2360. PAN M X, CHEN D Y, CHEN Y. Titanium mesh cage subsidence following anterior subtotal vertebrectomy for cervical spondylosis: the underlying mechanism and its effect on cervical neurologic function[J]. Chin J Tissue Eng Res, 2017, 21(15): 2355-2360. |
| [10] |
姬林松, 王艳萍, 陆廷盛, 等. 3D打印多孔钛合金骨小梁融合器与自体髂骨治疗脊髓型颈椎病[J]. 中国组织工程研究, 2022, 26(18): 2817-2822. JI L S, WANG Y P, LU T S, et al. 3D printed porous titanium alloy fusion cage and autologous iliac bone in the treatment of cervical spondylotic myelopathy[J]. Chin J Tissue Eng Res, 2022, 26(18): 2817-2822. |
| [11] |
CHEN Y Q, LV G, WANG B, et al. A comparison of anterior cervical discectomy and fusion (ACDF) using self-locking stand-alone polyetheretherketone (PEEK) cage with ACDF using cage and plate in the treatment of three-level cervical degenerative spondylopathy: a retrospective study with 2-year follow-up[J]. Eur Spine J, 2016, 25(7): 2255-2262. |
| [12] |
李玉伟, 王海蛟, 崔巍, 等. 超声刮匙在颈椎前路椎间盘切除融合术中应用的安全性和有效性评价[J]. 中华医学杂志, 2020, 100(9): 669-673. LI Y W, WANG H J, CUI W, et al. Clinical safety and efficiency of ultrasonic bone curette used in anterior cervical discectomy and fusion surgery[J]. Natl Med J China, 2020, 100(9): 669-673. |
| [13] |
LI S H, PENG J J, XU R Y, et al. Comparison of the surgeries for the ossification of the posterior longitudinal ligament-related cervical spondylosis: a PRISMA-compliant network meta-analysis and literature review[J]. Medicine (Baltimore), 2021, 100(9): e24900. |
| [14] |
WANG H, YANG R N, LIU H, et al. Comparison of interventions for cervical ossification of posterior longitudinal ligament: a systematic review and network meta-analysis[J]. World Neurosurg, 2021, 155: 1-12. |
| [15] |
ZHOU J, LI X L, ZHOU X G, et al. Anterior decompression and hybrid reconstruction with titanium mesh cage plus plate and self-locking stand-alone cage for the treatment of three-level cervical spondylotic myelopathy[J]. J Clin Neurosci, 2017, 43: 196-201. |
| [16] |
LIU X W, CHEN Y, YANG H S, et al. The application of a new type of titanium mesh cage in hybrid anterior decompression and fusion technique for the treatment of continuously three-level cervical spondylotic myelopathy[J]. Eur Spine J, 2017, 26(1): 122-130. |
| [17] |
WEBER M H, FORTIN M, SHEN J, et al. Graft subsidence and revision rates following anterior cervical corpectomy: a clinical study comparing different interbody cages[J]. Clin Spine Surg, 2017, 30(9): E1239-E1245. |
| [18] |
苏再发, 吴培增, 王芳泰, 等. 终板切除对终板-钛网界面应力分布影响的三维有限元分析[J]. 骨科, 2011, 2(1): 9-12. SU Z F, WU P Z, WANG F T, et al. Three-dimensional finite element analysis of the mechanical changes of meshcage-endplate interface following endplate resection[J]. Orthop J, 2011, 2(1): 9-12. |
| [19] |
RAPUANO B E, LEE J J, MACDONALD D E. Titanium alloy surface oxide modulates the conformation of adsorbed fibronectin to enhance its binding to α5β1 integrins in osteoblasts[J]. Eur J Oral Sci, 2012, 120(3): 185-194. |
| [20] |
OLIVARES-NAVARRETE R, GITTENS R A, SCHNEIDER J M, et al. Osteoblasts exhibit a more differentiated phenotype and increased bone morphogenetic protein production on titanium alloy substrates than on poly-ether-ether-ketone[J]. Spine J, 2012, 12(3): 265-272. |
| [21] |
裴国献. 着力打造3D打印在骨科应用的技术平台[J]. 中华创伤骨科杂志, 2016, 18(1): 4-5. PEI G X. Construct a technical platform for application of 3D printing in orthopaedics[J]. Chin J Orthop Trauma, 2016, 18(1): 4-5. |
| [22] |
陈雄生, 赵寅, 周盛源, 等. 前路骨化物整块切除术治疗颈椎后纵韧带骨化症[J]. 中华骨科杂志, 2018, 38(24): 1480-1492. CHEN X S, ZHAO Y, ZHOU S Y, et al. Anterior cervical ossified posterior longitudinal ligament en bloc resection for the treatment of cervical ossification of posterior longitudinal ligament[J]. Chin J Orthop, 2018, 38(24): 1480-1492. |




