2. 050017 石家庄,河北医科大学研究生院;
3. 06100 河北 沧州,沧州市中心医院:麻醉科;
4. 06100 河北 沧州,沧州市中心医院:老年内科;
5. 066000 河北 秦皇岛,秦皇岛市第一医院麻醉科
2. Graduate School of Hebei Medical University, Shijiazhuang, Hebei Province, 050017;
3. Department of Anesthesiology, Cangzhou Central Hospital, Cangzhou, Hebei Province, 061000;
4. Department of Gerontology, Cangzhou Central Hospital, Cangzhou, Hebei Province, 061000;
5. Department of Anesthesiology, First Hospital of Qinhuangdao, Qinhuangdao, Hebei Province, 066600, China
随着人口老龄化的加剧,围术期神经认知功能障碍(perioperative neurocognitive disorders, PND)的发生率显著升高,严重影响老龄患者的康复,给家庭和社会带来了沉重负担。PND不仅可以表现为注意力和记忆力受损为特征的认知能力改变,而且在精神情绪等方面也可发生改变[1]。围术期手术及麻醉药物造成的应激反应能够诱发老龄患者焦虑行为的增加[2],但机制尚未明确。一氧化碳(CO)作为血红蛋白在血红素加氧酶1(heme oxygenase-1, HO-1)催化下的重要代谢产物,多项研究表明CO参与了抗炎、抗缺血再灌注损伤等多种病理生理过程[3-4];已有研究表明,外源性CO可通过抑制星形胶质细胞炎性表达,改善失血性休克后大鼠的焦虑样行为[5]。外源性CO通过改善线粒体功能障碍,抑制线粒体诱发的过度自噬[6],减轻脓毒血症模型小鼠的肺脏损伤[7]。然而,目前外源性CO能否通过抑制星形胶质细胞过度自噬改善老龄大鼠围术期应激后焦虑样行为尚不明确。本研究拟通过建立围术期应激模型,探讨水溶外源性一氧化碳释放分子3(carbon monoxide-releasing molecule 3, CORM-3)对老龄大鼠术后焦虑样行为的作用及其机制,为临床应用提供参考。
1 材料与方法 1.1 实验动物及分组本研究经沧州市中心医院动物伦理委员会批准。清洁级健康雄性SD大鼠,18~20月龄,体质量600~650 g, 由辽宁长生生物技术股份有限公司提供(许可证号:SCXK[辽]2020-0001)。饲养条件:所有大鼠饲养于沧州中心医院动物饲养室内。室内温度设定在(24±1)℃,湿度维持在40%~60%,12 h/12 h明-暗周期交替。采用随机数字表法分为3组(n=12):假手术组(S组)、腹腔探查组(P组)、腹腔探查+CORM-3组(PC组)。P组和PC组大鼠通过腹腔探查并揉肠50 min制备围术期应激模型,S组大鼠只开腹不进行腹腔探查及揉肠;PC组大鼠在手术结束后即刻、24、48 h使用微量泵经尾缘静脉以250 μL/min注射CORM-3(4 mg/kg),S组和P组大鼠仅经尾缘静脉注射等量生理盐水。其中,CORM-3 [fac-Ru(CO)3Cl(κ2-H2NCH2CO2)] 是人工合成的稳定型水溶性过度金属羰基配位化合物,Ru(Ⅱ)配合物通过与血浆蛋白的化学作用迅速释放CO,并可维持有效剂量长达24 h[8],本实验中的剂量根据本课题组前期研究及预实验确定[6]。
1.2 主要试剂及仪器 1.2.1 试剂CORM-3购自美国Selleck公司,改进型柠檬酸钠试剂、免疫封闭液、神经胶质纤维酸性蛋白(GFAP)抗体、Ub抗体、Cy3、FITC、组织裂解液、loading buffer、Quickblock封闭液购自上海碧云天生物技术有限公司,神经元标记抗核抗体(NeuN)、钙离子接头蛋白-1(Iba-1)抗体购自美国Abcam公司,微管相关蛋白-2(MAP-2)抗体购自博士德生物工程有限公司,Beclin1抗体、LC3α/β抗体购自万类生物科技有限公司。
1.2.2 仪器荧光显微镜购自广州市明美光电技术有限公司,体视显微镜购自北京天诺翔科学仪器有限公司,旷场试验视频分析软件购自上海吉量软件科技有限公司,高架十字迷宫视频分析软件购自上海欣软信息科技有限公司。
1.3 CORM-3的制备取4 mg粉末状CORM-3(分子量294.61),1 mL生理盐水溶解,配置浓度为4 mg/mL浓度,过滤,无菌条件下分装为400 μL,-20 ℃保存,注射时提前融解。
1.4 围术期应激模型的制备P组和PC组大鼠8%七氟烷行麻醉诱导后,面罩下自主呼吸吸入4%~5%七氟烷麻醉维持,保留自主呼吸,将大鼠仰卧位固定于铺有温毯的操作台上,设定温毯加热温度为37.0 ℃,建立肛温、血氧饱和度、呼吸及心电图监测。消毒铺巾,利多卡因浸润麻醉,在大鼠上腹部经腹正中线作长约10 cm的切口,用止血钳钝性分离肌肉暴露腹膜,剪开腹膜进入腹腔,用生理盐水浸润的棉签按肝、脾、左肾、右肾、小肠及结肠的顺序进行探查,持续10 min;之后用拇指和食指由十二指肠端向盲肠端对肠壁进行轻柔摩擦,摩擦后放回腹腔,持续揉肠40 min;揉肠结束后关闭腹腔,手术结束后使用0.1%的盐酸罗哌卡因2 mL进行局部浸润麻醉作为术后镇痛。S组大鼠仅开腹,不进行腹腔探查及揉肠操作,其余操作同上述两组。
1.5 行为学试验 1.5.1 旷场试验所有大鼠于手术后第7天行旷场试验。采用方形旷场,在旷场的底部(60 cm×60 cm× 45 cm)画出16个等大的方格,中央四格作为中央格,其余作为外周格。将大鼠放入旷场的中央格处后, 使用动物行为学视频分析软件记录5 min内大鼠位于中央格内的停留时间。每只大鼠实验结束后,使用75%的乙醇将旷场的底部擦拭干净,以消除气味残留。通过大鼠中央格停留时间百分比=中央格停留时间/总时间×100%,评估大鼠的焦虑程度。
1.5.2 高架十字迷宫试验所有大鼠于旷场试验结束后第2天行高架十字迷宫试验。高架十字迷宫正中间是一个正方形(10 cm×10 cm)的中央区,由四周2个开放臂(50 cm×10 cm)和2个闭合臂(50 cm×10 cm)交叉构成,高架距地面45 cm。测试时将大鼠面朝开放臂置于中央区,使用SuperMaze动物行为学视频分析软件记录5 min内大鼠进入开放臂和闭合臂的次数及相应的停留时间。每只大鼠实验结束后,使用75%的乙醇擦拭干净,以消除气味残留。用大鼠开放臂停留时间百分比=开放臂停留时间/总时间×100%,以及开放臂进入次数百分比=进入开放臂次数/总的探索次数×100%,评估大鼠焦虑程度。
1.6 免疫荧光染色于高架十字迷宫试验结束后,每组各取6只大鼠,8%七氟烷麻醉诱导,4%~5%七氟烷进行麻醉维持,将注射针插入左心室至主动脉,开放生理盐水灌注,心耳流出清亮液体后,改为10%甲醛固定液,直至动物呈僵硬状,取脑组织,在10%甲醛内固定48 h后制作石蜡切片。选取距离-2.8 mm到-2.9 mm含有杏仁核部位的组织切片,切片脱蜡水化后用改进型柠檬酸钠试剂煮沸20 min行抗原修复并冷却至室温,磷酸缓冲盐溶液(PBS)洗涤3次后使用1% Triton X-100溶液孵育20 min,免疫封闭液封闭1 h。分别加入小鼠抗大鼠GFAP单克隆IgG(稀释比1 ∶100),山羊抗鼠Iba-1单克隆IgG(稀释比1 ∶200),小鼠抗大鼠MAP-2单克隆IgG(稀释比1 ∶100),小鼠抗大鼠NeuN单克隆IgG(稀释比1 ∶200);分别加入兔抗大鼠Beclin1多克隆IgG(稀释比1 ∶100),兔抗大鼠Ub多克隆IgG(稀释比1 ∶100),4 ℃下孵育过夜。于第2天滴加二抗,Cy3标记山羊抗小鼠IgG(稀释比1 ∶500)、Cy3标记驴抗山羊IgG(稀释比1 ∶500)和FITC标记山羊抗兔IgG(稀释比1 ∶500),室温下孵育1 h,DAPI标记细胞核。由不知分组情况的病理技术人员在荧光显微镜下观察杏仁核区GFAP/Beclin1/DAPI、GFAP/Ub/DAPI,Iba-1/Beclin1/DAPI、Iba-/Ub/DAPI、MAP-2/Beclin1/DAPI、MAP-2/Ub/DAPI及NeuN阳性细胞的表达。每组随机选取6个高倍视野(350 μm×220 μm)采用Image J软件分析目的蛋白Beclin1、Ub与GFAP、Iba-1、MAP-2的共表达系数;通过NeuN在每个高倍视野中的阳性细胞数,表示神经元密度。
1.7 Western blot检测高架十字迷宫试验结束后每组各取3只大鼠,在七氟烷吸入麻醉下盐水经左心室-主动脉灌注,待右心耳流出清亮液体后断头处死大鼠,在体视显微镜下分离杏仁核,取100 mg在4 ℃裂解液中充分剪碎并充分匀浆。4 ℃条件下,12 000×g离心5 min,离心半径8 cm,取上清液即为总蛋白。BCA法测定蛋白浓度后,加入loading buffer,100 ℃煮沸5 min进行蛋白变性。每孔上样40 μg,经电泳后将蛋白转到PVDF膜,Quickblock封闭液封闭10 min,加入兔抗大鼠LC3α/β多克隆IgG(稀释比1 ∶500),4 ℃孵育过夜。第2天经Western洗涤缓冲液(TBS-T)膜3次后分别加入二抗,采用电化学发光法发光显影,GAPDH作为内参蛋白,使用Image J软件分析目的条带灰度值。
1.8 电镜标本制备高架十字迷宫实验结束后每组取3只大鼠,方法同上述组织病理学取样,在体视显微镜下取杏仁核组织样置入戊二醛溶液中固定48 h,包埋、切片之后,使用透射电子显微镜(型号:JEM-1400,日本)下观察线粒体、自噬小体等超微结构。
1.9 统计学分析采用SPSS 25.0软件进行统计学分析,符合正态分布的计量资料以x±s,组间比较采用单因素方差分析,采用Turkey进行组间两两比较,采用GraphPad Prism 8进行统计作图,检验水准α=0.05。
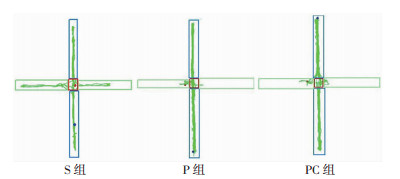
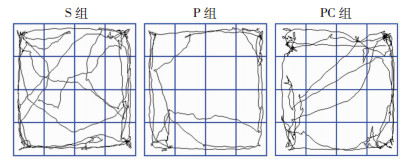
2 结果 2.1 动物行为学与S组比较,P组和PC组大鼠开放臂停留时间百分比、开放臂进入次数百分比、中央格停留时间百分比显著下降(P < 0.05);与P组比较,PC组上述指标显著增加(P < 0.05,表 1,图 1~2)。
| 组别 | 开放臂时间百分比 | 开放臂次数百分比 | 中央格时间百分比 |
| S组 | 25.45±5.92 | 65.70±7.44 | 7.92±3.06 |
| P组 | 13.34±2.45a | 48.69±2.96a | 1.98±1.23a |
| PC组 | 18.73±3.31ab | 59.80±2.05ab | 4.68±1.74ab |
| a:P < 0.05,与S组比较;b:P < 0.05,与P组比较 | |||
|
| 蓝色臂为闭合臂,绿色臂为开放臂 图 1 3组大鼠高架十字迷宫活动轨迹 |
|
| 图 2 3组大鼠旷场试验活动轨迹 |
2.2 神经元NeuN免疫荧光染色
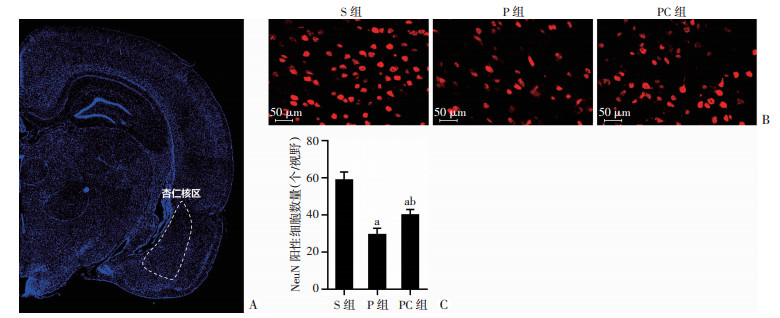
与S组比较,P组和PC组大鼠杏仁核区NeuN阳性细胞数量(神经元)显著减少(P < 0.05);与P组比较,PC组大鼠杏仁核区NeuN阳性细胞数量显著增加(P < 0.05,图 3)。
|
| A:杏仁核区示意图;B:NeuN免疫荧光染色结果;C:神经元数量统计分析 a:P < 0.05,与S组比较,;b:P < 0.05,与P组比较 图 3 免疫荧光染色观察3组大鼠杏仁核区NeuN变化 |
2.3 免疫荧光染色
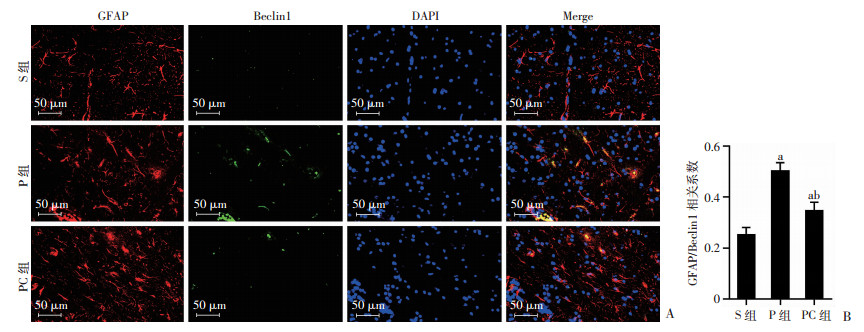
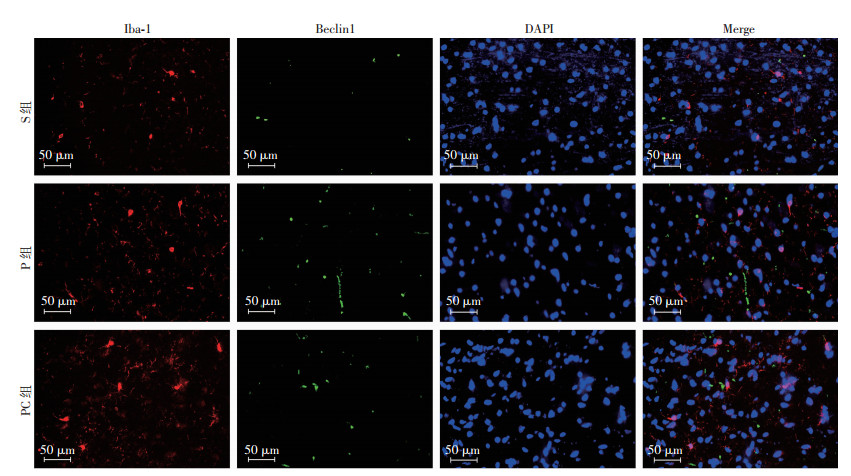
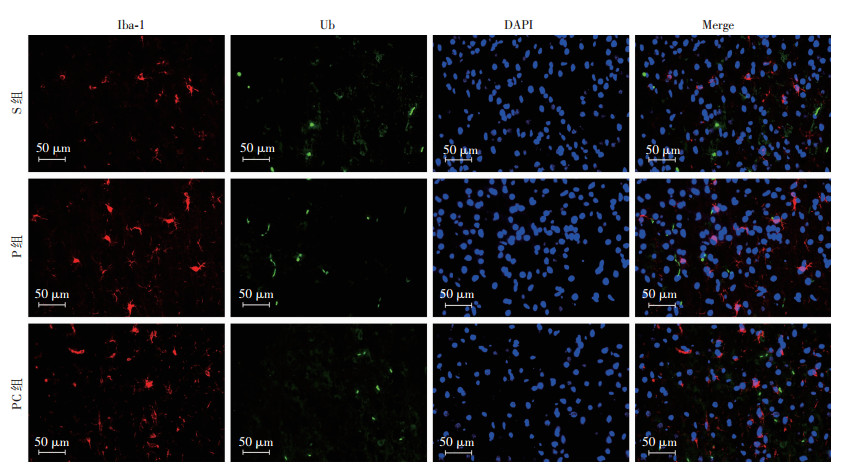
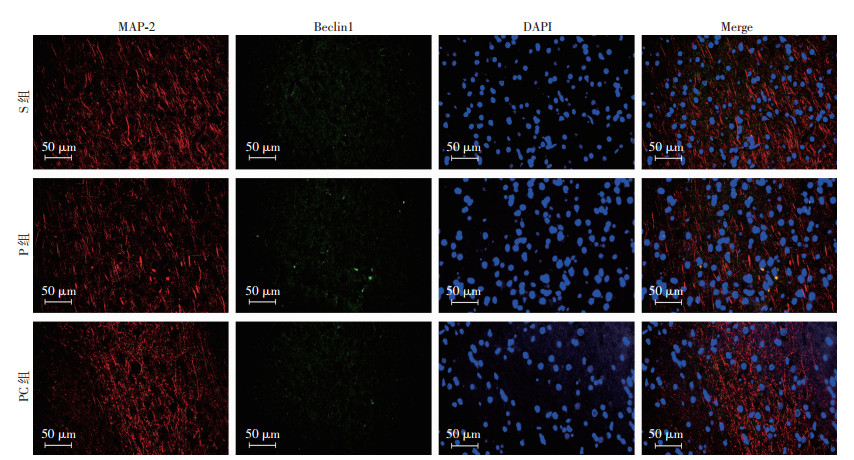
与S组比较,P组和PC组大鼠杏仁核区星形胶质细胞内Beclin1和Ub表达上调(P < 0.05);与P组比较,PC组大鼠上述指标表达下调(P < 0.05,图 4~5)。3组大鼠杏仁核区小胶质细胞和神经元内Beclin1和Ub表达差异无统计学意义(表 2,图 6~9)。
|
| A:免疫荧光染色观察GFAP/Beclin1/DAPI;B:统计分析结果 a:P < 0.05,与S组比较;b:P < 0.05,与P组比较 图 4 免疫荧光染色观察3组大鼠杏仁核区GFAP/Beclin1/DAPI变化 |

|
| A:免疫荧光染色观察GFAP/Ub/DAPI;B:统计分析结果 a:P < 0.05,与S组比较;b:P < 0.05,与P组比较 图 5 免疫荧光染色观察3组大鼠杏仁核区GFAP/Ub/DAPI变化 |
| 组别 | Iba-1/Beclin1相关系数 | Iba-1/Ub相关系数 | MAP-2/Beclin1相关系数 | MAP-2/Ub相关系数 |
| S组 | 0.22±0.01 | 0.24±0.03 | 0.23±0.02 | 0.30±0.03 |
| P组 | 0.24±0.02 | 0.27±0.01 | 0.26±0.02 | 0.32±0.02 |
| PC组 | 0.23±0.02 | 0.26±0.02 | 0.23±0.03 | 0.31±0.02 |
| F | 1.65 | 2.68 | 2.70 | 0.96 |
| P | 0.225 | 0.101 | 0.100 | 0.404 |
|
| 图 6 免疫荧光染色观察3组大鼠杏仁核区Iba-1/Beclin1/DAPI变化 |
|
| 图 7 免疫荧光染色观察3组大鼠杏仁核区Iba-1/Ub/DAPI变化 |
|
| 图 8 免疫荧光染色观察3组大鼠杏仁核区MAP-2/Beclin1/DAPI变化 |

|
| 图 9 免疫荧光染色观察3组大鼠杏仁核区MAP-2/Ub/DAPI变化 |
2.4 Western blot检测结果
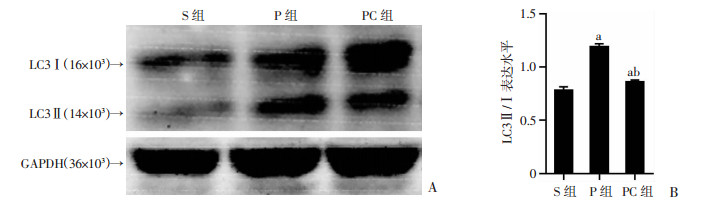
与S组比较,P组和PC组大鼠杏仁核内LC3Ⅱ/Ⅰ的比值上调(P < 0.05);与P组比较,PC组大鼠杏仁核内LC3Ⅱ/Ⅰ的比值下调(P < 0.05,图 10)。
|
| A:Western blot检测结果;B:半定量分析 a:P < 0.05,与S组比较;b:P < 0.05,与P组比较 图 10 Western blot检测3组大鼠杏仁核区蛋白 |
2.5 电镜观察
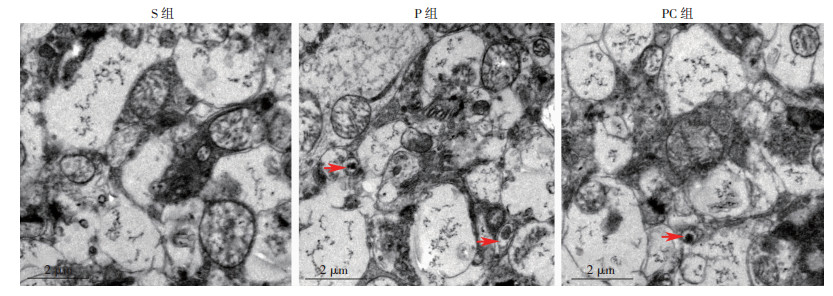
透射电镜下观察,S组大鼠杏仁核区细胞器形态正常,可见丰富的正常线粒体等细胞器,未见自噬小体;P组大鼠杏仁核区线粒体肿胀、线粒体嵴断裂,可见自噬小体;PC组大鼠上述指标较P组明显得到改善(图 11)。
|
| 红色箭头表示自噬小体 图 11 透射电镜下观察3组大鼠杏仁核区神经细胞形态学变化 |
3 讨论
本实验参照文献[9]报道的方法并加以改进,采用在七氟烷麻醉下腹腔探查和揉肠的方法模拟老龄患者围术期应激的病理生理过程。高架十字迷宫试验和旷场试验是国际公认的用于评价焦虑状态动物模型情绪反应的经典方法[10]。其中,高架十字迷宫中开放臂停留时间百分比和开放臂进入次数百分比可用来评价大鼠的焦虑程度;旷场试验中中央格停留时间百分比也可以用来评价大鼠的焦虑程度。本实验结果显示,老龄大鼠术后高架十字迷宫开放臂停留时间百分比、开放臂进入次数百分比以及旷场试验中央格停留时间百分比显著下降,以上结果显示,围术期应激可导致老龄大鼠术后焦虑样行为。
杏仁核作为中枢神经边缘系统的重要组成部分,在调节情绪变化和应激恐惧中发挥着重要作用,焦虑行为与杏仁核功能密切相关。杏仁核神经元功能受损参与了焦虑行为的发生与发展,文献[11]的研究也证实了小鼠焦虑样行为与神经元损伤有关。本实验结果显示,老龄大鼠围术期应激后杏仁核区神经元数量显著下降,以上结果显示杏仁核区神经元损伤可能与术后焦虑样行为增加相关。
自噬广泛存在于真核细胞中,是一种双向调节的溶酶体降解途径,在应激时激活细胞自噬可提供能量或在损伤后清除受损的细胞器或蛋白质维持细胞存活[12];而过度诱发的细胞自噬可造成细胞死亡。已有研究表明,认知功能障碍、情绪变化等神经功能障碍与自噬通量的增加相关[13]。本实验结果显示,围术期应激后自噬相关蛋白Beclin1及Ub在星形胶质细胞内表达上调,而小胶质细胞及神经元内自噬相关蛋白表达并无差异;同时,杏仁核区LC3Ⅱ/Ⅰ的比值上调,并通过透射电镜观察到杏仁核区自噬小体形成。以上结果显示,围术期应激后造成了杏仁核区星形胶质细胞过度自噬。星形胶质细胞作为广泛存在于中枢神经系统中的细胞,在调节谷氨酸神经递质的转运中发挥了重要作用[14];星形胶质细胞过度自噬,可干扰杏仁核区谷氨酸等神经递质的转运,谷氨酸的大量积聚造成持续神经元兴奋性可导致神经元死亡[15],从而导致焦虑行为显著增加。结合行为学结果,围术期应激造成大鼠焦虑样行为的增加,可能与杏仁核区星形胶质细胞自噬过度激活可能与术后焦虑行为增加相关。
CORM-3作为一种水溶性CO化合物,可在体内持续24 h以上释放CO,从而发挥抗炎、抗凋亡的作用[3]。外源性CO能够通过改善线粒体膜电位水平,减少细胞内氧化应激造成的活性氧增加,线粒体内DNA释放[16];活性氧及线粒体DNA释放可诱发细胞内自噬信号通路的过度活化,造成细胞功能障碍和死亡[17]。既往研究表明,CORM-3对创伤后应激大鼠的认知功能障碍及情绪变化具有改善作用[18],能够减少失血性休克复苏大鼠的焦虑样行为[5]。本实验结果显示,CORM-3尾缘静脉注射后的围术期应激老龄大鼠,高架十字迷宫开放臂停留时间百分比、开放臂进入次数百分比以及旷场试验中央格停留时间百分比显著升高;杏仁核区神经元数量增加,星形胶质细胞内自噬相关蛋白Beclin1、Ub表达下调,LC3Ⅱ/Ⅰ的比值下调,透射电镜下线粒体形态显著改善。以上结果显示,CORM-3可能通过抑制杏仁核区星形胶质细胞过度自噬,增加神经元数量,从而改善术后焦虑行为。
本研究参考文献[19]报道的方法使用了Iba-1作为小胶质细胞的标记蛋白,但已有研究证明TMEM119及CX3CR1等标记蛋白能够进一步排除巨噬细胞在中枢神经系统中的干扰[20],我们也将进一步探讨使用其他小胶质细胞标记蛋白进行该模型的研究。另外,抑制星形胶质细胞过度自噬如何减轻神经元损伤的机制还需进一步探索。
综上,外源性CO能够改善老龄大鼠围术期应激后的焦虑样行为,其机制可能与抑制杏仁核区星形胶质细胞过度自噬相关。
| [1] |
NEYMARK M I, SHMELEV V V, RAKHMONOV A A. Violations of higher mental functions and their correction in patients undergoing video laparoscopic cholecystectomy under conditions of inhalation anesthesia with sevoflurane[J]. Khirurgiia, 2020(8): 69-74. |
| [2] |
KAGERBAUER S M, MARTIN J, ULM B, et al. Influence of perioperative stress on central and peripheral oxytocin and arginine-vasopressin concentrations[J]. J Neuroendocrinol, 2019, 31(10): e12797. |
| [3] |
ZHANG L M, ZHANG D X, FU L, et al. Carbon monoxide-releasing molecule-3 protects against cortical pyroptosis induced by hemorrhagic shock and resuscitation via mitochondrial regulation[J]. Free Radic Biol Med, 2019, 141: 299-309. |
| [4] |
BERRINO E, CARRADORI S, ANGELI A, et al. Dual carbonic anhydrase Ⅸ/Ⅻ inhibitors and carbon monoxide releasing molecules modulate LPS-mediated inflammation in mouse macrophages[J]. Antioxidants (Basel), 2021, 10(1): 56. |
| [5] |
ZHANG D X, ZHENG W C, BAI Y, et al. CORM-3 improves emotional changes induced by hemorrhagic shock via the inhibition of pyroptosis in the amygdala[J]. Neurochem Int, 2020, 139: 104784. |
| [6] |
RYTER S W. Heme oxygenase-1/carbon monoxide as modulators of autophagy and inflammation[J]. Arch Biochem Biophys, 2019, 678: 108186. |
| [7] |
KUO Y W, HARRIS R S, HESS D R, et al. Endogenous carbon monoxide production and diffusing capacity of the lung for carbon monoxide in Sepsis-induced acute respiratory distress syndrome[J]. Crit Care Explor, 2020, 2(12): e0286. |
| [8] |
SANTOS-SILVA T, MUKHOPADHYAY A, SEIXAS J D, et al. CORM-3 reactivity toward proteins: the crystal structure of a Ru(Ⅱ) dicarbonyl-lysozyme complex[J]. J Am Chem Soc, 2011, 133(5): 1192-1195. |
| [9] |
CAO Y Y, LIU T T, LI Z Q, et al. Neurofilament degradation is involved in laparotomy-induced cognitive dysfunction in aged rats[J]. Aging, 2020, 12(24): 25643-25657. |
| [10] |
HOU J Q, WANG C, MA D, et al. The cardioprotective and anxiolytic effects of Chaihujialonggumuli Granule on rats with anxiety after acute myocardial infarction is partly mediated by suppression of CXCR4/NF-κB/GSDMD pathway[J]. Biomed Pharmacother, 2021, 133: 111015. |
| [11] |
ALVES DE LIMA K, RUSTENHOVEN J, DA MESQUITA S, et al. Meningeal γδ T cells regulate anxiety-like behavior via IL-17a signaling in neurons[J]. Nat Immunol, 2020, 21(11): 1421-1429. |
| [12] |
董训虎, 陈明亮, 叶枫, 等. 氮芥通过激活腺苷酸活化蛋白激酶/自噬通路抑制角质形成细胞增殖活力[J]. 第三军医大学学报, 2019, 41(14): 1295-1300. DONG X H, CHEN M L, YE F, et al. Nitrogen mustard inhibits keratinocyte proliferation by activating AMPK/autophagy pathway[J]. J Third Mil Med Univ, 2019, 41(14): 1295-1300. |
| [13] |
CHO S, JUNG Y J, SUH E C, et al. The recovery from transient cognitive dysfunction induced by propofol was associated with enhanced autophagic flux in normal healthy adult mice[J]. Brain Res, 2018, 1700: 99-108. |
| [14] |
SCOGGIN J L, TAN C, NGUYEN N H, et al. An enzyme-based electrochemical biosensor probe with sensitivity to detect astrocytic versus glioma uptake of glutamate in real time in vitro[J]. Biosens Bioelectron, 2019, 126: 751-757. |
| [15] |
KUO Y M, HSU P C, HUNG C C, et al. Soluble epoxide hydrolase inhibition attenuates excitotoxicity involving 14, 15-epoxyeicosatrienoic acid-mediated astrocytic survival and plasticity to preserve glutamate homeostasis[J]. Mol Neurobiol, 2019, 56(12): 8451-8474. |
| [16] |
FU L, ZHANG D X, ZHANG L M, et al. Exogenous carbon monoxide protects against mitochondrial DNA-induced hippocampal pyroptosis in a model of hemorrhagic shock and resuscitation[J]. Int J Mol Med, 2020, 45(4): 1176-1186. |
| [17] |
MATTSON M P, LONGO V D, HARVIE M. Impact of intermittent fasting on health and disease processes[J]. Ageing Res Rev, 2017, 39: 46-58. |
| [18] |
LI Y, ZHANG L M, ZHANG D X, et al. CORM-3 ameliorates neurodegeneration in the amygdala and improves depression- and anxiety-like behavior in a rat model of combined traumatic brain injury and hemorrhagic shock[J]. Neurochem Int, 2020, 140: 104842. |
| [19] |
ITO D, TANAKA K, SUZUKI S, et al. Enhanced expression of Iba1, ionized calcium-binding adapter molecule 1, after transient focal cerebral ischemia in rat brain[J]. Stroke, 2001, 32(5): 1208-1215. |
| [20] |
SNIJDERS G J L J, VAN ZUIDEN W, SNEEBOER M A M, et al. A loss of mature microglial markers without immune activation in schizophrenia[J]. Glia, 2021, 69(5): 1251-1267. |




