2. 041000 山西 临汾,临汾市中心医院乳腺甲状腺外科
2. Department of Breast and Thyroid Surgery, Linfen Central Hospital, Linfen, Shanxi Province, 041000, China
近年来,随着健康意识的提高以及查体的普及,甲状腺癌有逐年增多的趋势[1-3]。但甲状腺癌的治疗模式并无明显改变,手术仍是最有效的治疗方式[4]。传统的开放手术使患者颈部留有明显疤痕,影响患者美观,降低生活质量。19世纪末,为改善甲状腺手术后患者的颈部外观,GAGNER[5]和LIRICI等[6]首先报道腔镜下甲状腺手术方式。但由于长而直的手术器械在腔镜下操作容易受“筷子效应”的影响,限制了其在较为复杂的甲状腺癌手术中的广泛应用[7-8]。2007年,KANG等[9-10]将达芬奇机器人应用于甲状腺手术,此后机器人手术在甲状腺癌的应用逐渐增多,且证明其疗效与安全性能达到开放手术的效果。由于机器人手术系统具有3D视野、机器人扶镜以及可弯曲的内关节器械等优势,使其比普通腔镜手术更适合进行精准复杂操作[11-12]。甲状腺全切加双中央区清扫作为治疗甲状腺癌的主要术式之一,对术后甲状旁腺功能和喉返神经影响也最大,而既往在有关机器人手术对这一术式的比较研究较少。为了进一步准确探讨机器人手术治疗甲状腺癌的疗效与安全性,本研究分析乳腺甲状腺外科机器人手术与开放手术进行甲状腺全切加双侧中央区淋巴结清扫术的甲状腺癌患者的临床资料及治疗结果,为甲状腺癌手术治疗术式选择提供依据。
1 资料与方法 1.1 病例资料 1.1.1 研究对象选择采用回顾性病例对照研究方法,收集2018年1月至2020年5月在陆军军医大学第一附属医院诊断为甲状腺癌并住院接受手术治疗的病例共229例。其中采用单侧腋窝双侧乳晕入路机器人手术105例(机器人组),年龄24~67岁,男性14例,女性91例。本研究中采用的机器人手术设备为达芬奇手术系统(DaVinci® S or Si, Intuitive Surgical Inc., Sunnyvale, CA, USA)。开放组124例,采用传统开放手术,年龄19~63岁,男性29例,女性95例。为了减少选择性偏移,两组患者手术切除范围均相同(甲状腺全切+双侧中央区淋巴结清扫术),并由同一组医师完成。本研究获得陆军军医大学第一附属医院伦理委员会审批[(B)KY2021158]。
1.1.2 纳入标准① 术后病理确诊为甲状腺乳头状癌;②病灶最大径 < 2 cm;③侧颈部无明显肿大或明确的转移淋巴结;④手术切除范围为甲状腺全切+双侧中央区淋巴结清扫。
1.1.3 排除标准① 既往甲状腺手术史或颈部放疗史;②肿瘤侵出甲状腺后被膜并侵及喉返神经、食管、气管或颈总动脉等重要结构;③术后失访。
1.2 方法 1.2.1 手术方法开放组:麻醉成功后,患者取仰卧位,肩部垫高,头后仰过伸,常规铺巾。沿胸骨切迹上缘2 cm取长5~10 cm弧形切口,在颈阔肌深面游离皮瓣,上至甲状软骨上缘,下达胸骨柄上缘,两侧到胸锁乳突肌中线以外。纵行切开颈白线,显露甲状腺双侧叶,向双侧甲状腺实质内分别注入纳米碳约0.2 mL,用于负显甲状旁腺并示踪区域淋巴结。于气管前离断甲状腺峡部,游离左甲状腺上级,切断并结扎甲状腺上极血管。游离左甲状腺下极,切断并结扎甲状腺下极血管,紧贴甲状腺真被膜游离甲状腺组织。游离甲状腺外侧,切断结扎甲状腺中静脉。向前提拉甲状腺下极,辨认并保护喉返神经,切断Berry韧带,完整切除左侧甲状腺叶。同法切除右侧甲状腺。充分显露左中央区,于气管前提起中央区组织,于气管中线处切断,沿胸骨柄上缘平面向上向左分离脂肪淋巴组织,显露并保护左喉返神经,将左颈总动脉至气管之间的淋巴组织一并切除。同法完成右中央区清扫,右侧同时清扫喉返神经后方的淋巴脂肪组织。尽量保护并原位保留甲状旁腺。对于无法保留或血运障碍的甲状旁腺进行同侧胸锁乳突肌内注射移植。蒸馏水冲洗术野,于患侧甲状腺残腔置入引流管1根经原切口一侧引出并固定,缝合颈白线,逐层间断缝合颈阔肌、皮下组织。医用粘合胶粘合皮肤切口。
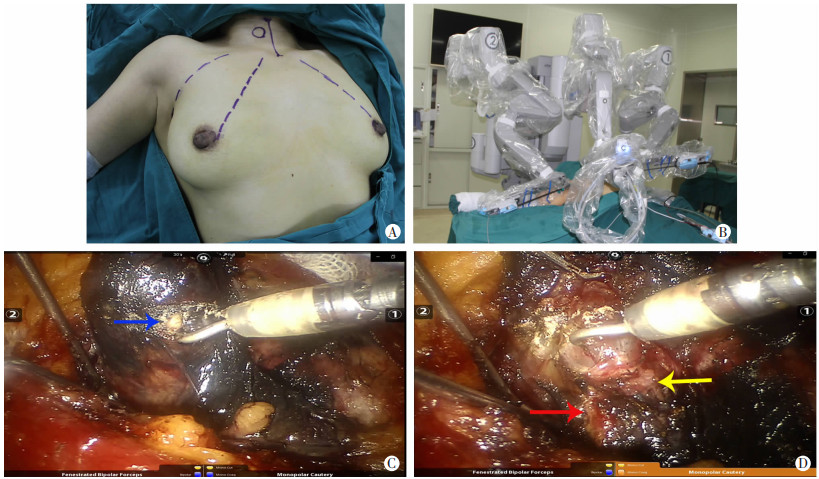
机器人组:麻醉及体位同开放组,但需将右侧上肢外展。采用的UABA手术入路参照文献[13-14]进行:分别于左、右乳晕内侧缘以及右侧腋窝标记切口,长1~2 cm,并标记其至双侧胸锁关节或锁骨内三分之一处的Trocar穿刺路径(图 1A)。沿标记线皮下注射肾上腺素盐水200~400 mL(含罗哌卡因20 mL+1 mg盐酸肾上腺素),使穿刺隧道皮下组织间隙充分肿胀,经标记切口分别置入Trocar并在胸骨上窝会师,将机械臂与Trocar相连接,置入观察镜和机器人专用操作器械(图 1B)。充入CO2,设定充气压力6 mmHg。镜下皮瓣游离范围、纳米炭应用、甲状腺切除、中央区清扫方法以及喉返神经保护与开放手术大致相同。不同之处为甲状旁腺保护方法采用超精细被膜解剖技术[13-14]。自甲状腺下极处紧贴甲状腺真被膜切断甲状腺下动、静脉后,提起甲状腺下极,切开并保留甲状腺后方的真被膜,辨认甲状旁腺,保留上位及下位甲状旁腺及其三级血管分支,同时尽可能保留甲状腺下动脉的上行支以及甲状腺上动脉的下行支,以完整保留甲状旁腺血供(图 1C、D)。
|
|
蓝色箭头示真被膜下甲状旁腺;红色箭头示保留完好的被膜下甲状旁腺;黄色箭头示甲状旁腺供应血管 A: UABA入路切口与穿刺径路标记; B: UABA入路手术操作中机械臂与操作器械摆放位置; C: 甲状腺腺叶切除过程中发现的真被膜下甲状旁腺; D: 完整保留的真被膜下甲状旁腺及其血供 图 1 UABA入路机器人甲状腺癌手术中真被膜下旁腺的识别与保护方法 |
甲状腺及中央区淋巴结清扫完成后,将左侧乳晕的机械臂及Trocar拆除,换用取标本专用Trocar(直径2 cm),取出切除的甲状腺和中央区淋巴组织[14]。蒸馏水彻底冲洗术野,再次置入机器人专用Trocar并连接机械臂,4-0可吸收线间断缝合颈白线,于患侧甲状腺残腔置入引流管1根经左乳晕切口引出并固定,双侧癌时引流管植入病灶较大一侧。拆除机械臂及Trocar,关闭切口。
1.2.2 术后处理及观察指标患者术后甲状腺素抑制及131I治疗参照中国甲状腺癌诊治指南(2018版)进行。主要观察指标包括暂时性及永久性甲状旁腺功能减退发生率,暂时性及永久性喉返神经损伤发生率;次要指标包括手术时间、术中出血量、术中甲状旁腺移植情况、术后出血情况(需要打开伤口或外科处理的出血)、是否有手术区域感染,术后3 d引流量、切除中央区淋巴结数、术后患者满意度以及甲状腺球蛋白(TG)水平。通过查阅门诊病历及电话随访了解甲状旁腺功能减退以及声音嘶哑的发生情况,发生声音嘶哑或甲状旁腺功能减退后在6个月内恢复者为暂时性,否则为永久性。电话询问患者音质的变化, 如是否说话易疲劳以及是否能发高音等,询问患者术后满意度。复查彩超了解是否有局部复发。
1.3 统计学分析采用SPSS 19.0软件进行统计分析。检验计量资料方差齐、呈正态分布时采用t检验,反之则采用Mann-Whitney U检验,计数资料比较采用χ2检验或者非参数检验,P < 0.05为差异有统计学意义。
2 结果 2.1 两组患者基线与手术结果比较两组患者基线资料见表 1。两组患者术中出血量比较差异无统计学意义。机器人组手术时间及术后3 d引流量明显大于开放组(P < 0.05)。两组患者切除淋巴结总数及淋巴结癌转移数差异无统计学意义。机器人组病理标本中检出旁腺(误切)比例低于开放组,但差异无统计学意义(17.14% vs 20.97%)。开放组甲状旁腺移植的比例明显高于机器人组(P < 0.05),见表 2。
| 组别 | n | 性别(男/女) | 年龄/岁 | BMI/kg·m-2 | 肿瘤直径/mm | 病灶(单发/多发) |
| 开放组 | 124 | 29/95 | 36.36±8.58 | 23.30±3.57 | 10.72±4.34 | 71/53 |
| 机器人组 | 105 | 14/91 | 43.52±10.03 | 23.67±3.88 | 10.37±3.99 | 58/47 |
| χ2/t值 | 3.768 | 5.822 | 0.751 | 0.631 | 0.094 | |
| P值 | 0.052 | < 0.001 | 0.454 | 0.529 | 0.759 |
| 组别 | n | 手术时间/min | 术中出血/mL | 术后3 d引流/mL | 清扫淋巴结数/枚 | 转移淋巴结数/枚 | 病理标本检出甲状旁腺 | 甲状旁腺移植 |
| 开放组 | 124 | 113.98±46.03 | 50.48±13.67 | 120.79±49.96 | 12.97±6.77 | 2.15±2.84 | 26(20.97) | 81(65.32) |
| 机器人组 | 105 | 156.57±37.87 | 50.31±23.37 | 141.57±43.16 | 11.23±6.77 | 1.47±2.40 | 18(17.14) | 3(2.86) |
| χ2/t值 | 7.559 | 0.068 | 3.649 | 1.926 | 1.930 | 0.536 | 95.517 | |
| P值 | < 0.001 | 0.946 | < 0.001 | 0.055 | 0.055 | 0.464 | < 0.001 |
2.2 两组患者术后并发症
开放组术后暂时性声音嘶哑发生率为8.06%,高于机器人组(5.71%),差异无统计学意义,但永久性声音嘶哑发生率开放组高于机器人组,差异有统计学意义(P < 0.05)。开放组术后暂时性及永久性甲状旁腺功能减退发生率均高于机器人组(P < 0.05)。两组手术对术后血钙影响差异明显,机器人组术后暂时性及永久性低钙血症发生率均低于开放组(P < 0.05)。两组患者术后半年说话时仍不能发高音或说话易疲劳发生率机器人组低于开放组(P < 0.05)。两组患者术后均未出现需要二次手术止血的情况发生。机器人组术后无感染发生,开放组有1例术后出现手术区域感染,抗感染后治愈出院, 见表 3。
| 组别 | n | 甲状旁腺功能减退 | 低钙血症 | 声音嘶哑 | 说话易疲劳/不能发高音 | |||||
| 暂时性 | 永久性 | 暂时性 | 永久性 | 暂时性 | 永久性 | |||||
| 开放组 | 124 | 80(64.52) | 7(5.65) | 96(77.42) | 7(5.65) | 10(8.06) | 7(5.65) | 21(16.94) | ||
| 机器人组 | 105 | 30(28.57) | 0(0.00) | 67(63.81) | 0(0.00) | 6(5.71) | 0(0.00) | 4(3.81) | ||
| χ2值 | 29.429 | - | 5.134 | - | 0.483 | - | 10.073 | |||
| P值 | < 0.001 | 0.016 | 0.023 | 0.016 | 0.487 | 0.016 | 0.002 | |||
2.3 甲状旁腺移植与术后甲状旁腺功能减退发生情况
机器人组有3例术中行甲状旁腺移植,均移植甲状旁腺1枚,术后无永久性甲状旁腺功能减退发生。开放组81例术中行甲状旁腺移植,术中未移植甲状旁腺病例中暂时性及永久性甲状旁腺功能减退发生率均高于移植病例(P < 0.05),见表 4。
| 组别 | n | 暂时性甲状旁腺功能减退 | 永久性甲状旁腺功能减退 |
| 未移植 | 43 | 34(79.07) | 6(13.95) |
| 移植 | 81 | 48(59.26) | 1(1.23) |
| χ2 | 4.922 | - | |
| P | 0.027 | 0.007 |
2.4 术后131I治疗及随访情况
术后开放组与机器人组接受131I治疗的例数比较,差异无统计学意义。术后6个月时,患者非TSH刺激状态TG水平比较,两组差异无统计学意义。术后经12~36个月的随访,两组均未发现术区明显肿瘤复发。131I治疗、复发情况及TG结果见表 5。
| 组别 | n | 131I治疗 | 术后非TSH刺激状态TG水平 |
| 开放组 | 124 | 37(29.84) | 0.040(0.040~0.245) |
| 机器人组 | 105 | 23(21.90) | 0.040(0.040~0.180) |
| χ2/Z | 1.851 | 0.675 | |
| P | 0.174 | 0.500 |
术后随访发现,两组患者手术结束1年后颈部不适发生率差异无统计学意义。机器人组患者术后3个月内均有不同程度的胸部隧道区域的麻木感,但半年后逐渐减轻,1年后均完全恢复。机器人组患者术后满意度高于开放组(P < 0.05)。机器人组患者术后满意度(比较满意+非常满意)达到100%,见表 6。
| 组别 | n | 满意度 | 颈部与胸部不适感 | ||||
| 非常满意 | 比较满意 | 不满意 | 完全恢复 | 仍感不适 | |||
| 开放组 | 124 | 92(74.20) | 16(12.90) | 16(12.90) | 112(90.32) | 12(9.68) | |
| 机器人组 | 105 | 103(98.10) | 2(1.90) | 0 | 88(83.81) | 17(16.19) | |
| χ2 | 26.113 | 2.181 | |||||
| P | < 0.001 | 0.140 | |||||
3 讨论 3.1 UABA入路机器人甲状腺癌手术的疗效
机器人设备在甲状腺癌手术中的疗效可达到开放手术的效果,而且由于避免了颈部切口,对维持颈部外观有明显美容优势。目前应用较多的为经腋窝入路(transaxillary approach,TAA)、双侧腋窝双侧乳晕入路(bilateral axilla-bilateral areola,BABA)以及经口入路(tansoral robotic thyroidectomy, TORT)等机器人手术方式[7, 15-17]。UABA入路的机器人手术报道尚较少。本研究结果显示,UABA入路机器人手术与开放手术相比,两组在切除淋巴结总数、转移淋巴结数、术后非TSH刺激状态TG水平相似,且两组患者均未出现复发转移,说明机器人手术治疗甲状腺癌的彻底性与开放手术有相同的疗效,与既往研究结果类似[2, 18]。由于UABA入路与BABA入路相比减少了1个腋窝隧道,创伤更小,通过专用腔镜拉钩协助能获得良好的术野显露,在此基础上进行精细有效的手术操作完成甲状腺全切和双侧中央区清扫。
3.2 UABA入路机器人甲状腺手术的安全性与开放手术相比,机器人甲状腺癌手术的安全性能达到相同的效果,但其术后并发症发生率尤其是甲状旁腺功能减退和喉返神经损伤的发生率等方面尚未能证明更有优势[2, 18-22]。本研究结果显示,机器人组患者永久性声音嘶哑发生率明显低于开放组,术后暂时性和永久性甲状旁腺功能减退发生率以及术后暂时性和永久性低钙血症发生率均明显低于开放组,说明机器人手术在保护甲状旁腺以及喉返神经方面均有明显优势。半年后仍不能发高音或说话易疲劳的发生率比较,机器人组明显低于开放组。不能发高音或说话易疲劳说明声带的运动功能受到不同程度的影响,很大程度上与喉返神经的损伤有关,也说明了机器人手术在保护喉返神经方面的优势。这可能是由于本研究中的机器人手术采用了超精细被膜解剖技术,保留了大部分的甲状腺背侧的真被膜。由于大部分甲状旁腺是在甲状腺真被膜以外,而且甲状旁腺的三级血供也与甲状腺真被膜关系密切,真被膜的保留有利于甲状旁腺及其血供[13-14]的保护,尤其是对于真被膜下甲状旁腺,传统的被膜解剖技术无法保留[23]。而超精细被膜解剖技术通过对背侧真被膜的保留有利于辨认并保留真被膜下甲状旁腺,从而最大限度地减少术后甲状旁腺功能减退的发生。此外,由于喉返神经全程均在甲状腺真被膜外走行,尤其是喉返神经在其入喉处往往与甲状腺后被膜关系密切,而机器人手术全程均是使用超声刀或电钩等能量器械进行操作,机器人手术中保留甲状腺背侧的真被膜相当于增加了能量器械与喉返神经间的安全距离,从而减少了对喉返神经的损伤机会或减轻其损伤程度。而开放手术由于人眼识别能力和人手操作精度的限制尚无法实现超精细被膜解剖,从而导致较高的喉返神经损伤和甲状旁腺损伤发生率。对未侵及局部重要结构以及无侧颈部转移的甲状腺癌,甲状腺全切加双侧中央区淋巴结清扫是切除范围最大的手术方式,也最容易出现甲状旁腺功能减退以及喉返神经损伤。而对喉返神经以及甲状旁腺的保护程度是反映手术精细程度和安全性的最重要的指标。目前对于这一术式在机器人与开放手术的比较研究较少。本研究对比了这一术式在机器人手术与开放手术的应用效果,其结果更能准确反映机器人超精细被膜解剖技术的应用效果。
甲状腺术中发现误切甲状旁腺或甲状旁腺血运障碍时进行甲状旁腺移植是减少永久性甲状旁腺功能减退发生机会的一种补救措施[23-24]。开放组甲状旁腺移植患者亚组中永久性甲状旁腺功能减退发生率明显低于未行移植的亚组,说明旁腺移植可在一定程度上减少永久性甲状旁腺功能减退的发生,但开放组甲状旁腺移植亚组仍有少数患者发生了永久性甲状旁腺功能减退,说明甲状旁腺移植并不能完全避免永久性甲状旁腺功能减退的发生,因此术中应立足于原位保留甲状旁腺。尽管机器人组甲状旁腺移植比例明显低于开放组,但机器人组永久性甲状旁腺功能减退发生率明显低于开放组,说明机器人超精细被膜解剖技术比开放组传统的被膜解剖技术在保护甲状旁腺方面有明显优势。
3.3 UABA入路机器人手术有利于保护患者颈部外观,提高患者满意度机器人手术由于避免了颈部切口容易被年轻女性患者接受,本研究中机器人组有更多的年轻女性患者,与前期的研究结果类似[2, 25-26]。术后满意度调查发现机器人组术后颈胸部不适感与开放组相比无显著差异。UABA机器人组由于比开放组增加了3个胸壁隧道的创伤,在术后半年内均有不同程度的胸前隧道区麻木感,但1年后均能完全恢复。而且由于机器人手术避免了颈部切口,维持了原有的颈部外观,从而达到术后100%的满意度。
本研究基于甲状腺全切加双中央区淋巴结清扫术式对UABA入路机器人手术与开放手术进行对比研究,结果显示,机器人甲状腺手术是甲状腺癌安全有效的治疗方式,且由于其采用的超精细被膜解剖技术操作更加精准,与开放手术相比,能更好地保护甲状旁腺和喉返神经,从而能够降低术后甲状旁腺功能减退和喉返神经损伤的发生率。由于颈部无切口,能保护颈部完美外观,提高术后患者满意度,从而提高患者生活质量。
本研究不足之处在于:①为回顾性研究,手术方式的选择主要依据患者的意愿,可能存在一定程度的选择偏倚;②根据声音嘶哑状况反映喉返神经的损伤情况可能会导致喉返神经损伤情况被低估;③不同医师的手术水平可能会有差异,两组手术者均为单中心的同一组医师,可能无法准确反映本领域的平均水平,因此可能会对手术结果产生影响;④纳入病例数有限,随访时间较短,尚不能准确反映最终的治疗结果,需要开展多中心随机对照研究验证本研究的结果;⑤由于UABA入路在世界范围内应用不多,需研究对比这一入路与TAA、BABA以及TORT等入路的疗效与安全性的差异。
| [1] |
SIEGEL R L, MILLER K D, JEMAL A. Cancer statistics, 2018[J]. CA Cancer J Clin, 2018, 68(1): 7-30. |
| [2] |
JACOBS D, TORABI S J, GIBSON C, et al. Assessing national utilization trends and outcomes of robotic and endoscopic thyroidectomy in the United States[J]. Otolaryngol Head Neck Surg, 2020, 163(5): 947-955. |
| [3] |
陈灵勰, 邱伟华, 谈坚. 单孔腔镜甲状腺手术应用现状与前景[J]. 中国普通外科杂志, 2018, 27(11): 1471-1476. CHEN L X, QIU W H, TAN J. Application status and prospects of single-site endoscopic thyroidectomy[J]. Chin J Gen Surg, 2018, 27(11): 1471-1476. |
| [4] |
田文, 郗洪庆. 分化型甲状腺癌外科诊疗进展及展望[J]. 中国实用外科杂志, 2020, 40(1): 78-82. TIAN W, XI H Q. Current status and future perspectives in differentiated thyroidcancer[J]. Chin J Pract Surg, 2020, 40(1): 78-82. |
| [5] |
GAGNER M. Endoscopic subtotal parathyroidectomy in patients with primary hyperparathyroidism[J]. Br J Surg, 2005, 83(6): 875. |
| [6] |
LIRICI M M, HVSCHER C S G, CHIODINI S, et al. Endoscopic right thyroid lobectomy[J]. Surg Endosc, 1997, 11(8): 877. |
| [7] |
LANG B H H, WONG C K H, TSANG J S, et al. A systematic review and meta-analysis comparing outcomes between robotic-assisted thyroidectomy and non-robotic endoscopic thyroidectomy[J]. J Surg Res, 2014, 191(2): 389-398. |
| [8] |
LANG B H H, LO C Y. Technological innovations in surgical approach for thyroid cancer[J]. J Oncol, 2010, 2010: 1-6. |
| [9] |
KANG S W, JEONG J J, YUN J S, et al. Robot-assisted endoscopic surgery for thyroid cancer: experience with the first 100 patients[J]. Surg Endosc, 2009, 23(11): 2399-2406. |
| [10] |
KANG S W, JEONG J J, NAM K H, et al. Robot-assisted endoscopic thyroidectomy for thyroid malignancies using a gasless transaxillary approach[J]. J Am Coll Surg, 2009, 209(2): e1-e7. |
| [11] |
NEWMAN J G, KUPPERSMITH R B, O'MALLEY B W Jr. Robotics and telesurgery in otolaryngology[J]. Otolaryngol Clin N Am, 2011, 44(6): 1317-1331. |
| [12] |
CHOI J Y, BAE I E, KIM H S, et al. Comparative study of bilateral axillo-breast approach endoscopic and robotic thyroidectomy: propensity score matching analysis of large multi-institutional data[J]. Ann Surg Treat Res, 2020, 98(6): 307. |
| [13] |
QI X W, DU J Z, LIU H X, et al. First report of in situ preservation of a subcapsular parathyroid gland through super-meticulous capsular dissection during robotic radical thyroidectomy[J]. Surg Oncol, 2019, 28: 9-13. |
| [14] |
LIU P F, ZHANG Y, QI X W, et al. Unilateral axilla-bilateral areola approach for thyroidectomy by Da Vinci robot: 500 cases treated by the same surgeon[J]. J Cancer, 2019, 10(16): 3851-3859. |
| [15] |
CHOE J H, KIM S W, CHUNG K W, et al. Endoscopic thyroidectomy using a new bilateral axillo-breast approach[J]. World J Surg, 2007, 31(3): 601-606. |
| [16] |
BYEON H K, KOH Y W. The new era of robotic neck surgery: the universal application of the retroauricular approach[J]. J Surg Oncol, 2015, 112(7): 707-716. |
| [17] |
TAE K, JI Y B, SONG C M, et al. Safety and efficacy of transoral robotic and endoscopic thyroidectomy: the first 100 cases[J]. Head Neck, 2020, 42(2): 321-329. |
| [18] |
JIANG W J, YAN P J, ZHAO C L, et al. Comparison of total endoscopic thyroidectomy with conventional open thyroidectomy for treatment of papillary thyroid cancer: a systematic review and meta-analysis[J]. Surg Endosc, 2020, 34(5): 1891-1903. |
| [19] |
HINSON A M, KANDIL E, O'BRIEN S, et al. Trends in robotic thyroid surgery in the United States from 2009 through 2013[J]. Thyroid, 2015, 25(8): 919-926. |
| [20] |
CHOI J Y, BAE I E, KIM H S, et al. Comparative study of bilateral axillo-breast approach endoscopic and robotic thyroidectomy: propensity score matching analysis of large multi-institutional data[J]. Ann Surg Treat Res, 2020, 98(6): 307. |
| [21] |
DIONIGI G, KIM H Y, WU C W, et al. Neuromonitoring in endoscopic and robotic thyroidectomy[J]. Updat Surg, 2017, 69(2): 171-179. |
| [22] |
叶卫东, 郭伯敏, 樊友本. 腔镜甲状腺手术多种入路的探索和未来发展[J]. 外科理论与实践, 2019, 24(6): 498-502. YE W D, GUO B M, FAN Y B. Endoscopic thyroidectomy via various approaches: exploration and future[J]. J Surg Concepts Pract, 2019, 24(6): 498-502. |
| [23] |
田文, 徐震纲, 姜可伟, 等. 甲状腺外科医师委员会.甲状腺手术中甲状旁腺保护专家共识[J]. 中国实用外科杂志, 2018, 38(10): 1108-1113. TIAN W, XU Z G, JIANG K W, et al. Expert consensus statement on parathyroid protection in thyroidectomy[J]. Chin J Pract Surg, 2018, 38(10): 1108-1113. |
| [24] |
WANG B, ZHU C R, LIU H, et al. The effectiveness of parathyroid gland autotransplantation in preserving parathyroid function during thyroid surgery for thyroid neoplasms: a meta-analysis[J]. PLoS One, 2019, 14(8): e0221173. |
| [25] |
ARORA A, SWORDS C, GARAS G, et al. The perception of scar cosmesis following thyroid and parathyroid surgery: a prospective cohort study[J]. Int J Surg, 2016, 25: 38-43. |
| [26] |
CHOI Y, LEE J H, KIM Y H, et al. Impact of postthyroidectomy scar on the quality of life of thyroid cancer patients[J]. Ann Dermatol, 2014, 26(6): 693. |




