2. 400037 重庆,陆军军医大学(第三军医大学)第二附属医院病理科;
3. 210002 南京,南京大学医学院附属金陵医院内分泌科
2. Department of Pathology, Second Affiliated Hospital, Army Medical University (Third Military Medical University), Chongqing, 400037;
3. Department of Endocrinology, Affiliated Jinling Hospital, Medical College of Nanjing University, Nanjing, Jiangsu Province, 210002, China
垂体瘤(pituitary adenomas)是源于垂体前叶的常见良性肿瘤,在一般人群中的发病率高达16.7%[1],常见症状有激素分泌紊乱、视野缺损及头痛等肿瘤占位症状。约2/3的垂体瘤患者会出现激素分泌紊乱,其中泌乳素(prolactin,PRL)分泌紊乱的患者占22%~66%,生长激素(growth hormone,GH)分泌紊乱的患者占8%~16%[2],同时多激素分泌紊乱少见[3]。已知临床中绝大多数垂体瘤是散发型的,但仍有约5%是由已知致病基因突变引起,具有遗传易感性。随着基因检测的发展与普及,目前研究发现抑癌基因多发性内分泌腺瘤病1型(multiple endocrine neoplasia type 1,MEN1)突变是引起垂体瘤发病的重要遗传因素之一[2, 4]。在MEN1中超过40%的患者会发生垂体瘤,其中13%是以垂体瘤作为首要临床表现[5-6]。而以垂体瘤为首要临床表现的MEN1常发生大腺瘤,侵袭性强,对治疗的反应率偏低[4, 6-8],且极易漏诊其他内分泌相关腺瘤,进一步降低患者的生活质量和寿命。本研究回顾性分析4例以垂体瘤首诊的MEN1患者的临床特点及诊治过程,以加强临床医师对该疾病的认知和重视。
1 资料与方法收集2016年10月至2020年12月因垂体瘤或垂体瘤术后至陆军军医大学第二附属医院就诊的4例MEN1患者资料。纳入研究对象参照2012年美国内分泌学会的MEN1诊断标准[9]:①临床标准:发生两种或多种与MEN1相关的原发性内分泌肿瘤(即甲状旁腺功能亢进或腺瘤、十二指肠胰腺肿瘤和垂体前叶肿瘤);②家系标准:确诊为MEN1患者的一级亲属中,发现具有一个MEN1相关的肿瘤;③遗传标准:携带有MEN1基因突变,可无临床症状及生化影像学证据,如MEN1基因突变携带者。符合以上任何1点即可诊断为MEN1。同时排除所有单发内分泌相关腺瘤患者,如单发垂体瘤、单发胰腺神经内分泌肿瘤、单发甲状旁腺瘤等。本研究经陆军军医大学第二附属医院医学伦理委员会审批通过(2021-研第-035-01)。回顾性分析4例患者的临床表现、生化指标、影像学资料、免疫组化染色及基因检测结果和转归,并复习相关文献。
2 结果 2.1 一般临床资料4例患者,其中男性1例,女性3例,起病年龄16~ 57岁,平均38岁,延迟诊断1~7年,一般临床资料见表 1。其中3例患者临床表现为手足增粗、鼻大唇厚等肢端肥大症状;同时,病例1、4在病程中逐渐出现双眼视物模糊,病例1、2逐渐出现头痛、头晕或恶心呕吐。病例3因健康体检意外发现垂体瘤,无明显临床表现。患者均自诉无特殊病史和家族遗传史。
| 临床资料 | 病例1 | 病例2 | 病例3 | 病例4 |
| 性别 | 女 | 男 | 女 | 女 |
| 就诊年龄/岁 | 50 | 23 | 35 | 64 |
| 延迟诊断时间/年 | 2 | 7 | 1 | 7 |
| 就诊原因 | 头痛2年,术后14个月再发头痛2个月 | 头晕、头痛伴恶心呕吐 | 体检发现垂体占位 | 双眼视物模糊7年 |
| 首诊科室 | 内分泌科 | 神经外科 | 内分泌科 | 神经外科 |
| 肢端肥大症 | 有 | 有 | 无 | 有 |
| 视力下降 | 有 | 无 | 无 | 有 |
| 垂体瘤分泌激素 | GH | GH+PRL | 无 | GH+PRL |
| 垂体瘤大小 | 1.5 cm×2.7 cm×2.0 cm | 6.2 cm×7.7 cm×6.1 cm | 0.3 cm×0.4 cm | 2.2 cm×1.3 cm×1.4 cm |
| 合并受累内分泌腺体 | 甲状旁腺瘤 | 右侧甲状旁腺瘤 胰腺神经内分泌肿瘤 |
双侧甲状旁腺瘤、胰腺神经内分泌肿瘤、双侧肾上腺占位 | 甲状旁腺占位、胰头占位 |
| 基因检测 | 未检测 | c.249_252delGTCT (p.Ile85Serfs*33) |
c.1277delG (p.Gly426Alafs*19) |
未检测 |
| 既往病史 | 腹壁脂肪瘤切除术、高血压2年 | 胃穿孔手术后 | 支气管或肺类癌术后 | 高血压、糖尿病10年 |
2.2 实验室检查结果
有3例患者入院查随机血清生长激素(GH)、胰岛素样生长因子(IGF-1)显著高于正常值(OGTT试验中GH谷值≥1 ng/mL[10]),其中2例同时合并PRL升高;4例患者的血清甲状旁腺激素(parathyroid hormone, PTH) 均高于正常范围,其中3例合并高钙血症(表 2)。血常规、糖化血红蛋白、甲功八项、皮质醇节律无明显异常。
| 病例 | 性别 | 检测时间 | GRH/μg·L-1 | IGF-1/ng·mL-1 | GH谷值/ng·mL-1 | PRL/ng·mL-1 | PTH/pg·mL-1 | 血钙/mmol·L-1 | ACTH/ng·L-1 |
| 1 | 女 | 治疗前 | 12.70 | 878 | 8.32 | 3.92 | 155.9 | 3.50 | 16.80 |
| 治疗后 | 9.70 | 364 | - | <0.60 | 101.7 | 2.77 | 63.76 | ||
| 2 | 男 | 治疗前 | >40.00 | 1 005 | 157.00 | 7 329.00 | 660.9 | 3.63 | 28.47 |
| 治疗后 | 1.86 | 303 | 1.04 | 149.79 | 101.7 | 2.68 | 163.10 | ||
| 3 | 女 | 治疗前 | 1.34 | 202 | - | 32.33 | 1 098.1 | 2.80 | 17.40 |
| 治疗后 | - | - | - | - | 69.0 | 2.05 | 17.40 | ||
| 4 | 女 | 治疗前 | >40.00 | 451 | 79.70 | 126.00 | 93.9 | 2.44 | 65.97 |
| 治疗后 | 0.92 | 173 | - | 3.03 | - | - | 42.82 | ||
| 治疗后为患者末次随访时间;GRH:生长激素释放激素;IGF-1:胰岛素生长因子-1;GH: 生长激素;PRL:泌乳素;PTH:甲状旁腺激素;ACTH:促肾上腺皮质激素;-:未查 | |||||||||
2.3 影像学检查结果
鞍区MRI检查:病例1提示垂体瘤术后改变;病例2、4提示垂体大腺瘤,病例3提示垂体微腺瘤(图 1)。甲状腺及甲状旁腺超声检查:4例均发现甲状旁腺低回声结节。腹部CT检查:病例3双侧肾上腺增生、胰腺尾部病变;病例4发现胰腺头部见团块样不均匀低密度影。无痛胃/肠镜检查:病例2及病例4行此检查,结果提示结肠/胃多发息肉。双能X线骨密度测量:4例均提示不同程度的骨量减少或骨质疏松。

|
| 白色箭头示垂体瘤 图 1 3例垂体瘤患者鞍区MRI影像表现 |
2.4 诊疗经过与转归
病例1于2014年10月在外院确诊为“生长激素垂体大腺瘤”,并行经蝶窦入路垂体瘤切除术,术后头痛症状未缓解,于是2016年10月至我院查生长激素释放激素(GRH)为12.7 μg/L、IGF-1为878 ng/mL、PTH为155.9 pg/mL,予以规律皮下注射长效奥曲肽(20 mg/月),激素控制一般。又于2019年在外院复查,发现PTH升高,完善检查提示“甲状旁腺瘤”,行左侧甲状旁腺瘤切除术。至2019年2月,患者再次因“头痛”至我院查GRH为12 μg/L、IGF-1为494 ng/mL,再次使用皮下注射长效奥曲肽(20 mg/月),激素控制仍一般。后定期每月在我院随访,于2021年4月换用醋酸兰瑞肽(肌肉注射90 mg,1次/d)治疗,随访至2021年10月激素仍未完全缓解(表 2)。
病例2从16岁开始出现肢端肥大症状,23岁出现头痛、恶心呕吐于2019年10月至我院,查PTH、血钙、GH及PRL结果皆高于正常值,完善头颅MRI、甲状腺及旁腺超声等检查,提示可能垂体大腺瘤、甲状旁腺低回声结节及胰腺头尾部占位。先后于神经外科、普外科及消化内科分别行鞍区肿瘤切除术、右侧甲状旁腺瘤切除术及胰腺头尾部穿刺活检术,术后免疫组化染色或病理证实GH+PRL混合型垂体瘤(图 2)、甲状旁腺腺瘤及胰腺神经内分泌肿瘤(G1期)。术后7个月复查内分泌激素示GRH 1.1 μg/L,IGF-1 191 ng/mL,PRL >200 ng/mL,治疗后部分激素缓解;复查鞍区MRI示瘤体残余而行放射治疗,同时嘱院外规律使用溴隐亭(2.5 mg, 2次/d)。随访至2021年6月,放射治疗12个月后查内分泌激素示:GRH 1.86 μg/L,IGF-1 303 ng/mL,PRL 149.79 ng/mL,PRL较术前有所改善,继续规律使用溴隐亭(2.5 mg,2次/d)。
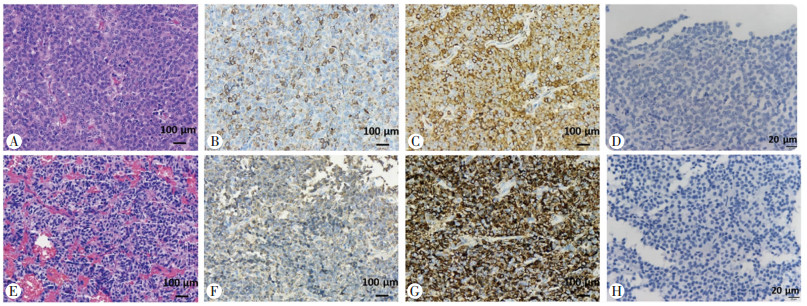
|
| A~D:病例2;E~H:病例4;A、E:HE染色;B、F:IHC染色示GH阳性 GH阳性免疫染色(黄色)位于细胞质中;C、G:IHC染色示PRL阳性 PRL阳性免疫染色(黄色)广泛分布于细胞质和细胞核中;D、H:IHC阴性对照 图 2 病例2和病例4 GH+PRL混合型垂体腺瘤病理学表现 |
病例3于2019年10月至外院体检发现垂体微腺瘤,至我院进一步诊治,查血钙及PTH皆高于正常范围,完善超声、CT等检查,提示合并甲状旁腺增生、双侧肾上腺结节和胰腺尾部占位,先后于肝胆外科和普外科行胰尾部肿瘤切除术及右侧甲状腺部分切除+左下甲状旁腺切除术,术后免疫组化染色证实为胰腺神经内分泌肿瘤(G1)和甲状旁腺腺瘤,定期随访,至2021年4月复查MRI示垂体瘤未见增大,内分泌激素正常。
病例4于2020年12月至我院诊疗垂体瘤过程中,查GH、PRL高于正常值,同时PTH显著升高,完善相关影像学检查,发现合并甲状旁腺增生和胰头占位,于神经外科行经蝶窦入路垂体瘤切除术,免疫组化证实为GH+PRL混合型瘤(图 2),胰头占位和甲状旁腺增生暂未处理,2021年1月复查示GRH 0.92 μg/L、IGF-1 173 ng/mL、PRL 3.03 ng/mL,后未再次随访。
4例患者末次随访激素情况见表 2。
2.5 基因检测结果病例2、3完善全外显子组基因测序,发现2个MEN1基因突变位点(表 1)。病例2为MEN1基因c.249_252delGTCT杂合突变;病例3为MEN1基因c.1277delG杂合突变,病例3家属(母亲和2个女儿)经Sanger家系验证,发现女儿1携带MEN1基因突变,此突变位点为首次报道(图 3)。
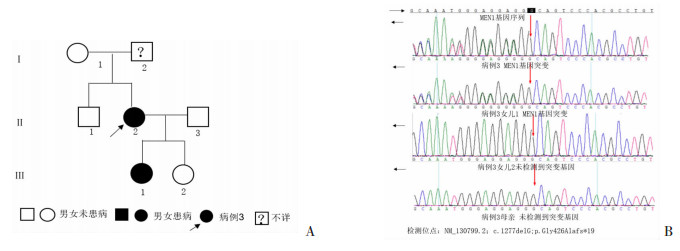
|
| 图 3 病例3的家系图(A)及家属Sanger测序图(B) |
3 讨论
MEN1是一种罕见的常染色体显性遗传病,因位于染色体11q13的抑癌基因MEN1突变所致,发病率为(1~3)/100 000[5]。临床特征常同时或先后累及2个及以上的内分泌腺肿瘤,其中,垂体瘤是仅次于甲状旁腺肿瘤和十二指肠胰腺肿瘤最常见的第三类肿瘤(40%)。此外,MEN1还会发生非内分泌腺肿瘤,如脂肪瘤、支气管/肺类癌、血管纤维瘤等(< 5%)[11-12],现已有报道称,确诊为MEN1的女性患乳腺癌风险增加[13]。本组4例患者均因垂体瘤首诊,同时合并甲状旁腺功能亢进,其中,病例2合并胰腺神经内分泌肿瘤,病例3合并双侧肾上腺占位和胰腺神经内分泌肿瘤,病例4合并胰头占位,均符合MEN1的临床诊断。
研究报道,MEN1患者的垂体瘤相关临床表现与散发型垂体瘤相似,女性多发[14],可发生在任意年龄段,国外有5~83岁患者的报道[15]。本病多为大腺瘤、侵袭性强,垂体瘤中多激素混合型少见,但在MEN1中多激素混合型相对常见,如PRL+ACTH、GH+PRL[4-5, 16]。本组4例患者,其中女性3例,男性1例,起病于不同年龄段,与文献报道一致,有3例功能性大腺瘤,其首诊时均表现出明显的垂体瘤占位导致的头痛或视野缺损及因GH过量分泌导致的肢端肥大症等严重症状,其中病例2和病例4同时过量分泌GH+PRL,且病例2因起病于青春期误把肢端肥大症状理解为青春期发育过快而延误诊断7年,初诊时GRH(>40 μg/L)和PRL(7 329 ng/mL)已异常升高,垂体瘤最大直径达7.7 cm。病例3为无功能垂体微腺瘤,无明显临床表现,经实验室生化及影像学筛查发现,已同时累及3个相关内分泌腺瘤,行基因检测发现MEN1突变基因,最终确诊MEN1。
MEN1的诊断标准有临床诊断、家系诊断及遗传诊断。目前国内仍主要依靠临床诊断,易造成延迟诊断甚至漏诊。因此,推荐早期行基因检测并提供相关遗传咨询,让患者及家属正确认识本病,以期早确诊并及时开始合理治疗。本组4例MEN1,病例2、3及病例3家属在医师强烈建议下,同意接受MEN1基因检测,且分别检测出2个MEN1基因杂合突变位点:c.249_252delGTCT和c.1277delG,后者为首次发现的MEN1突变位点,这将为MEN1的遗传研究提供新的数据,并及时确诊病例3的女儿1为MEN1基因携带者。其目前无任何临床表现,建议定期监测(1次/1~3年)生化及影像学变化。余2例均临床诊断为MEN1。因此,对于MEN1患者及家庭成员,应尽早行基因检测明确诊断,是管理和治疗的关键[17]。
研究报道,MEN1相关腺瘤比散发性内分泌腺瘤预后差,同时因累及多个腺体,使病情更复杂多变,但目前治疗原则仍与散发性腺瘤一致[9]。通过文中4例患者发现,越早诊断并启动多学科联合诊疗,其预后及生活质量更好。4例患者中,病例3在尚未出现临床症状时就行临床及基因诊断以明确MEN1,虽然,此时甲状旁腺、胰腺、双侧肾上腺已受累,但患者依从性好,辅以多学科联合诊疗,其预后及生活质量最佳,同时,其女儿1基因诊断为MEN1,嘱其定期随访,以早发现、早诊治,提高生存期。余3例患者均在起病2~7年后才通过临床或基因诊断明确为MEN1,虽及时辅以多学科联合干预,但相关内分泌激素仅部分缓解。
综上所述,本研究显示,对于首诊垂体瘤的MEN1患者,早期诊断并启动多学科联合干预,有利于改善患者及其家属的生活质量和预期寿命。因此,临床上以垂体瘤初诊的患者,尤其是功能型大腺瘤,临床医师应警惕MEN1,并意识其为多内分泌腺瘤疾病。建议此类患者常规完善内分泌激素和钙磷电解质及相关影像学检查,一旦发现2个及以上内分泌腺体病变,患者及其家属应尽早完善MEN1基因检测,同时联合多学科制定个体化诊疗方案,期待最大化改善患者预后及生存期。故在临床诊治中提高对MEN1的认识及诊治,对防止漏诊、误诊有重要的临床意义。
利益冲突声明 所有作者声明不存在利益冲突。
| [1] |
母义明. 垂体瘤诊治进展[J]. 解放军医学杂志, 2017, 42(7): 576-582. MU Y M. Pituitary adenomas: an overview of clinical features, diagnosis and treatment[J]. Med J Chin PLA, 2017, 42(7): 576-582. |
| [2] |
MOLITCH M E. Diagnosis and treatment of pituitary adenomas: a review[J]. JAMA, 2017, 317(5): 516-524. |
| [3] |
LOPES M B S. The 2017 World Health Organization classification of tumors of the pituitary gland: a summary[J]. Acta Neuropathol, 2017, 134(4): 521-535. |
| [4] |
KAMILARIS C D C, STRATAKIS C A. Multiple endocrine neoplasia type 1 (MEN1): an update and the significance of early genetic and clinical diagnosis[J]. Front Endocrinol (Lausanne), 2019, 10: 339. |
| [5] |
AL-SALAMEH A, CADIOT G, CALENDER A, et al. Clinical aspects of multiple endocrine neoplasia type 1[J]. Nat Rev Endocrinol, 2021, 17(4): 207-224. |
| [6] |
MARQUES N V, KASUKI L, COELHO M C, et al. Frequency of familial pituitary adenoma syndromes among patients with functioning pituitary adenomas in a reference outpatient clinic[J]. J Endocrinol Invest, 2017, 40(12): 1381-1387. |
| [7] |
VERGÈS B, BOUREILLE F, GOUDET P, et al. Pituitary disease in MEN type 1 (MEN1): data from the France-Belgium MEN1 multicenter study[J]. J Clin Endocrinol Metab, 2002, 87(2): 457-465. |
| [8] |
ROGOZIŃSKI D, GILIS-JANUSZEWSKA A, SKALNIAK A, et al. Pituitary tumours in MEN1 syndrome—the new insight into the diagnosis and treatment[J]. Endokrynol Pol, 2019, 70(5): 445-452. |
| [9] |
THAKKER R V, NEWEY P J, WALLS G V, et al. Clinical practice guidelines for multiple endocrine neoplasia type 1 (MEN1)[J]. J Clin Endocrinol Metab, 2012, 97(9): 2990-3011. |
| [10] |
中华医学会神经外科学分会, 中国垂体腺瘤协作组, 中华医学会内分泌学分会. 中国肢端肥大症诊治指南(2013版)[J]. 中华医学杂志, 2013, 93(27): 2106-2111. Neurosurgery Branch of Chinese Medical Association, China Pituitary Adenoma Collaborative Group, Endocrinology Branch of Chinese Medical Association. Guidelines for the diagnosis and treatment of acromegaly (2013 editon)[J]. Nat Med J China, 2013, 93(27): 2106-2111. |
| [11] |
HU W M, ZHANG Q, HUANG L H, et al. Identification of novel variants in MEN1: a study conducted with four mul-tiple endocrine neoplasia type 1 patients[J]. Horm Metab Res, 2020, 52(11): 788-795. |
| [12] |
FROST M, LINES K E, THAKKER R V. Current and emerging therapies for PNETs in patients with or without MEN1[J]. Nat Rev Endocrinol, 2018, 14(4): 216-227. |
| [13] |
DREIJERINK K M, GOUDET P, BURGESS J R, et al. Breast-cancer predisposition in multiple endocrine neoplasia type 1[J]. N Engl J Med, 2014, 371(6): 583-584. |
| [14] |
LLOYD R V, JIN L, FIELDS K, et al. Effects of estrogens on pituitary cell and pituitary tumor growth[J]. Pathol Res Pract, 1991, 187(5): 584-586. |
| [15] |
VANNUCCI L, MARINI F, GIUSTI F, et al. MEN1 in children and adolescents: data from patients of a regional referral center for hereditary endocrine tumors[J]. Endocrine, 2018, 59(2): 438-448. |
| [16] |
TROUILLAS J, LABAT-MOLEUR F, STURM N, et al. Pituitary tumors and hyperplasia in multiple endocrine neoplasia type 1 syndrome (MEN1): a case-control study in a series of 77 patients versus 2509 non-MEN1 patients[J]. Am J Surg Pathol, 2008, 32(4): 534-543. |
| [17] |
DE LAAT J M, VAN LEEUWAARDE R S, VALK G D. The importance of an early and accurate MEN1 diagnosis[J]. Front Endocrinol (Lausanne), 2018, 9: 533. |




