2. 400038 重庆,陆军军医大学(第三军医大学):药学与检验医学系生药学与中药学教研室
2. Department of Pharmacognosy and Traditional Chinese Medicine, Faculty of Pharmacy and Laboratory Medicine, Army Medical University (Third Military Medical University), Chongqing, 400038, China
舒芬太尼作为强效阿片类镇痛药,广泛应用于临床麻醉术中及术后镇痛。剂量相关的呼吸抑制,是包括舒芬太尼在内的芬太尼类药物的主要副作用,常常导致不良临床后果[1-3]。既往研究表明,有患者术后返回病房十余小时后,因为术后阿片类镇痛药物的使用,发生呼吸遗忘[4]。如何实现舒芬太尼的个体化用药,减少其副作用所致不良后果发生率,是目前精准麻醉的时代要求。
舒芬太尼主要由细胞色素同工酶CYP3A4代谢,摄入抑制CYP3A4活性的药物或食物会抑制舒芬太尼代谢,延长其呼吸抑制作用[5]。同时,CYP3A4*1G与CYP3A5*3等位基因存在高度遗传相关性,且CYP3A4和CYP3A5具有交叉底物特异性[6],推测CYP3A4和CYP3A5基因多态性可能是舒芬太尼药代动力学和药效动力学个体差异的分子基础。据此,本研究拟对不同CYP3A4和CYP3A5基因型的腹腔镜手术患者应用舒芬太尼术后自控静脉镇痛(patient-controlled intravenous analgesia,PCIA)的效果进行评价,探索CYP3A4和CYP3A5基因多态性对舒芬太尼PCIA是否具有影响。
1 资料与方法 1.1 一般资料本研究系单中心前瞻性观察性研究,经陆军军医大学第一附属医院临床伦理委员会审批(批件文号:KY2020124),并在中国临床试验注册中心网站注册(注册号:ChiCTR2000037436)。纳入2020年11月至2021年9月我院普外科和泌尿外科的住院患者,所有患者签署本研究知情同意书。纳入标准:①拟行腹腔镜手术;②年龄18~59岁;③ASA(美国麻醉医师协会)分级Ⅰ~Ⅲ级;④体质指数(BMI)18~28。排除标准:①严重心肺血管疾病、糖尿病、肝/肾功能损害;②有慢性疼痛病史、精神病史;③术前有低血容量症或低血压;④芬太尼类药物过敏史及药物滥用;⑤酗酒、吸毒或者长期使用止痛药;⑥孕妇、哺乳期妇女;⑦术前1周内服用过可抑制或诱导CYP3A酶表达的药物或食物;⑧术前2周用过单氨氧化酶抑制剂者。
1.2 CYP3A4与CYP3A5基因多态性检测与随机化分组本研究基于课题组前期预试验基因检测结果,将受试者分为Ⅰ类(CYP3A4纯合突变,或CYP3A4杂合突变合并CYP3A5纯合突变)、Ⅱ类(CYP3A4杂合突变合并CYP3A5杂合突变)、Ⅲ类(CYP3A4野生型,或CYP3A4杂合突变合并CYP3A5野生型);Ⅰ、Ⅱ、Ⅲ类人群分布频率约为10%、30%、60%。参研人员分为3组:临床采样及术后访视人员(L组)、基因检测人员(J组)和随机化人员(S组)。L组获取患者口腔拭子标本并送交J组。J组人员使用CytoTech CYP3AX试剂盒(上海默禾医疗科技有限公司)完成基因型检测,将结果传给S组。S组人员根据3类人群分布频率,采用随机信封法以Ⅰ类人群100%概率、Ⅱ类人群1/3概率、Ⅲ类人群1/6概率以及各组男女1 ∶1比例抽取入A、B、C 3组,以期检测满300例受试者基因型前能达到每组30例观察对象。L组于术中抽取患者3 mL动脉血于抗凝管,3 000 r/min离心10 min,提取细胞沉淀,Sanger测序法作DNA测序(上海美吉生物科技有限公司),比对两种基因检测方法结果,以sanger测序法结果为准。L组人员完成术后随访和相关临床资料收集。术后镇痛随访剔除病例包括:输液通道堵塞、镇痛泵故障、镇痛效果不良需随访人员调高镇痛背景剂量和负荷剂量。L组人员在以上过程中对患者基因型及分组均不知情,所有观察指标收集完毕后,第1次揭盲受试者A、B、C组别,对观察指标进行统计分析,第2次揭盲Ⅰ、Ⅱ、Ⅲ类人群与A、B、C对应分组情况。
1.3 麻醉实施3组患者进入手术间后,常规心电、血压、血氧饱和度监测,行BIS麻醉深度监测,建立静脉通道。采用咪达唑仑0.05 mg/kg、依托咪酯0.2 mg/kg、顺式阿曲库铵0.15 mg/kg、舒芬太尼0.5 μg/kg快速诱导,术中采用静吸复合维持麻醉,吸入1%七氟醚,TCI丙泊酚2~3 μg·mL-1·kg-1,TCI瑞芬太尼1~3 ng·mL-1·kg-1,每30~40 min间断推注顺阿曲库铵0.15 mg/kg,术中维持BIS值在40~65。
1.4 术后镇痛及随访根据成人手术后疼痛处理专家共识设置术后镇痛方案[7]:手术结束前30 min,静脉推注帕瑞昔布钠40 mg;爱朋全自动注药泵PCIA镇痛泵配置:150 μg舒芬太尼和10 mg地塞米松溶于0.9%生理盐水配制为150 mL镇痛液,镇痛泵背景剂量1 mL/h,单次注射剂量1 mL,极限量15 mL,锁定时间10 min。术毕开始运行镇痛泵,持续至术后48 h。术后12、24、48 h随访患者术后镇痛情况。
1.5 观察指标记录3组患者术后12、24、48 h VAS镇痛评分、Ramsay镇静评分、舒芬太尼用量、镇痛泵按压次数及恶心呕吐发生情况。
1.6 统计学分析采用SPSS 23.0统计软件进行分析,计量资料采用单因素方差分析,以x±s表示,计数资料采用χ2检验。检验水准α=0.05。
2 结果 2.1 基因检测结果本研究收集256项病例并完成所有病例基因型检测时,完成各组30例观察对象的目标,不再继续入组。CytoTech CYP3AX试剂盒检测结果与Sanger测序法DNA测序结果100%一致,观察指标统计分析完成后,揭盲公开3组基因型人群分类,A、B、C 3组患者分别对应Ⅰ、Ⅱ、Ⅲ类人群。
2.2 3组患者基本资料的比较按标准剔除病例后,最后纳入统计病例数为A组23例、B组24例、C组27例。3组患者年龄、性别、BMI、ASA分级差异无统计学意义(表 1)。
| 组别 | n | 年龄/岁,x±s | 男/女(例) | BMI(x±s) | ASA分级 Ⅰ/Ⅱ/Ⅲ级(例) |
| A组 | 23 | 50.94±6.15 | 12/11 | 23.85±2.80 | 0/23/0 |
| B组 | 24 | 49.57±8.16 | 14/10 | 24.02±2.12 | 0/24/0 |
| C组 | 27 | 51.71±5.41 | 14/13 | 23.38±2.32 | 0/27/0 |
| P | 0.53 | 0.88 | 0.23 | 1.00 |
2.3 3组各时间点VAS镇痛评分的比较
A、B、C 3组患者术后各时间点VAS评分差异无统计学意义(表 2)。
| 组别 | n | 术后12 h | 术后24 h | 术后48 h |
| A组 | 23 | 3.61±1.62 | 3.04±1.15 | 2.43±0.59 |
| B组 | 24 | 3.38±0.88 | 2.67±0.64 | 2.54±0.51 |
| C组 | 27 | 3.15±0.82 | 2.63±0.69 | 2.30±0.61 |
| F | 1.01 | 1.76 | 1.18 | |
| P | 0.37 | 0.18 | 0.31 |
2.4 3组各时间点镇静评分的比较
术后12 h, C组Ramsay镇静评分显著高于A组(P < 0.05);术后24、48 h,A、B、C 3组Ramsay评分差异无统计学意义(表 3)。
| 组别 | n | 术后12 h | 术后24 h | 术后48 h |
| A组 | 23 | 1.87±0.34 | 2.00±0.00 | 2.00±0.00 |
| B组 | 24 | 2.00±0.00 | 2.08±0.41 | 2.00±0.00 |
| C组 | 27 | 2.15±0.53a | 2.00±0.00 | 2.00±0.00 |
| F | 3.44 | 1.09 | 0 | |
| P | 0.04 | 0.34 | 1.00 | |
| a:P < 0.05, 与A组比较 | ||||
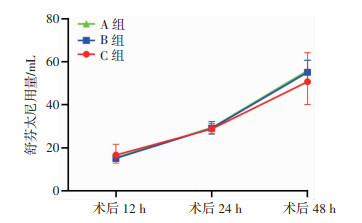
2.5 3组各时间点舒芬太尼用量的比较
3组患者术后各时间点舒芬太尼用量差异无统计学意义(图 1)。
|
| 图 1 3组患者术后各时间点舒芬太尼用量的比较(x±s,分) |
2.6 3组各时间点镇痛泵按压次数的比较
3组患者术后各时间点镇痛泵按压次数差异无统计学意义(图 2)。

|
| 图 2 3组患者各时间点镇痛泵按压次数的比较(x±s) |
2.7 3组各时间点恶心呕吐不良反应发生率的比较
3组患者在各时间点的恶心呕吐发生率差异无统计学意义(P>0.05,表 4)。
| 组别 | n | 术后12 h | 术后24 h | 术后48 h |
| A组 | 23 | 5(22) | 0 | 0 |
| B组 | 24 | 6(25) | 0 | 0 |
| C组 | 27 | 10(37) | 0 | 0 |
| P | 0.443 | 1.00 | 1.00 |
3 讨论
本试验结果显示,在相同PCIA镇痛设置基础上,3组患者术后12、24、48 h的VAS评分、镇痛泵舒芬太尼用量及按压次数、恶心呕吐发生率差异均无统计学意义。舒芬太尼主要通过细胞色素酶CYP3A4代谢,CYP3A4的酶活性受单核苷酸多态性(SNPs)的影响[8]。在亚洲人群中CYP3A4最常见的SNP形式是CYP3A4*1G [9],其频率高达38.99%[10]。有研究表明在老年患者全髋关节置换术后CYP3A4*1G突变型患者舒芬太尼PCIA用量显著低于野生型患者[11],与药物基因组学结果一致。也有研究表明CYP3A4*1G基因型多态性对宫颈癌患者术后舒芬太尼消耗量、VAS评分及镇静反应程度无影响[12],该研究还提到CYP3A4*1G基因可能与其他基因存在交互作用,共同影响舒芬太尼的药物效应。既往发现CYP3A4*1G与CYP3A5*3等位基因存在高度遗传相关性,且CYP3A4和CYP3A5存在交叉底物特异性[13], 但CYP3A5*3可能催化其他代谢途径,对抗CYP3A4的药物效应[14]。本试验结果显示CYP3A4*1G和CYP3A5*3多态性共同作用对舒芬太尼术后PCIA没有影响。
国际疼痛研究协会将疼痛定义为一种与实际或潜在的组织损伤相关的不愉快感觉和情感体验[15]。任何个体疼痛感受都受生理和心理的双重影响,因此疼痛带有主观性,通常很难准确地测量和评估。疼痛不一定与刺激有关,疼痛感知的强度和组织损伤的严重程度之间可能也没有直接联系[16]。已有研究表明P2RX7基因多态性可能参与了人类疼痛敏感性的调节[17],影响个体对镇痛的需求。鉴于疼痛感知的复杂性,舒芬太尼的药代动力学与抑制疼痛感知的药效可能并不完全一致,单一的基于药物基因组学探究镇痛药的疗效,忽略了个体本身对疼痛感受的差异性,其结果可能并不准确。本研究选取腹部腔镜手术,手术时间相对短、切口小、术中出血量少、术后镇痛中重度VAS评分发生率低[18],可能对研究结果有一定影响。
在精准医学的时代背景下,基于患者个体特征制订麻醉方案已成麻醉学发展趋势。但麻醉学科所涉及的代谢酶、转运蛋白、受体基因相关基因组学研究并不成熟,而且与临床实践相距甚远[19],目前麻醉学的精准医学多聚焦于基因多态性相关的麻醉药物代谢,但临床麻醉不是单一的药物作用,术后疼痛的发生率及疼痛程度更是取决于多种因素,除镇痛药物的作用外,还包括性别、年龄、手术部位、手术类型、病理生理状态等,药物基因组学对术后镇痛的影响可能在胸科、骨科等术后疼痛剧烈的手术中才能表现出明显的个体差异,为了达到良好的镇痛效果,这类手术术后常加大镇痛用药剂量,同时也增加药物不良反应发生率,药物基因组学或许有一定指导用药价值。
综上,本试验结果显示CYP3A4和CYP3A5基因多态性对腹腔镜手术舒芬太尼PCIA无明显影响,这可能是舒芬太尼药代动力学差异与疼痛感知差异相互影响所致。单纯基于药物基因组学指导个体化镇痛用药,并非适用于围术期镇痛的所有情况。
| [1] |
GIACCARI L G, COPPOLINO F, AURILIO C, et al. Sufentanil sublingual for acute post-operative pain: a systematic literature review focused on pain intensity, adverse events, and patient satisfaction[J]. Pain Ther, 2020, 9(1): 217-230. |
| [2] |
刘畅, 康焰. 镇痛镇静与循环呼吸: 如何评价及怎样抉择?[J]. 中华重症医学电子杂志(网络版), 2017, 3(4): 291-295. LIU C, KANG Y. How to evaluate and select sedatives and analgesics considering their cardiovascular and respiratory effects?[J]. Chin J Crit Care Intensive Care Med Electron Ed, 2017, 3(4): 291-295. |
| [3] |
陈园园, 李香豫, 许鹏飞, 等. 芬太尼类物质研究进展[J]. 中国药科大学学报, 2020, 51(6): 724-730. CHEN Y Y, LI X Y, XU P F, et al. Research advances of fentanyl and fentanyl-related substances[J]. J China Pharm Univ, 2020, 51(6): 724-730. |
| [4] |
SAJITH B. Respiratory depression: a case study of a postoperative patient with cancer[J]. Clin J Oncol Nurs, 2018, 22(4): 453-456. |
| [5] |
陈吉生. 新编临床药物学[M]. 北京: 中国中医药出版社, 2013. CHEN J S. New clinical pharmatology[M]. Beijing: China Press of Traditional Chinese Medicine, 2013. |
| [6] |
LIU S, SHI X, TIAN X, et al. Effect of CYP3A4 1G and CYP3A5 3 polymorphisms on pharmacokinetics and pharmacodynamics of ticagrelor in healthy Chinese subjects[J]. Front Pharmacol, 2017, 8: 176. |
| [7] |
中华医学会麻醉学分会. 成人手术后疼痛处理专家共识[J]. 临床麻醉学杂志, 2017, 33(9): 911-917. Society of Anesthesiology of Chinese Medical Association. Expert consensus on postoperative pain management in adults[J]. J Clin Anesthesiol, 2017, 33(9): 911-917. |
| [8] |
GENVIGIR F D, SALGADO P C, FELIPE C R, et al. Influence of the CYP3A4/5 genetic score and ABCB1 polymorphisms on tacrolimus exposure and renal function in Brazilian kidney transplant patients[J]. Pharmacogenet Genomics, 2016, 26(10): 462-472. |
| [9] |
DONG Z L, LI H, CHEN Q X, et al. Effect of CYP3A4*1G on the fentanyl consumption for intravenous patient-controlled analgesia after total abdominal hysterectomy in Chinese Han population[J]. J Clin Pharm Ther, 2012, 37(2): 153-156. |
| [10] |
HU Y F, TU J H, TAN Z R, et al. Association of CYP3A4*18B polymorphisms with the pharmacokinetics of cyclosporine in healthy subjects[J]. Xenobiotica, 2007, 37(3): 315-327. |
| [11] |
王琳, 朱贤平, 罗宇, 等. CYP3A4*1G基因多态性对老年患者全髋置换术后舒芬太尼药效学的影响[J]. 中华危重症医学杂志(电子版), 2018, 11(2): 90-93. WANG L, ZHU X P, LUO Y, et al. Effects of CYP3A4*1G genetic polymorphism on pharmacokinetics of sufentanil in elder patients undergoing total hip replacement[J]. Chin J Crit Care Med Electron Ed, 2018, 11(2): 90-93. |
| [12] |
胡纯嘏. CYP3A4*1G基因多态性对舒芬太尼术后镇痛的影响[D]. 衡阳: 南华大学, 2015. HU C G. Association of CYP3A4 gene polymorphisms with sufentanil analgesic effect[D]. Hengyang: University of South China, 2015. |
| [13] |
ZHANG W, YUAN J J, KAN Q C, et al. Influence of CYP3A5*3 polymorphism and interaction between CYP3A5*3 and CYP3A4*1G polymorphisms on post-operative fentanyl analgesia in Chinese patients undergoing gynaecological surgery[J]. Eur J Anaesthesiol, 2011, 28(4): 245-250. |
| [14] |
RAGIA G, DAHL M L, MANOLOPOULOS V G. Influence of CYP3A5 polymorphism on the pharmacokinetics of psychiatric drugs[J]. Curr Drug Metab, 2016, 17(3): 227-236. |
| [15] |
COHEN M, QUINTER J, VAN RYSEWYK S. Reconsidering the International Association for the Study of Pain definition of pain[J]. Pain Rep, 2018, 3(2): e634. |
| [16] |
RINGKAMP M, DOUGHERTY P M, RAJA S N. Anatomy and physiology of the pain signaling process[M]. Amsterdam: Elsevier, 2018: 3-10.e1.
|
| [17] |
KAMBUR O, KAUNISTO M A, WINSVOLD B S, et al. Genetic variation in P2RX7 and pain tolerance[J]. Pain, 2018, 159(6): 1064-1073. |
| [18] |
CACHEMAILLE M, GRASS F, FOURNIER N, et al. Pain intensity in the first 96 hours after abdominal surgery: a prospective cohort study[J]. Pain Med, 2020, 21(4): 803-813. |
| [19] |
俞卫锋, 王天龙, 严敏. 精准麻醉: 从理想走进现实[J]. 中华麻醉学杂志, 2017(5): 516-519. YU W F, WANG T L, YAN M. Precision anesthesia: from ideal to reality[J]. Chin J Anesthesi, 2017(5): 516-519. |




