上尿路尿路上皮癌(upper urinary tract urothelial carcinoma,UTUC)在临床上相较于其他类型尿路上皮癌更为少见,在所有尿路上皮癌中约占5%~10%,其侵袭性较膀胱癌等其他类型的尿路上皮癌更强。约2/3的UTUC在明确诊断时就已浸润至肌层,而这一比例在膀胱癌中仅占15%~25%[1]。UTUC患者的标准手术方式为根治性肾输尿管切除术,其中约30%的患者在术中会同时行盆腔淋巴结清扫术,但术后复发率仍较高且预后较差。据统计,患者术后3年生存率不足50%[2-3]。尚未见报道能有效预测UTUC的进展情况及预后的分子标记物,亦缺少与UTUC治疗相关的有效靶点及相应药物[4]。因此,寻找与UTUC相关的免疫组化分子标记物意义重大。
细胞角蛋白(cytokeratin,CK)作为细胞骨架的一种中间丝蛋白,几乎分布于所有的上皮细胞,在上皮源性的恶性肿瘤中广泛表达[5]。其中CK5和CK20均能够于上皮细胞基底层特异性表达,常见分布于消化道黏膜细胞和泌尿系的伞状细胞中。在发生癌变的细胞中,CK5和CK20仍可持续性表达,而在非上皮来源的癌变细胞或组织中则不表达[6]。本研究拟通过免疫组化的方法对UTUC肿瘤组织中的CK5和CK20进行检测,进而探讨其不同表型与患者的临床特点之间是否存在关系,及其预测UTUC预后的价值。
1 资料与方法 1.1 试验资料收集我科于2012年12月至2018年12月期间收治的UTUC患者。纳入标准:①术前常规完善计算机断层扫描(computer tomography,CT)或磁共振成像(magnetic resonance imaging,MRI)检查提示单侧UTUC;②手术方式采取UTUC标准术式,即患侧根治性肾输尿管切除术;③术后病检结果证实为UTUC;④临床资料完整且详尽,术后完成长期有效随访。排除标准:术前已行其他辅助治疗。本研究已获得重庆医科大学附属第一医院伦理委员会批准[2020年科研伦理(2020-328)]
1.2 随访方式患者随访方式为术后第一年内每3个月随访一次,第二年每6个月随访一次,第三年及以后每年随访一次,随访观察的指标为肿瘤特异性生存率(cancer-specific survival,CSS)、总体生存率(overall survival,OS),随访截止日期为2021年8月31日。
1.3 试验方法免疫组化染色完全按照试剂盒标准操作进行:所有组织蜡块切片均经常规脱蜡、梯度乙醇水化、高温抗原修复之后,将切片置于3% H2O2中以阻断内源性过氧化物酶,分别加入CK5抗体(购于Zenbio公司,1 ∶100稀释)、CK20抗体(购于Zenbio公司,1 ∶200稀释),37 ℃培养箱内培育15 min,然后予以磷酸盐缓冲液(phosphate buffer solution,PBS)(pH=7.4)冲洗3次,每次冲洗3 min,DAB显色、苏木精复染,梯度乙醇脱水,中性树胶封片,镜下阅片。以PBS代替一抗作为阴性对照。
1.4 结果判定光镜下见细胞质着棕黄色或者棕褐色视为CK5及CK20阳性表达。切片均在40倍显微镜下进行观察评估,在40倍放大视野中随机选择5个400倍视野进行观察。依据CK5及CK20免疫组化染色相关文献[7],视野中阳性细胞占比>10%为阳性结果,≤10%为阴性结果。
1.5 统计学方法采用SPSS 26.0软件进行统计学分析,利用χ2检验对CK5及CK20的表达与肿瘤临床病理特征进行比较,利用Kaplan-Meier生存曲线分析以及多因素COX比例风险回归模型进行患者预后分析,以P < 0.05为差异有统计学意义。
2 结果 2.1 一般资料本研究共纳入符合标准患者101例,其中男性59例,女性42例。中位年龄67(34~90)岁,中位随访时间48(3~100)个月。T分期:≤T2期73例,>T2期28例。肿瘤病理分级:低级别25例,高级别76例。淋巴结转移29例,无淋巴结转移72例。肿瘤直径:≤2 cm 40例,>2 cm 61例。
2.2 UTUC肿瘤组织中CK5与CK20组合亚型与临床病理特点的关系UTUC肿瘤组织中CK5及CK20表达的组合亚型共分为4种,其中CK5+CK20-组30例(29.7%)、CK5+CK20+组32例(31.7%)、CK5-CK20-组26例(25.7%)、CK5-CK20+组13例(12.9%)。χ2检验结果显示,不同组合亚型在年龄、T分期及有无淋巴结转移等临床特点的分布方面比较差异有统计学意义(P < 0.05),在性别、肿瘤直径、肿瘤位置、肿瘤分级等临床特点方面比较差异无统计学意义(P>0.05)。见图 1、表 1。
|
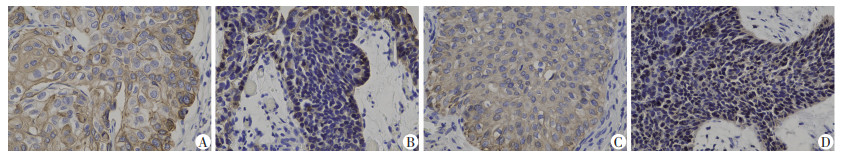
| A: CK5+; B: CK5-; C: CK20+; D: CK20- 图 1 UTUC肿瘤组织中CK5及CK20免疫组化染色结果(×400) |
| 变量 | n | CK5+CK20- | CK5+CK20+ | CK5-CK20- | CK5-CK20+ | P |
| 性别 | 0.073 | |||||
| 男 | 59(58.4) | 12(11.9) | 22(21.8) | 18(17.8) | 7(6.9) | |
| 女 | 42(41.6) | 18(17.8) | 10(9.9) | 8(7.9) | 6(6.0) | |
| 年龄/岁 | 0.041 | |||||
| <67 | 46(45.5) | 20(19.8) | 13(12.9) | 8(7.9) | 5(4.9) | |
| ≥67 | 55(54.5) | 10(9.9) | 19(18.9) | 18(17.8) | 8(7.9) | |
| 肿瘤直径/cm | 0.284 | |||||
| ≤2 | 40(39.6) | 9(8.9) | 13(12.9) | 14(13.9) | 4(3.9) | |
| >2 | 61(60.4) | 21(20.8) | 19(18.8) | 12(11.9) | 9(8.9) | |
| 病理分级 | 0.676 | |||||
| 低级别 | 25(24.8) | 7(6.9) | 7(6.9) | 6(6.0) | 5(5.0) | |
| 高级别 | 76(75.2) | 23(22.7) | 25(24.8) | 20(19.8) | 8(7.9) | |
| T分期 | 0.008 | |||||
| <T2 | 73(72.3) | 20(19.8) | 25(24.8) | 23(22.7) | 5(5.0) | |
| ≥T2 | 28(27.7) | 10(9.9) | 7(6.9) | 3(3.0) | 8(7.9) | |
| 淋巴结 | 0.001 | |||||
| 阴性 | 72(71.3) | 23(22.7) | 27(26.8) | 21(20.9) | 1(0.9) | |
| 阳性 | 29(28.7) | 7(6.9) | 5(5.0) | 5(5.0) | 12(11.8) | |
| 肿瘤位置 | 0.315 | |||||
| 肾盂 | 48(47.5) | 16(15.8) | 18(17.8) | 9(8.9) | 5(5.0) | |
| 输尿管 | 53(52.5) | 14(13.9) | 14(13.9) | 17(16.8) | 8(7.9) |
2.3 UTUC肿瘤组织中CK5与CK20不同组合亚型与患者预后的Kaplan-Meier单因素分析
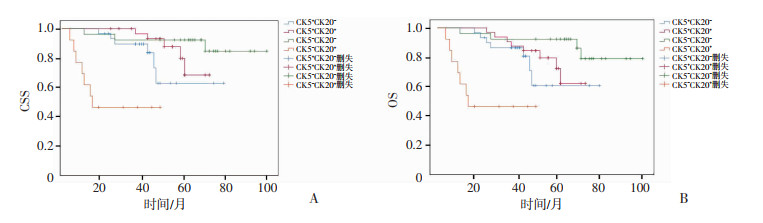
将CK5与CK20的4种组合亚型分别与患者的OS及CSS进行Kaplan-Meier单因素分析并绘制生存曲线,Log-Rank检验显示:CK5与CK20各组合亚型在患者OS、CSS的生存曲线的其差异具有统计学意义(P < 0.001),其中CK5-CK20+组预后较其他3组明显更差(图 2)。
|
| A:CSS Kaplan-Meier生存曲线;B:OS Kaplan-Meier生存曲线 图 2 不同CK5与CK20组合亚型的CSS、OS的Kaplan-Meier生存曲线 |
2.4 UTUC预后相关因素COX回归模型分析
COX单因素回归分析显示:T分期、有无淋巴结转移、肿瘤直径、CK5与CK20组合亚型是影响UTUC患者术后OS(P < 0.05)和CSS(P < 0.05)的危险因素。因COX单因素回归分析中可见肿瘤病理分级相对危险度(HR)在OS组为2.722,在CSS组为3.362,且临床中多种肿瘤预后与肿瘤病理分级密切相关,因此,在COX多因素逐步分析时亦将肿瘤病理分级纳入研究因素中。结果发现,肿瘤病理分级、T分期、有无淋巴结转移及CK5-CK20+组合均为影响UTUC患者预后的独立危险因素。见表 2、表 3。
| 变量 | OS | CSS | |||||
| P | HR | 95%CI | P | HR | 95%CI | ||
| 性别 | |||||||
| 女 | 1.000 | 1.000 | |||||
| 男 | 0.479 | 0.756 | 0.349~1.639 | 0.437 | 0.711 | 0.301~1.680 | |
| 年龄/岁 | |||||||
| <67 | 1.000 | 1.000 | |||||
| ≥67 | 0.469 | 1.35 | 0.599~3.039 | 0.439 | 1.433 | 0.576~3.565 | |
| 位置 | |||||||
| 肾盂 | 1.000 | 1.000 | |||||
| 输尿管 | 0.416 | 0.725 | 0.335~1.572 | 0.870 | 0.931 | 0.394~2.196 | |
| 肿瘤直径/cm | |||||||
| ≤2 | 1.000 | 1.000 | |||||
| >2 | 0.020 | 3.205 | 1.205~8.523 | 0.034 | 3.269 | 1.097~9.746 | |
| 淋巴结 | |||||||
| 阴性 | 1.000 | 1.000 | |||||
| 阳性 | <0.001 | 14.295 | 5.878~34.766 | <0.001 | 12.814 | 4.829~34.000 | |
| 病理分级 | |||||||
| 低级别 | 1.000 | 1.000 | |||||
| 高级别 | 0.103 | 2.722 | 0.817~9.074 | 0.056 | 3.362 | 0.782~14.448 | |
| T分期 | |||||||
| ≤T2 | 1.000 | 1.000 | |||||
| >T2 | <0.001 | 10.706 | 4.495~25.499 | <0.001 | 14.412 | 5.200~39.944 | |
| CK5+CK20- | 1.000 | 1.000 | |||||
| CK5+CK20+ | 0.572 | 0.742 | 0.264~2.088 | 0.249 | 0.489 | 0.145~1.651 | |
| CK5-CK20- | 0.061 | 0.286 | 0.077~1.057 | 0.05 | 0.228 | 0.052~0.999 | |
| CK5-CK20+ | 0.002 | 5.608 | 1.911~16.459 | 0.001 | 6.235 | 2.017~19.277 | |
| 变量 | OS | CSS | |||||
| P | HR | 95%CI | P | HR | 95%CI | ||
| 病理分级 | 0.037 | 4.885 | 1.103~21.629 | 0.024 | 7.421 | 1.302~42.293 | |
| T分期 | 0.005 | 4.376 | 1.574~12.168 | 0.002 | 7.072 | 2.113~23.667 | |
| 淋巴结阳性 | <0.001 | 9.269 | 3.224~26.649 | 0.002 | 6.641 | 2.032~21.701 | |
| CK5-CK20+ | 0.015 | 5.663 | 1.392~23.050 | 0.007 | 7.962 | 1.763~35.955 | |
3 讨论
UTUC相较于其他部位的尿路上皮癌往往恶性程度更高,约30%~60%的UTUC患者在初次就诊时肿瘤即已侵入其他部位。既往研究表明,UTUC的肿瘤分期、分级以及有无淋巴结转移是影响预后的重要因素[1, 8]。有研究报道,GATA3、CK5、CK20等免疫组化指标与膀胱尿路上皮癌(bladder urothelial carcinoma,BUC)的预后休戚相关,在一定程度上能有助于预测BUC的肿瘤分级、分期及预后情况[7, 9]。与BUC相比,尽管目前存在一些针对与UTUC预后相关的免疫组化分子标记物的研究[10-11],但由于缺乏多中心临床研究验证,其可靠性仍需进一步确认,且针对与UTUC预后相关的免疫组化分子标记物的研究总体仍较少。因此,为了适应临床实际需求,在本研究中,我们采用免疫组化法检测了101例UTUC患者的肿瘤组织中CK5及CK20的表达情况,探究其是否与UTUC预后之间存在某种关联,以期发现新的影响UTUC预后的重要因素。
CK5是目前细胞角蛋白家族中应用于免疫组化染色法检测中常见的基底细胞标志物,对于保持上皮细胞形态的完整性起着至关重要的作用,其常作为免疫组化染色法诊断基底样型乳腺癌的重要分子标记物,且与肿瘤的淋巴结转移、骨转移呈正相关。当CK5表达阳性时患者预后往往较差[12-13]。有研究报道CK5可作为膀胱癌、肺鳞癌等恶性肿瘤的预后标志物,而其表达阴性或低表达时患者预后更差[14-15]。
CK20是细胞角蛋白家族中广泛应用于多种肿瘤免疫组化染色检测的另一常见分子标记物,既往研究中,CK20被发现多于膀胱尿路上皮的伞状细胞中阳性表达,尤其是在发生癌变、肿瘤转移等情况下,其表达量会明显增加[16]。研究发现,多个系统的癌性病变的肿瘤组织中均能见到CK20的阳性表达,如消化系统的胃腺癌、结直肠癌、胆囊腺癌等,泌尿系统的尿道移行细胞癌,生殖系统的卵巢黏液腺癌以及皮肤癌等。也有部分癌性病变的肿瘤组织中CK20表达阴性,如小细胞肺癌、卵巢非黏液腺癌、肾细胞癌、乳腺癌等[17]。
本研究中,对101例UTUC患者的肿瘤组织进行石蜡切片处理后进一步对其中的CK5及CK20行免疫组化染色并观察,根据CK5及CK20的表达情况分为CK5+CK20-、CK5+CK20+、CK5-CK20-和CK5-CK20+等4组。χ2检验结果显示CK5与CK20的不同组合亚型与患者年龄、T分期及有无淋巴结转移等临床特点密切相关,且差异具有统计学意义。通过2组不同的生存曲线可知,CK5-CK20+组患者的OS及CSS较其余3组均明显更低,且差异有统计学意义,说明CK5-CK20+组合预后最差,这与国外关于CK5及CK20对于UTUC患者预后影响的相关研究结论一致[18]。既往研究报道,BUC中CK5表达阴性及CK20表达阳性时,膀胱尿路上皮癌的淋巴管及淋巴结侵袭性更低[14];由此可以推测,本研究中CK5-CK20+组合较其余3组预后更差的原因可能与此有关。但目前关于UTUC预后与CK5、CK20相关性的研究较少,故仍需更多的分子生物学方面的研究以进一步验证此推测。
本研究COX多因素回归分析结果提示肿瘤病理分级、T分期、有无淋巴结转移及CK5-CK20+均为影响UTUC患者预后的独立危险因素。其中高级别肿瘤死亡及复发风险较低级别肿瘤均明显更高,即肿瘤级别越高,预示UTUC患者预后越差,这与国内外相关研究结果一致[19-20]。肿瘤分期与UTUC患者预后密切相关,肿瘤早期患者与晚期患者在生存率方面比较差异有统计学意义[19],这与本研究结果一致,提示肿瘤分期越早,患者预后情况越好,也提示我们在UTUC治疗中早发现、早诊断、早治疗的重要性。本研究结果提示存在淋巴结转移的UTUC患者预后情况较无淋巴结转移的患者明显更差,其死亡、复发风险较后者均明显更高,这与SIMONE等[21]研究结果一致。CK5-CK20+组合患者发生死亡及复发风险较其余3组均更高,这也预示该亚型组合患者的预后情况更差,本研究结果与SIKIC等[18]的研究结果相一致。
本研究仍存在一定的局限性:①所有患者为电话随访,随访结果有可能不准确。②本研究为回顾性研究,在患者的选择上可能存在偏倚。③本研究为单中心研究,未同时纳入多家医疗机构数据导致研究患者数量较少,仅为101例,且随访时间不够长,以CK5及CK20预测UTUC患者预后情况的可行性有一定限制。④本次研究未纳入围术期是否接受放化疗、靶向治疗、免疫治疗等可能延长患者OS、CSS的指标。
综上所述,CK5及CK20与UTUC患者的CSS及OS显著相关,是影响CSS及OS的独立危险因素。当二者联合表达为CK5-CK20+时,患者的术后生存情况较差,且肿瘤分期更高、更易发生淋巴结转移。因此,可通过CK5及CK20的表达情况对UTUC预后情况做一定程度的预测,但其可行性仍需进一步的多中心、前瞻性研究证实。
| [1] |
ROUPRÊT M, BABJUK M, BURGER M, et al. European association of urology guidelines on upper urinary tract urothelial carcinoma: 2020 update[J]. Eur Urol, 2021, 79(1): 62-79. |
| [2] |
ROSENBERG J E, HOFFMAN-CENSITS J, POWLES T, et al. Atezolizumab in patients with locally advanced and metastatic urothelial carcinoma who have progressed following treatment with platinum-based chemotherapy: a single-arm, multicentre, phase 2 trial[J]. Lancet, 2016, 387(10031): 1909-1920. |
| [3] |
JAN H C, YANG W H, OU C H. Combination of the preoperative systemic immune-inflammation index and monocyte-lymphocyte ratio as a novel prognostic factor in patients with upper-tract urothelial carcinoma[J]. Ann Surg Oncol, 2019, 26(2): 669-684. |
| [4] |
KIM J, AKBANI R, CREIGHTON C J, et al. Invasive bladder cancer: genomic insights and therapeutic promise[J]. Clin Cancer Res, 2015, 21(20): 4514-4524. |
| [5] |
刘鑫, 王一星, 李冠宏, 等. Cytokeratin和CD133在肺腺癌患者外周血中的联合检测及临床病理分析[J]. 第三军医大学学报, 2017, 39(20): 2004-2009. LIU X, WANG Y X, LI G H, et al. Combined detection and clinical pathological analysis of peripheral blood CK and CD133 in primary lung adenocarcinoma patients[J]. J Third Mil Med Univ, 2017, 39(20): 2004-2009. |
| [6] |
MAI K T, BALL C G, BELANGER E C. Noninvasive papillary basal-like urothelial carcinoma: a subgroup of urothelial carcinomas with immunohistochemical features of basal urothelial cells associated with a high rate of recurrence and progression[J]. Appl Immunohistochem Mol Morphol, 2016, 24(8): 575-582. |
| [7] |
张静琦, 周晓洲, 石家仲, 等. 联合CK5和CK20免疫染色分析鉴别膀胱癌亚型[J]. 临床泌尿外科杂志, 2020, 35(4): 257-263. ZHANG J Q, ZHOU X Z, SHI J Z, et al. Combination of CK5 and CK20 immunostaining analysis for identifying subtypes of bladder cancer[J]. J Clin Urol, 2020, 35(4): 257-263. |
| [8] |
WANG Q, GAN X D, LI F, et al. PM2.5 exposure induces more serious apoptosis of cardiomyocytes mediated by Caspase3 through JNK/P53 pathway in hyperlipidemic rats[J]. Int J Biol Sci, 2019, 15(1): 24-33. |
| [9] |
INOUE S, MIZUSHIMA T, FUJITA K, et al. GATA3 immunohistochemistry in urothelial carcinoma of the upper urinary tract as a urothelial marker and a prognosticator[J]. Hum Pathol, 2017, 64: 83-90. |
| [10] |
SCARPINI S, ROUPRÊT M, RENARD-PENNA R, et al. Impact of the expression of Aurora-A, p53, and MIB-1 on the prognosis of urothelial carcinomas of the upper urinary tract[J]. Urol Oncol, 2012, 30(2): 182-187. |
| [11] |
XIONG G Y, LIU J, TANG Q, et al. Prognostic and predictive value of epigenetic biomarkers and clinical factors in upper tract urothelial carcinoma[J]. Epigenomics, 2015, 7(5): 733-744. |
| [12] |
MAI K T, BUSCA A, BELANGER E C. Flat intraurothelial neoplasia exhibiting diffuse immunoreactivity for CD44 and cytokeratin 5 (urothelial stem cell/basal cell markers): a variant of intraurothelial neoplasia commonly associated with muscle-invasive urothelial carcinoma[J]. Appl Immunohistochem Mol Morphol, 2017, 25(7): 505-512. |
| [13] |
王昭君, 卢鸯鸯, 戴燕燕, 等. CK5/6在浸润性乳腺癌中的表达及预后意义[J]. 医学研究杂志, 2020, 49(12): 99-103. WANG Z J, LU Y Y, DAI Y Y, et al. Expression and prognostic significance of CK5/6 in invasive breast cancer[J]. J Med Res, 2020, 49(12): 99-103. |
| [14] |
ECKSTEIN M, WIRTZ R M, GROSS-WEEGE M, et al. mRNA-expression of KRT5 and KRT20 defines distinct prognostic subgroups of muscle-invasive urothelial bladder cancer correlating with histological variants[J]. Int J Mol Sci, 2018, 19(11): 3396. |
| [15] |
MA Y F, FAN M Y, DAI L, et al. Expression of p63 and CK5/6 in early-stage lung squamous cell carcinoma is not only an early diagnostic indicator but also correlates with a good prognosis[J]. Thorac Cancer, 2015, 6(3): 288-295. |
| [16] |
OSMANOV Y I, GAIBOV Z A, KOGAN E A, et al. Comparative morphological characteristics and immunophenotype of urothelial carcinomas of the renal pelvis and bladder[J]. Arkh Patol, 2018, 80(5): 23-32. |
| [17] |
PATSCHAN O, SJÖDAHL G, CHEBIL G, et al. A molecular pathologic framework for risk stratification of stage T1 urothelial carcinoma[J]. Eur Urol, 2015, 68(5): 824-832. |
| [18] |
SIKIC D, KECK B, WACH S, et al. Immunohistochemiocal subtyping using CK20 and CK5 can identify urothelial carcinomas of the upper urinary tract with a poor prognosis[J]. PLoS One, 2017, 12(6): e0179602. |
| [19] |
王庆伟, 张涛, 文建国, 等. 上尿路尿路上皮癌预后多因素分析及术后再发膀胱癌危险因素分析[J]. 临床泌尿外科杂志, 2018, 33(5): 385-389. WANG Q W, ZHANG T, WEN J G, et al. Analysis of multivariate prognosis of upper urinary tract urothelial carcinoma and risk factors of postoperative bladder cancer[J]. J Clin Urol, 2018, 33(5): 385-389. |
| [20] |
KEELEY F X Jr, BIBBO M, BAGLEY D H. Ureteroscopic treatment and surveillance of upper urinary tract transitional cell carcinoma[J]. J Urol, 1997, 157(5): 1560-1565. |
| [21] |
SIMONE G, PAPALIA R, LORETO A, et al. Independent prognostic value of tumour diameter and tumour necrosis in upper urinary tract urothelial carcinoma[J]. BJU Int, 2009, 103(8): 1052-1057. |




