胸椎旁神经阻滞(thoracic paravertebral block,TPVB)是一种在靠近胸段脊神经出椎间孔附近注射局部麻醉药以达到阻滞同侧胸部躯体和交感神经的技术[1]。目前临床上TPVB广泛应用于胸部手术患者的围术期镇痛管理,其镇痛的机制主要与胸椎旁间隙的解剖结构相关,胸椎旁间隙为胸椎两侧的楔形间隙,内含脂肪组织、脊神经根、肋间神经、胸神经背支、交通支、交感神经链和肋间动静脉等结构,其内侧缘由椎体、椎间盘和椎间孔构成,向内经椎间孔与硬膜外间隙相连,外侧缘为肋间隙,前缘为胸膜,后缘为肋横突上韧带(superior costal transverse ligament,SCTL)[2]。
随着可视化技术的发展,超声引导下TPVB自2009年SHIBATA等[3]报道后越来越受到推崇,然而由于其解剖因素导致操作技术难度大,仍不可避免出现阻滞失败、气胸、血胸、低血压、局麻药中毒、脊神经损伤甚至全脊麻[4-6],很多临床医生望而却步。以往认为超声引导下TPVB操作的关键在于针尖需突破SCTL注射局麻药才能阻滞成功,然而COSTACHE等[7]在SCTL浅面进行染料注射,尸体上仍能观察到染料在胸椎旁间隙扩散,由此提出胸椎旁间隙不是真正的封闭解剖室,SCTL并不是药物的扩散的屏障。PIRACCINI等[8]更是提出SCTL是一个筋膜平面阻滞的新靶点。CHO等[9]使用显微CT证实了胸椎旁间隙是一个非常狭窄的空间,肋间后血管非常靠近胸膜,SCTL未形成胸椎旁间隙封闭后壁,在SCTL浅面注射可以扩散至胸椎旁间隙。同时也提出需要临床进一步验证。研究表明横突-胸膜中点(mid-point transverse process to pleura,MTP)阻滞应用于单孔胸腔镜手术患者,可取得良好的术后镇痛效果[10-11]。我们在临床实践中发现,MTP阻滞靶点测算耗时较多,无明确图像标志且不便于可视化技术实时操作,注药效果存在不确定性。目前在SCTL浅面行TPVB仅检索到个案。本研究旨在对比超声引导下SCTL浅面与深面注射局部麻药的TPVB用于胸腔镜手术患者术后镇痛的效果及恢复质量,探索SCTL在超声引导下TPVB中是否可以作为注药靶点的参照标志。
1 资料与方法 1.1 一般资料选取2021年5月至2021年9月本院胸外科择期行胸腔镜手术的住院患者106例,其中男性50例,女性56例,平均年龄55岁。纳入标准:年龄为18~78周岁,发育正常,男女不限;美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级,Ⅰ~Ⅱ级;BMI,18.5~28 kg/m2;拟行胸腔镜手术患者;自愿接受术后静脉镇痛泵。排除标准:拟行急症手术;怀孕和哺乳期妇女;凝血功能异常者;菌血症、脓毒血症患者或行穿刺部位感染者;对罗哌卡因或利多卡因过敏的患者;合并神经系统疾患、脊柱疾病(畸形或外伤)、脊柱手术史,胸背部皮肤感觉异常者。采用随机数字表法将患者分为2组:SCTL浅面阻滞组(S组)和SCTL深面阻滞组(T组)。本研究已通过本院医学伦理委员会批准[(A)KY2021006]。受试者均签署知情同意书。
1.2 麻醉方案 1.2.1 麻醉前准备拟行胸腔镜手术的患者,入室后吸氧并开放外周静脉通路,监测无创血压(noninvasive blood pressure,NIBP)、心率(heart rate,HR)、心电图(electrocardiogram,ECG)、经皮动脉血氧饱和度(percutaneous arterial oxygen saturation,SpO2)。开放外周静脉通路后,静脉注射咪达唑仑注射液0.03 mg/kg,桡动脉穿刺置管后,行连续有创血动脉血压监测。
1.2.2 麻醉过程麻醉诱导:依托咪酯0.3 mg/kg、枸橼酸舒芬太尼注射液0.4 μg/kg、顺式阿曲库铵0.15 mg/kg,行双腔支气管导管插管后,按照普胸手术常规进行机械控制通气,维持SpO2≥95%。术中调节丙泊酚2~ 4 μg/mL(效应室药物浓度)、瑞芬太尼2~4 ng/mL (效应室药物浓度)靶控输注,将麻醉深度监测BIS值维持在40~60,间断追加顺式阿曲库铵维持肌松,术中管理同临床操作常规。手术结束前30 min,静注帕瑞昔布钠40 mg,术毕连接静脉镇痛泵(枸橼酸舒芬太尼注射液300 μg+地佐辛注射液5 mg+氟比洛芬酯注射液200 mg+注射用盐酸托烷司琼15mg+生理盐水)配制成300 mL, 参数:背景剂量3 mL/h,追加2 mL/次,锁时10 min。待肌松测试TOF++++和意识清醒后,拔除气管导管,随即行超声引导下胸椎旁神经阻滞。
1.2.3 胸椎旁神经阻滞方法S组患者取健侧卧位,使用便携式彩色多普勒超声诊断仪(型号:S9,深圳开立生物医疗科技股份有限公司),高频线阵探头进行旁矢状位扫描,目标节段T5~T6节段胸椎旁间隙,定位T5棘突后将探头逐渐向外侧移动,直至显像并识别出SCTL、胸膜,采用超声引导下平面外穿刺技术,穿刺针尖达到SCTL浅面(未突破SCTL),回抽无血、无气之后开始缓慢注射0.375%盐酸罗哌卡因注射液20 mL(AstraZeneca公司,瑞典)。T组患者采用S组相同的超声定位方法,采用平面外穿刺技术,穿刺针突破SCTL,针尖位于SCTL深面,回抽无血、无气之后开始缓慢注射0.375%盐酸罗哌卡因注射液20 mL(AstraZeneca公司,瑞典)。
1.3 观察指标记录超声图像定位时间(探头放置于皮肤至识别出SCTL的时间)、神经阻滞穿刺时间(穿刺针刺入皮肤至开始注射药物的时间)、测量超声图像下针尖至胸膜的距离、观察超声图像上是否显示胸膜下压及穿刺相关并发症,评估阻滞后5、10、20、30 min和4、12、24 h(T0~6)静息和运动(咳嗽)状态下视觉模拟评分(visual analogue score,VAS)。VAS评分0~10分,(0分=无疼痛,10分=难以忍受的最剧烈的疼痛); 观察术后24 h内镇痛泵使用情况(舒芬太尼用量、首次按压时间、有效按压次数、实际按压次数);记录术后24 h恢复质量40项评分量表(quality of recovery-40,QOR-40)[12]评分,QOR-40是一份包含40个项目的问卷,每项评分1~5分,总分40~200分,40分代表极差的恢复质量,200分代表极好的恢复质量,总共涵盖了5个部分包括情感状态、身体舒适度、自理能力、心理支持和疼痛。
1.4 统计学分析采用SPSS 26.0统计软件进行分析。对符合正态分布的计量资料用x±s表示,组间比较采用两独立样本t检验; 偏态分布的计量资料以中位数(四分位数间距)[M(P25, P75)]表示,组间比较采用秩和检验;计数资料用例表示,组间比较采用χ2检验或Fisher确切概率法,检验水准:α=0.05。
2 结果 2.1 2组患者一般情况比较106例患者纳入此次研究,按随机数字表法分为2组(S组、T组),每组各53例,S组有4例患者因手术方式中转开胸退出研究,T组有2例患者穿刺时入血管未能注药退出研究,最终100例患者完成研究,S组49例,T组51例。2组患者性别、年龄、BMI、麻醉时间、手术时间差异无统计学意义(表 1)。
| 组别 | n | 男/女 | 年龄/岁 | BMI/kg·m-2 | 麻醉时间/h | 手术时间/h |
| S组 | 49 | 21/28 | 55.46±7.94 | 22.99±2.23 | 3.37±1.01 | 2.54±0.94 |
| T组 | 51 | 25/26 | 54.76±8.49 | 23.34±2.72 | 3.27±0.87 | 2.46±0.80 |
| 统计量 | 0.382 | 0.428 | -0.718 | 0.544 | 0.450 | |
| P值 | 0.537 | 0.670 | 0.475 | 0.588 | 0.654 |
2.2 2组患者超声引导下TPVB比较
S组穿刺时间为65(54.5,69.0)s,T组穿刺时间为76(67.0,89.0)s,与T组相比,S组穿刺时间缩短(P<0.05);S组超声测量针尖至胸膜距离为(3.41±0.79)mm,T组超声测量针尖至胸膜距离为(2.97±0.68)mm,S组超声测量针尖至胸膜距离更远(P<0.05);S组有15例能在超声图像下观察到胸膜下压,T组51例均能在超声图像上观察到胸膜下压,差异有统计学意义(P<0.05);T组出现1例硬膜外阻滞,S组0例硬膜外阻滞,差异无统计学意义;2组超声图像定位时间差异无统计学意义(表 2)。2组患者均未出现血胸、气胸、局麻药中毒、全脊麻。
| 组别 | n | 超声图像定位时间/s | 穿刺时间/s | 超声测量针尖至胸膜距离/mm | 超声图像观察到胸膜下压 | 硬膜外阻滞 |
| S组 | 49 | 23.41±3.93 | 65(54.5,69.0) | 3.41±0.79 | 15a | 0 |
| T组 | 51 | 23.92±4.18 | 76(67.0,89.0) | 2.97±0.68 | 51 | 1 |
| 统计量 | -0.632 | -4.676 | 2.966 | 53.600 | - | |
| P值 | 0.529 | <0.001 | 0.004 | <0.001 | 1.000 |
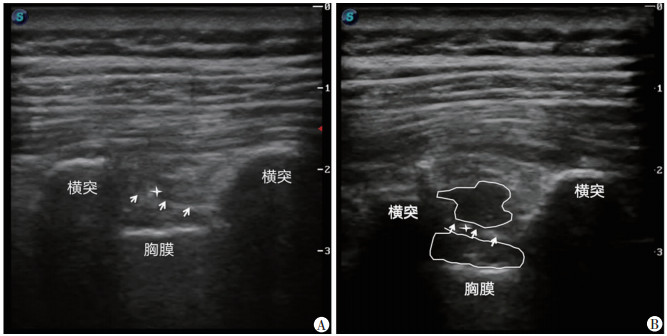
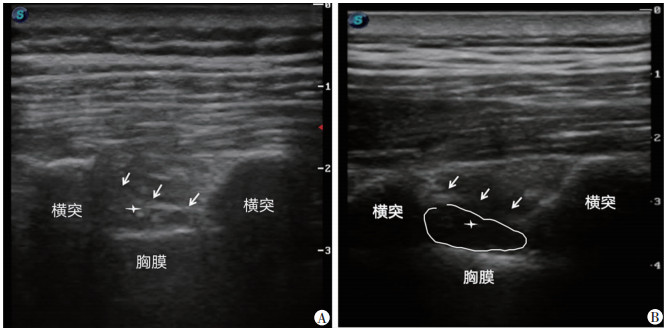
S组注药前超声图像显示如图 1A,注药后可观察到药物在SCTL上方扩撒,此后逐渐观察到胸椎旁间隙缓慢增宽,药物渗透至胸椎旁间隙(图 1B),结果显示:在SCTL浅面注药,药物可以沿SCTL上方及下方同时扩散。T组注药前超声图像显示(图 2A):注药后可观察到药物在胸椎旁间隙扩散(图 2B)。
|
|
箭头:SCTL;星号:针尖位置;线条包绕区域:药物扩散 A:S组注药前;B:S组注药后药物扩散 图 1 超声引导下SCTL浅面阻滞胸椎旁神经超声表现 |
|
|
箭头:SCTL;星号:针尖位置;线条包绕区域:药物扩散 A:T组注药前;B:T组注药后药物扩散 图 2 超声引导下SCTL深面阻滞胸椎旁神经超声表现 |
2.3 2组患者静息和运动(咳嗽)状态下各时间点VAS评分比较
记录2组患者5、10、20、30 min和4、12、24 h(T0~6)的VAS评分来评估术后疼痛程度,结果显示:2组患者在静息状态下T0~6的VAS评分差异无统计学意义(表 3);在运动(咳嗽)状态下,T6时,S组VAS评分为2(1,3)分,T组VAS评分为1(1,2)分,差异有统计学意义(P<0.05),但由于此时间点S组及T组VAS评分均属于轻度疼痛评分范围,可认为没有临床差异,在T0~5时各时间点VAS评分差异无统计学意义(表 4),以上结果显示2组患者静息和运动(咳嗽)状态下各时间点镇痛效果相当。
| 组别 | n | T0 | T1 | T2 | T3 | T4 | T5 | T6 |
| S组 | 49 | 1(1,2) | 1(0,2) | 1(0,1) | 0(0,1) | 0(0,1) | 1(0,2) | 0(0,1) |
| T组 | 51 | 1(0,2) | 0(0,1) | 0(0,1) | 0(0,1) | 0(0,1) | 1(0,2) | 0(0,1) |
| 统计量 | -1.725 | -1.495 | -0.571 | -0.373 | -0.538 | -0.088 | -1.065 | |
| P值 | 0.085 | 0.135 | 0.568 | 0.709 | 0.591 | 0.930 | 0.287 |
| 组别 | n | T0 | T1 | T2 | T3 | T4 | T5 | T6 |
| S组 | 49 | 2(2,3) | 2(1,3) | 1(1,2) | 1(0.5,2) | 1(0,2) | 2(1,3) | 2(1,3) |
| T组 | 51 | 2(1,3) | 2(1,2) | 1(1,2) | 1(0,2) | 2(1,2) | 2(1,3) | 1(1,2) |
| 统计量 | -1.586 | -1.431 | -0.204 | -0.200 | -0.748 | -0.839 | -2.907 | |
| P值 | 0.113 | 0.152 | 0.839 | 0.841 | 0.455 | 0.402 | 0.004 |
2.4 2组患者术后24 h内镇痛泵使用情况
观察2组患者术后24 h内镇痛泵使用情况作为VAS评分的补充,进一步评估术后镇痛的效果。结果显示:2组患者在舒芬太尼用量、首次按压时间、有效按压次数、实际按压次数方面差异无统计学意义(表 5),进一步表明2组患者在术后24 h内的镇痛效果无差异。
| 组别 | n | 24 h舒芬太尼用量/μg | 首次按压时间/h | 有效按压次数 | 实际按压次数 |
| S组 | 49 | 76(74,81) | 9.57(4.28,14.45) | 2(1.0,4.5) | 2(1.0,4.5) |
| T组 | 51 | 76(74,82) | 9.75(4.37,22.58) | 2(1.0,4.0) | 2(1.0,5.0) |
| 统计量 | -0.070 | -0.305 | -0.136 | -0.115 | |
| P值 | 0.944 | 0.760 | 0.892 | 0.908 |
2.5 2组患者术前和术后24h QOR-40评分比较
术前QOR-40评分分析结果显示:2组患者术前QOR-40评分的总分及在情感状态、身体舒适度、自理能力、心理支持和疼痛5个方面的评分差异无统计学意义(表 6),表明2组患者基线评分具有可比性。术后24 h QOR-40评分分析发现:2组患者术后24 h QOR-40评分(包括情感状态、身体舒适度、自理能力、心理支持和疼痛5个方面)及QOR-40总分差异无统计学意义(表 7),表明2组患者术后恢复质量相当。
| 组别 | n | 情绪状态 | 身体舒适度 | 自理能力 | 心理支持 | 疼痛 | QOR-40总分 |
| S组 | 49 | 44(44, 45) | 59(59, 60) | 25(25, 25) | 35(35, 35) | 35(35, 35) | 199(197, 200) |
| T组 | 51 | 44(44, 45) | 60(59, 60) | 25(25, 25) | 35(35, 35) | 35(35, 35) | 199(198, 200) |
| 统计量 | -0.123 | -1.961 | <0.001 | -1.726 | -0.502 | -1.247 | |
| P值 | 0.902 | 0.050 | 1.000 | 0.084 | 0.615 | 0.212 |
| 组别 | n | 情绪状态 | 身体舒适度 | 自理能力 | 心理支持 | 疼痛 | QOR-40总分 |
| S组 | 49 | 42(41, 44) | 55(54, 57) | 12(11, 14) | 34(28, 35) | 35(34, 35) | 177(168.5, 181.5) |
| T组 | 51 | 41(40, 43) | 56(52, 57) | 12(11, 13) | 34(28, 35) | 35(34, 35) | 175(166.0, 183.0) |
| 统计量 | -1.040 | -0.07 | -0.471 | -0.820 | -0.180 | -0.128 | |
| P值 | 0.298 | 0.994 | 0.638 | 0.412 | 0.857 | 0.898 |
3 讨论
本研究结果显示:在胸腔镜手术患者术后镇痛中,超声引导下SCTL浅面或深面注射局部麻醉药的TPVB联合术后PCIA,2组患者静息和运动(咳嗽)状态下各时间点VAS评分、24 h内镇痛泵使用情况无明显差异,均能为患者提供相当的镇痛效果。
GORNALL等[12]制定了QOR-40,是恢复质量的全球衡量标准。它包含5个部分:情绪状态、身体舒适度、自理能力、心理支持和疼痛,旨在提高量表的有效性、可靠性和反应性。本研究中2组患者术后24 h的QOR-40评分相当,表明两种神经阻滞方式联合PCIA可提供相当的恢复质量。
TPVB是指将局部麻醉药物注射到胸椎旁间隙内,但具体的注药靶点并没有明确,主要依靠超声引导下注药产生胸膜下压征作为参考,但这样操作贴近胸膜等重要脏器,而且胸椎旁间隙包含肋间动静脉且位于SCTL深面,同时非常贴近胸膜[2],穿刺针突破SCTL时易损伤血管、胸膜,容易导致出血及气胸等风险[4],本研究中T组操作时出现2例因穿刺针突破SCTL时损伤血管,未能进行注药,T组还出现1例硬膜外阻滞,有研究报道TPVB存在硬膜外阻滞及全脊麻的风险[6]。
为了提高安全性,注药靶点上移远离中轴胸膜、血管、神经是TPVB改良的趋势。目前有研究选择横突-胸膜中点注药已经取得良好的临床效果[10],但该注药点并不能精确靶点,由于个体差异,胸椎旁间隙的深度是不确定的,横突-胸膜中点位置可能在SCTL浅面,也可能在SCTL深面。如果胸椎旁间隙偏深,横突-胸膜中点位置可能会位于SCTL深面,这与经典TPVB是一致的;如果椎旁间隙偏窄,横突-胸膜中点位置可能还是在SCTL浅面,故MTP阻滞的镇痛效果可能与SCTL浅面与深面阻滞胸椎旁神经均有关系。
本研究中S组由于穿刺的靶点位于SCTL浅面,穿刺深度变浅,缩短了穿刺时间,在SCTL浅面阻滞可以有效避开血管、胸膜等高风险解剖结构,故穿刺时的风险、难度大大降低,同时还能取得和深面阻滞相当的临床镇痛效果。COŞARCAN等[13]发现于SCTL浅面注药,可以观察到胸膜下压征,也观察到很好的临床效果。本研究中有部分患者可识别胸膜下压征(S组15例,T组51例),这与文献报道也是相符合的。2组患者均能在超声下识别SCTL并作为超声定位参照标志,不再单纯依赖超声下注药产生胸膜下压征。我们还提出这样的猜想:TPVB达到镇痛效果亦不能单独依靠胸膜下压来下定论,注药后随着呼吸周期中胸腔室间压力梯度变化[14],以及药物的缓慢渗透作用,而逐渐起效达到临床镇痛效果,这也是我们后续需要进一步思考以及验证的。
综上所述,肋横突上韧带可作为超声引导下TPVB注药参照物,超声引导下SCTL浅面与深面注药用于TPVB联合PCIA,均可为胸腔镜手术患者提供有效镇痛效果及相当术后恢复质量,但超声引导下SCTL浅面注射局部麻醉药的TPVB操作方式更加简便、快捷与安全,是一种可以给胸腔镜手术患者术后提供有效镇痛以及促进恢复质量的辅助方式。
| [1] |
KARMAKAR M K. Thoracic paravertebral block[J]. Anesthesiology, 2001, 95(3): 771-780. |
| [2] |
陈韦东, 谭炜浩, 钟锦涛, 等. 胸椎旁神经阻滞技术的研究进展[J]. 中国临床解剖学杂志, 2021, 39(1): 111-114. CHEN W D, TAN W H, ZHONG J T, et al. Research progress of thoracic paravertebral block[J]. Chin J Clin Anat, 2021, 39(1): 111-114. |
| [3] |
SHIBATA Y, NISHIWAKI K. Ultrasound-guided intercostal approach to thoracic paravertebral block[J]. Anesth Analg, 2009, 109(3): 996-997. |
| [4] |
D'ERCOLE F, ARORA H, KUMAR P A. Paravertebral block for thoracic surgery[J]. J Cardiothorac Vasc Anesth, 2018, 32(2): 915-927. |
| [5] |
PACE M M, SHARMA B, ANDERSON-DAM J, et al. Ultrasound-guided thoracic paravertebral blockade: a retrospective study of the incidence of complications[J]. Anesth Analg, 2016, 122(4): 1186-1191. |
| [6] |
ALBI-FELDZER A, DUCEAU B, NGUESSOM W, et al. A severe complication after ultrasound-guided thoracic paravertebral block for breast cancer surgery: total spinal anaesthesia: a case report[J]. Eur J Anaesthesiol, 2016, 33(12): 949-951. |
| [7] |
COSTACHE I, SINCLAIR J, FARRASH F A, et al. Does paravertebral block require access to the paravertebral space?[J]. Anaesthesia, 2016, 71(7): 858-859. |
| [8] |
PIRACCINI E, BYRNE H, TADDEI S. Superior costotransverse ligament: a new target for fascial plane blocks[J]. Reg Anesth Pain Med, 2020, rapm-2020-101315. DOI: 10.1136/rapm-2020-101315.[Onlineahead of print].
|
| [9] |
CHO T H, KIM S H, O J, et al. Anatomy of the thoracic paravertebral space: 3D micro-CT findings and their clinical implications for nerve blockade[J]. Reg Anesth Pain Med, 2021, 46(8): 699-703. |
| [10] |
陈旭, 章蔚, 王迪, 等. 超声引导下横突-胸膜中点阻滞与胸椎旁神经阻滞用于单孔胸腔镜手术后镇痛效果的比较[J]. 临床麻醉学杂志, 2020, 36(12): 1173-1176. CHEN X, ZHANG W, WANG D, et al. Comparison of postoperative analgesic effects between ultrasound-guided mid-point transverse process to pleura block and thoracic paravertebral block in patients undergoing uniportal video-assisted thoracoscopic surgery[J]. J Clin Anesthesiol, 2020, 36(12): 1173-1176. |
| [11] |
COSTACHE I, DE NEUMANN L, RAMNANAN C J, et al. The mid-point transverse process to pleura (MTP) block: a new end-point for thoracic paravertebral block[J]. Anaesthesia, 2017, 72(10): 1230-1236. |
| [12] |
GORNALL B F, MYLES P S, SMITH C L, et al. Measurement of quality of recovery using the QoR-40: a quantitative systematic review[J]. Br J Anaesth, 2013, 111(2): 161-169. |
| [13] |
COŞARCAN S K, DOǦAN A T, ERÇELEN Ö, et al. Superior costotransverse ligament is the main actor in permeability between the layers? Target-specific modification of erector spinae plane block[J]. Reg Anesth Pain Med, 2020, 45(8): 674.1-675. |
| [14] |
NIELSEN M V, MORIGGL B, HOERMANN R, et al. Are single-injection erector spinae plane block and multiple-injection costotransverse block equivalent to thoracic paravertebral block?[J]. Acta Anaesthesiol Scand, 2019, 63(9): 1231-1238. |




