颈椎病是临床常见的颈椎退行性疾病,依据其病理特征及临床表现主要分为神经根型、脊髓型、交感型及椎动脉型[1]。神经根型颈椎病是指由于颈椎间盘退变突出及其继发的周围结构的骨赘增生等病灶压迫颈神经根所引起的上肢对应区域的感觉、运动障碍为主要表现的临床疾病[2-3]。物理治疗、药物治疗等保守治疗对神经根型颈椎病的疗效令人满意,但对于保守治疗无效的患者,手术治疗便成为了唯一选择[4-6]。经前路颈椎间盘切除融合术(anterior cervical discectomy and fusion,ACDF)是公认的治疗神经根型颈椎病的金标准手术,其具有手术时间短、出血量少、疗效确切等优点[7],但手术存在的全麻风险、食管损伤风险及融合术式带来的节段活动度降低、邻近节段退变加速等缺点让人无法忽视[8-9]。为了进一步降低手术创伤及风险,经后路颈椎内镜手术(posterior percutaneous endoscopic cervical foraminotomy,PECD)得以快速发展[10]。作为微创手术,PECD有着手术创伤小、术后恢复快、手术费用低及保留节段活动度等优点[11-12]。研究表明,PECD与ACDF治疗神经根型颈椎病的临床疗效相当[11, 13]。但目前,使用经椎板入路全内镜下椎间盘部分切除术治疗神经根型颈椎病的研究国内少有报道。因此,本研究对经椎板入路全内镜下椎间盘部分切除术治疗神经根型颈椎病的临床疗效进行回顾性分析。
1 资料与方法 1.1 一般资料2018年5月至2019年12月,共纳入30例本院骨科收治的神经根型颈椎病患者,其中女性16例,男性14例,年龄15~71(50.0±12.1)岁。患者的人群特征见表 1。术前所有患者行颈椎动力位X片评估颈椎稳定性,并行颈椎MRI及CT检查明确神经根受压情况。本研究符合本院人体试验伦理委员会所制定的伦理学标准(2020年科伦审第32号),并取得患者的知情同意。
| 项目 | 数值 |
| 性别 | |
| 女性 | 16 |
| 男性 | 14 |
| 年龄/岁 | 50.0±12.1 |
| 手术节段 | |
| C3/4 | 2 |
| C4/5 | 1 |
| C5/6 | 12 |
| C6/7 | 15 |
| 手术时间/min | 84.5±36.5 |
| 术中出血量/mL | 20.5±11.8 |
纳入标准:①单侧的神经根性疼痛,6周保守治疗效果不佳;②MRI或CT显示的与症状相符的单节段颈椎间盘突出,可伴有钩椎关节骨赘增生;③轻度的脊髓病变(Nurick分级≤3级)。
排除标准:①关节突关节增生所致的神经根管狭窄患者;②椎间孔极外侧型椎间盘突出;③合并有颈椎失稳;④合并有颈椎手术史;⑤合并有脊柱感染、脊柱肿瘤等疾病;⑥症状与影像不符;⑦严重的脊髓病变(Nurick分级>3级)。
1.2 手术方法手术材料及器械设备:镜下操作使用经皮颈椎内镜(Spinendos, 德国)。
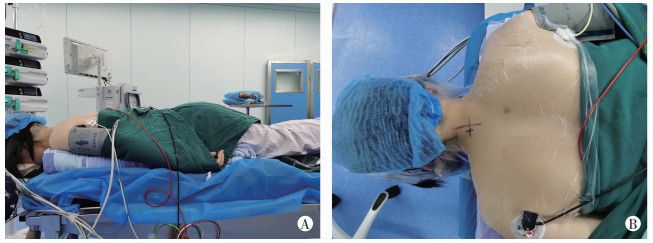
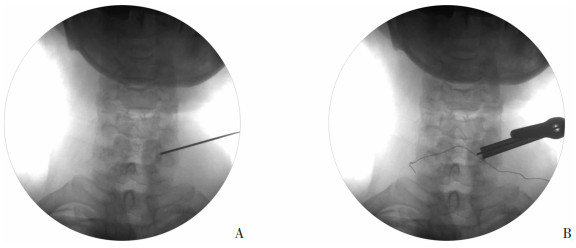
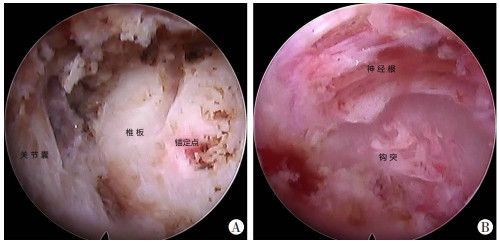
手术步骤:所有手术由同一名高级脊柱外科医师完成。手术均在局部麻醉以及镇痛药物辅助下完成。患者取俯卧位,头部使用Mayfield头架或Doro头架进行牵引固定,使颈部处于轻微过伸位(图 1A),C形臂X线透视确认手术节段下位椎体患侧椎弓根内侧缘的体表投影处(图 1B),局部局麻满意后,使用顿头穿刺针穿刺定位于椎弓根投影内侧缘(图 2A),C形臂X线透视确认位置后,于皮肤做约1 cm横行切口,沿穿刺针置入逐级扩张套管,并使用环锯进行锚定标记(图 2B),随后放置工作通道及脊柱内镜。在持续生理盐水灌洗下,使用射频电极及镜下抓钳清理局部软组织及止血,暴露锚定位置,并进一步确定椎板及关节突关节关节囊(图 3A)。在保护关节囊不被破坏的前提下,使用磨钻于椎板和侧块交界处磨除部分骨质进行椎板开窗到达硬膜囊,由开窗口向头侧清理硬膜外脂肪,暴露神经根,于神经根腋部取出突出的髓核组织并行纤维环成形术,若患者合并有钩椎关节增生,则使用磨钻于腋部对增生的骨质进行磨除(图 3B)。当镜下观察到神经根表面血管扩张、神经根松弛,则证明已充分减压。局部彻底止血后,移除操作设备,全层缝合切口1针。切口无需放置引流管,术后患者无需佩戴颈托。
|
| A:手术体位侧面大体图;B:手术体位正面大体图及椎弓根内侧缘的体表定位标记 图 1 患者手术体位正侧位 |
|
| A:术中透视下,穿刺针固定于椎弓根内侧缘;B:术中透视下,使用环锯进行椎板锚定 图 2 患者术中穿刺及锚定透视图 |
|
| A:内镜下椎板背侧结构;B:内镜下神经根腋部结构 图 3 患者术中颈椎椎板及减压后椎管内镜镜下观察 |
1.3 随访观察
统计手术时间、术中出血量和术中相关并发症等数据,所有患者术后行CT检查。术前、术后及末次随访时记录患者颈部功能障碍指数(neck disability index,NDI)评分、颈部视觉模拟(visual analog scale,VAS)评分及上肢VAS评分。
1.4 统计学分析使用SPSS 22.0统计软件,符合正态分布的计量资料以x±s表示,术前、术后及末次随访时的NDI评分、颈部VAS评分及上肢VAS评分采用重复测量的方差分析进行比较,进一步两两比较采用Bonferroni分析,P < 0.05为差异有统计学意义。
2 结果30例患者均成功完成手术,术后复查颈椎CT见神经根压迫解除。手术时间30~200(84.5±36.5)min,术中出血量5~50(20.5±11.8)mL。术中及术后均未观察到神经血管损伤及其他严重并发症。患者随访时间为9~23(14.3±4.0)个月。NDI评分由术前(61.3±13.2)分降低至术后(26.6±7.4)分(P < 0.01),末次随访时进一步降低至(9.8±3.5)分(P < 0.01)。术前颈部及上肢VAS评分分别为(5.2±0.7)分和(6.5±1.1)分,术后分别降低至(3.1±0.7)分和(2.8±0.7)分(P < 0.01),末次随访时进一步降低至(0.6±0.8)分和(0.5±0.6)分(P < 0.01)。随访期间内,所有患者均无颈椎失稳表现。
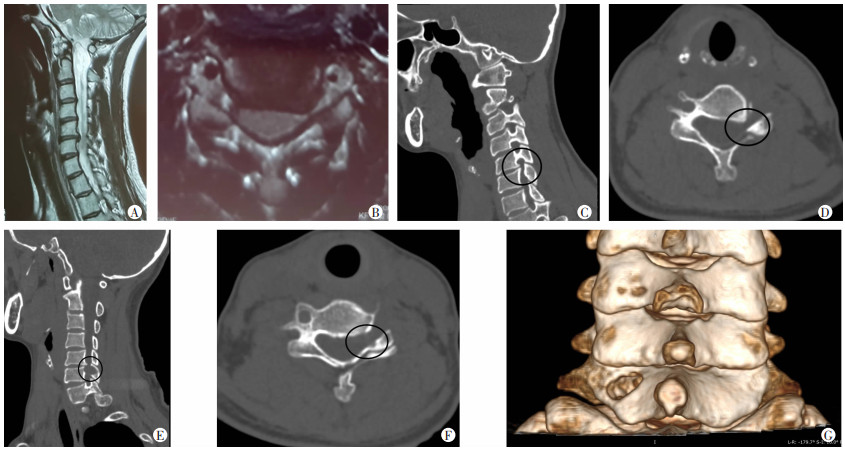
典型病例:患者女性,29岁,因“颈痛伴左上肢疼痛3个月余”入院,诊断为C6/7神经根型颈椎病,入院后第3天行经椎板入路全内镜下椎间盘部分切除术。患者术前及术后影像表现见图 4。患者钩椎关节骨赘可被磨除,椎间孔狭窄缓解。
|
| A~D:患者术前颈椎MRI图像及CT图像;E~G:患者术后颈椎CT图像及CT三维重建图像 图 4 典型病例术前及术后影像表现 |
3 讨论
神经根型颈椎病是临床上常见的颈肩部及上肢疼痛的病因之一,已成为全世界卫生组织的巨大负担[2]。通常认为神经根型颈椎病是由颈椎退变所致的椎间盘突出及椎体骨赘增生等原因压迫相应脊神经根产生,其典型临床表现为颈肩部僵硬感、上肢麻木疼痛、感觉异常及肌力减退等,在颈椎MRI及CT检查上通常可见到相应突出物压迫神经根的典型影像学表现[3, 5]。对于神经根型颈椎病的治疗通常以保守治疗为主,据文献报道,大多数患者可在保守治疗下达到症状的完全缓解,然而,对于保守治疗效果不佳的患者,手术治疗便成为了首选[14]。ACDF是被公认为治疗神经根型颈椎病的金标准手术,其手术疗效确切,被广泛用于神经根型颈椎病的治疗[15]。然而身为开放融合手术,其相对较大的手术创伤、颈前部重要器官、血管、神经的损伤风险、融合术式带来的节段活动度降低及高额的手术费用等缺点越来越受到人们的关注[8-9, 16-17]。为了进一步降低手术创伤,且随着微创手术技术的不断发展,RUETTEN等[12]率先报道了使用PECD治疗神经根型颈椎病的临床疗效。作为过渡手术,PECD仅对压迫神经根的椎间盘或骨赘进行局部切除,保留了相对健康的正常组织结构,避免了融合所带来的一系列并发症[11, 18]。研究报道,PECD临床疗效显著,患者术后颈部及上肢疼痛明显降低,手术节段的活动度也得到了保留,有着手术创伤小、术后恢复快、手术费用低等优点[13, 19]。且PECD在全身麻醉及局部麻醉下都可实施,为手术医师及患者提供了更多选择。全身麻醉可避免患者的术中痛苦体验及术中刺激所致的主动活动,但全身麻醉下患者无法及时反馈神经刺激,增加了术中神经损伤的风险;局部麻醉可依据患者术中反馈及时调整手术操作,一定程度上减少了神经骚扰,但具有患者术中体验差的缺点,也增加了患者术中刺激后主动活动所致的意外损伤风险。因此,PECD逐渐成为治疗神经根型颈椎病的一个新选择。
然而,传统的PECD选择关节突关节与椎板交界点(V点)作为手术入路(Key-hole入路),为了进入椎管暴露受压的神经根,常需要磨除部分关节突关节[12, 20]。尽管磨除小于50%的关节突关节对颈椎稳定性无显著影响[18, 21-22],但微创手术的目的在于在尽可能减少对于正常组织医源性损伤的同时达到手术疗效。关节突关节是颈椎重要的承接结构之一,Key-hole入路为解除神经根压迫,破坏了其正常的结构,增加了术后远期颈椎失稳的风险[23-24],且关节突关节具有完整的关节囊、关节面、半月板等关节结构,任何对于其正常结构的破坏都将加速其退变,导致局部炎症因子聚集及椎旁关节的骨性关节炎,进而引起颈部的轴性疼痛[25-26]。为了进一步减少PECD对正常组织的医源性损伤,我们采用经椎板入路进入椎管。颈椎椎板并无重要的承接稳定作用,椎板的部分缺损对颈椎稳定性影响十分有限[27]。经椎板入路保留了正常的关节突关节结构,减少了术后颈椎失稳的风险,同时也避免了因术中损伤所致的关节退变加速,降低了术后发生关节突关节源性轴性颈痛的可能性。随访结果显示,患者术后颈部VAS显著下降,且在随访期间持续下降,无明显继发颈痛出现。
与此同时,传统的Key-hole入路,操作区域位于神经根的上方,当需要进行腹侧减压时,常需要对神经根进行牵拉,这增加了术中神经根损伤的风险,易导致术后患者一过性的感觉、肌力减弱等症状[11, 28-29],且研究表明,钩椎关节增生发生率高,是常见的神经根压迫原因之一[30-31]。若术中难以完成神经根腹侧病灶的清除,单纯的摘除软性突出物或背侧切开减压常效果不佳。经椎板入路选择病变节段的下位或上位椎体椎板为进入点,操作通道斜行进入椎管,与神经根形成操作角度,从神经根的腋部或肩部进行腹侧减压,在保证充分减压的同时,减少了对神经根的牵拉,降低了术中发生神经根牵拉损伤的风险,且经椎板入路进入椎管后位于神经根腋部,可通过磨除部分椎弓根内上侧缘扩大腋部操作空间,暴露神经根腹侧钩椎关节,以完成对于钩椎关节增生骨赘的磨除,达到腹侧减压。随访结果表明,所有患者的腹侧病灶均被去除,术后上肢疼痛明显减轻,NDI评分显著下降,且未观察到明显神经根牵拉损伤表现。
经椎板入路选择颈椎椎板作为手术入路,孔道位于颈椎椎板与侧块连接处,V点的外下方,其上下方为邻近的关节突关节,内侧为颈椎椎板,外侧为颈椎侧块及椎弓根。由于神经根位于通道的内上方,因此使用磨钻创建通道时应使其具有一定的头倾角及内倾角。当进行穿刺定位时,可将穿刺针固定于患侧节段下位椎体椎弓根的侧块投影上,且使用顿头穿刺针进行穿刺定位可降低穿刺过程中血管损伤风险。颈椎内镜手术镜下识别结构困难大,错误的镜下定位会使得手术难度增加、时间延长,并会对正常结构产生不必要的破坏。在定位满意后,使用锚定技术进行标记,可指引镜下结构的识别,减少手术时间及难度。若突出椎间盘位于神经根肩部,则可选择病变节段上位椎体椎板为定位点,从神经根的外上方进行操作摘除突出的椎间盘。若突出的椎间盘位于旁中央区域,可磨除部分椎弓根内侧缘骨质,增大通道的内倾角,以便取出靠近内侧的突出椎间盘。若患者钩椎关节增生压迫神经根,可磨除部分椎弓根内上侧缘以扩大腋部操作空间进行神经根腹侧骨赘磨除。
本研究取得了比较满意的初期临床效果,患者的症状均在术后减轻。但本研究仍存在以下局限性:①研究结果为初期的临床疗效观察,缺乏对照,样本量较少;②仅使用临床评分量表对患者临床疗效进行评估,带有一定主观性,缺乏影像学评估;③随访过程中未见明显颈椎失稳表现,但椎板打孔对颈椎稳定性的影响仍需进一步生物力学有限元分析验证;④随访时间较短,其远期疗效仍需进一步探究。
综上所述,经椎板入路全内镜下椎间盘部分切除术可在保留关节突关节的同时完成神经根直接减压,缓解患者的神经根压迫症状,是神经根型颈椎病治疗的一种新选择,但远期疗效及影像学评估仍需进一步探究。
| [1] |
柯尊华, 王静怡. 颈椎病流行病学及发病机理研究进展[J]. 颈腰痛杂志, 2014, 35(1): 62-64. KE Z H, WANG J Y. Progress of epidemiology and pathogenesis of cervical spondylosis[J]. J Cervicodynia Lumbodynia, 2014, 35(1): 62-64. |
| [2] |
YOON S H. Cervical radiculopathy[J]. Phys Med Rehabilitation Clin N Am, 2011, 22(3): 439-446. |
| [3] |
张军. 神经根型颈椎病根性痛的解剖学基础和发病机理的研究[J]. 中国中医骨伤科杂志, 1999, 7(1): 49. ZHANG J. Study on anatomical basis and pathogenesis of radiculopathic cervical pain[J]. Chin J Aditional Med Aumatol Orthop, 1999, 7(1): 49. |
| [4] |
王天仪, 艾尔肯·萨德尔. 神经根型颈椎病的诊断与治疗[J]. 新疆医科大学学报, 2008, 31(4): 483-485. WANG T Y, AIERKEN S D E. Diagnosis and treatment of cervical radiculopathy[J]. J Xinjiang Med Univ, 2008, 31(4): 483-485. |
| [5] |
朱庆三, 顾锐. 神经根型颈椎病的定位诊断与治疗方法[J]. 中国脊柱脊髓杂志, 2007, 17(2): 93-95. ZHU Q S, GU R. Localization diagnosis and treatment of cervical radiculopathy[J]. Chin J Spine Spinal Cord, 2007, 17(2): 93-95. |
| [6] |
李建垒, 曹向阳, 宋永伟. 保守治疗神经根型颈椎病的研究现状[J]. 中国医药导刊, 2020, 22(9): 607-610. LI J L, CAO X Y, SONG Y W. Research status of conservative treatment of cervical spondylotic radiculopathy[J]. Chin J Med Guide, 2020, 22(9): 607-610. |
| [7] |
WRIGHT I P, EISENSTEIN S M. Anterior cervical discectomy and fusion without instrumentation[J]. Spine (Phila Pa 1976), 2007, 32(7): 772-774; discussion775. |
| [8] |
FOUNTAS K N, KAPSALAKI E Z, NIKOLAKAKOS L G, et al. Anterior cervical discectomy and fusion associated complications[J]. Spine (Phila Pa 1976), 2007, 32(21): 2310-2317. |
| [9] |
WANG M C, CHAN L, MAIMAN D J, et al. Complications and mortality associated with cervical spine surgery for degenerative disease in the United States[J]. Spine, 2007, 32(3): 342-347. |
| [10] |
RUETTEN S, KOMP M, MERK H, et al. Full-endoscopic cervical posterior foraminotomy for the operation of lateral disc herniations using 5.9-mm endoscopes: a prospective, randomized, controlled study[J]. Spine (Phila Pa 1976), 2008, 33(9): 940-948. |
| [11] |
HUANG J J, SUN H H, SHAO Z W, et al. Posterior full-endoscopic cervical discectomy in cervical radiculopathy: a prospective cohort study[J]. Clin Neurol Neurosurg, 2020, 195: 105948. |
| [12] |
RUETTEN S, KOMP M, MERK H, et al. A new full-endoscopic technique for cervical posterior foraminotomy in the treatment of lateral disc herniations using 6.9-mm endoscopes: prospective 2-year results of 87 patients[J]. Minim Invas Neurosurg, 2007, 50(4): 219-226. |
| [13] |
AHN Y, KEUM H J, SHIN S H. Percutaneous endoscopic cervical discectomy versus anterior cervical discectomy and fusion: a comparative cohort study with a five-year follow-up[J]. J Clin Med, 2020, 9(2): E371. |
| [14] |
王英杰. 神经根型颈椎病治疗现状与进展[J]. 中国矫形外科杂志, 2014, 22(9): 812-814. WANG Y J. Surgical treatment status and progress of CSR[J]. Orthop J China, 2014, 22(9): 812-814. |
| [15] |
CHU C W, KUNG S S, TSAI T H, et al. Anterior discectomies and interbody cage fusion without plate fixation for 5-level cervical degenerative disc disease: a 5-year follow-up[J]. Kaohsiung J Med Sci, 2011, 27(11): 524-527. |
| [16] |
郎昭, 田伟, 何达, 等. 颈前路术后早期并发症的危险因素分析[J]. 中华骨科杂志, 2017(3): 162-168. LANG Z, TIAN W, HE D, et al. Risk factors for early complications after anterior cervical spine surgery[J]. Chin J Orthop, 2017(3): 162-168. |
| [17] |
金大地, 王健, 瞿东滨. 颈椎前路手术早期并发症原因分析及对策[J]. 中华骨科杂志, 2005(2): 102-106. JIN D D, WANG J, QU D B. Analysis of early complications in anterior cervical spine surgery[J]. Chin J Orthop, 2005(2): 102-106. |
| [18] |
AHN Y, LEE S H, SHIN S W. Percutaneous endoscopic cervical discectomy: clinical outcome and radiographic changes[J]. Photomed Laser Surg, 2005, 23(4): 362-368. |
| [19] |
MANSFIELD H E, CANAR W J, GERARD C S, et al. Single-level anterior cervical discectomy and fusion versus minimally invasive posterior cervical foraminotomy for patients with cervical radiculopathy: a cost analysis[J]. Neurosurg Focus, 2014, 37(5): E9. |
| [20] |
KOMP M, OEZDEMIR S, HAHN P, et al. Full-endoscopic posterior foraminotomy surgery for cervical disc herniations[J]. Oper Orthop Traumatol, 2018, 30(1): 13-24. |
| [21] |
EPSTEIN N E. A review of laminoforaminotomy for the management of lateral and foraminal cervical disc herniations or spurs[J]. Surg Neurol, 2002, 57(4): 226-233;discussion233. |
| [22] |
EBRAHEIM N A, XU R M, BHATTI R A, et al. The projection of the cervical disc and uncinate process on the posterior aspect of the cervical spine[J]. Surg Neurol, 1999, 51(4): 363-367. |
| [23] |
NGUYEN J, CHU B, KUO C C, et al. Changes in foraminal area with anterior decompression versus keyhole foraminotomy in the cervical spine: a biomechanical investigation[J]. J Neurosurg Spine, 2017, 27(6): 620-626. |
| [24] |
CHEN B H, NATARAJAN R N, AN H S, et al. Comparison of biomechanical response to surgical procedures used for cervical radiculopathy: posterior keyhole foraminotomy versus anterior foraminotomy and discectomy versus anterior discectomy with fusion[J]. J Spinal Disord, 2001, 14(1): 17-20. |
| [25] |
CAVANAUGH J M, LU Y, CHEN C Y, et al. Pain generation in lumbar and cervical facet joints[J]. J Bone Joint Surg Am, 2006, 88(Suppl 2): 63-67. |
| [26] |
YU S W, SETHER L, HAUGHTON V M. Facet joint menisci of the cervical spine: correlative MR imaging and cryomicrotomy study[J]. Radiology, 1987, 164(1): 79-82. |
| [27] |
房敏, 沈国权, 严隽陶, 等. 颈椎主要结构生物力学特性实验研究[J]. 颈腰痛杂志, 2002, 23(2): 89-92. FANG M, SHEN G Q, YAN J T, et al. Biomachanical research on the main structure mechanical characteristics of the cervical vertebrae[J]. J Cervicodynia Lumbodynia, 2002, 23(2): 89-92. |
| [28] |
TONG Y X, HUANG Z H, HU C, et al. A comparison study of posterior cervical percutaneous endoscopic ventral bony decompression and simple dorsal decompression treatment in cervical spondylotic radiculopathy caused by cervical foraminal and/or lateral spinal Stenosis: a clinical retrospective study[J]. BMC Musculoskelet Disord, 2020, 21(1): 290. |
| [29] |
彭明, 戚超, 吕道静, 等. 显微内镜下颈椎后路椎间孔切开减压术的疗效探讨[J]. 中国修复重建外科杂志, 2010, 24(5): 513-516. PENG M, QI C, LYU D J, et al. Efficacy of posterior microendoscopic foraminotomy for cervical radiculopathy[J]. Chin J Reparative Reconstr Surg, 2010, 24(5): 513-516. |
| [30] |
LEE S H, SON D W, LEE J S, et al. Relationship between endplate defects, modic change, facet joint degeneration, and disc degeneration of cervical spine[J]. Neurospine, 2020, 17(2): 443-452. |
| [31] |
NGUYEN C, SANCHEZ K, ROREN A, et al. Anatomical specificities of the degenerated cervical spine: a narrative review of clinical implications, with special focus on targeted spinal injections[J]. Ann Phys Rehabil Med, 2016, 59(4): 276-281. |




