膀胱癌是我国泌尿系统最常见的恶性肿瘤,随着人均寿命的延长和人口老龄化问题的日益严重,膀胱癌的发病人数呈现出快速增长的趋势[1]。在新发的膀胱癌病例中,约75%的患者被诊断为非肌层浸润性膀胱癌(non-muscle-invasive bladder cancer,NMIBC)[2]。NMIBC的主要治疗方式是经尿道膀胱肿瘤切除术[3]。肿瘤切除术后常需要进行膀胱内灌注治疗,通过杀伤残留的肿瘤组织以及游离的肿瘤细胞以降低肿瘤复发和进展的风险[4-5]。目前常用的膀胱灌注治疗药物包括卡介苗、丝裂霉素、表柔比星和吉西他滨等[6]。虽然这些传统的药物可以达到一定的临床疗效,减少复发风险,但是由于药物生物利用率低,导致其治疗效果有限。此外,膀胱灌注治疗药物产生的毒副作用也限制其进一步的应用[7]。因此,急需发展高效的治疗策略,寻求新的药物或剂型来优化膀胱癌的灌注治疗。近年来,随着纳米技术的出现,肿瘤的治疗方式得到了极大的发展。纳米载药体系包括有机纳米载体和无机纳米载体。纳米载药体系可以提高药物稳定性和生物利用度,并降低药物毒副作用,其在膀胱灌注治疗中的应用已经受到广泛的关注。脂质体、高分子聚合物等有机纳米载药体系由于生物可降解、毒副作用低而被广泛应用于膀胱内的灌注研究。然而结构更稳定的无机纳米载体在膀胱灌注治疗中的研究却很少[8-9]。无机材料制备的介孔二氧化硅纳米粒子(mesoporous silica nanoparticles,MSN)由于具有大小可调控、比表面积大、结构稳定、易于功能化和生物相容性高等优点而越来越受重视[10-12]。本实验利用MSN包载化疗药物阿霉素(doxorubicin,DOX)来制备介孔二氧化硅纳米药物(MSN-DOX),研究其在人膀胱移行细胞癌细胞(T24细胞)中的细胞摄取行为、对T24细胞的增殖抑制效果以及凋亡作用,探究其在膀胱癌灌注治疗中的临床应用价值,为膀胱癌的灌注治疗提供新的思路。
1 材料与方法 1.1 材料与试剂RPMI1640培养基及胎牛血清购自美国HyClone公司;青链霉素混合液购自中国碧云天生物技术公司;胰蛋白酶消化液购自美国Gibico公司;磷酸盐缓冲溶液购自中国中杉金桥生物技术有限公司;Cell Counting Kit-8购自日本Dojindo公司;Hoechst 33342购自中国碧云天生物技术公司;BCA蛋白浓度检测试剂盒、SDS-PAGE凝胶、Western blot细胞裂解液、一抗稀释液和封闭液均购自中国碧云天生物技术公司;PVDF膜(0.2 μm) 购自美国Millipore公司;抗Cleaved Caspase-3抗体、抗PARP1抗体和抗β-actin抗体购自Cell Signaling Technology公司;Alexa Fluor 488标记山羊抗兔IgG和Alexa Fluor 488标记山羊抗小鼠IgG购自美国Invitrogen公司。
1.2 实验方法 1.2.1 细胞培养T24细胞购于ATCC细胞库, 在37 ℃、5%CO2的细胞孵箱中培养。培养液采用RPMI1640培养基加10%胎牛血清以及1%的青链霉素混合液,每2天更换1次培养液。
1.2.2 MSN的制备称取0.068 g三乙醇胺加入25 mL去离子水中,80 ℃下搅拌30 min。将380 mg溴化十六烷基三甲铵和95 mg水杨酸钠加入上述溶液中继续搅拌1 h。将4 mL正硅酸乙酯加入后继续磁力搅拌2 h。将上述溶液10 000 r/min离心10 min后倒掉上清,用去离子水和无水乙醇反复清洗6次,冷冻干燥得到含有溴化十六烷基三甲铵模板剂的二氧化硅纳米颗粒。将含有模板剂的二氧化硅纳米颗粒加入含有1 g硝酸铵的100 mL无水乙醇中,在80 ℃水浴中充分冷凝回流40 min。反应结束冷却至室温,用无水乙醇清洗6次,并冷冻干燥密封保存。
1.2.3 MSN-DOX的制备精密称量20 mg MSN固体粉末,缓慢加入1 mg/mL DOX溶液10 mL并超声溶解,避光室温搅拌过夜。采用高速离心法(10 000 r/min,10 min)去除游离的DOX,最后用去离子水离心洗涤2次,收集所有离心后的上清液用于载药量和包封率的测定,冻干获取MSN-DOX。
1.2.4 基本表征形貌观察:取适量的MSN和MSN-DOX置于去离子水中超声溶解,将铜网浸入样品溶液中,用滤纸吸去多余水分并置于通风处晾干,通过透射电子显微镜观察形貌。粒径及表面电荷测量:取适量的MSN和MSN-DOX置于去离子水中超声溶解,通过纳米粒度电位分析仪测量粒径及表面电荷。
1.2.5 MSN-DOX载药量和包封率的测量精密称取DOX 2 mg,用2 mL去离子水溶解配置成1 mg/mL的溶液并等比稀释,利用紫外-可见分光光度计测量各个浓度的标准DOX溶液在480 nm处的光密度值[D(480)],并绘制标准曲线。
精密测量MSN-DOX制备过程中收集上清液的体积,并利用紫外-可见分光光度计测量上清液在480 nm处的光密度值[D(480)],根据绘制的DOX标准曲线,计算上清液中浓度。根据以下公式计算MSN-DOX载药量和包封率。
1.2.6 MSN-DOX体外药物释放分析由于尿液的pH值波动范围较大,与饮食和病理因素等相关,其正常pH值介于4.5~8.0。因此,配置不同pH值(5.5、6.8和8.0)的PBS溶液作为释放液,观察纳米药物在不同pH条件下的药物释放行为。精密称取MSN-DOX 2 mg,分别用2 mL不同pH值的PBS溶液配置1 mg/mL的样品液,将样品液放入透析袋(MWCO 8 000~14 000 Da)中,再将透析袋置于5 mL相应的释放液中,避光,37 ℃下进行药物释放研究。在预定时间点取出1 mL释放液并补充新鲜相应pH的PBS溶液,通过紫外-可见分光光度计测量每个时间点释放液在480 nm处的光密度值[D(480)],根据标准曲线计算药物释放量,并绘制时间-累积释放百分比曲线观测MSN-DOX在不同pH值下的药物释放情况。
1.2.7 MSN-DOX细胞摄取分析取对数生长期的T24细胞,用PBS洗涤后胰酶消化,取1 mL的细胞悬液接种于激光共聚焦显微皿中,细胞数为1×105/mL。细胞孵箱中孵育24 h后加入DOX或MSN-DOX,继续孵育一段时间后去掉培养液,用PBS清洗3次,除去残留的药物。用Hoechst 33342染色10 min,再次用PBS清洗3次,每次3 min。最后加入1 mL无血清培养基,利用激光共聚焦显微镜观察各组细胞内的药物荧光信号强度,实验分组包括5 μg/mL DOX孵育0.5 h组,5 μg/mL DOX孵育2 h组,10 μg/mL DOX孵育0.5 h组,10 μg/mL DOX孵育2 h组,MSN-DOX(DOX浓度为5 μg/mL)孵育0.5 h组,MSN-DOX(DOX浓度为5 μg/mL)孵育2 h组,MSN-DOX(DOX浓度为10 μg/mL)孵育0.5 h组,MSN-DOX(DOX浓度为10 μg/mL)孵育2 h组。
1.2.8 MSN细胞毒性及MSN-DOX细胞增殖抑制分析将对数生长期的T24细胞用PBS洗涤后胰酶消化,以每孔3 000个细胞接种于96孔板中,在37 ℃、5%CO2的细胞培养箱中孵育24 h。分别加入不同浓度(10、20、40、80 μg/mL)的MSN与细胞共培养24 h和48 h,每孔加入100 μL提前配置好的CCK-8试剂,继续孵育2 h,用酶标仪检测每孔在450 nm波长处的光密度值[D(450)]。与空白组对照,观察不同浓度MSN的细胞毒性。
在同样的条件下将T24细胞接种在96孔板并孵育24 h,分别在培养液中加入DOX和含有相同DOX的MSN-DOX,再次孵育24 h或48 h,每孔加入100 μL提前配置好的CCK-8试剂,孵育2 h后用酶标仪检测每孔在450 nm处的光密度值[D(450)]。以空白组为对照,观察MSN-DOX细胞增殖抑制效果。
1.2.9 MSN-DOX细胞凋亡分析将对数生长期的T24细胞用胰酶消化,取1 mL细胞悬液(细胞数为5×105/mL)接种于细胞培养皿中,再加入5 mL含血清培养液培养24 h。更换培养液后加入MSN,DOX和MSN-DOX(DOX浓度为4 μg/mL)再次孵育48 h。用细胞刮的方法将贴壁细胞刮下使其悬浮于培养基中,将培养基全部转移到15 mL离心管中,1 200 r/min离心3 min。用1 mL PBS重悬细胞后加入到1.5 mL离心管,再次1 200 r/min离心3 min。加入适量的细胞裂解液混匀,放置于冰上作用30 min后12 000 ×g离心15 min,取上清液进行Western blot检测,分析Cleaved PARP和Cleaved Caspase-3的表达情况。
1.3 统计学分析所有实验至少进行3次,采用SPSS 25.0统计学软件分析数据。结果以 x±s表示,采用单因素方差分析,组间两两比较采用t检验。P < 0.05为差异具有统计学意义。
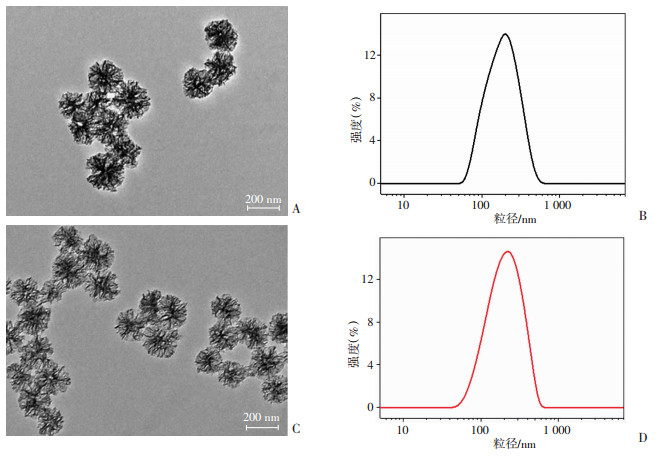
2 结果 2.1 物理化学表征成功制备出介孔二氧化硅纳米药物,其基本表征见图 1。MSN和MSN-DOX均呈球形,大小均匀,两者粒径无明显差异。通过动态光散射测量的MSN-DOX粒径大小为(203.6±3.0)nm(图 1D),与透射电镜结果一致。MSN和MSN-DOX表面电荷均为负电荷,分别为(-17.3±4.8) mV和(-8.1±4.7) mV。
|
| A:MSN透射电镜图像;B:MSN粒径分布;C:MSN-DOX透射电镜图像;D:MSN-DOX粒径分布 图 1 载药前后介孔二氧化硅纳米药物的基本表征 |
2.2 MSN-DOX的载药性能及体外药物释放
MSN具有介孔结构,通过将药物吸附在表面和内部的孔道达到载药的目的。本实验制备的介孔二氧化硅纳米药物的载药量为4.83%,包封率为10.15%。
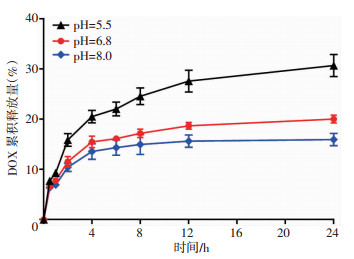
选取pH值为5.5、6.8和8.0的PBS溶液作为释放介质,观察MSN-DOX在不同pH值环境下的药物释放行为。药物从MSN-DOX中缓慢释放,前12 h释放速度较快,之后逐渐变缓(图 2)。药物释放速度以及总释放量与环境pH值相关, 在低pH值下,MSN与DOX电荷相互作用减弱,促进DOX的释放。在pH值为5.5时,药物释放速度约是pH值为8.0时的1.5倍。随着环境pH值的升高,药物的总释放量降低;在pH值为5.5、6.8和8.0时,24 h内药物总释放量分别为30.7%、20.0%和15.9%。结果表明MSN可以有效包载DOX,所形成的纳米药物缓慢释放所负载的药物,其释放速度和总释放量与环境pH值相关,环境pH值越低,药物释放速度越快,总释放量越高。
|
| 图 2 介孔二氧化硅纳米药物的体外药物释放情况 |
2.3 MSN-DOX在膀胱癌细胞中的内吞
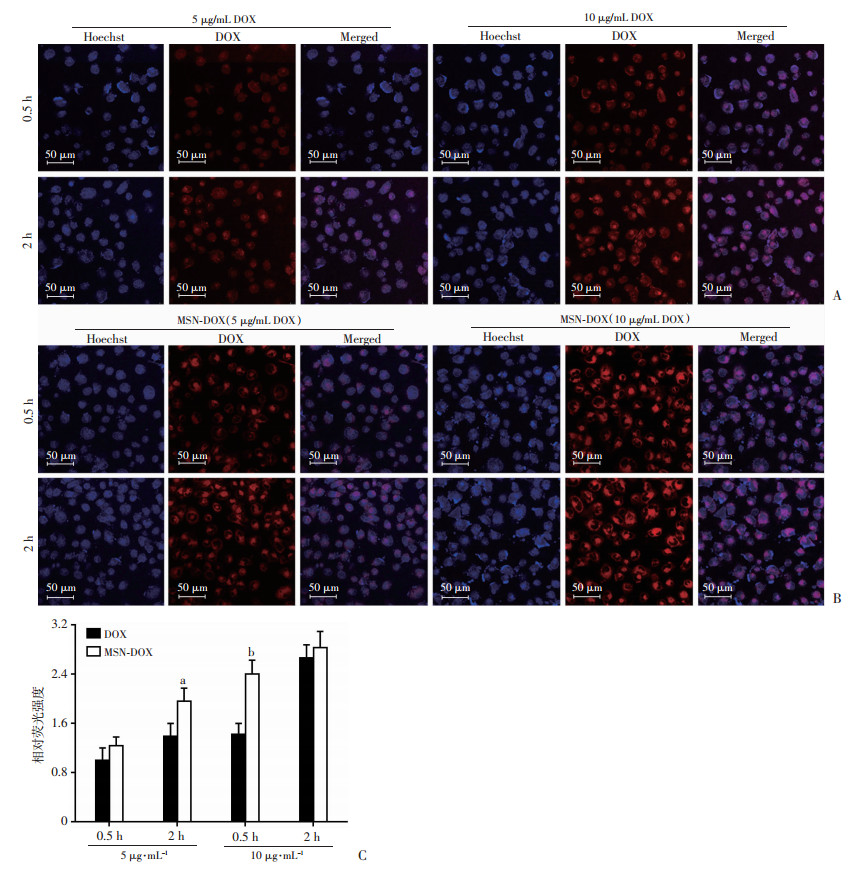
通过活细胞染色技术并利用激光共聚焦显微镜观察药物在T24细胞内的摄取情况。蓝色部分为Hoechst 33342染色的细胞核,红色部分为DOX荧光。如图 3所示,药物的红色荧光与细胞核的蓝色荧光基本重叠,表明DOX和MSN-DOX均可以有效地被T24细胞摄取,且大部分集中在细胞核内。随着DOX浓度的升高或药物孵育时间的延长,细胞内蓄积的药物增多。相比于DOX,MSN-DOX处理的细胞红色荧光普遍更强。为了进一步量化药物在细胞内的蓄积情况,用Image J软件评估药物的相对荧光强度。将5 μg/mL DOX孵育0.5 h组的荧光强度定义为1,相对荧光强度是指其他各组与5 μg/mL DOX孵育0.5 h组的荧光强度比值。如图 3C所示,MSN-DOX(DOX浓度为5 μg/mL)孵育2 h组的荧光强度是5 μg/mL DOX孵育2 h组荧光强度的1.4倍。当用10 μg/mL DOX孵育0.5 h时,MSN-DOX组的荧光强度是DOX组的1.7倍,且差异具有统计学意义(P < 0.01)。表明MSN-DOX较DOX能更有效的被膀胱癌细胞摄取。
|
| A、B:激光共聚焦显微镜观察不同浓度DOX及MSN-DOX孵育0.5 h或2 h后细胞内药物蓄积情况 Hoechst代表Hoechst 33342染色的细胞核;DOX代表阿霉素荧光图像;Merged代表两者的融合图像;C:不同处理组对应荧光强度的定量分析 a:P < 0.05,b:P < 0.01,与DOX组比较 图 3 阿霉素和介孔二氧化硅纳米药物在T24细胞中的摄取情况 |
2.4 MSN的生物相容性
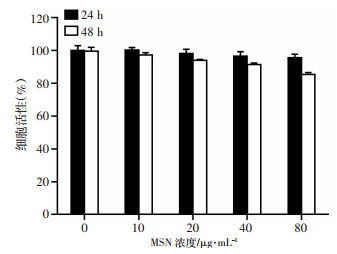
MSN具有优秀的生物相容性,与空白对照组(0 μg/mL MSN)相比,随着MSN浓度的升高和孵育时间的延长,T24细胞活性均未见明显降低。如图 4所示,即使MSN浓度达到80 μg/mL,孵育时间达到48 h,T24细胞活性仍维持在80%以上。表明MSN在实验浓度范围内不影响T24细胞的生长,毒性较低,可作为膀胱内药物递送的优良载体。
|
| 图 4 介孔二氧化硅纳米粒子对T24细胞活性的影响 |
2.5 MSN-DOX对膀胱癌细胞的增殖抑制
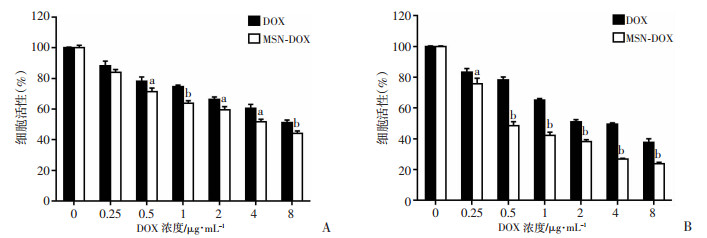
图 5显示了24 h和48 h的细胞存活率与药物浓度之间的关系,未处理的细胞作为参考。DOX和MSN-DOX均能够有效抑制T24细胞的生长,且呈现时间和剂量依赖性。随着药物浓度的升高,对T24细胞的生长抑制效果越强。在24 h时,MSN-DOX处理组T24细胞的增殖抑制效果均优于相对应药物浓度的DOX处理组(P < 0.05,图 5A)。在48 h时,MSN-DOX的增殖抑制效果较之DOX更加明显,且差异具有显著的统计学意义(P < 0.01,图 5B)。在药物细胞孵育24 h和48 h后,DOX的半抑制浓度(IC50)分别为(8.61±1.13)μg/mL和(3.19±0.14)μg/mL,明显高于MSN-DOX的(4.44±0.19)μg/mL和(0.78±0.05)μg/mL(P < 0.05)。结果表明,MSN-DOX可显著增强药物对细胞的增殖抑制效果。
|
| A:24 h;B:48 h a:P < 0.05,b:P < 0.01,与DOX组比较 图 5 不同浓度的阿霉素和介孔二氧化硅纳米药物孵育T24细胞不同时间后细胞活性变化 |
2.6 MSN-DOX促进膀胱癌细胞凋亡
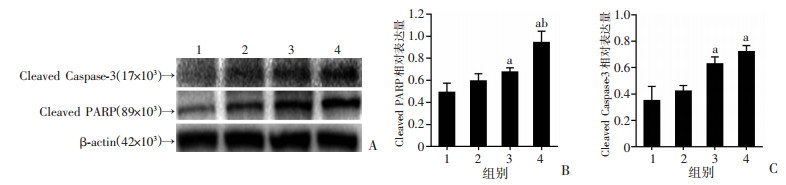
与对照组相比,DOX和MSN-DOX处理组细胞的凋亡相关蛋白表达明显增多,且MSN-DOX处理组表达量更多(图 6A)。定量分析显示MSN-DOX组Cleaved PARP表达量是对照组的1.9倍,DOX处理组Cleaved PARP表达量是对照组的1.4倍,且差异具有统计学意义(P < 0.05,图 6B)。DOX和MSN-DOX处理的两组细胞Cleaved Caspase-3表达相对于对照组增多(P < 0.05,图 6C),但两者之间差异无统计学意义。结果表明,MSN-DOX可以增加细胞凋亡相关蛋白的表达,促进T24细胞的凋亡。
|
|
1:对照组;2:MSN组;3:DOX组;4:MSN-DOX组;a:P < 0.05,与对照组比较;b:P < 0.05,与DOX组比较 A:Western blot检测各组T24细胞凋亡相关蛋白的表达变化;B、C:Cleaved PARP和Cleaved Caspase-3蛋白相对表达分析 图 6 阿霉素和介孔二氧化硅纳米药物处理T24细胞后凋亡相关蛋白的表达水平 |
3 讨论
膀胱癌术后高复发风险是临床面临的巨大挑战。虽然膀胱灌注化学制剂或免疫制剂可以减少复发,然而治疗效果有限,导致其复发率仍然相对较高。频繁的临床干预导致膀胱癌治疗成本昂贵[1, 13]。现如今,许多新型的技术和手段被开发用于优化膀胱癌灌注治疗[14],其中纳米技术的应用备受关注。纳米载药体系在膀胱癌的治疗中具有较大的优势,纳米载体包裹药物从而减少外界酶等物质对药物的降解作用,提高药物活性,并可以减少药物的毒副作用,增强药物治疗效果[15]。
本研究利用MSN包载化疗药物DOX用于膀胱癌的治疗。MSN的生物相容性取决于其粒径、形状、剂量、孔结构、组成以及合成方法[10]。本实验制备的MSN大小约为200 nm,内含孔隙,形状呈均匀的球形。CCK-8分析显示其生物相容性高,在实验浓度范围内不会产生毒副作用,可以作为安全的药物递送载体,与文献[12]报道一致。由于肿瘤组织中糖酵解增强和乳酸生成增加,肿瘤中的pH值通常低于正常组织,因此酸性敏感的药物递送系统在肿瘤治疗中具有一定的优势,可以增加药物在肿瘤中的释放[10]。MSN可以有效地包载化疗药物,形成的纳米药物大小均匀,结构稳定,且在体外表现出酸性环境促进药物释放的行为,这种药物释放行为将有利于杀伤膀胱癌细胞。细胞摄取研究发现,MSN-DOX可以促进药物在细胞内蓄积,且随着药物浓度和作用时间的延长而增加。高效的药物摄取是抗肿瘤效果良好的前提[16],T24细胞对MSN-DOX的有效摄取,提示其抗肿瘤作用的巨大潜力。CCK-8检测结果证明MSN-DOX具有良好的肿瘤抑制效果,明显优于DOX。凋亡分析表明MSN-DOX可以增加Cleaved PARP和Cleaved Caspase-3的表达,提示MSN-DOX可能是通过激活Caspase-3/PARP信号通路抑制膀胱癌细胞的增殖,并促进膀胱癌细胞凋亡。综上所述,本研究制备的介孔二氧化硅纳米药物性能优良,结构稳定,可以有效地被T24细胞摄取,增强肿瘤增殖抑制和凋亡作用。为进一步的体内和临床研究奠定基础,为开发高效安全的膀胱癌灌注治疗提供新的思路。
此外,靶向性纳米药物可以特异性作用于肿瘤细胞,减少对正常细胞的破坏作用,进一步减少副反应的发生并增强药物治疗效果,使得靶向性纳米药物成为研究的热点。目前靶向性纳米药物在膀胱癌的研究中主要包括利用透明质酸(靶向CD44受体)和靶向性多肽修饰纳米药物从而靶向膀胱癌[17-18]。由于介孔二氧化硅纳米粒子易于功能化的特性,可以通过表面修饰的方法赋予其肿瘤靶向性,实现更加精准高效的治疗,相信随着纳米技术的飞速发展,更为智能的纳米药物将会走进临床,改善膀胱癌的治疗。
| [1] |
DY G W, GORE J L, FOROUZANFAR M H, et al. Global burden of urologic cancers, 1990-2013[J]. Eur Urol, 2017, 71(3): 437-446. |
| [2] |
SANLI O, DOBRUCH J, KNOWLES M A, et al. Bladder cancer[J]. Nat Rev Dis Primers, 2017, 3(1): 1-19. |
| [3] |
BABJUK M, BÖHLE A, BURGER M, et al. EAU guidelines on non-muscle-invasive urothelial carcinoma of the bladder: update 2016[J]. Eur Urol, 2017, 71(3): 447-461. |
| [4] |
KAMAT A M, HAHN N M, EFSTATHIOU J A, et al. Bladder cancer[J]. Lancet, 2016, 388(10061): 2796-2810. |
| [5] |
GUO H, LI F, XU W, et al. Mucoadhesive cationic polypeptide nanogel with enhanced penetration for efficient intravesical chemotherapy of bladder cancer[J]. Adv Sci (Weinh), 2018, 5(6): 1800004. |
| [6] |
BABJUK M, BURGER M, COMPÉRAT E M, et al. European association of urology guidelines on non-muscle-invasive bladder cancer (TaT1 and carcinoma in situ)-2019 update[J]. Eur Urol, 2019, 76(5): 639-657. |
| [7] |
KOLAWOLE O M, LAU W M, MOSTAFID H, et al. Advances in intravesical drug delivery systems to treat bladder cancer[J]. Int J Pharm, 2017, 532(1): 105-117. |
| [8] |
TOMLINSON B, LIN T Y, DALL'ERA M, et al. Nanotechnology in bladder cancer: current state of development and clinical practice[J]. Nanomedicine (Lond), 2015, 10(7): 1189-1201. |
| [9] |
GUO H, XU W, CHEN J, et al. Positively charged polypeptide nanogel enhances mucoadhesion and penetrability of 10-hydroxycamptothecin in orthotopic bladder carcinoma[J]. J Control Release, 2017, 259: 136-148. |
| [10] |
BAEZA A, MANZANO M, COLILLA M, et al. Recent advances in mesoporous silica nanoparticles for antitumor therapy: our contribution[J]. Biomater Sci, 2016, 4(5): 803-813. |
| [11] |
BAYIR S, BARRAS A, BOUKHERROUB R, et al. Mesoporous silica nanoparticles in recent photodynamic therapy applications[J]. Photochem Photobiol Sci, 2018, 17(11): 1651-1674. |
| [12] |
DING B, SHAO S, YU C, et al. Large-pore mesoporous-silica-coated upconversion nanoparticles as multifunctional immunoadjuvants with ultrahigh photosensitizer and antigen loading efficiency for improved cancer photodynamic immunotherapy[J]. Adv Mater, 2018, 30(52): e1802479. |
| [13] |
JOICE G A, BIVALACQUA T J, KATES M. Optimizing pharmacokinetics of intravesical chemotherapy for bladder cancer[J]. Nat Rev Urol, 2019, 16(10): 599-612. |
| [14] |
QIU H P, GUO H, LI D, et al. Intravesical hydrogels as drug reservoirs[J]. Trends Biotechnol, 2020, 38(6): 579-583. |
| [15] |
CHEN C H, CHAN T M, WU Y J, et al. Review: application of nanoparticles in urothelial cancer of the urinary bladder[J]. J Med Biol Eng, 2015, 35(4): 419-427. |
| [16] |
ZHOU X, HE X, SHI K, et al. Injectable thermosensitive hydrogel containing erlotinib-loaded hollow mesoporous silica nanoparticles as a localized drug delivery system for NSCLC therapy[J]. Adv Sci (Weinh), 2020, 7(23): 2001442. |
| [17] |
LIN T, YUAN A, ZHAO X, et al. Self-assembled tumor-targeting hyaluronic acid nanoparticles for photothermal ablation in orthotopic bladder cancer[J]. Acta Biomater, 2017, 53: 427-438. |
| [18] |
SWEENEY S K, LUO Y, O'DONNELL M A, et al. Peptide-mediated targeting mesoporous silica nanoparticles: a novel tool for fighting bladder cancer[J]. J Biomed Nanotechnol, 2017, 13(2): 232-242. |





