经皮内镜腰椎间盘突出症髓核摘除术(percutaneous endoscopic lumbar discectomy, PELD)主要包括由YEUNG提出的YESS技术和HOOGLAND提出的TESSYS技术[1-2],此类手术是经椎间孔入路进行突出髓核摘除,与传统的开放手术相比,具有手术创伤小、出血量少及术后恢复快等优点[3-4]。随着PELD技术的不断改进和发展,该技术逐渐得到了越来越多的外科医师和患者的认可。目前,文献中有关PELD治疗腰椎间盘突出症的效果研究多为近期小样本量随访。其结果显示PELD术后患者疼痛于术后立刻缓解,生活质量得到明显改善,近期手术疗效满意[5-6]。而PELD治疗腰椎间盘突出症的长期疗效如何,文献少有报道。
本研究对2012年1月至2015年12月1 807例单节段腰椎间盘突出症行PELD手术患者进行至少5年的随访,以评价PELD术治疗腰椎间盘突出症的长期疗效,指导临床应用。
1 资料与方法 1.1 一般资料回顾性收集我科2012年1月至2015年12月行PELD手术患者的病例资料。纳入标准:①经影像学确诊为腰椎椎间盘突出症;②责任间隙为单节段突出;③术前、术后病例及影像学资料完整者。排除标准:①曾行开放性或微创腰椎手术;②伴有腰椎不稳,腰椎滑脱;③伴有腰椎退变性或先天性侧弯;④伴有腰椎骨折、结核、肿瘤。本研究严格遵照世界医学协会《赫尔辛基宣言》(2000年)实施研究,并获陆军军医大学伦理委员会批准(2019-研第013-01)。
1.2 数据采集及随访收集患者人口学数据,包括年龄、性别、体质指数(BMI)、突出节段、术前腰椎疾病的功能评分(the Oswestry disability index,ODI)、腰腿部疼痛视觉模拟评分(visual analogue scale,VAS)评分以及5年随访以上的随访资料(采用电话询问、邮件咨询、门诊随访等方式进行)。随访时间为术前,术后3个月、6个月、1年及末次随访。末次随访终点事件定义为患者出现术后并发症或者复发,即若患者随访未满5年出现术后并发症,则提前结束随访。
1.3 手术操作患者俯卧于体位架上,在C臂透视下定位,确认责任节段后,平行于椎间盘于体表划水平线,与水平线15°左右夹角作为穿刺线。常规消毒铺巾,在脊柱旁开10~15 cm处局部1%利多卡因麻醉。穿刺针穿刺,C臂透视下确认穿刺针位置后插入导丝,取出穿刺针后逐层插入扩张套筒行软组织扩张。C臂透视套筒定位于下位椎体上关节突后,放入环锯,磨除部分上关节突腹侧,置入7.3 mm工作通道,再次确认通道位置后,连接内镜成像系统。髓核钳摘除髓核组织,后用射频电极进行纤维环成形并止血。确认患者下肢症状缓解后,撤出内镜系统,拔出通道后缝合切口。
患者术后3 h佩戴硬腰围可下地活动,术后3周内戴硬腰带,1周后可行腰背肌锻炼。术后3个月、6个月、1年常规门诊随访。术后5年电话及邮件随访仍有疼痛患者,要求门诊复诊。
1.4 疗效评价采用ODI评分、腰痛及腿痛VAS评分评估手术疗效。记录术中及术后并发症、发生时间及治疗方式。记录患者术后复发的时间及治疗方式。术后复发定义为术后症状缓解达6个月以上,同一节段再次出现突出并引起相应症状,且经影像学证实。
1.5 统计学分析使用SPSS 23.0统计数据;计数资料以频数、百分比形式表示;计量资料以数据范围或x ±s形式表示;采用χ2检验分析复发患者年龄与腰椎间盘突出症的责任节段分组间的差异。
2 结果 2.1 纳入病例基线资料共1 807例纳入本研究,随访时间(6.36±1.08)年,随访率为94.08%。术前基线资料见表 1。
| 项目 | 数据 |
| 随访患者 | 1 706 |
| 失访人数 | 101 |
| 随访时间/月 | 47.0±15.4(13~88) |
| 男/女(例) | 1 006/700 |
| BMI/kg·cm2 | 23.9±3.2(15.5~38.7) |
| 术前ODI(%) | 58.5±13.2(18~98) |
| 术前腰背部VAS/分 | 5.5±1.3(1~9) |
| 术前腿部VAS/分 | 4.8±1.8(0~9) |
| 突出节段 | |
| 2/3 | 9(0.5) |
| 3/4 | 70(4.1) |
| 4/5 | 1 027(60.2) |
| 5/1 | 600(35.2) |
2.2 疗效评价 2.2.1 ODI及VAS评分改变
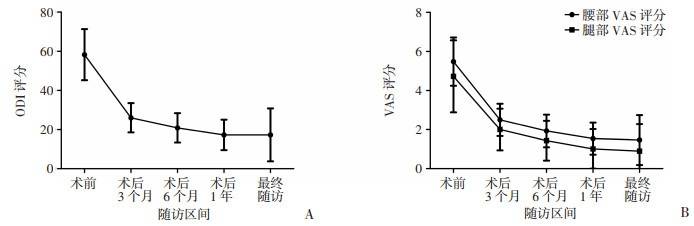
患者术后疗效评价采用ODI及VAS评分,患者术后ODI改变见图 1A,腰腿部VAS评分见图 1B。术后1年ODI评分较术后3、6个月明显下降。腰部术后1年VAS评分较术后3、6个月明显下降。腿部VAS评分,各时间点较术前均有下降。
|
| A:ODI评分随随访时间推移改变趋势;B:腰、腿部VAS评分随随访时间推移改变趋势 图 1 各随访区间ODI评分及腰腿部VAS评分改变 |
2.2.2 手术并发症
本组术后发生腰椎间隙感染2例,采取清创引流方式治疗;腰椎间盘囊肿2例、邻椎节段突出2例,均采取保守治疗。共计并发症发生9例,发生率为0.53%。
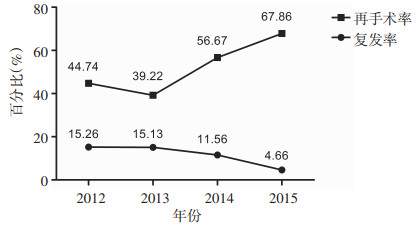
2.2.3 术后复发总体复发率为10.38%,总体再手术率5.98%,复发患者再手术率50.85%。复发率与再手术率与年份关系见图 2。复发患者中最短复发时间为术后6个月,最长复发时间为术后72个月,平均(27.42±18.66)个月。术后1年及2年为复发高峰时间(60、31例),见图 3。复发患者5例行微创内镜椎间盘切除(microendoscopic discectomy,MED)术,24例行经椎间孔椎体植骨融合(transforaminal lumbar interbody fusion,TLIF) 术,42例行PELD术,1例行开放减压术,18例行神经根封闭术,87例患者选择保守治疗。
|
| 图 2 经皮椎间孔镜术后复发率与再手术率随年份的变化 |

|
| 图 3 经皮椎间孔术后复发时间统计 |
将复发患者以10岁为年龄段分段,显示患者>60岁后复发率及再手术率明显上升,以81~ < 90岁患者复发率及再手术率最高(表 2)。将患者以腰椎间盘突出症的责任节段进行比较,腰3/4节段椎间盘突出复发率略高于其他突出节段患者,但各突出节段间复发率无统计学差异,见图 4。
| 年龄分段/岁 | n | 复发率 | 再手术率 |
| 10~ < 20 | 57 | 4(7.02) | 2(3.51) |
| 20~ < 30 | 208 | 15(7.21) | 3(1.44) |
| 30~ < 40 | 310 | 33(10.65) | 19(6.13) |
| 40~ < 50 | 497 | 53(10.66) | 26(5.23) |
| 50~ < 60 | 274 | 28(10.22) | 12(4.38) |
| 60~ < 70 | 216 | 24(11.11) | 16(7.41) |
| 70~ < 80 | 115 | 15(13.04) | 9(7.83) |
| 80~ < 90 | 29 | 5(17.24) | 3(10.34) |

|
| 图 4 经皮椎间孔镜手术节段与复发率的关系 |
2.2.4 术后未缓解患者
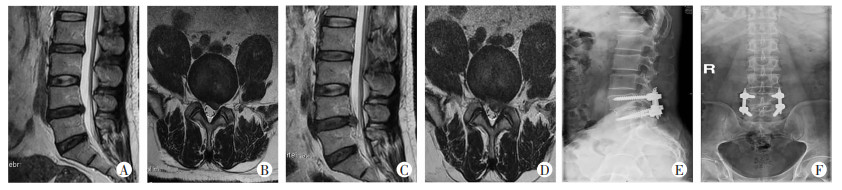
术后共计11例患者症状未缓解,其中1例行MED术,5例行TLIF术,5例行保守治疗,见图 5。
|
| A、B:患者术前腰椎间盘磁共振提示腰4/5节段椎间盘突出;C、D:患者行PELD术后腰椎间盘磁共振提示腰4/5突出仍存在,症状未缓解;E、F:患者术后保守治疗无效,术后1个月即行腰4/5椎间融合术 图 5 腰椎间盘突出症患者行PELD术术前及术后影像学资料 |
3 讨论
椎间孔镜技术最早是1997年由YEUNG提出的YESS技术[1]。2002年,HOOGLAND教授等[2]报道了在YESS技术基础上的发展,创新地提出了经进入椎管内直接行神经根松解和减压的THESSYS技术,得到脊柱微创领域学者的广泛认可。THESSYS技术的核心在于工作通道置于椎间盘后的椎管内,内镜下为椎管内容物,可进行神经根完整的显露及减压。为将工作通道完全置入椎管内,需要进行关节突成形。HOOGLAND教授最初设计多种不同型号的环锯进行扩孔,以磨除上关节突腹侧部分。后又改进为不同型号的骨钻,由于其钝头对椎管内容基本无损伤,因此更为安全。微创手术发展至今,经皮内镜髓核摘除术已经成熟,微创的方式加快了术后康复,同时椎旁肌的剥离减少有效避免了术后顽固性的腰痛[7-8]。然而微创手术长期随访结果报道较少,其远期疗效、手术并发症率、术后复发情况需要进一步随访报道。故本课题组针对2012-2015年共计1 807名患者进行了5年随访,进一步探究椎间孔技术治疗腰椎间盘突出症的疗效。
3.1 经皮内镜治疗腰椎间盘突出症疗效分析随访过程中,ODI及VAS呈下降趋势,多数患者于5年随访时均取得满意疗效。经皮内镜治疗腰椎间盘突出症展现出良好的有效性。内镜下,视野暴露好,充分的视野暴露外加光源的辅助及水的冲洗使之能够对神经根,包括神经根内外侧、腹侧及侧隐窝进行充分减压。同时能解除突出髓核对窦锥神经压迫,术后腰背部疼痛明显缓解。同时该术式拥有对椎旁肌肉剥离少、周围结构破坏少的特点,使患者术后恢复更快,能够更早下地行走并进行功能锻炼[9-10]。在EUN等[11]的一篇10年以上随访文献中提及,对经皮椎间孔镜术后患者进行(11.22±0.83)年的随访,结果显示:患者腰背部疼痛VAS评分于末次随访明显较术前下降,生活质量ODI评分于末次随访明显低于术前评分。平均椎间隙高度为术前椎间隙高度的81.54%,且未见腰椎不稳患者出现。
患者于最终随访时(5年),腿部VAS评分仍持续下降,而VAS腰部评分于术后1年与最终随访(5年)无明显差异。与腰部疼痛及整体生活质量不同,患者术后下肢疼痛及麻木的好转是一个长期康复过程,于术后1年时疼痛评分仍未到达平台期,康复时间需大于1年,这与目前的随访结果不相同。AHN等[12]曾报道单纯椎间盘摘除术后10年随访结果,显示术后6个月时腿部VAS评分趋于稳定,在后续随访中无下降趋势,于术后6个月、1年、2年、3年及4年至最终随访无明显差异。
3.2 经皮内镜术后并发症情况在整体随访过程中,我们发现少数患者术后出现并发症,包括椎间盘囊肿、椎间隙感染等,总体并发症率为0.53%。在2020年报道的Meta分析里,PELD术后总体并发症率为5.8%,较本团队统计复发率高[13]。并发症与手术技术及术者经验密切相关,该病例队列已排除学习曲线问题,故并发症率相对下降。熟练的手术操作及丰富的经验可在一定程度上避免上述并发症的发生。经皮内镜术对于手术医师微创解剖学要求较高,对于器械及内镜技术的掌握需要一定经验的积累。AHN等[14]通过学习曲线研究,表明椎间孔镜手术医师需积累35例手术病例才可以达到稳定的手术疗效阶段。术者的技术决定了术中减压是否彻底,减压不彻底可能导致术后症状未明显改善或短期内再突出。一个完善的培训课程,如手术视频讲解、模型或尸体的模拟操作,可有效缩短学习曲线。
椎间盘囊肿为极少见术后并发症,多数报道为对椎间盘囊肿的个案分析,并未统计具体并发症率[15-16]。本课题组经大样本统计分析得出,术后椎间盘囊肿并发症率为0.12%。椎间盘囊肿往往引起患者腰背部疼痛以及下肢放射性疼痛,甚至出现感觉及运动障碍[16]。对于椎间盘囊肿的发生机制目前存在争议,曾有报道猜测椎间盘囊肿的出现可能与硬膜外血肿形成及血肿吸收障碍相关[15, 17]。根据本团队操作经验猜测,可能为术中纤维环存在破口,手术中取出髓核组织后,未对破损的纤维环进行电凝重建,故破损游离的纤维环进一步退变导致术后囊肿形成。腰椎术后椎间隙感染率为0.1%~0.4%[18],这与我们的随访结果(0.18%)相符。术后椎间隙感染首先应考虑是否存在手术无菌操作不当。其次,患者的个体因素亦可能导致术后感染率升高,如合并糖尿病或存在其他器官或组织感染。故术前对于患者血糖的控制尤其重要。对于术前静脉血中白细胞或中性粒细胞升高的患者应谨慎考虑手术治疗,需待血象正常后再实施手术。随访中,有11名患者术后症状没有明显缓解,术后1周内复查MRI提示神经根及硬膜囊依旧存在压迫,考虑为术中减压不彻底所致。
腰椎间盘突出症术后复发一直是该术式存在的问题。在我们的调查中,患者总体复发率为10.38%,较文献报道复发率高(5.8%)[13]。然而,对于腰椎间盘突出症术后随访,目前文献大多为1~3年随访结果,长期随访结果少见,可能存在远期随访复发患者漏筛情况。其次患者总体再手术率为5.98%(复发患者再手术率为50.85%),远小于腰椎间盘突出症复发率。目前大多文献报道腰椎间盘突出症复发率与再手术率相同,可能误将再手术率确认为复发率,复发患者中保守治疗的患者可能存在漏筛选情况,需要进一步考证[19-20]。同时椎间孔镜复发率与开放手术复发率无统计学差异,证明腰椎间盘突出症术后复发与患者自身因素等也相关[3-4]。如年龄、性别、吸烟、糖尿病、高血压、外伤、术后不恰当的功能锻炼等均相关。同时也与影像学因素相关,如椎间隙高度、腰椎动力位sROM值、突出的类型等[20]。其中年龄与复发的关系争议较大,KIM等[21]曾通过全国人口数据库调查了15 817名患者,显示行微创下单纯椎间盘摘除术患者年龄大于57岁时再手术率有所升高。也有部分文献报道年龄并不存在与复发的相关性[8, 22]。本研究显示年龄在60岁以上复发率明显呈上升趋势,对于老年患者来讲,髓核退变更加严重,退变脱水的髓核呈小块状零散分布,同时术中纤维环破口较青年人恢复愈合缓慢,零散的髓核组织更易自破口再次突出。然而由于老年患者多伴有多系统疾病,选择椎间融合术等全麻手术风险相对较高。局麻下椎间孔镜手术术后恢复快,下床时间早,故仍可作为老年患者手术选择方式之一。
有关复发后治疗方式的选择,曾有Meta分析纳入970名患者,综合分析得出,复发患者保守治疗与手术治疗相比,短期及中期疗效手术治疗较保守治疗效果好,手术治疗患者ODI及腰腿部VAS评分明显低于保守治疗患者。然而在长期随访中,并无确凿证据显示手术治疗优于保守治疗[23]。在本研究中,49.15%的复发患者选择保守治疗,对于腰椎间盘突出症复发治疗方式的选择,不应盲目选择再次行椎管减压或椎间融合,保守治疗仍可有满意疗效,对于保守治疗无效的患者,再可考虑采取手术治疗的方式。
3.3 本研究的局限性本研究基于大样本的长期随访,对于经皮内镜术后疗效进行了评估。但本研究为回顾性、单中心研究。有待进一步进行多中心前瞻性研究。
综上所述,经皮椎间孔镜下椎间盘髓核切除术对于治疗腰椎间盘突出症有良好的有效性及安全性,术后腰背部疼痛及下肢放射痛得到有效缓解,长期随访显示并发症发生率低。该术式可作为治疗腰椎间盘突出症的可选术式之一。
| [1] |
DEEN H G. Posterolateral endoscopic excision for lumbar disc herniation: surgical technique, outcome, and complications in 307 consecutive cases[J]. Spine (Phila Pa 1976), 2002, 27(18): 2081-2082;authorreply2081-2. |
| [2] |
HOOGLAND T, SCHUBERT M, MIKLITZ B, et al. Transforaminal posterolateral endoscopic discectomy with or without the combination of a low-dose chymopapain: a prospective randomized study in 280 consecutive cases[J]. Spine (Phila Pa 1976), 2006, 31(24): E890-E897. |
| [3] |
KIM M, LEE S, KIM H S, et al. A comparison of percutaneous endoscopic lumbar discectomy and open lumbar microdiscectomy for lumbar disc herniation in the Korean: a meta-analysis[J]. Biomed Res Int, 2018, 2018: 9073460. |
| [4] |
RUAN W F, FENG F, LIU Z Y, et al. Comparison of percutaneous endoscopic lumbar discectomy versus open lumbar microdiscectomy for lumbar disc herniation: a meta-analysis[J]. Int J Surg, 2016, 31: 86-92. |
| [5] |
KIM H S, PAUDEL B, JANG J S, et al. Percutaneous endoscopic lumbar discectomy for all types of lumbar disc herniations (LDH) including severely difficult and extremely difficult LDH cases[J]. Pain Physician, 2018, 21(4): E401-E408. |
| [6] |
CHOI K C, KIM J S, RYU K S, et al. Percutaneous endoscopic lumbar discectomy for L5-S1 disc herniation: transforaminal versus interlaminar approach[J]. Pain Physician, 2013, 16(6): 547-556. |
| [7] |
RUETTEN S, KOMP M, MERK H, et al. Full-endoscopic interlaminar and transforaminal lumbar discectomy versus conventional microsurgical technique: a prospective, randomized, controlled study[J]. Spine (Phila Pa 1976), 2008, 33(9): 931-939. |
| [8] |
YAO Y, LIU H, ZHANG H Y, et al. Risk factors for recurrent herniation after percutaneous endoscopic lumbar discectomy[J]. World Neurosurg, 2017, 100: 1-6. |
| [9] |
MAYER H M, BROCK M. Percutaneous endoscopic lumbar discectomy (PELD)[J]. Neurosurg Rev, 1993, 16(2): 115-120. |
| [10] |
TENENBAUM S, ARZI H, HERMAN A, et al. Percutaneous posterolateral transforaminal endoscopic discectomy: clinical outcome, complications, and learning curve evaluation[J]. Surg Technol Int, 2011, 21: 278-283. |
| [11] |
EUN S S, LEE S H, SABAL L A. Long-term follow-up results of percutaneous endoscopic lumbar discectomy[J]. Pain Physician, 2016, 19(8): E1161-E1166. |
| [12] |
AHN Y, LEE U, KIM W K, et al. Five-year outcomes and predictive factors of transforaminal full-endoscopic lumbar discectomy[J]. Medicine (Baltimore), 2018, 97(48): e13454. |
| [13] |
CHEN X L, CHAMOLI U, VARGAS CASTILLO J, et al. Complication rates of different discectomy techniques for symptomatic lumbar disc herniation: a systematic review and meta-analysis[J]. Eur Spine J, 2020, 29(7): 1752-1770. |
| [14] |
AHN S S, KIM S H, KIM D W. Learning curve of percutaneous endoscopic lumbar discectomy based on the period (early vs. late) and technique (in-and-out vs. in-and-out-and-in): a retrospective comparative study[J]. J Korean Neurosurg Soc, 2015, 58(6): 539-546. |
| [15] |
HA S W, JU C I, KIM S W, et al. Clinical outcomes of percutaneous endoscopic surgery for lumbar discal cyst[J]. J Korean Neurosurg Soc, 2012, 51(4): 208-214. |
| [16] |
AYDIN S, ABUZAYED B, YILDIRIM H, et al. Discal cysts of the lumbar spine: report of five cases and review of the literature[J]. Eur Spine J, 2010, 19(10): 1621-1626. |
| [17] |
KIM J S, CHOI G, LEE C D, et al. Removal of discal cyst using percutaneous working channel endoscope via transforaminal route[J]. Eur Spine J, 2009, 18(Suppl 2): 201-205. |
| [18] |
CARRAGEE E J, SPINNICKIE A O, ALAMIN T F, et al. A prospective controlled study of limited versus subtotal posterior discectomy: short-term outcomes in patients with herniated lumbar intervertebral discs and large posterior anular defect[J]. Spine (Phila Pa 1976), 2006, 31(6): 653-657. |
| [19] |
AHN Y, LEE S H. Outcome predictors of percutaneous endoscopic lumbar discectomy and thermal annuloplasty for discogenic low back pain[J]. Acta Neurochir (Wien), 2010, 152(10): 1695-1702. |
| [20] |
HUANG W, HAN Z, LIU J, et al. Risk factors for recurrent lumbar disc herniation: a systematic review and meta-analysis[J]. Medicine (Baltimore), 2016, 95(2): e2378. |
| [21] |
KIM C H, CHUNG C K, CHOI Y, et al. The selection of open or percutaneous endoscopic lumbar discectomy according to an age cut-off point: nationwide cohort study[J]. Spine (Phila Pa 1976), 2015, 40(19): E1063-E1070. |
| [22] |
SHIMIA M, BABAEI-GHAZANI A, SADAT B E, et al. Risk factors of recurrent lumbar disk herniation[J]. Asian J Neurosurg, 2013, 8(2): 93-96. |
| [23] |
CHEN B L, GUO J B, ZHANG H W, et al. Surgical versus non-operative treatment for lumbar disc herniation: a systematic review and meta-analysis[J]. Clin Rehabil, 2018, 32(2): 146-160. |




