2. 430000 武汉,泰康同济医院;
3. 430000 武汉,金银潭医院;
4. 430000 武汉,火神山医院
2. Taikang Tongji Hospital, Wuhan, Hubei Province, 430000;
3. Jinyintan Hospital, Wuhan, Hubei Province, 430000;
4. Wuhan Huoshenshan Hospital, Wuhan, Hubei Province, 430000, China
新型冠状病毒肺炎(coronavirus disease-2019,COVID-19)是由“SARS-CoV-2”(severe acute respiratory syndrome coronavirus 2)引起的一种新发的急性呼吸道传染性疾病,截至目前,全球感染者已超过1.7亿,多个国家仍处于紧急状态。COVID-19的主要特点是传播速度快、人群普遍易感性。COVID-19患者以发热、干咳、乏力为主要表现,重症患者多在发病1周后出现呼吸困难和/或低氧血症,严重者可快速进展为急性呼吸窘迫综合征、脓毒症休克、难以纠正的代谢性酸中毒和出凝血功能障碍及多器官功能衰竭等[1-2]。多项研究提示血管紧张素转化酶2(angiotensin- converting enzyme 2,ACE2)是SARS-CoV-2的功能受体[3-4],在COVID-19患者发病过程中起着至关重要的作用,因为它提供了SARS-COV-2攻击人类细胞的途径。ACE2除了在肺泡上皮细胞高度表达外,在肝肾等其他器官组织中也有表达,因此肝肾等也是SARS-CoV-2攻击的主要靶器官。有部分研究数据提示:14%~53% COVID-19患者合并肝功能损伤[5-8],表现为丙氨酸氨基转氨酶(ALT)和天门冬氨酸氨基转氨酶(AST)水平的升高;0.5%~29% COVID-19患者合并肾功能损伤[9-12],表现为血清肌酐(Cr)的升高。文献报道肝肾功能损伤的比例差异较大,推测与各项研究对象来源、特征和是否合并基础病等因素有关,且尚未见COVID-19患者中肝肾功能损伤发生的流行病学特征、肝肾功能损伤的临床特征及其与疾病重症化和死亡风险相关性的研究报道。因此, 本研究纳入湖北省武汉市3所收治COVID-19患者的医院,并且排除合并肝肾基础疾病的COVID-19患者,共3 548例COVID-19患者参与研究。本研究全面分析了COVID-19患者中肝肾功能主要指标(ALT、AST、Cr)的分布特征及其与COVID-19患者发生重症化与死亡风险的相关性,以期提高强化临床医师对该类患者的认识和重视,为该类患者的早期防治和预后判断提供科学依据。
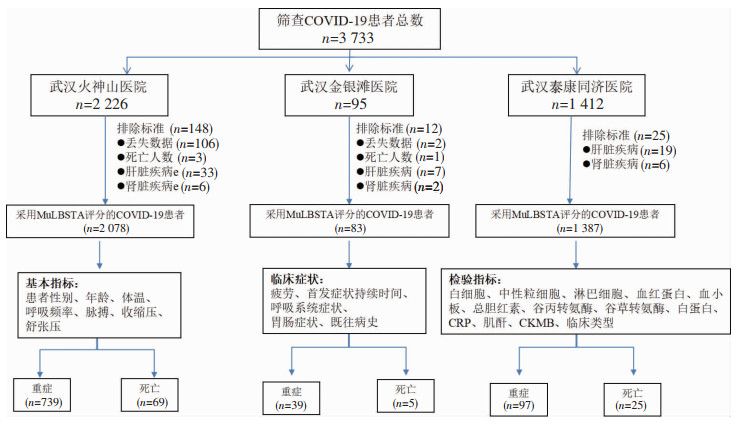
1 资料与方法 1.1 研究对象本研究经过陆军军医大学第二附属医院伦理委员会批准(2020-研第073-01)。收集2020年2月4日至2020年4月16日在湖北省武汉市的火神山医院、金银潭医院、泰康同济医院确诊并且接受治疗的3 733例COVID-19患者为研究对象。按照世界卫生组织(WHO)临时指南和中国国家卫生与健康委员会发布的指南,通过接触史、临床表现、胸部计算机化X线体层照相术(CT)及咽拭子逆转录-聚合酶链式反应(RT-PCR)检测,明确诊断为COVID-19。排除标准:(1)合并肝脏(病毒性肝炎、肝囊肿、肝硬化、肝癌等)和肾脏(急/慢性肾炎、肾功能衰竭、肾占位病变、肾结石、肾囊肿和糖尿病肾病等)相关基础病患者;(2)入院48 h死亡及相关实验室检查指标缺失者。最终3 548例COVID-19患者纳入分析,见图 1。
|
| 图 1 纳入排除流程图 |
1.2 指标及其采集方法
经过批准,由专人通过电子病历进行信息提取并填写自行设计的病例信息提取表,主要提取信息包括:(1)患者一般人口学特征,姓名、住院号(ID)、年龄、性别等;(2)基础病史,慢性阻塞性肺疾病、2型糖尿病(T2DM)、高血压、冠心病、脑血管疾病、慢性肝病、慢性肾病等;(3)临床症状,发热、咳嗽、咯血、疲劳、胸闷、呼吸困难、呕吐、腹痛、腹泻、食欲减退等;(4)实验室检查,白细胞(WBC)、血小板(PLT)、血红蛋白(HGB)、肝功、肾功、凝血功能、C反应蛋白(C-reactive protein,CRP)、降钙素原、肌酸肌酶同工酶(creatine kinase-MB,CKMB)、白细胞介素-6(IL-6)、免疫球蛋白M(IgM)、免疫球蛋白G(IgG)等;(5)诊断分型和住院期间是否死亡。
1.3 指标异常标准临床实验室指标是否异常,按照病例来源医院(火神山医院、金银潭医院、泰康同济医院)执行标准进行判断,以血清中ALT > 50 U/L、AST > 60 U/L和Cr > 111 μmol/L判断为升高。将AST和Cr指标均正常的患者定义为肝肾功能正常者,AST和Cr指标中任一升高的患者定义为肝或肾功能损伤者,而AST和Cr指标均升高者定义为肝肾功能同时损伤者。
1.4 统计学分析采用SPSS 23.0统计软件进行分析。连续变量以中位数(四分位数范围)或x±s表示,分类变量以n(%) 表示。呈正态分布的连续变量,组间比较采用t检验,非正态分布则采用Mann-Whitney U检验;分类变量的组间比较采用χ2检验,若n<5,则采用Fisher精确检验。采用Logistic回归筛选并逐步校正相关因素,以比值比(OR)及95%可信区间(CI)表示其发生重症及死亡的风险。P < 0.05被认为差异具有统计学意义。
2 结果 2.1 COVID-19患者的基本特征2020年2月4日至2020年4月16日,在火神山医院、金银潭医院、泰康同济医院确诊且接受治疗共3 733例COVID-19患者,其中符合纳入排除标准的有3 548例,男性和女性分别为1 724例(48.59%)、1 824例(51.41%);年龄(59.34±14.76)岁,中位年龄61.0岁,最小4岁,最大99岁;>60岁以上患者1 864例(52.54%);ALT、AST、Cr升高的比例分别为14.6%(513/3 548)、3.4%(119/3 548)、2.8%(101/3 548);AST和Cr指标中任一升高(肝或肾功能损伤)的患者比例为5.7%(202/3 548);AST和Cr均升高(肝功和肾功均损伤)患者的比例为0.25%(9/3 548)。
2.2 COVID-19患者中ALT、AST、Cr检测值分布特征3 548例COVID-19患者中,ALT、AST、Cr检测值均呈非正态分布(P < 0.01),具体分布情况见表 1。
| 指标 | x±s | 最小值 | 百分位数(%) | 最大值 | ||||||||||||
| 5 | 10 | 20 | 25 | 30 | 40 | 50 | 60 | 70 | 75 | 80 | 90 | 95 | ||||
| ALT/U·L-1 | 35.05±96.24 | 0.6 | 8.80 | 10.80 | 13.60 | 15.00 | 16.60 | 20.00 | 24.20 | 28.90 | 35.70 | 36.30 | 41.40 | 61.71 | 86.76 | 5 150.8 |
| AST/U·L-1 | 28.67±39.67 | 3.4 | 12.60 | 13.90 | 16.02 | 17.00 | 17.80 | 19.84 | 22.50 | 26.00 | 33.40 | 37.35 | 37.35 | 38.01 | 51.08 | 1 731.0 |
| Cr/μmol·L-1 | 68.20±45.25 | 1.5 | 39.43 | 44.09 | 49.80 | 52.00 | 54.20 | 57.83 | 62.40 | 67.10 | 72.50 | 75.74 | 79.40 | 94.01 | 97.87 | 945.6 |
2.3 ALT、AST、Cr升高与COVID-19患者重症及死亡发生的风险关系
与ALT正常的COVID-19患者相比,ALT升高的患者发生重症和死亡的风险均未显著增加;与AST正常的COVID-19患者相比,AST升高的患者发生重症[OR(95%CI):2.88(1.57-3.32)]和死亡[OR(95%CI): 4.76(2.52-8.99)]的风险均显著升高;与Cr正常的COVID-19患者相比,Cr升高的患者发生重症[OR(95%CI):2.87(1.93-4.27)]和死亡[OR(95%CI):5.75 (3.02-1 093)]的风险也均显著升高。
肝或肾功能损伤者和肝肾功能均损伤者发生重症的风险分别是肝肾功能正常者的2.32倍(95%CI:1.73-3.10)和11.40倍(95%CI:2.36-54.98),发生死亡的风险分别是肝肾功能正常者的5.21倍(95%CI:3.10-8.75)和13.53倍(95%CI:2.76-66.32),见表 2。
| 指标 | 分类 | n | 死亡 | 重症 | |||||||||
| 否 | 是 | χ2 | P值 | OR(95%CI) | 普通 | 重症 | χ2 | P值 | OR(95%CI) | ||||
| ALT/U·L-1 | ≤50 | 3 035 | 2 960 | 75 | 0.737 | 0.391 | 1 | 2 288 | 747 | 0.027 | 0.869 | 1 | |
| >50 | 513 | 497 | 16 | 1.27(0.73-2.20) | 385 | 128 | 1.02(0.82-1.26) | ||||||
| AST/U·L-1 | ≤60 | 3 429 | 3 350 | 79 | 27.857 | < 0.001 | 1 | 2 604 | 825 | 19.961 | < 0.001 | 1 | |
| >60 | 119 | 107 | 12 | 4.76(2.52-8.99) | 69 | 50 | 2.88(1.57-3.32) | ||||||
| Cr/μmol·L-1 | ≤111 | 3 447 | 3 368 | 79 | 36.106 | < 0.001 | 1 | 2 620 | 827 | 29.248 | < 0.001 | 1 | |
| >111 | 101 | 89 | 12 | 5.75(3.02-1093) | 53 | 48 | 2.87(1.93-4.27) | ||||||
| 肝肾功能正常 | 3 337 | 3 268 | 69 | 60.719 | < 0.001 | 1 | 2 553 | 784 | 47.249 | < 0.001 | 1 | ||
| 肝或肾功能损伤 | 202 | 182 | 20 | 5.21(3.10-8.75) | 118 | 84 | 2.32(1.73-3.10) | ||||||
| 肝肾功能均损伤 | 9 | 7 | 2 | 13.53(2.76-66.32) | 2 | 7 | 11.40(2.36-54.98) | ||||||
| 肝肾功能正常:AST和Cr指标均正常者;肝或肾功能损伤:AST和Cr指标中任一升高者;肝肾功能均损伤:AST和Cr指标均升高者 | |||||||||||||
2.4 不同特征COVID-19患者中肝肾功能损伤的发生情况
根据AST和Cr是否升高将COVID-19患者分为肝肾功能正常、肝或肾功能损伤和肝肾功能均损伤3组,不同特征人群中肝肾功能损伤发生情况存在一定的差异,其中男性、年龄>60岁、合并高血压、合并肺部疾病、CRP升高和CKMB升高等特征患者中的肝肾功能发生损伤的比例显著高于肝肾功能正常的患者(P < 0.05),见表 3。
| 指标 | 合计(n=3548) | 正常(n=3337) | 肝肾任一损伤(n=202) | 肝和肾均损伤(n=9) | χ2 | P值 | |
| 性别 | 女 | 1 824(51.41) | 1 749(95.89) | 72(3.95) | 3(0.16) | 22.621 | 0.000 |
| 男 | 1 724(48.59) | 1 588(92.11) | 130(7.54) | 6(0.35) | |||
| 年龄/岁 | ≤60 | 1 684(47.46) | 1 597(94.83) | 86(5.11) | 1(0.06) | 6.914 | 0.032 |
| >60 | 1 864(52.54) | 1 740(93.35) | 116(6.22) | 8(0.43) | |||
| 乏力 | 无 | 1 789(50.42) | 1 677(93.74) | 105(5.87) | 7(0.39) | 2.928 | 0.231 |
| 有 | 1 759(49.58) | 1 660(94.37) | 97(5.51) | 2(0.11) | |||
| 体温/℃ | ≤37 | 1 276(35.96) | 1 202(94.20) | 71(5.56) | 3(0.24) | 0.090 | 0.956 |
| >37 | 2 272(64.04) | 2 135(93.97) | 131(5.77) | 6(0.26) | |||
| 高血压/mmHg | 无 | 2 637(74.32) | 2 502(94.88) | 128(4.85) | 7(0.27) | 13.531 | 0.001 |
| 有 | 911(25.68) | 835(91.66) | 74(8.12) | 2(0.22) | |||
| 糖尿病 | 无 | 3 225(90.89) | 3 041(94.29) | 175(5.43) | 9(0.28) | 5.557 | 0.062 |
| 有 | 323(9.10) | 296(91.64) | 27(8.36) | 0(0) | |||
| 冠心病 | 无 | 3 417(96.31) | 3 218(94.18) | 190(5.56) | 9(0.26) | 3.366 | 0.186 |
| 有 | 131(3.69) | 119(90.84) | 12(9.16) | 0(0) | |||
| 肺部疾病 | 无 | 3 390(95.55) | 3 195(94.25) | 188(5.55) | 7(0.21) | 9.900 | 0.007 |
| 有 | 158(4.45) | 142(89.87) | 14(8.86) | 2(1.27) | |||
| 咳嗽 | 无 | 1 242(35.01) | 1 155(92.99) | 82(6.60) | 5(0.40) | 4.671 | 0.097 |
| 有 | 2 306(64.99) | 2 182(94.62) | 120(5.20) | 4(0.17) | |||
| 咳痰 | 无 | 3 106(87.54) | 2 921(94.04) | 177(5.70) | 8(0.26) | 0.016 | 0.992 |
| 有 | 442(12.46) | 416(94.12) | 25(5.66) | 1(0.23) | |||
| 呼吸困难 | 无 | 2 710(76.38) | 2 568(94.76) | 138(5.09) | 4(0.15) | 12.980 | 0.002 |
| 有 | 838(23.62) | 769(91.77) | 64(7.64) | 5(0.60) | |||
| 胸闷 | 无 | 2 829(79.74) | 2 664(94.17) | 159(5.62) | 6(0.21) | 1.101 | 0.557 |
| 有 | 719(20.26) | 673(93.60) | 43(5.98) | 3(0.42) | |||
| 咯血 | 无 | 3 539(99.75) | 3 328(94.04) | 202(5.71) | 9(0.25) | 0.571 | 0.752 |
| 有 | 9(0.25) | 9(100.00) | 0(0) | 0(0) | |||
| 呕吐 | 无 | 3 469(97.77) | 3 262(94.03) | 198(5.71) | 9(0.26) | 0.268 | 0.875 |
| 有 | 79(2.23) | 75(94.94) | 4(5.06) | 0(0) | |||
| 腹痛 | 无 | 3 511(98.96) | 3 302(94.05) | 200(5.70) | 9(0.26) | 0.101 | 0.951 |
| 有 | 37(1.04) | 35(94.59) | 2(5.41) | 0(0) | |||
| 腹泻 | 无 | 3 359(94.67) | 3 159(94.05) | 191(5.69) | 9(0.27) | 0.512 | 0.774 |
| 有 | 189(5.33) | 178(94.18) | 11(5.82) | 0(0) | |||
| 食欲减退 | 无 | 2 601(73.31) | 2 447(94.08) | 149(5.73) | 5(0.19) | 1.472 | 0.479 |
| 有 | 947(26.69) | 890(93.98) | 53(5.60) | 4(0.42) | |||
| WBC/109·L-1 | 3.6~9.5 | 3 159(89.04) | 2 983(94.43) | 174(5.51) | 2(0.06) | 83.446 | < 0.001 |
| < 3.6 | 162(4.57) | 155(95.68) | 7(4.32) | 0(0) | |||
| >9.5 | 227(6.40) | 199(87.67) | 21(9.25) | 7(3.08) | |||
| 中性粒细胞绝对值异常(%) | 1.8~6.3 | 3 025(85.26) | 2 872(94.94) | 151(4.99) | 2(0.07) | 71.745 | < 0.001 |
| < 1.8 | 183(5.16) | 170(92.90) | 13(7.10) | 0(0) | |||
| >6.3 | 340(9.58) | 295(86.76) | 38(11.18) | 7(2.06) | |||
| 淋巴细胞绝对值异常(%) | 1.1~3.2 | 2 679(75.51) | 2 559(95.52) | 117(4.37) | 3(0.11) | 46.595 | < 0.001 |
| < 1.1 | 825(23.25) | 737(89.33) | 82(9.94) | 6(0.73) | |||
| >3.2 | 44(1.24) | 41(93.18) | 3(6.82) | 0(0) | |||
| HGB/g·L-1 | 135~175 | 1 145(32.27) | 1 088(95.02) | 56(4.89) | 1(0.09) | 3.925 | 0.141 |
| < 135 | 2 403(67.73) | 2 249(93.59) | 146(6.08) | 8(0.33) | |||
| PLT/109·L-1 | 125~135 | 3 113(87.74) | 2 938(94.38) | 169(5.43) | 6(0.19) | 35.646 | < 0.001 |
| < 125 | 177(4.99) | 151(85.31) | 23(12.99) | 3(1.69) | |||
| > 135 | 258(7.27) | 248(96.12) | 10(3.88) | 0(0) | |||
| 胆红素/μmol·L-1 | ≤26 | 3 471(97.83) | 3 277(94.41) | 188(5.42) | 6(0.17) | 64.905 | < 0.001 |
| >26 | 77(2.17) | 60(77.92) | 14(18.18) | 3(3.90) | |||
| CRP/mg·L-1 | ≤4 | 2 216(62.46) | 2 138(96.48) | 78(3.52) | 0(0) | 67.648 | < 0.001 |
| > 4 | 1 332(37.54) | 1 199(90.02) | 124(9.31) | 9(0.68) | |||
| CKMB/U·L-1 | ≤24 | 3 226(90.92) | 3 049(94.51) | 172(5.33) | 5(0.15) | 22.611 | < 0.001 |
| > 24 | 322(9.08) | 288(89.44) | 30(9.32) | 4(1.24) |
2.5 肝肾功能检测指标异常与重症COVID-19患者的相关性
3548例COVID-19患者中,重症及以上病例875例(24.7%),以重症为因变量,采用单因素Logistic回归筛选出重症独立的相关因素(包括年龄、肺部疾病、呼吸困难、胸闷、高血压、WBC异常、中性粒细胞绝对值异常、淋巴细胞绝对值异常、胆红素异常、HGB降低、白蛋白异常、CRP升高、CKMB升高等)作为校正因素,逐步进行校正,以分析肝或/和肾损伤与重症发生的相关性。
由表 4可见,逐步校正年龄、基础疾病、临床表现及实验室监测指标后(Model 3),肝或肾功能损伤的人群重症发生的风险是肝肾功能正常人群的1.612倍(95%CI:1.168-2.224),但未发现肝肾功能均损伤患者重症发生风险显著升高(P=0.484),估计与该组样本量较小有关。
| 校正模型 | B | S.E | Wals | Sig. | Exp (B) | OR的95%CI | ||
| 下限 | 上限 | |||||||
| 未校正因素 | 正常 | 40.777 | < 0.001 | |||||
| 肝或肾损伤 | 0.841 | 0.148 | 32.062 | < 0.001 | 2.318 | 1.733 | 3.101 | |
| 肝和肾损伤 | 2.433 | 0.803 | 9.187 | 0.002 | 11.397 | 2.363 | 54.975 | |
| Model 1 | 正常 | 35.996 | < 0.001 | |||||
| 肝或肾损伤 | 0.834 | 0.154 | 29.492 | < 0.001 | 2.303 | 1.704 | 3.112 | |
| 肝和肾损伤 | 2.139 | 0.815 | 6.886 | 0.009 | 8.492 | 1.718 | 41.969 | |
| Model 2 | 正常 | 27.909 | < 0.001 | |||||
| 肝或肾损伤 | 0.746 | 0.157 | 22.647 | < 0.001 | 2.109 | 1.551 | 2.869 | |
| 肝和肾损伤 | 1.950 | 0.825 | 5.583 | 0.018 | 7.027 | 1.394 | 35.418 | |
| Model 3 | 正常 | 8.841 | 0.012 | |||||
| 肝或肾损伤 | 0.477 | 0.164 | 8.449 | 0.004 | 1.612 | 1.168 | 2.224 | |
| 肝和肾损伤 | 0.598 | 0.855 | 0.489 | 0.484 | 1.819 | 0.340 | 9.727 | |
| Model 1:校正年龄(>60岁);Model 2:Model 1+高血压、肺部疾病+呼吸困难、胸闷;Model 3:Model 2 +白细胞(WBC)异常+中性粒细胞绝对值、淋巴细胞绝对值、血红蛋白(HGB)、胆红素、白蛋白降低,CRP、CKMB升高 | ||||||||
2.6 肝肾功能损伤与COVID-19患者死亡的相关性
3548例COVID-19患者中,住院期间死亡91例(2.6%)。以住院期间死亡为因变量,采用单因素Logistic回归筛选出死亡的独立相关因素(包括年龄、肺部疾病、呼吸困难、食欲减退、中性粒细胞绝对值异常、淋巴细胞绝对值异常、胆红素异常、CRP升高等)为校正因素,逐步进行校正,以分析肝或/和肾损伤与死亡发生的相关性。
如表 5所示,逐步校正年龄、基础疾病、临床表现及实验室监测指标后(Model 3),肝或肾功能损伤的人群发生住院期间死亡的风险是肝肾功能正常人群的2.907倍(95%CI:1.612-5.242),但未发现肝肾功能均损伤患者发生住院期间死亡风险显著升高[P=0.555, OR(95%CI):0.552(0.077-3.967)],估计与该组样本量较小有关。
| 校正模型 | B | S.E | Wals | Sig. | Exp(B) | OR的95%CI | ||
| 下限 | 上限 | |||||||
| 未校正因素 | 正常 | 46.498 | < 0.001 | |||||
| 肝或肾损伤 | 1.650 | 0.265 | 38.710 | < 0.001 | 5.205 | 3.095 | 8.751 | |
| 肝和肾损伤 | 2.605 | 0.811 | 10.319 | 0.001 | 13.532 | 2.761 | 66.322 | |
| Model 1 | 正常 | 41.275 | < 0.001 | |||||
| 肝或肾损伤 | 1.613 | 0.269 | 35.899 | < 0.001 | 5.017 | 2.960 | 8.503 | |
| 肝和肾损伤 | 2.228 | 0.819 | 7.395 | 0.007 | 9.286 | 1.863 | 46.275 | |
| Model 2 | 正常 | 33.037 | < 0.001 | |||||
| 肝或肾损伤 | 1.551 | 0.278 | 31.149 | < 0.001 | 4.717 | 2.736 | 8.134 | |
| 肝和肾损伤 | 1.510 | 0.887 | 2.896 | 0.089 | 4.527 | 0.795 | 25.766 | |
| Model 3 | 正常 | 13.290 | 0.001 | |||||
| 肝或肾损伤 | 1.067 | 0.301 | 12.576 | < 0.001 | 2.907 | 1.612 | 5.242 | |
| 肝和肾损伤 | -0.595 | 1.007 | 0.349 | 0.555 | 0.552 | 0.077 | 3.967 | |
| Model 1:校正年龄(>60岁);Model 2:Model 1+肺部疾病+呼吸困难、食欲减退;Model 3:Model 2 +中性粒细胞绝对值、淋巴细胞绝对值、胆红素、CRP | ||||||||
3 讨论
本研究是一个样本量较大的,系统回顾COVID-19患者中肝肾功能损害(ALT、AST、Cr)的临床特征,并分析相关指标特征与COVID-19患者重症化、住院期间死亡相关性风险的研究。结果显示,ALT升高的COVID-19患者发生重症和死亡的风险与ALT正常的患者相比无明显升高;而AST、Cr升高的COVID-19患者与AST、Cr正常患者相比,发生重症和死亡的风险均显著升高(P < 0.05);肝或肾损伤的COVID-19患者中男性、年龄>60岁、合并高血压、肺部疾病、CRP升高和CKMB升高等发生的比例也显著高于肝肾功能正常的患者(P < 0.05),表明肝或肾损伤的COVID-19患者更易发生多器官功能损伤。而多器官功能损害会增加COVID-19患者的重症化风险及病死率,通过早期的干预可以预防COVID-19患者的重症化,降低其病死率,并提高这类患者的治愈率。
在3548例COVID-19患者中,重症及以上患者有875例(24.7%),住院期间死亡患者有91例(2.6%),本研究分别以重症、死亡为因变量,采用单因素Logistic回归模型筛选出重症、死亡独立的相关因素作为校正因素,结果发现,肝或肾功能损伤的人群中重症及住院期间死亡发生的风险均较肝肾功能正常人群高(P < 0.05),预示着肝或肾功能损伤在COVID-19患者中发生重症及死亡的风险增加。
根据最新COVID-19患者有限的尸检和局部活检结果显示,SARS-CoV-2可累及肺、心脏、肝脏、肾脏、脑组织等多个器官[13-16]。此外在COVID-19患者中,会出现ALT和AST的异常升高,并且在重症患者中ALT和AST升高更为明显[7]。对1名死于COVID-19患者肝脏病变标本的病理研究结果显示:中度微泡脂肪变性,轻度小叶和门静脉活动性炎,提示SARS-CoV-2可导致肝脏损害进而引起转氨酶升高[17]。此外,还有药物原因,患者治疗过程中使用的各种药物会潜在地损伤肝脏[18-19];COVID-19患者重要的临床表现之一是低氧状态,这会影响到肝细胞的氧供应,肝细胞缺氧损伤后也会引起转氨酶升高[20];另外,一些COVID-19患者本身有基础的肝脏疾病[21],合并COVID-19后也会加重肝组织损伤。
相关研究表明血管紧张素转换酶2 (ACE2)是SARS-CoV-2的主要功能受体[3],因此富含ACE2的器官就成为SARS-CoV-2攻击人类细胞的主要场所。SARS-CoV-2感染后继发的多器官损伤机制包括病毒的直接毒性、内皮细胞损伤和血栓炎症、免疫反应失调以及肾素血管紧张素醛固酮系统(renin-angiolensin-aldosterone,RAAS)失调[22]。尽管这些机制在COVID-19病理生理学中的相对重要性目前尚不完全清楚,但其中ACE2介导的病毒入侵和组织损伤,以及RAAS失调,可能是COVID-19所独有的。ACE2在肺泡上皮Ⅱ型细胞、鼻杯状分泌细胞、胆管细胞、结肠细胞、食管角质形成细胞、胃肠道上皮细胞、胰腺β细胞、肾近端小管和足细胞中表达[23-25]。研究发现,SARS-CoV-2可与胆管细胞上的ACE2结合,导致胆管细胞功能障碍,引发全身炎症反应,导致肝脏损伤从而引起转氨酶升高[26]。
既然ACE2是SARS-CoV-2的主要功能受体,而ACE2又在肾脏组织中高表达,提示肾脏也是病毒侵犯的重要靶器官[27]。WRAPP等[28]解析了SARS-CoV-2的刺突(Spike,S)糖蛋白结构,该研究提供了SARS-CoV-2与ACE2具有更高亲和力的生物物理和结构的证据。SARS-CoV-2是利用高度糖基化的同源三聚体S糖蛋白进入宿主细胞,且ACE2与SARS-CoV-2的S糖蛋白的亲和力是SARS冠状病毒的10~20倍,提示SARS-CoV-2传染性更强,更容易发生肾脏损伤[29]。此外,身体的血液均需要通过肾脏过滤,血液中的SARS-CoV-2可通过ACE2感染肾脏,除了增加肾脏的SARS-CoV-2载量外,内皮细胞及肾小管上皮细胞的ACE2与病毒结合,使内皮细胞被病原体标记,使其成为宿主免疫系统识别和攻击的目标,最终也导致肾脏损伤。尽管SARS-CoV-2感染涉及肾脏的确切发病机制尚不清楚,但SARS-CoV-2引起的急性肾损伤(acute kidney injury,AKI)伴发的脓毒症、多器官衰竭和休克等相关并发症仍是COVID-19患者预后不良的重要原因[30]。
为预防COVID-19患者的重症化及降低病死率,我们需要早期识别与COVID-19患者疾病严重程度和预后不良相关的风险因素,因为合并器官功能损害的COVID-19患者重症化和病死的风险会增加,所以按照世卫组织筛查和分诊指南,准确评估COVID-19患者预后不良的危险因素是早期干预并改善患者预后的关键。与此同时,识别有重症化倾向的患者,可以帮助医护工作者及时对患者分类,转运至有救治设备及能力的单位(ICU)。
而从本研究结果来看,COVID-19患者的AST、Cr异常人群与患者的重症化及病死率有显著的关联,是预测COVID-19患者预后的重要因素;本研究对象来自多个中心,全部符合纳入排除标准,具有较好的代表性。研究显示与肝肾功能检查正常的COVID-19患者相比,AST、Cr异常的患者发生重症化及死亡的风险明显更高,多器官功能损伤会增加患者的病死率,并且在COVID-19患者中尤为明显,对于此类高风险患者,应在救治过程中密切关注AST、Cr指标的动态演变过程,密切观察病情、生命体征及各个靶器官功能变化,早期的干预可以预防COVID-19患者重症化,降低其病死率,并提高这类患者的救治成功率。
但本研究仍存在一定的局限性,个别病例并没有足够的病史,而COVID-19患者出现临床症状时会有不同的潜伏期,我们采用的数据是患者入院时的数据,对于住院期间的肝肾功能变化情况不甚了解。早期的研究中,降钙素原和血小板计数是疾病严重程度[31-32]的潜在预测因子,但是,本研究表明COVID-19患者合并肝肾功能异常指标的动态变化及其合并因素仍可为COVID-19患者的重症化和死亡风险提供预测依据,这些异常参数需在病程中密切监测,在后续的研究中仍需进一步被验证。
| [1] |
WU Z Y, MCGOOGAN J M. Characteristics of and important lessons from the coronavirus disease 2019 (COVID-19) outbreak in China[J]. JAMA, 2020, 323(13): 1239. |
| [2] |
WIERSINGA W J, RHODES A, CHENG A C, et al. Pathophysiology, transmission, diagnosis, and treatment of coronavirus disease 2019 (COVID-19): a review[J]. JAMA, 2020, 324(8): 782-793. |
| [3] |
YAN R H, ZHANG Y Y, LI Y N, et al. Structural basis for the recognition of SARS-CoV-2 by full-length human ACE2[J]. Science, 2020, 367(6485): 1444-1448. |
| [4] |
BEYERSTEDT S, CASARO E B, RANGEL É B. COVID-19: angiotensin-converting enzyme 2 (ACE2) expression and tissue susceptibility to SARS-CoV-2 infection[J]. Eur J Clin Microbiol Infect Dis, 2021, 40(5): 905-919. |
| [5] |
CHEN N S, ZHOU M, DONG X, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study[J]. Lancet, 2020, 395(10223): 507-513. |
| [6] |
HUANG C L, WANG Y M, LI X W, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China[J]. Lancet, 2020, 395(10223): 497-506. |
| [7] |
GUAN W J, NI Z Y, HU Y, et al. Clinical characteristics of coronavirus disease 2019 in China[J]. N Engl J Med, 2020, 382(18): 1708-1720. |
| [8] |
WANG D W, HU B, HU C, et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China[J]. JAMA, 2020, 323(11): 1061-1069. |
| [9] |
DIAO B, WANG C H, WANG R S, et al. Human kidney is a target for novel severe acute respiratory syndrome coronavirus 2 infection[J]. Nat Commun, 2021, 12(1): 2506. |
| [10] |
ZHOU F, YU T, DU R H, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study[J]. Lancet, 2020, 395(10229): 1054-1062. |
| [11] |
CHEN T, WU D, CHEN H L, et al. Clinical characteristics of 113 deceased patients with coronavirus disease 2019: retrospective study[J]. BMJ, 2020. |
| [12] |
YANG X B, YU Y, XU J Q, et al. Clinical course and outcomes of critically ill patients with SARS-CoV-2 pneumonia in Wuhan, China: a single-centered, retrospective, observational study[J]. Lancet Respir Med, 2020, 8(5): 475-481. |
| [13] |
WICHMANN D, SPERHAKE J P, LVTGEHETMANN M, et al. Autopsy findings and venous thromboembolism in patients with COVID-19: a prospective cohort study[J]. Ann Intern Med, 2020, 173(4): 268-277. |
| [14] |
CALABRESE F, PEZZUTO F, FORTAREZZA F, et al. Pulmonary pathology and COVID-19: lessons from autopsy. The experience of European pulmonary pathologists[J]. Virchows Arch, 2020, 477(3): 359-372. |
| [15] |
FALASCA L, NARDACCI R, COLOMBO D, et al. Postmortem findings in Italian patients with COVID-19: a descriptive full autopsy study of cases with and without comorbidities[J]. J Infect Dis, 2020, 222(11): 1807-1815. |
| [16] |
DUARTE-NETO A N, MONTEIRO R A A, DA SILVA L F F, et al. Pulmonary and systemic involvement in COVID-19 patients assessed with ultrasound-guided minimally invasive autopsy[J]. Histopathology, 2020, 77(2): 186-197. |
| [17] |
XU Z, SHI L, WANG Y J, et al. Pathological findings of COVID-19 associated with acute respiratory distress syndrome[J]. Lancet Respir Med, 2020, 8(4): 420-422. |
| [18] |
宣自学, 张国兵, 叶晓兰, 等. 新型冠状病毒肺炎患者肝损的原因分析[J]. 中国药理学通报, 2020, 36(4): 591-592. XUAN Z X, ZHANG G B, YE X L, et al. Cause analysis of liver injury in patients infected by novel coronavirus and suggestion of drug monitoring[J]. Chin Pharmacol Bull, 2020, 36(4): 591-592. |
| [19] |
郭伟锋, 梁彦彦. 中药治疗病毒性肝炎的疗效观察[J]. 中国医药指南, 2011, 9(31): 184-185. GUO W F, LIANG Y Y. Clinical effect of traditional Chinese medicine in treatment of viral hepatitis[J]. Guide China Med, 2011, 9(31): 184-185. |
| [20] |
雷偲艺, 彭虹, 罗新华. 新型冠状病毒肺炎引起肝损伤的致病机制及病毒性肝炎肝硬化患者的防护策略[J]. 临床肝胆病杂志, 2020, 36(7): 1619-1622. LEI S Y, PENG H, LUO X H. Pathogenic mechanism of liver injury caused by coronavirus disease 2019 and protective strategies for patients with viral hepatitis cirrhosis[J]. J Clin Hepatol, 2020, 36(7): 1619-1622. |
| [21] |
ZHANG C, SHI L, WANG F S. Liver injury in COVID-19: management and challenges[J]. Lancet Gastroenterol Hepatol, 2020, 5(5): 428-430. |
| [22] |
GUPTA A, MADHAVANM V, SEHGAL K, et al. Extrapulmonary manifestations of COVID-19[J]. Nat Med, 2020, 26(7): 1017-1032. |
| [23] |
ZHAO Y, ZHAO Z X, WANG Y J, et al. Single-cell RNA expression profiling of ACE2, the receptor of SARS-CoV-2[J]. Am J Respir Crit Care Med, 2020, 202(5): 756-759. |
| [24] |
DING Y Q, HE L, ZHANG Q L, et al. Organ distribution of severe acute respiratory syndrome (SARS) associated coronavirus (SARS-CoV) in SARS patients: implications for pathogenesis and virus transmission pathways[J]. J Pathol, 2004, 203(2): 622-630. |
| [25] |
HAMMINGI, TIMENS W, BULTHUIS M L, et al. Tissue distribution of ACE2 protein, the functional receptor for SARS coronavirus. A first step in understanding SARS pathogenesis[J]. J Pathol, 2004, 203(2): 631-637. |
| [26] |
ZHAO B, NI C, GAO R, et al. Recapitulation of SARS-CoV-2 infection and cholangiocyte damage with human liver ductal organoids[J]. Protein Cell, 2020, 11(10): 771-775. |
| [27] |
AHMADIAN E, HOSSEINIYAN KHATIBI S M, RAZI SOOFIYANI S, et al. Covid-19 and kidney injury: Pathophysiology and molecular mechanisms[J]. Rev Med Virol, 2021, 31(3): e2176. |
| [28] |
WRAPP D, WANG N, CORBETT K S, et al. Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation[J]. Science, 2020, 367(6483): 1260-1263. |
| [29] |
HATMALM M, ALSHAER W, AL-HATAMLEH M A I, et al. Comprehensive structural and molecular comparison of spike proteins of SARS-CoV-2, SARS-CoV and MERS-CoV, and their interactions with ACE2[J]. Cells, 2020, 9(12): E2638. |
| [30] |
BEZERRA R, TELES F, MENDONCA P B, et al. Outcomes of critically ill patients with acute kidney injury in COVID-19 infection: an observational study[J]. Ren Fail, 2021, 43(1): 911-918. |
| [31] |
LIPPI G, PLEBANI M. Procalcitonin in patients with severe coronavirus disease 2019 (COVID-19): A meta-analysis[J]. Clin Chim Acta, 2020, 505: 190-191. |
| [32] |
LIPPI G, PLEBANI M, HENRYB M. Thrombocytopenia is associated with severe coronavirus disease 2019 (COVID-19) infections: a meta-analysis[J]. Clin Chim Acta, 2020, 506: 145-148. |




