IgG4相关性疾病(IgG4-related disease, IgG4-RD)是以多发脏器肿大、血清IgG4升高为特点的一类受免疫系统调控的慢性纤维化炎症性疾病,但亦有30%~50%的患者血清IgG4仍处于正常水平[1-2]。其相对罕见,病因及发病机制尚不明确,常累及多个系统、跨多个学科,诊断多依靠血清IgG4及组织IgG4检查。目前尚缺乏统一的诊断与治疗标准,此疾病无论是在早期或进展后均易误诊或漏诊。由于易形成肿块性病变,常被误诊为恶性肿瘤。因此,提高对该疾病的认识,是早期诊断、改善预后的关键。本研究回顾性分析29例IgG4-RD的临床特征,了解血清IgG4升高对诊断IgG4-RD的临床意义,提高对IgG4-RD的认识和临床诊断水平。
1 资料与方法 1.1 研究对象在陆军军医大学第一附属医院医疗大数据平台上,收集2010年1月至2020年11月就诊于我院诊断为IgG4-RD的临床资料。目前IgG4-RD的诊断主要依据2011年日本发布的综合诊断标准及2012年国际病理学界发表的IgG4-RD病理表现的诊断共识[3]:① 1个或多个器官出现弥漫性/局限性肿胀或肿块的临床表现;②血清IgG4升高浓度>135 mg/dL(1.35 g/L);③组织病理学检查,包括显著的淋巴细胞、浆细胞浸润和纤维化,以及IgG4(+)浆细胞浸润[IgG4(+)/IgG(+)>40%,且IgG4(+)浆细胞>10个/高倍视野]。①+ ②+③可确定诊断;①+③很可能诊断;①+②可能诊断。同时应排除恶性肿瘤(如淋巴瘤)、结缔组织病(如干燥综合征)及其他与IgG4-RD类似的疾病[4]。纳入标准:怀疑IgG4-RD,有血清学IgG4及/或病理学检查结果的患者。排除标准:病理学证实非IgG4-RD的患者。
1.2 方法统计患者基本信息(性别、年龄)、首发症状、累及器官、血清IgG4水平、影像学表现、病理诊断、治疗及疗效;回顾分析IgG4水平升高对诊断IgG4-RD的临床意义。
1.3 统计学分析根据统计资料分布类型,临床资料、血清学检查结果采用描述性统计分析,连续性资料若符合正态分布以x±s表示,若不符合正态分布以M(P25, P75)表示。2组间正态分布数据比较采用t检验,非正态分布数据比较采用Mann-Whitney U检验。多组间正态分布数据比较采用单因素方差分析,多样本间的两两比较采用LSD-t检验,非正态分布资料采用Kruskal-Wallis秩和检验。计数资料统计描述采用率、构成比、相对比表示,计数资料组间比较采用卡方检验。相关性分析采用Pearson’s或者Spearman相关性分析。所有统计资料用SPSS 22.0进行分析。P < 0.05为差异有统计学意义。
2 结果 2.1 病例基本信息符合入选条件的共33例患者,其中男性18例,年龄26~77(51.4±13.8)岁;女性15例,年龄33~78(54.6±11.6)岁。参考2011年IgG4-RD综合诊断标准[3],结合临床表现、实验室检查、病理及免疫组织化学染色、治疗疗效等资料,IgG4升高、最终病理排除4例非IgG4-RD。29例诊断IgG4-RD,男性18例,年龄26~77 (51.4±13.8)岁;女性11例,年龄18~78(50.3± 15.7)岁;男∶女=1.64∶1。其中3例确诊、很可能诊断2例、可能诊断24例。
2.2 首发症状29例患者中,首发症状表现为颌下腺肿大7例,咳嗽5例,气促4例,多浆膜腔积液4例,多发淋巴结肿大3例,黄疸3例,眼肿胀2例,腹痛、腹胀2例,腰痛1例,多发皮损1例,右下唇包块、右乳包块、颈部包块各1例,发热1例,贫血1例。
2.3 累及器官诊断IgG-RD患者受累器官及与国内外研究的比较见表 1。29例IgG-RD患者淋巴结受累最常见,多为多发淋巴结肿大,其次为颌下腺肿大及肺脏受累(肺部斑片、结节或肿块、支气管壁增厚),肝脏(表现为黄疸、门脉高压)、泪腺/眼睑(泪腺增大、眼睑肿胀)、胸膜(胸水)、心包膜(心包积液)、胰腺(肿胀、占位)、皮肤(包块)、胆道(梗阻)、腮腺(肿大)、肾脏、乳腺(包块)均可受累。
| 受累器官 | 本研究 | 张盼盼等[5] | INOUE等[6] | WALLACE等[7] | EBBO等[8] |
| 淋巴结 | 8(29.6) | 195(56.4) | 34(14.0) | 34(27.2) | 19(76.0) |
| 颌下腺 | 6(22.2) | 182(52.6) | 35(28.0) | ||
| 肺 | 6(22.2) | 97(28.0) | 13(5.5) | 22(17.6) | 8(32.0) |
| 肝脏 | 5(18.5) | ||||
| 泪腺/眼睑 | 3(11.1) | 161(46.5) | 53(23.0) | 28(22.4) | |
| 胸膜/胸水 | 3(11.1) | 21(6.1) | |||
| 胰腺 | 2(7.4) | 133(38.4) | 142(60.0) | 24(19.2) | 13(52.0) |
| 心包膜 | 2(7.4) | 4(1.2) | 2(1.6) | ||
| 皮肤 | 2(7.4) | 22(6.4) | 2(1.6) | ||
| 胆道 | 1(3.7) | 88(25.4) | 13(5.5) | 12(9.6) | 8(32.0) |
| 腮腺 | 1(3.7) | 75(21.7) | 34(14.5) | 21(16.8) | |
| 肾脏 | 1(3.7) | 24(6.9) | 54(23.0) | 15(2.8) | 11(44.0) |
| 乳腺 | 1(3.7) |
2.4 实验室检查 2.4.1 血清IgG4水平
3例确诊IgG4-RD患者血清IgG4介于323~2 000 mg/dL(正常参考值:5~154 mg/dL);2例很可能诊断IgG4-RD患者血清IgG4介于57.3~70.7 mg/dL;24例可能诊断IgG4-RD患者血清IgG4介于168~1 910(715±570)mg/dL。4例非IgG4-RD患者血清IgG4介于233~896 mg/dL。
2.4.2 血清IgG水平29例患者中,13例检测了血清IgG,其中7例IgG升高(正常参考值:782~1 680 mg/dL),2例很可能诊断IgG4-RD患者血清IgG4、IgG均处于正常参考范围,4例非IgG4-RD患者血清IgG也处于正常参考范围。
2.5 病理结果① 3例确诊病例中,2例免疫组化染色IgG(+),阳性细胞热点区IgG4(+)约50个/HPF,IgG4(+)/IgG(+)≥30%;1例确诊IgG4相关性肾小管间质肾炎,CD138间质浆细胞(+),IgG4散在浆细胞(+)。②2例很可能诊断IgG4-RD,病理组织均有淋巴细胞、浆细胞浸润及纤维组织增生。免疫组化IgG(+)、IgG4(+),但未报告IgG4(+)与IgG(+)比值。③可能诊断IgG4-RD 24例,8例病理无典型IgG4-RD病理描述,16例无病理结果。④IgG4升高、最终病理提示非IgG4-RD 4例,1例ANCA核周型阳性、最终诊断“ANCA相关性血管炎肾损害伴亚急性肾小管间质”,1例确诊淋巴瘤,2例为结核性渗出性多浆膜腔积液。
2.6 治疗及治疗后疗效确诊IgG4-RD 3例中,1例予糖皮质激素联合免疫抑制剂治疗,1例单用糖皮质激素,1例予随访观察。很可能诊断2例因主要表现为颈部淋巴结肿大,症状轻微,未予治疗。可能诊断24例中4例予激素联合免疫抑制剂(吗替麦考酚酯、甲氨蝶呤片、硫唑嘌呤)治疗,3例单用糖皮质激素,1例单用免疫抑制剂,16例予随访观察。10例患者治疗后均反应良好,病灶缩小和/或IgG4降低。
2.7 典型病例患者,男性,62岁,以“咳嗽、咳少量黄黏痰、痰中带少量鲜红色血丝伴活动后明显气促”为主要临床表现,当地医院胸部CT提示“右侧大量胸腔积液,右肺压缩性不张,右肺门区见不规则形软组织影,双肺多发大小不等结节影;纵隔内多发肿大淋巴结;心包积液”,考虑“晚期肺癌”,为明确诊治来我院。患者既往有高血压、脑梗死。吸烟史40余年,吸烟指数20包年;偶饮酒。家族史无特殊。入院查体:心率109次/min,呼吸20次/min,血压152/106 mmHg,血氧饱和度(SO2)98%,呼吸稍促,右侧胸腔积液体征,余查体正常。
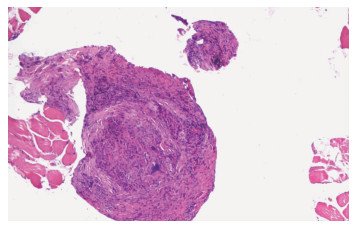
入院后行胸腔穿刺提示胸水为渗出性,CEA正常,X-Pert阴性。2次胸膜活检,第1次病理示:纤维组织增生,轻度慢性炎;第2次病理示:肉芽肿性炎(图 1),免疫组化提示IgG(-)、IgG4(-)。胸水脱落细胞学检查见较多炎性细胞及散在间皮细胞,未见肿瘤细胞。胸水引流后查胸腹部CT(2019年10月10日)示:右肺中下叶实变不张,右肺门区强化不均;双侧颈部4区、双侧锁骨上、双肺门、纵隔、膈上、肝门部及腹膜后多发淋巴结肿大;右侧胸腔、叶间裂积液。纤支镜检查示:双侧支气管吸出较多分泌物,右主支气管黏膜粗糙不平,右亚隆突增粗,右上叶开口及各段支气管黏膜均显粗糙不平,右上各段支气管开口均显缩小,于右上后段行黏膜刷检,未见癌细胞、分枝杆菌检测阴性;于右上叶活检,病理示黏膜慢性炎。多肿瘤标志物(-);T-Spot阴性;血清IgG4 264mg/dL;ANCA谱、ANCA、ACE、自身抗体谱15项、BALF G试验均阴性。
|
| 图 1 胸膜组织细胞染色观察(HE×20) |
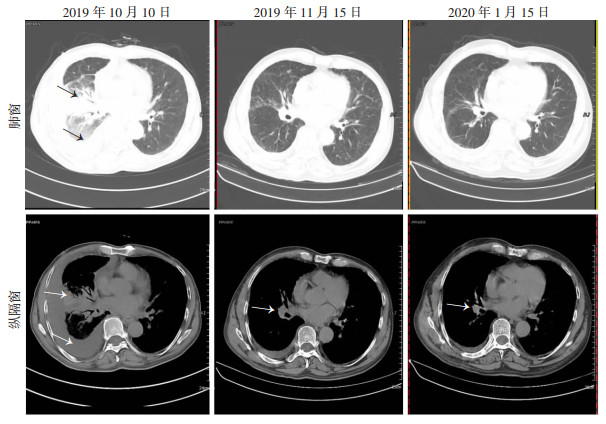
根据2011年日本发布的IgG4-RD综合分类标准,本病例诊断IgG4-RD肺浸润可能,拟行肺穿刺活检明确,患者拒绝,遂予“醋酸泼尼松片(强的松) 40 mg口服qd”诊断性治疗1个月,复查胸部CT(2019年11月15日)示:双肺病灶较前明显减少、吸收,右侧胸腔积液较前吸收减少,纵隔及双肺门淋巴结较前有所减小。后逐渐减量至10 mg qd维持,3个月后复查病灶基本吸收完全(图 2)。停药随访至今,无特殊不适。
|
| 箭头示IgG4-RD肺浸润病灶 图 2 不同时间点的胸部CT扫描显示病变的变化 |
本病例通过排除其他疾病、实验室检查及诊断性治疗后诊断“IgG4-RLD”。胸膜组织病理免疫组化提示IgG(-)、IgG4(-),考虑可能跟病理取材较少且局限有关。
3 讨论IgG4-RD是一种慢性自身免疫介导的炎症性系统性疾病,2018年5月11日,IgG4-RD被列入国家卫生健康委员会等5部门联合制定的《第一批罕见病目录》。其组织病理特点为IgG4(+)浆细胞浸润、席纹状纤维化、闭塞性脉管炎及嗜酸性粒细胞浸润[1],可累及腺体、眼眶、鼻窦、腹膜后、胰腺、胆管、肺、肾、肝、淋巴结,甚至血管、脑垂体、皮肤等多器官[9-10]。早期临床表现无特异性,随着疾病进展,临床表现与受累器官或组织相关,同时可有局部压迫症状及相应部位功能障碍。
IgG4是IgG 4个亚型之一,正常人静脉血中IgG4仅占IgG 1%~7%。病原体感染导致抗原呈递细胞(antigen presenting cell, APC)表面Toll样受体(Toll-likereceptor, TLR)和NOD样受体(nucleotide-binding oligomerization domain-likereceptor, NLR)激活可能是IgG4-RD发生的启动因素[11]。APC表面的模式识别受体激活后,促进B细胞活化和IgG4产生,同时进行抗原呈递,促进CD4+T细胞激活,分化并产生IL-4、IL-5、IL-13、IL-21等细胞因子,进一步促进B细胞活化、转化为浆细胞,产生IgG4并促进Ig类别转换[12-13]。炎症状态下蛋白酶激活,可将IgG裂解为Fab和F(ab’)2片段,IgG4(ab’)2片段与抗铰链区抗体特异性结合形成免疫复合物,激活补体系统。另因IgG4重链脯氨酸改变为丝氨酸,导致其重链非共价键连接不紧密,二硫键功能不完善,且IgG4结合Fc受体能力弱,可导致半个分子脱落后与其他IgG4分子的一半进行重组,妨碍了IgG4与抗原的交联反应,抑制了免疫复合物沉积和中性粒细胞产生IL-8,最终抑制固有免疫反应。IgG4通过Fc-Fc相互作用和IgG的Fc段结合,作为一种自身抗体和体内抗原进行反应,导致疾病的发生[14-15]。一系列免疫反应最终导致组织器官内IgG4(+)的浆细胞浸润。
本研究通过回顾分析2010年1月至2020年11月我院IgG4-RD临床资料,依据上述综合诊断标准,确诊、可能性大和可能的患者分别占10.3%、6.9%和82.8%。部分诊断可能IgG4-RD病理结果显示无明显IgG4、IgG浸润,或Ig[3]与IgG(+)比值较低,考虑可能跟取材组织较局限、不能代表全部有关;另部分患者未行活检,与症状轻微患者拒绝有创检查、受累组织获取困难等有关。
本研究结果显示,IgG4-RD男性多发,男∶女=1.64∶1,其中中老年(大于40岁)占89.7%,与其他报道基本一致[7]。29例患者中有5例肝脏受累,而2017年发表的一篇包括346例IgG4相关性疾病病例分析[5]及其他国外研究[7-8]均未见肝脏受累报道。受累器官中淋巴结、肺脏比例高于INOUE等[6]及WALLACE等[7]研究,低于EBBO等[8]研究,而泪腺/ 眼睑、胰腺、胆道、肾脏受累比例均低于INOUE、WALLACE、EBBO等研究。提示IgG4-RD器官受累存在种族差异,与张盼盼等[5]研究结果一致。另外,首发症状有咳嗽、气促、多浆膜腔积液、多发淋巴结肿大、黄疸、腹痛、腹胀、皮损、发热等,无明显特异性。29例IgG4-RD,血清IgG4升高比例为93.1%,IgG升高比例为53.8%,约6.9% IgG4-RD血清IgG4处于正常范围;与我国2017年一项大样本研究结果一致[5]。推测初诊IgG4-RD血清IgG4水平可能跟机体细胞及体液免疫、蛋白水平等有关。另有部分患者血清IgG4升高,但最终病理证实非IgG4-RD(ANCA相关血管炎、淋巴瘤、结核性多浆膜腔积液)。提示IgG4-RD的诊断需要结合临床症状、影像学表现、实验室检查及病理结果,但均无特异性。29例IgG4-RD中,19例予随访观察,10例予糖皮质激素和/或免疫抑制剂治疗,均反应良好,病灶缩小,IgG4降低,预后得到改善。
综上所述,IgG4-RD中老年男性好发,可累及多器官,有不同首发症状及临床表现。血清IgG4水平是IgG4-RD诊断的重要参考指标,约93%患者血清IgG4高于正常参考范围;但即使血清IgG4升高,诊断IgG4-RD也需排除肿瘤性疾病、血管炎、感染性疾病、Castleman病及其他结缔组织病等。另外,即使血清IgG4处于正常范围,也不能完全排除IgG4-RD。IgG4-RD为一种罕见病,需要各科临床医师共同关注,提高对IgG4-RD的认识水平,做到早期诊断,避免漏诊和误诊,改善预后。
| [1] |
KAMISAWA T, ZEN Y, PILLAI S, et al. IgG4-related disease[J]. Lancet, 2015, 385(9976): 1460-1471. |
| [2] |
KATABATHINA V S, KHALIL S, SHIN S, et al. Immunoglobulin G4-related disease: recent advances in pathogenesis and imaging findings[J]. Radiologic Clinics North America, 2016, 54(3): 535-551. |
| [3] |
UMEHARA H, OKAZAKI K, MASAKI Y, et al. Comprehensive diagnostic criteria for IgG4-related disease (IgG4-RD), 2011[J]. Mod Rheumatol, 2012, 22(1): 21-30. |
| [4] |
KHOSROSHAHI A, WALLACE Z S, CROWE J L, et al. International consensus guidance statement on the management and treatment of IgG4-related disease[J]. Arthr Rheumatol, 2015, 67(7): 1688-1699. |
| [5] |
张盼盼, 赵继志, 张文. IgG4相关性疾病346例临床特征分析[J]. 中华内科杂志, 2017, 56(9): 644-649. ZHANG P P, ZHAO J Z, ZHANG W. The clinical characteristics of 346 patients with IgG4-related disease[J]. Chin J Intern Med, 2017, 56(9): 644-649. |
| [6] |
INOUE D, YOSHIDA K, YONEDA N, et al. IgG4-related disease: dataset of 235 consecutive patients[J]. Medicine (Baltimore), 2015, 94(15): e680. |
| [7] |
WALLACE Z S, DESHPANDE V, MATTOO H, et al. IgG4-related disease: clinical and laboratory features in one hundred twenty-five patients[J]. Arthr Rheumatol, 2015, 67(9): 2466-2475. |
| [8] |
EBBO M, DANIEL L, PAVIC M, et al. IgG4-related systemic disease[J]. Medicine, 2012, 91(1): 49-56. |
| [9] |
CHEUK W, CHAN J K. IgG4-related sclerosing disease: a critical appraisal of an evolving clinicopathologic entity[J]. Adv Anat Pathol, 2010, 17(5): 303-332. |
| [10] |
MARITATI F, PEYRONEL F, VAGLIO A. IgG4-related disease: a clinical perspective[J]. Rheumatology (Oxford), 2020, 59(suppl 3): iii123-iii131. |
| [11] |
TOMOHIRO W, KOUHEI Y, SAORI F, et al. Activation of Toll-like receptors and NOD-like receptors is involved in enhanced IgG4 responses in autoimmune pancreatitis[J]. Arthr Rheumatol, 2011, 64(3): 914-924. |
| [12] |
AKIYAMA M, YASUOKA H, YAMAOKA K, et al. Enhanced IgG4 production by follicular helper 2 T cells and the involvement of follicular helper 1 T cells in the pathogenesis of IgG4-related disease[J]. Arthr Res Ther, 2016, 18: 167. |
| [13] |
MAEHARA T, MORIYAMA M, NAKASHIMA H, et al. Interleukin-21 contributes to germinal centre formation and immunoglobulin G4 production in IgG4-related dacryoadenitis and sialoadenitis, so-called Mikulicz's disease[J]. Ann Rheum Dis, 2012, 71(12): 2011-2019. |
| [14] |
RISPENS T, OOIEVAAR-DE HEER P, VERMEULEN E, et al. Human IgG4 binds to IgG4 and conformationally altered IgG1 via Fc-Fc interactions[J]. J Immunol, 2009, 182(7): 4275-4281. |
| [15] |
RISPENS T, OOIJEVAAR-DE HEER P, BENDE O, et al. Mechanism of immunoglobulin G4 fab-arm exchange[J]. J Am Chem Soc, 2011, 133(26): 10302-10311. |




