肺浸润性黏液腺癌(mucinous lung invasive adenocarcinoma, MLIA)是肺腺癌中一种比较少见的特殊亚型,分化较好,恶性程度较低。国外报道MLIA约占肺腺癌的0.25%[1],国内报道约占肺腺癌的0.14%[2]。MLIA在影像学上可表现为孤立型和弥漫型,孤立型MLIA又可表现为实性结节或肿块影、亚实性结节影及不规则囊腔影,其中以实型结节或肿块型最多见[1, 3]。我们在临床实践中发现实性孤立性肺浸润性黏液腺癌(solid solitary mucinous lung invasive adenocarcinoma, SS-MLIA)常表现出与实性孤立性肺浸润性非黏液腺癌(solid solitary non-mucinous lung invasive adenocarcinoma, SS-NMLIA)不同的影像学特征,甚至与一些肺良性病变的CT征象相似,极易误诊而延误患者治疗。目前国内外关于实性孤立性肺浸润性黏液腺癌CT征象方面的报道较少。本研究通过对比SS-MLIA与SS-NMLIA的临床特征及CT征象,探讨SS-MLIA的特征性CT表现,为提高SS-MLIA的诊断正确率,改善患者预后提供临床研究数据。
1 资料与方法 1.1 临床资料回顾性收集2014-2020年于本院诊治的47例SS-MLIA(黏液腺癌组)及277例SS-NMLIA(对照组)患者的临床及CT资料。对照组中,5例浸润性腺癌以贴壁生长方式为主,183例以腺泡状生长方式为主,37例以乳头状生长方式为主,9例以微乳头状生长方式为主,43例以实体生长方式为主。纳入标准:①经手术病理证实;②CT表现为孤立性结节或肿块。排除标准:①CT检查前接受过抗肿瘤治疗;②CT检查与手术时间间隔超过1月。本研究已获得本院伦理委员会审批(2019-062)。
1.2 检查方法采用GE Discovery 750 HD CT扫描仪行胸部CT扫描,患者取仰卧位,扫描前行呼吸训练,平扫及动脉期扫描范围从肺尖到肋膈角水平,静脉期仅对病灶行局部扫描。扫描参数:管电压120 kV,管电流自动毫安秒,扫描层厚及层间距均为5 mm。增强扫描时采用非离子型碘对比剂碘海醇(300 mgI/mL),经肘正中静脉注射,注射剂量为1.5 mL/kg,注射速率为3.0 mL/s,动脉期扫描延迟时间为30 s,静脉期扫描延迟时间为120 s。扫描结束后将原始图像重建为1.25 mm层厚的薄层图像,并传入PACS系统。
1.3 图像分析由2名分别具有10年及13年工作经验的放射科医师采用双盲法在PACS系统上共同阅片分析,意见不一致时,经协商讨论后达成一致。观察分析的CT征象包括:①肿瘤大小,在CT肺窗图像上(窗宽为1 600 HU;窗位为-600 HU)测量肿瘤最长径及其最大垂直径,取其平均值作为肿瘤大小;②受累肺叶,即右肺上叶、右肺中叶、右肺下叶、左肺上叶及左肺下叶;③肿瘤边界,清楚或模糊;④肿瘤边缘,有无分叶及毛刺征;⑤肿瘤内部特征,有无充气支气管征、含气腔隙(包括空腔及空洞)及钙化;⑥与邻近胸膜的关系,有无胸膜牵拉征或紧贴胸膜;⑦CT增强表现,有无血管造影征(即增强后肿瘤内出现明显强化的肺血管影)、有无液性无强化低密度区、动脉期及静脉期的CT净强化值(△CT动脉期=动脉期CT值-平扫CT值;△CT静脉期=静脉期CT值-平扫CT值)。
1.4 统计学分析采用SPSS 25.0统计软件,符合正态分布的定量资料以x±s表示,采用两独立样本t检验分析组间差异;不符合正态分布的定量资料以M±Q表示,采用Mann-Whitney U检验分析组间差异;定性资料采用χ2检验分析组间差异,P < 0.05为差异有统计学意义。
2 结果 2.1 两组临床特征的比较黏液腺癌组与对照组患者的性别、年龄、吸烟史及临床TNM分期差异均无统计学意义(表 1)。
| 临床特征 | 黏液腺癌组(n=47) | 对照组(n=277) | 统计值 | P值 |
| 性别 | χ2=0.220 | 0.639 | ||
| 男 | 26(55.32) | 143(51.62) | ||
| 女 | 21(44.68) | 134(48.38) | ||
| 年龄(岁) | 40~81(60.89±8.64) | 24~83(60.14±10.51) | t=0.463 | 0.644 |
| 吸烟史 | χ2=0.838 | 0.360 | ||
| 有 | 22(46.81) | 110(39.71) | ||
| 无 | 25(53.19) | 167(60.29) | ||
| 临床分期 | χ2=0.000 | 0.988 | ||
| Ⅰ~Ⅱ | 35(74.47) | 206(74.37) | ||
| Ⅲ~Ⅳ | 12(25.53) | 71(25.63) |
2.2 两组平扫CT征象的比较
黏液腺癌组与对照组间肿瘤平均直径差异无统计学意义。黏液腺癌组多位于双肺下叶(59.57%),对照组多位于双肺上叶(55.96%),两组差异有统计学意义(P < 0.05)。黏液腺癌组充气支气管征、钙化及紧贴胸膜的出现率(分别为38.30%、19.15%、44.68%)均显著高于对照组(分别为18.41%、2.17%、27.44%),而胸膜牵拉征出现率(36.17%)显著低于对照组(81.59%),两组差异均有统计学意义(P < 0.05),而两组边界况、分叶征、毛刺征及含气腔隙的出现率差异均无统计学意义(表 2,图 1、2)。
| 平扫CT征象 | 黏液腺癌组(n=47) | 对照组(n=277) | 统计值 | P值 |
| 肿瘤直径/mm | 23.00±19.50 | 21.50±15.50 | Z=-0.537 | 0.591 |
| 受累肺叶 | χ2=10.582 | 0.004 | ||
| 双肺上叶 | 16(34.04) | 155(55.96) | ||
| 右肺中叶 | 3(6.38) | 28(10.11) | ||
| 双肺下叶 | 28(59.57) | 94(33.94) | ||
| 边界 | χ2=0.099 | 0.752 | ||
| 清楚 | 44(93.62) | 252(90.97) | ||
| 模糊 | 3(6.38) | 25(9.03) | ||
| 分叶征 | χ2=0.059 | 0.808 | ||
| 有 | 44(93.62) | 265(95.67) | ||
| 无 | 3(6.38) | 12(4.33) | ||
| 毛刺征 | χ2=1.616 | 0.204 | ||
| 有 | 8(17.02) | 71(25.63) | ||
| 无 | 39(82.98) | 206(74.37) | ||
| 充气支气管征 | χ2=9.481 | 0.002 | ||
| 有 | 18(38.30) | 51(18.41) | ||
| 无 | 29(61.70) | 226(81.59) | ||
| 含气腔隙 | χ2=0.105 | 0.746 | ||
| 有 | 11(23.40) | 59(21.30) | ||
| 无 | 36(76.60) | 218(78.70) | ||
| 钙化 | χ2=22.542 | < 0.001 | ||
| 有 | 9(19.15) | 6(2.17) | ||
| 无 | 38(80.85) | 271(97.83) | ||
| 胸膜牵拉征 | χ2=44.207 | < 0.001 | ||
| 有 | 17(36.17) | 226(81.59) | ||
| 无 | 30(63.83) | 51(18.41) | ||
| 紧贴胸膜 | χ2=5.696 | 0.017 | ||
| 有 | 21(44.68) | 76(27.44) | ||
| 无 | 26(55.32) | 201(72.56) |
|
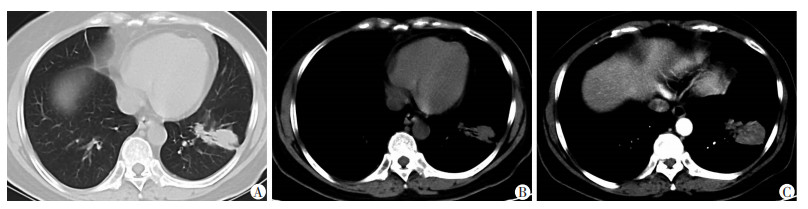
| A:横断面CT肺窗图像 示左肺下叶肿块影,其内见充气支气管征,局部与胸膜紧贴;B、C:横断面CT纵隔窗平扫及动脉期增强图像 示病灶强化程度较低,其内见血管造影征 图 1 实性孤立性肺浸润性黏液腺癌患者(女性,59岁)CT表现 |
|
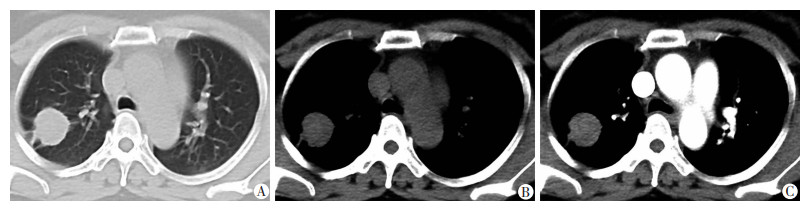
| A:横断面CT肺窗图像 示右肺上叶肿块影伴胸膜牵拉征;B、C:横断面CT纵隔窗平扫及动脉期增强图像 示病灶明显强化 图 2 实性孤立性肺浸润性非黏液腺癌患者(女性,47岁)CT表现 |
2.3 两组增强CT征象的比较
黏液腺癌组33例患者行CT增强扫描,对照组218例患者行CT增强扫描。从增强CT的表现来看,黏液腺癌组血管造影征及液性无强化低密度区的出现率(分别为51.52%、27.27%)均显著高于对照组(分别为26.15%、11.93%)(P均<0.05)。从强化程度来看,黏液腺癌组△CT动脉期及△CT静脉期显著低于对照组(P均<0.05,表 3,图 1、2)。
| CT征象 | 黏液腺癌组(n=33) | 对照组(n=218) | 统计值 | P值 |
| 血管造影征 | χ2=8.872 | 0.003 | ||
| 有 | 17(51.52) | 57(26.15) | ||
| 无 | 16(48.48) | 161(73.85) | ||
| 无强化低密度区 | χ2=4.419 | 0.036 | ||
| 有 | 9(27.27) | 26(11.93) | ||
| 无 | 24(72.73) | 192(88.07) | ||
| 强化程度/Hu | ||||
| △CT动脉期 | 13.0±15.0 | 28.0±25.0 | Z=-4.312 | < 0.001 |
| △CT静脉期 | 18.0±23.5 | 35.0±25.0 | Z=-3.875 | < 0.001 |
3 讨论
SS-MLIA在临床中较为少见,误诊率较高。目前已有较多学者对SS-MLIA与肺内良性病变的影像学特征进行了比较[4-5],但就SS-MLIA与SS-NMLIA影像学特征对比分析方面的研究尚少,且样本量均较小[6]。识别SS-MLIA与SS-NMLIA的影像学差异,探明SS-MLIA的特征性CT表现,有助于提高该病的术前诊断正确率。本研究首先比较SS-MLIA与SS-NMLIA的临床特征,结果显示两组男女发病率无显著差异。这与梁拥辉等[6]的研究结果一致。本研究发现两组患者年龄、吸烟史及临床分期差异均无统计学意义,其中SS-MLIA好发于中老年人,且与吸烟相关性不大,与王晓梅等[7]的研究结果相符。
本研究从肿瘤大小、部位、边界、边缘、内部征象及与胸膜的关系等几个方面比较了SS-MLIA与SS-NMLIA的CT平扫特征的差异。结果显示两组肿瘤的平均直径差异无统计学意义。从肿瘤部位来看,SS-MLIA好发于双肺下叶,而SS-NMLIA好发于双肺上叶,与梁拥辉等[6]的研究结果一致。从肿瘤边界及边缘特征来看,两组表现相似,即多数肿瘤边界清楚,边缘常见分叶,少数可见毛刺。分叶征表现为肿瘤边缘凹凸不平,犹如花瓣状,系肿瘤细胞向各个方向的生长速度不均衡或受到邻近肺组织的阻挡所致,是肺癌常见的CT征象之一。毛刺征则表现为自肿瘤边缘向周围肺实质伸展的、不与胸膜相连的、放射状的细短线条影,近肿瘤端多较粗,而远端多较细,与肿瘤细胞沿周围间质浸润生长有关。从肿瘤内部征象来看,SS-MLIA充气支气管征及钙化的出现率均显著高于SS-NMLIA,差异有统计学意义,而两者含气腔隙的出现率差异无统计学意义。充气支气管征表现为病灶内条状或分枝状气体密度影,多见于黏液腺癌。这可能与SS-MLIA肿瘤细胞主要沿肺泡壁生长,邻近支气管破坏较轻有关。而SS-NMLIA时肿瘤细胞主要表现为腺泡状、乳头状、微乳头状或实体生长方式,有报道以微乳头及实体生长方式为主的浸润性腺癌更容易压迫或破坏周围肺实质,因而充气支气管征的出现率较低[8-9]。SS-MLIA和SS-NMLIA均可发生瘤内钙化,SS-MLIA瘤内钙化的病理基础为腺癌细胞分泌较多黏液,容易出现钙盐沉积[10-11];SS-NMLIA瘤内钙化与肿瘤生长迅速导致瘤内缺血缺氧,继而发生坏死及营养不良性钙化有关[12]。我们认为肺黏液腺癌钙化的发生率更高可能与本研究中大部分SS-NMLIA患者的临床分期为Ⅰ~Ⅱ期,肿瘤多数较小,因而坏死发生率较低有关。含气腔隙表现为肿瘤内局灶性气体密度影,其病理基础可能与肿瘤内残存支气管、小气道受累狭窄形成气肿囊腔或肿瘤坏死后形成空洞有关[13]。邵元伟等[14]分析了16例肺黏液腺癌的CT征象,其空泡征的发生率为67.85%,明显高于本研究含气腔隙的出现率(23.40%),分析原因可能在于前者样本量较少及肺黏液腺癌的纳入标准不同。从肿瘤与胸膜的关系来看,肿瘤与胸膜紧贴者多见于SS-MLIA,而胸膜牵拉征则多见于SS-NMLIA。胸膜牵拉征与瘤体内成纤维反应引起瘢痕形成,其收缩力通过邻近的肺间质传导至脏层胸膜。由于肺黏液腺癌的成纤维反应较轻,故胸膜牵拉征的出现率较低[6]。包盈莹等[15]报道的118例结节型肺黏液腺癌中,胸膜牵拉征出现率仅为39%,与本研究结果相似。
从增强CT表现来看,本研究结果显示:SS-MLIA血管造影征及液性无强化低密度区的出现率均显著高于SS-NMLIA,且动脉期及静脉期的CT净强化值显著低于SS-NMLIA。这些差异均与SS-MLIA的病理生长方式明显有别于SS-NMLIA有关。肺黏液腺癌时肿瘤细胞沿肺泡壁贴壁式生长,肺的支架结构仍然存在,其内血管不易受侵,因而容易出现血管造影征;同时,肿瘤细胞会分泌大量黏液充填肺泡腔,因而增强时肿瘤强化程度较低,甚至可无强化,当有黏液湖形成时,瘤内可出现液性无强化低密度区。而SS-NMLIA主要以腺泡状、乳头、微乳头及实体生长方式为主,易侵犯肿瘤内部血管,因此在增强扫描时不易出现血管造影征。这些发现与多数学者的研究结果相符[4-7, 9, 13-14]。
综上所述,SS-MLIA与SS-NMLIA有着明显不同的CT表现,其中SS-MLIA的典型CT表现为下叶分布、充气支气管征、钙化及紧贴胸膜,增强时强化程度较轻,常见血管造影征及液性无强化低密度区。正确识别SS-MLIA的特征性CT征象,有助于提高其术前诊断正确率,改善患者预后。
| [1] |
NIE K, NIE W, ZHANG Y X, et al. Comparing clinicopathological features and prognosis of primary pulmonary invasive mucinous adenocarcinoma based on computed tomography findings[J]. Cancer Imaging, 2019, 19(1): 47. |
| [2] |
宾怀有, 龙腾河, 滕才钧. 原发性肺黏液腺癌的CT表现与病理学对照研究[J]. 广西医学, 2014, 36(4): 527-529. BIN H Y, LONG T H, TENG C J. Comparative study on CT manifestations and pathological of primary pulmonary mucus adenocarcinoma[J]. Guangxi Med J, 2014, 36(4): 527-529. |
| [3] |
WANG T, YANG Y, LIU X, et al. Primary invasive mucinous adenocarcinoma of the lung: prognostic value of CT imaging features combined with clinical factors[J]. Korean J Radiol, 2021, 22(4): 652-662. |
| [4] |
方新勇, 邝平定, 张敏鸣. 肺原发黏液腺癌的CT征象分析[J]. 临床放射学杂志, 2019, 38(5): 840-844. FANG X Y, KUANG P D, ZHANG M M. Analysis of the CT features of primary lung mucinous adenocarcinoma[J]. J Clin Radiol, 2019, 38(5): 840-844. |
| [5] |
梁拥辉, 郭爱菊, 师新宇, 等. 肺孤立性实性结节61例采用CT检查对黏液腺癌与结核球鉴别诊断价值的评估[J]. 中华肿瘤防治杂志, 2021, 28(1): 62-66. LIANG Y H, GUO A J, SHI X Y, et al. CT differential diagnosis of primary nodular mucinous adenocarcinoma and tuberculoma: Evaluation of 61 solitary solid nodules[J]. Chin J Cancer Prev Treat, 2021, 28(1): 62-66. |
| [6] |
梁拥辉, 曹捍波, 王梅, 等. 孤立型肺黏液腺癌与非黏液性浸润性肺腺癌的CT对比研究[J]. 临床放射学杂志, 2020, 39(12): 2415-2418. LIANG Y H, CAO H B, WANG M, et al. CT comparative study of solitary pulmonary mucionous adenocarcinoma and non-mucionous invasive pulmonary adenocarcinoma[J]. J Clin Radiol, 2020, 39(12): 2415-2418. |
| [7] |
王晓梅, 王靖红, 吴重重, 等. 原发性肺浸润型黏液腺癌的多层螺旋CT表现[J]. 中国医学影像学杂志, 2015, 23(9): 691-694. WANG X M, WANG J H, WU C C, et al. Multi-slice spiral CT features of lung primary invasive mucinous adenocarcinoma[J]. Chin J Med Imaging, 2015, 23(9): 691-694. |
| [8] |
LI Q, LI X, LI X Y, et al. Histological subtypes of solid-dominant invasive lung adenocarcinoma: differentiation using dual-energy spectral CT[J]. Clin Radiol, 2021, 76(1): 77.e1-77.77.e7. |
| [9] |
何小群, 罗天友, 李琦, 等. 浸润性肺腺癌不同病理亚型的临床病理及CT特征分析[J]. 第三军医大学学报, 2020, 42(19): 1950-1956. HE X Q, LUO T Y, LI Q, et al. Clinicopathological characteristics and CT features of invasive adenocarcinoma of the lung with different pathological subtypes[J]. J Third Mil Med Univ, 2020, 42(19): 1950-1956. |
| [10] |
王庆宜, 李万湖, 张德贤, 等. 原发性肺浸润型黏液腺癌影像学表现及病理特点[J]. 中华肿瘤防治杂志, 2020, 27(8): 647-652, 657. WANG Q Y, LI W H, ZHANG D X, et al. Imaging findings and pathological features of primary lung invasive mucinous adenocarcinoma[J]. Chin J Cancer Prev Treat, 2020, 27(8): 647-652, 657. |
| [11] |
高菲, 陈亮. 原发性肺黏液腺癌结合病理的CT表现及临床征象[J]. 中国实验诊断学, 2018, 22(5): 852-856. GAO F, CHEN L. Combined with pathological analysis of CT findings and clinical signs of primary lung mucinous adenocarcinoma[J]. Chin J Lab Diag, 2018, 22(5): 852-856. |
| [12] |
ZHU Y H, WANG X, ZHANG J, et al. Low enhancement on multiphase contrast-enhanced CT images: an independent predictor of the presence of high tumor grade of clear cell renal cell carcinoma[J]. AJR Am J Roentgenol, 2014, 203(3): 295-300. |
| [13] |
谭小妹, 邓东, 韦艳静. 原发性肺浸润型黏液腺癌的多层螺旋CT征象分析[J]. 微创医学, 2019, 14(2): 153-156. TAN X M, DENG D, WEI Y J. Multi-slice spiral CT features of primary pulmonary invasive mucinous adenocarcinoma[J]. J Minim Invasive Med, 2019, 14(2): 153-156. |
| [14] |
邵元伟, 滕敏敏, 王晓蕾, 等. 原发性肺浸润性黏液腺癌的临床病理特征与CT表现[J]. 中国临床医学影像杂志, 2020, 31(10): 719-722, 726. SHAO Y W, TENG M M, WANG X L, et al. Clinicopathological features and CT findings of primary pulmonary invasive mucinous adenocarcinoma[J]. J China Clin Med Imaging, 2020, 31(10): 719-722, 726. |
| [15] |
包盈莹, 雷永霞, 李新春, 等. 肺浸润性黏液腺癌的CT及18F-FDG PET/CT表现[J]. 中国医学影像学杂志, 2019, 27(11): 815-819. BAO Y Y, LEI Y X, LI X C, et al. CT and 18F-FDG PET/CT features of pulmonary invasive mucinous adenocarcinoma[J]. Chin J Med Imaging, 2019, 27(11): 815-819. |




