声带任克水肿为声带浅固有层弥漫性蛋白基质潴留所致,是引起嗓音功能障碍的常见疾病之一,其发病因素多样。临床表现主要为声音嘶哑及音调低沉,呈进行性加重,可伴有异物感及咳嗽等,严重时可出现呼吸不畅,甚至喉梗阻,影响患者的生活质量和身心健康[1]。其病因主要与吸烟、不合理用嗓、咽喉反流等相关。现阶段治疗方案尚未统一,多数学者认为手术为主要的治疗手段。目前手术联合抑酸治疗声带任克水肿的报道甚少,现将我院的相关治疗经验报告如下。
1 资料与方法 1.1 临床资料回顾性分析2016年4月至2019年12月在我科诊断为双侧声带任克水肿伴有咽喉反流并住院手术治疗的47例患者的临床资料,其中男性43例,女性4例,年龄38~62(47.1±8.2)岁。40例男性和2例女性长期吸烟,且术前仍未戒烟。根据术后是否选择抑酸治疗分为抑酸组(n=27)和非抑酸组(n=20)。抑酸组中男性24例,女性3例,年龄38~54(44.1±8.8)岁;非抑酸组中男性19例,女性1例,年龄42~62(48.3±7.5)岁。按YONEKAWA声带任克水肿程度的分度方法[2],在动态喉镜下进行分度,Ⅱ度21例(男性18例,女性3例),Ⅲ度26例(男性25例,女性1例)。所有患者无其他咽喉或全身疾病,均选择手术治疗。
对患者术前进行严格评估,详细讲解诊治方案及可能出现的结果,患者均自愿配合,签署知情同意书,相关资料送医院伦理委员会备案[伦审(科研)S2018-037-01]。选取正常嗓音的医务工作者及其家属、患者家属等作为健康对照组,共56例,其中男性50例,女性6例,年龄31~55(45.8±7.6)岁。35例男性和1例女性有长期吸烟史。所有研究对象近期无“上呼吸道感染”病史,且无哮喘等其他呼吸系统疾病史,无咽喉手术及疾病史,无精神及神经系统疾病。健康对照组动态喉镜检查示双侧声带无明显异常。
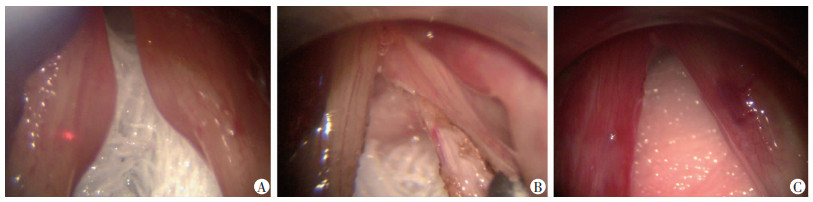
1.2 治疗方法 1.2.1 手术治疗手术均在全麻气管插管显微支撑喉镜直视下进行,采用显微微瓣技术,切开声带中后份黏膜(图 1A);吸除任克氏层多余的水肿组织,切除多余的黏膜(图 1B),良好复位微瓣,尽可能保证双侧声带前份黏膜的完整(图 1C)。手术均由同一医师完成。
|
| A:CO2激光切开黏膜;B:切除黏膜下水肿组织;C:复位黏膜瓣 图 1 显微支撑喉镜手术方法 |
1.2.2 抑酸治疗
术前反流症状指数量表(Reflux Symptom Index, RSI)评分≥13分或反流体征指数量表(Reflux Finding Score, RFS)评分≥7分判定为存在咽喉反流。药物治疗方案:患者于饭前30~60 min口服艾司奥美拉唑镁肠溶片20 mg,每天2次,持续8周[3]。8周后改为20 mg,每天口服1次,连续2周;此后改为10 mg口服,每天1次,2周后停药。
1.2.3 其他治疗所有病例要求戒烟、戒酒,予以声保健指导,术后1周内禁声,术后1个月内休声,1个月以后嘱患者正常、正确用声。RSI或RFS量表评分中存在1项症状或体征者,予以正确饮食方式的指导。
1.2.4 随访于术后1、3、6个月进行声音嘶哑程度主观评估、动态喉镜检查和嗓音声学分析,并进行嗓音障碍指数(voice handicap index, VHI)调查。嗓音声学分析指标主要有噪/谐比(NHR)、基频微扰(jitter)、基频(F0)以及振幅微扰(shimmer)。
1.3 嗓音声学分析检测采用德国XION动态喉镜及嗓音分析系统(Divas v2.30)对所有研究对象进行动态喉镜检查以及嗓音声学分析。受试者端坐于屏蔽室内,经口行动态喉镜检查;头戴式麦克风与口距离约30 cm,使用嗓音分析系统(Divas v2.30)进行嗓音声学分析,得出相关参数,包括NHR、shimmer、F0、jitter[4]。
1.4 VHI评分VHI由功能(F)、生理(P)和情感三部分组成,每部分有10个条目,总共有30个条目。每条的备选项按照等级0-从未出现、1-几乎没有、2-有时出现、3-几乎经常出现、4-经常出现分别计为0~4分,分别计算各部分的得分。专业培训后的调查员对受试对象进行相关项目的讲解,协助其客观、真实地回答各条目问题[5]。
1.5 咽喉反流评分咽喉反流评分由专人在术前谈话时利用RSI与RFS进行评分并记录[3]。
1.6 统计学分析采用SPSS 20.0统计软件。计量资料以x±s表示,两组间比较采用独立样本t检验,多组组间比较采用单因素方差分析检验。P < 0.05被认为差异有统计学意义。
2 结果 2.1 动态喉镜随访术后3个月时,30例(63.83%)患者声带恢复良好,见声带瘢痕;17例(36.17%)声带局部有肉芽形成,肉芽逐渐自行消失。至术后6个月,抑酸组有1例复发再次手术,非抑酸组有3例复发,1例抑酸保守治疗,2例再次手术治疗。
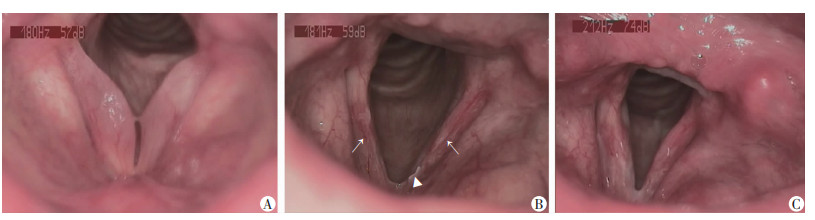
典型病例分析:患者男性,47岁。术前动态喉镜图像见图 2A,术后3个月时见声带瘢痕,局部见肉芽(图 2B),至6个月时肉芽消失(图 2C)。
|
| A:术前;B:术后3个月声带局部见瘢痕(↑)及肉芽(△);C:术后6个月肉芽消失 图 2 典型病例动态喉镜随访情况 |
2.2 嗓音指标比较
抑酸及非抑酸组F0术前与健康对照组相比均降低,NHR、jitter及shimmer与健康对照组相比均升高,且差异具有统计学意义(P < 0.05)。术后1、3、6个月,抑酸及非抑酸组F0逐渐升高,其余3个嗓音声学指标均有一定程度的降低,声音嘶哑逐渐减轻。术后1个月时,抑酸及非抑酸组之间上述指标无明显差异;在第3、6个月时,抑酸组F0大于非抑酸组,NHR、jitter及shimmer小于非抑酸组,差异有统计学意义(P < 0.05),抑酸及非抑酸组与健康对照组相比仍存在明显差异(P < 0.05,表 1)。
| 组别 | 例数 | F0 | jitter | shimmer | NHR |
| 抑酸组 | |||||
| 术前 | 27 | 202.64±54.55a | 2.48±0.59a | 5.69±0.64a | 0.17±0.07a |
| 术后1个月 | 27 | 225.21±44.21 | 2.58±0.65 | 5.47±0.55 | 0.16±0.09 |
| 术后3个月 | 26 | 231.46±47.61ab | 1.48±0.47ab | 3.21±0.38ab | 0.13±0.05ab |
| 术后6个月 | 24 | 254.78±50.62ab | 0.51±0.08ab | 2.17±0.43ab | 0.12±0.06ab |
| 非抑酸组 | |||||
| 术前 | 20 | 204.07±50.31a | 2.71±0.44a | 5.38±0.51a | 0.18±0.08a |
| 术后1个月 | 20 | 219.86±49.60 | 2.49±0.59 | 5.30±0.48 | 0.16±0.04 |
| 术后3个月 | 19 | 237.71±45.08 | 1.60±0.55 | 3.46±0.62 | 0.14±0.04 |
| 术后6个月 | 18 | 249.33±49.92 | 0.66±0.12 | 2.44±0.37 | 0.14±0.07 |
| 健康对照组 | 56 | 263.51±36.71 | 0.22±0.07 | 1.49±0.61 | 0.11±0.05 |
| a:P < 0.05,与健康对照组比较;b:P < 0.05,与非抑酸组比较 | |||||
2.3 VHI量表评估
患者术前VHI各项评分较健康对照组明显增加,差异具有统计学意义(P < 0.05);术后1、3、6个月功能(F)评分、生理(P)评分、情感(E)评分及总评分(T)逐渐降低,各时间点抑酸组与非抑酸组各项评分无明显差异,术后6个月时,两组各项评分与健康组比较均无明显差异(表 2)。
| 组别 | 例数 | F(功能) | P(生理) | E(情感) | T(总分) |
| 抑酸组 | |||||
| 术前 | 27 | 15.13±3.33a | 21.30±4.00a | 5.88±1.74a | 42.31±4.04a |
| 术后1个月 | 27 | 5.77±1.36 | 15.12±3.77 | 4.55±1.48 | 25.44±3.38 |
| 术后3个月 | 26 | 4.78±1.87 | 8.21±3.60 | 3.37±1.60 | 16.36±2.73 |
| 术后6个月 | 24 | 4.44±1.50 | 6.22±3.71 | 3.04±1.81 | 13.70±2.80 |
| 非抑酸组 | |||||
| 术前 | 20 | 15.33±3.19a | 22.44±3.70a | 5.42±1.99a | 43.19±4.31a |
| 术后1个月 | 20 | 6.12±1.38 | 16.03±3.41 | 4.69±1.48 | 26.54±3.37 |
| 术后3个月 | 19 | 5.37±1.44 | 7.74±3.79 | 3.05±1.34 | 16.16±3.44 |
| 术后6个月 | 18 | 4.77±1.16 | 7.00±3.35 | 2.92±1.01 | 14.69±2.00 |
| 健康对照组 | 56 | 3.67±1.49 | 4.33±1.09 | 2.11±0.38 | 10.11±1.13 |
| a:P < 0.05,与健康对照组比较 | |||||
3 讨论
声带任克水肿是黏膜固有层浅层的水肿,伴有纤维化、炎性渗出或出血等。黏膜上皮可无任何病理改变,也可表现为过度增生、角化或角化不全,严重时局部有息肉形成。吸烟、声音滥用、胃食管反流刺激都被认为是任克氏水肿形成的重要原因。进行性加重的声音嘶哑是最常见的症状[6]。其治疗包括戒烟、嗓音维护、抑酸药物口服、局部注射类固醇激素及手术治疗,以手术治疗为主[7]。VHI量表[8]及jitter、shimmer、NHR可良好评估疗效。
目前手术方法包括显微微瓣吸引、显微吸切、激光及水肿压窄术等。显微吸引术较激光手术术后声音质量恢复更好[9-10]。本研究任克水肿Ⅱ、Ⅲ度的患者选择显微微瓣吸引术,采取支撑喉镜显微镜下外侧微瓣技术,切开黏膜,吸除任克氏层多余的积液,切除多余的黏膜,复位微瓣。与SHIBA等[11]及李丹凤等[12]选择YONEKAWA分型中的Ⅱ、Ⅲ度任克水肿手术治疗的手术方案一致,术后疗效满意。
研究证实胃食管反流与声带任克水肿的发病有密切联系[13-14]。李丹凤等[12]报告对于伴有咽喉反流的Ⅰ度及部分Ⅱ度任克水肿患者给予抑酸等治疗后可达到满意效果。KANTAS等[15]的病例对照研究结果表明:对伴有咽喉反流的声带任克水肿患者抗酸治疗1个月有效,经治疗后,患者症状明显缓解,声带水肿明显减轻,对照组未接受抑酸治疗,则相关症状及体征无改善。抑酸治疗对伴有反流的声带任克水肿有效,但能否通过保守疗法治愈声带任克水肿未见报道。手术仍为治疗任克水肿的重要方法[11]。
伴有反流的手术患者术后是否规律地进行抑酸治疗,目前少有报道。本研究发现任克水肿患者术后声音嘶哑症状逐渐减轻。VHI评分在术前患者组明显比健康对照组高,说明患者的生理、功能、情感都被声带任克水肿影响。手术治疗后,评分明显降低,且在术后6个月时与健康对照组比较已无明显差异;但术后1、3、6个月抑酸组与非抑酸组之间相比无明显差异,这可能与患者术前嗓音质量相对较差、对术后恢复预期相对较低的原因有关。在嗓音功能方面,抑酸及非抑酸组因任克水肿、声带水肿致F0较健康对照组降低;jitter、shimmer、NHR较健康对照组升高,随着术后时间的推移,伴随着创面的修复和肿胀的消退,抑酸及非抑酸组F0逐渐升高,其余4个指标均有一定程度的降低。术后1个月时,抑酸及非抑酸组之间上述指标无明显差异,但在第3、6个月时,抑酸组F0大于非抑酸组,jitter、shimmer、NHR小于非抑酸组,这说明抑酸治疗可使声带恢复得更好、更快。两组嗓音功能指标相比健康对照组差,与MARTINS等[16]报告的声带任克水肿患者在显微外科手术及戒烟治疗6个月后声音嘶哑较健康对照组仍较差的结论相一致。
综上所述,声带任克水肿采用显微支撑喉镜手术治疗效果肯定,对伴有咽喉反流的患者抑酸治疗可提高嗓音质量。然而,本研究属于小样本研究,且观察时间相对较短,有效治疗方案仍有待进一步研究数据和长时间观察予以验证。
| [1] |
TAVALUC R, HERMAN H, LIN J, et al. Does reinke's edema grade determine premalignant potential?[J]. Ann Otol Rhinol Laryngol, 2018, 127(11): 812-816. |
| [2] |
YONEKAWA H. A clinical study of Reinke's edema[J]. Auris Nasus Larynx, 1988, 15(1): 57-78. |
| [3] |
李进让, 肖水芳, 李湘平, 等. 咽喉反流性疾病诊断与治疗专家共识(2015年)解读[J]. 中华耳鼻咽喉头颈外科杂志, 2016, 51(5): 327-332. LI J R, XIAO S F, LI X P, et al. Explanation of the experts consensus on diagnosis and treatment of laryngopharyngeal reflux disease (2015)[J]. Chin J Otorhinolaryngol Head Neck Surg, 2016, 51(5): 327-332. |
| [4] |
杨莉, 干强, 杨贵军, 等. 女性声带息肉术后发声功能恢复的时间观察[J]. 第三军医大学学报, 2016, 38(24): 2625-2628. YANG L, GAN Q, YANG G J, et al. Recovery time of phonation function in female patients after vocal polyp surgery[J]. J Third Mil Med Univ, 2016, 38(24): 2625-2628. |
| [5] |
SEIFPANAHI S, JALAIE S, NIKOO M R, et al. Translated versions of voice handicap index (VHI)-30 across languages: a systematic review[J]. Iran J Public Health, 2015, 44(4): 458-469. |
| [6] |
URA-SABAT K, MORAWSKA J, DOMKA W, et al. The assessment of phonatory and ventilatory functions in patients after microsurgery for Reinke's edema[J]. Adv Clin Exp Med, 2020, 29(7): 865-871. |
| [7] |
HAMDAN A L, KHALIFEE E, ABI AKL P R, et al. Pathogenic role of reinke's edema in snoring and obstructive sleep apnea[J]. J Voice, 2020, 34(3): 456-459. |
| [8] |
WATANABE T, KANEKO K, SAKAGUCHI K, et al. Vocal-fold vibration of patients with Reinke's edema observed using high-speed digital imaging[J]. Auris Nasus Larynx, 2016, 43(6): 654-657. |
| [9] |
TAVALUC R, TAN-GELLER M. Reinke's edema[J]. Otolaryngol Clin North Am, 2019, 52(4): 627-635. |
| [10] |
LIANG F Y, CHEN R H, LIN P L, et al. Correction to: Two-handed tying technique in vocal fold mucosa microsuture for the treatment of Reinke's edema[J]. Eur Arch Otorhinolaryngol, 2019, 276(7): 2023. |
| [11] |
SHIBA Y, MIZOJIRI G, NOZAKI T. Vocal function in Reinke's edema: degree of the lesion and indication of the operation[J]. Nihon Jibiinkoka Gakkai Kaiho, 1992, 95(9): 1345-1351. |
| [12] |
李丹凤, 石力, 岳波, 等. 双侧声带任克氏间隙水肿个体化分级治疗的临床分析[J]. 临床医学研究与实践, 2020, 5(6): 3-4, 9. LI D F, SHI L, YUE B, et al. Clinical analysis of individualized grading therapy for bilateral vocal cord Reinke's edema[J]. Clin Res Pract, 2020, 5(6): 3-4, 9. |
| [13] |
LECHIEN J R, SAUSSEZ S, NACCI A, et al. Association between laryngopharyngeal reflux and benign vocal folds lesions: a systematic review[J]. Laryngoscope, 2019, 129(9): E329-E341. |
| [14] |
LECHIEN J R, HAMDAN A L, SAUSSEZ S. Laryngopharyngeal reflux and benign lesions of the vocal folds[J]. Eur Arch Otorhinolaryngol, 2019, 276(1): 277-278. |
| [15] |
KANTAS I, BALATSOURAS D G, KAMARGIANIS N, et al. The influence of laryngopharyngeal reflux in the healing of laryngeal trauma[J]. Eur Arch Otorhinolaryngol, 2009, 266(2): 253-259. |
| [16] |
MARTINS R H G, TAVARES E L M, PESSIN A B B. Are vocal alterations caused by smoking in reinke's edema in women entirely reversible after microsurgery and smoking cessation?[J]. J Voice, 2017, 31(3): 380.e11-380.380.e14. |




