我国西部地区3 000 m以上高原接近250万平方公里,主要集中在青藏高原,高原地区的社会和经济活动日益繁荣,为广大高原居民、开拓者、旅游观光人员等提供良好的医学保障显得十分重要。高原环境影响人体的主要因素是缺氧,高原低氧对机体的功能和代谢产生一系列的影响,还可以直接引起急性高原病(acute mountain sickness,AMS),而脑是对缺氧敏感的组织,高原脑水肿是一种潜在致命危险的综合征,也是急性高原病中的危重症之一,发病率占高原病的3%左右且死亡率高,多发生在海拔4000 m以上的地区[1-3]。
多项研究证实,高海拔造成急性脑氧合减少可能是AMS的主要原因[4-5],脑组织氧合的实时监测对防止AMS非常重要。目前脑氧合监测主要有创与无创两种方式,有创监测主要通过有创操作直接检测颈静脉球氧饱和度、脑组织氧分压、动静脉血氧饱和度等,但因其有创、操作复杂只能用于术中或ICU危重症患者。近年来由近红外光谱(near-infrared spectroscopy,NIRS)技术衍生的无创脑氧饱和度(regional cerebral oxygen saturation,rcSO2)监测逐渐应用于临床[6-7],因其连续、无创、操作简单等优点已广泛应用于ICU、手术麻醉中。有研究表明rcSO2的降低与AMS症状评分之间呈正相关,NIRS脑氧监测技术对AMS的诊断和治疗具有重要价值[5]。INVOS 5100C是美国美敦力公司生产的NIRS脑氧仪,过去的研究发现INVOS对检测脑缺氧事件更敏感[8];目前国内相继有公司研发了NIRS脑氧仪,如EGOS-600(苏州爱琴)、MNIR-P100(重庆名希)、BRS-1(北京中科博锐)。这4种仪器均采用NIRS技术,其检测的最大理论海拔高度均为3 000 m,而一旦超过该海拔高度,这些仪器的使用状况如何尚不清楚。此外,这4种仪器使用近红外光波长的数量、发射光的强度、光检测器的灵敏度、光发射器和光检测器之间的间隔、加权动脉-静脉血液比率和计算算法、正常值范围等方面也各不相同,3种国产仪器与美敦力相比的检测效果如何尚不清楚。由于目前缺乏rcSO2算法的金标准[9-12],临床上rcSO2检测结果的准确性无法直接进行对比。
本研究通过将EGOS-600、MNIR-P100和BRS-1等3种国产品牌与美敦力的INVOS 5100C进行对比研究,评价4种近红外脑氧仪在平原和模拟4 500 m高海拔环境中的检测效果,旨在探讨超过3 000 m的高原环境下rcSO2监测仪的检测效果以及国产与进口品牌之间的性能差异,这将为3 000~4 500 m高原环境下rcSO2监测仪的使用选择,以及国产rcSO2监测仪的品质提升和推广应用提供理论依据。
1 资料与方法 1.1 一般资料 1.1.1 仪器设备本研究将试验地点所处海拔高度(约300 m)定义为平原海拔高度,采用贵航集团设计建造的低压氧舱减压至57.7 kPa模拟4500 m海拔高度,维持舱内温度22~26 ℃。选用在国内上市的INVOS 5100C、EGOS-600、MNIR-P100和BRS-1等4种近红外脑氧仪对受试者进行无创rcSO2监测,采用多参数标准监护仪(深圳迈瑞,型号PM9000)测量受试者的BP、HR、SPO2等生命体征。
1.1.2 受试者选择本研究为前瞻性队列研究,2021年3月3~16日共招募到陆军军医大学18~22岁174名健康志愿者,其排除标准为:①既往有严重高原反应史;②近期严重上呼吸道感染。③有严重的心肺疾病、精神疾病等。试验过程中出现危及受试者健康甚至生命的严重情况或受试者要求退出试验则试验中止。将所有受试者随机分为6组,12名因高原环境不适中途退出,11名因传感器脱落等其他原因未收集到有效数据。最终纳入151名身高(172.8±4.5)cm,BMI(22.55±2.22)kg/m2的男性健康志愿者。受试者对研究内容知情,签署知情同意书。本研究经陆军军医大学第二附属医院伦理委员会审批同意(2021-研第017-01)。
1.2 研究方案 1.2.1 样本量估算过程使用Bland-Altman方法进行一致性评价,目前尚无公认的样本量计算方法,Bland-Altman方法的创始人BLAND和ALTMAN本人也只是经验性地推荐认为其样本量不应少于100例[13],本文采用基于Monte-Carlo模拟的方法计算样本量[14],公式如下:
受试者在进入低压氧舱前,休息10 min后在安静环境及坐姿状态下,在平原(300 m)按照随机序列分别使用4种脑氧仪检测每位受试者的rcSO2,此测量值为基线rcSO2。并且采用多参数监护仪检测同一时刻受试者的SpO2、HR、BP,同时还记录无创脑氧仪的检测成功率、响应时间等数据。完成平原检测后受试者进入低压氧舱,减压至海拔4 500 m高度气压3 h后,在受试者静息状态下再次按照随机顺序分别使用4种脑氧仪进行无创rcSO2检测,记录无创脑氧仪的检测成功率、响应时间等数据。监测并记录受试者的生命体征。检测时无创血压袖带置于受试者的左上臂测量血压,右手食指监测SpO2及HR。用酒精棉签消毒受试者前额皮肤后,将rcSO2监测仪探头置于眉弓上方,并将探头完全避光,检测部位进行清洁并避免强光照射,操作严格按照设备说明书和临床常规使用方法进行。
1.3 评价指标与分析 1.3.1 仪器响应时间参照通用的仪器响应时间定义[15],本研究其规定为传感器固定在受试者前额开始采集信号起,至仪器最终达到稳定监测值时所需的时间间隔。
1.3.2 反映脑缺氧的一致性比较参照TOMLIN等[16]的方法,当受试者rcSO2测量值降低超过rcSO2基线值的20%,或受试者rcSO2测量值小于绝对值的50%时,则认为受试者发生了脑缺氧。采用配对χ2检验,以进口的美敦力INVOS 5100C作为标准,比较其他3种无创脑氧仪模拟高原环境下rcSO2检测值反映脑缺氧受试者的差异。
1.3.3 一致性比较 1.3.3.1 rcSO2测量值的一致性由于每种仪器的测量范围不同,无法直接进行测量值的一致性比较,需要将数据标准化后进行数据分析。公式为z=(X-μ)/σ,其中X-μ为离均差,σ表示标准差。采用Bland-Altman方法,以美敦力INVOS 5100C的rcSO2作为基准,分别进行平原和模拟4 500 m高海拔时rcSO2测量值的一致性分析。
1.3.3.2 rcSO2值下降幅度的一致性为对比研究4种仪器检测受试者从平原至模拟高原环境时rcSO2值下降幅度的一致性,以INVOS 5100C的rcSO2下降百分比作为标准,即△rcSO2(%)=(平原rcSO2-高原rcSO2)/平原rcSO2×100%,采用Bland-Altman方法[17],将其他3种国产脑氧仪的△rcSO2(%)与INVOS 5100C的△rcSO2(%)做一致性分析。
1.4 统计学方法采用SPSS 25、MedCalc 19.0.7软件进行统计学分析。计量资料以x±s表示,正态分布连续变量对比采用t检验、方差分析,非正态分布数据采用非参数检验;相关性采用Pearson检验;率的比较采用χ2检验,当数据不符合χ2检验要求时,采用基于Monte Carlo的Fisher’s确切概率法。使用配对χ2(McNemar’s test)检验[16]评估设备之间在检测rcSO2的显著差异。一致性比较采用Bland-Altman方法。P < 0.05认为有统计学意义。
2 结果 2.1 近红外脑氧仪器性能参数与适用的海拔高度4种脑氧仪均能连续监测,INVOS 5100C、EGOS-600和MNIR-P100等2种仪器的探测深度相同,而BRS-1的探测深度稍浅,EGOS-600和BRS-1使用的近红外光波长和数量完全一致,但二者的测量范围和rcSO2正常值范围却有所不同;4种仪器使用的近红外光波长、数量、传感器光源和探测器之间距离以及算法等各有不同。根据4种近红外脑氧仪的说明书,EGOS-600和MNIR-P100和BRS-1等3种国产仪器理论的最高适用海拔高度均为3 000 m,而进口的INVOS 5100C的最高适用海拔高度为3 048 m。可见,这4种近红外脑氧仪理论的最高适用海拔高度都在3 000 m左右,详见表 1。
| 近红外脑氧仪 | INVOS 5100C | EGOS-600 | MNIR-P100 | BRS-1 |
| 检测原理 | NIRS | NIRS | NIRS | NIRS |
| 监测方式 | 连续 | 连续 | 连续 | 连续 |
| 使用波长/nm | 730、810 | 760、810、840 | 730、850 | 760、810、840 |
| 传感器光源与探测器距离 | 30 mm和40 mm | 30 mm和40 mm | 30 mm和40 mm | 20 mm和30 mm |
| rcSO2正常值范围(%) | 58~82 | 58~68 | 60~85 | 58~82 |
| 测量范围 | 15~95 | 0~100 | 0~100 | 50~90 |
| 仪器通道数 | 4 | 4 | 2 | 6 |
| 理论适用海拔高度范围/m | 0~3 048 | 约-350~3 000a | 约-400~3 000a | 约-400~3 000a |
| 理论适用温度范围/℃ | 16~32 | 5~40 | 5~40 | 0~40 |
| 理论适用气压范围/hPa | … | 670~1 060 | 700~1 060 | 700~1 060 |
| a:根据气压换算结果 | ||||
2.2 4种近红外脑氧仪在高海拔环境的响应时间及检出成功率
4种近红外光谱脑氧仪在平原和模拟海拔4 500 m环境中检测成功率均为100%。INVOS 5100C、EGOS-600、MNIR-P100、BRS-1在平原响应时间分别为(2.13±0.34)、(6.60±1.23)、(2.87±0.48)、(2.65±0.47)s,在高原响应时间分别为(2.22±0.41)、(6.83±1.25)、(2.86±0.49)、(2.67±0.49)s,EGOS-600的响应时间较其余3种仪器平均延长3 s以上(P < 0.05)。在4500 m海拔环境下,MNIR-P100和BRS-1的响应时间与平原环境相比变化不明显,二者差异无统计学意义(P>0.05),而INVOS 5100C和EGOS-600的响应时间相对于平原环境略有增加(P < 0.05),详见表 2。
| 仪器品牌 | 平原(海拔300 m) | 高原(海拔4 500 m) | P |
| INVOS 5100C | 2.13±0.34 | 2.22±0.41 | 0.000 1 |
| EGOS-600 | 6.60±1.23 | 6.83±1.25 | <0.000 1 |
| MNIR-P100 | 2.87±0.48 | 2.86±0.49 | 0.565 4 |
| BRS-1 | 2.65±0.47 | 2.67±0.49 | 0.318 9 |
2.3 4种近红外脑氧仪在平原及高海拔环境的一致性分析及不同设备测量rcSO2差异
由于每种仪器检测的正常值范围不同,通常将rcSO2相对于基线下降超过20%或rcSO2绝对值<50%定义为脑缺氧。模拟4 500 m高原环境下,脑氧仪设备检测到一定的rcSO2严重下降的受试者数量。当INVOS 5100C达到了相对于基线20%的下降阈值时,EGOS-600、MNIR-P100、BRS-1分别有78.1%、94.7、76.1%的受试者未到该下降阈值;当INVOS 5 100C未达到相对于基线20%的下降阈值时,EGOS-600、MNIR-P100、BRS-1分别有1%、0%、1%的受试者达到该下降阈值;当INVOS 5100C的rcSO2测量值低于50%的绝对阈值时,EGOS-600、MNIR-P100、BRS-1分别有52.9%、54.6%、54.3%未达到该绝对阈值;当INVOS 5100C的rcSO2测量值高于50%的绝对阈值时,其余3种国产仪器rcSO2测量值低于50%的绝对阈值的发生率均为0%;且P值均小于0.000,差异有统计学意义。
将3种国产脑氧仪测量结果与INVOS5100进行一致性分析。Bland Altman图分析表明,平原rcSO2测量值与INVOS 5100C相比,EGOS-600、MNIR-P100、BRS-1的相对百分比偏差分别为0.5、-0.7、0.2,一致性界限分别为(-3.4~4.5)、(-2.7~1.4)、(-1.9~2.2),见图 1。高原rcSO2测量值与INVOS 5100C相比,EGOS-600、MNIR-P100、BRS-1的相对百分比偏差为1.4、2.4、2.2,一致性界限为(-1.4~4.2)、(0.6~4.1)、(-0.4~4.9),见图 2。可见,无论是平原还是模拟4 500 m海拔高度,3种国产脑氧仪与美敦力INVOS 5100C的rcSO2检测值都具有较好的一致性,但随海拔升高与INVOS 5100C的rcSO2测量值相对百分比偏差稍增大。在平原(300 m)环境下,BRS-1和INVOS 5100C的rcSO2测量值一致性较EGOS-600和MNIR-P100更好,在模拟4 500 m海拔高度,EGOS-600和INVOS 5100C的rcSO2测量值一致性较BRS-1和MNIR-P100更好。

|
| A: 爱琴与美敦力; B: 名希与美敦力; C: 中科博锐与美敦力 图 1 在平原(300 m)美敦力和3种近红外脑氧仪测量rcSO2一致性分析 |

|
| A: 爱琴与美敦力; B: 名希与美敦力; C: 中科博锐与美敦力 图 2 在模拟海拔高度(4 500 m) 美敦力和3种近红外脑氧仪测量rcSO2一致性分析 |
受试者从平原上升至模拟4 500 m高海拔环境后,其rcSO2值会下降,但每种仪器针对同一受试者rcSO2测量值及下降幅度各不相同。从平原至4 500 m高海拔环境后,与INVOS 5100C相比,EGOS-600、MNIR-P100、BRS-1的rcSO2测量值下降百分比偏差分别为-21.5、-24.7、-19.8,一致性界限分别为(-41.4~-1.9)、(-39.9~-9.4)、(-41.4~1.8),详见图 3。可见,上升至4 500 m高海拔环境后,3种国产仪器与INVOS 5100C的rcSO2测量值下降幅度百分比一致性较差,其中BRS-1的一致性结果比EGOS-600、MNIR-P100更好。

|
| A:爱琴与美敦力; B:名希与美敦力; C:中科博锐与美敦力 图 3 INVOS 5100C和3种近红外脑氧仪测量rcSO2平原至高原相对基线下降百分比的一致性分析 |
2.4 4种近红外脑氧仪测量rcSO2与SpO2的相关性分析
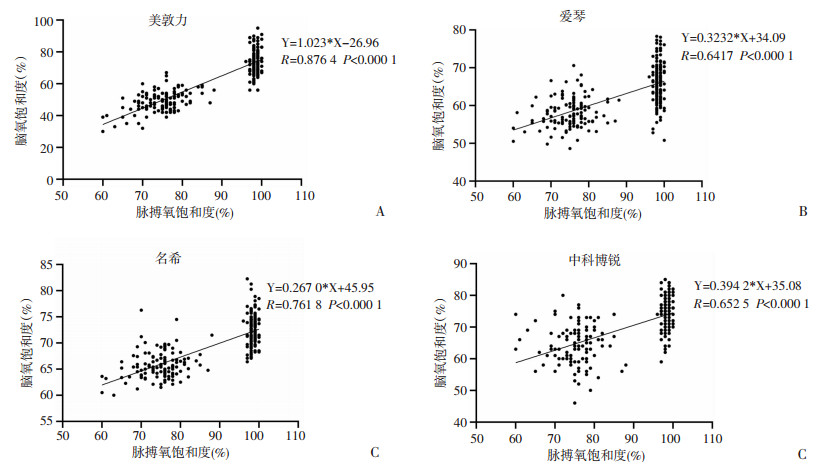
INVOS5100、EGOS-600、MNIR-P100与BRS-1测量的rcSO2与SpO2相关性系数为0.876 4(P < 0.000 1)、0.641 7(P < 0.000 1)、0.761 8(P < 0.000 1)、0.652 5(P < 0.000 1),详见图 4。
|
| A: 美敦力; B: 爱琴; C: 名希; D: 中科博锐 图 4 脑氧饱和度与脉搏氧饱和度的相关性分析 |
3 讨论
我国西藏地区平均海拔3 000 m以上,平均气压<0.07 MPa,冬季寒冷-20~-30 ℃、干燥,相对湿度低于20%;夏季潮湿,相对湿度>95%。因此在高海拔、低气压的环境影响下,医疗设备的各种性能可能会下降,使用寿命也会缩短[18]。NIRS技术衍生的脑血氧定量法是目前唯一的非侵入式床旁rcSO2监测技术,其脑氧仪体积小,便携性高,能实现无创、实时、连续、定量监测人体脑组织的氧合状况,能够在高海拔环境中提供有效的医疗卫生保障[19]。相关文献表明rcSO2是AMS的客观评价指标[4-5],但未发现近红外脑氧仪在高原环境下的对比应用研究;因此我们选用4种常用近红外脑氧仪对比在高原环境下的检测效果。
本研究结果显示,4种近红外脑氧仪规定适用的最高海拔高度均在3 000 m左右。本研究模拟4 500 m高海拔环境,结果显示4种仪器能够成功检测rcSO2,且rcSO2测定值与SpO2均有良好的相关性[20-21],能够反映高原低氧环境下rcSO2的变化。无论在平原还是在模拟4 500 m的高海拔环境,4种脑氧仪的检测成功率均为100%。EGOS-600的响应时间较长,原因可能是本次受试者均为男性,皮肤油脂较多影响EGOS-600传感器的感应。在模拟4 500 m海拔环境下,INVOS 5100C和EGOS-600的响应时间比平原分别增加了平均约0.1 s和0.2 s。我们进一步将rcSO2数据进行Z-score标准化,应用bland-altman法检验其一致性,结果显示3种国产仪器与INVOS 5100C的标准化rcSO2之间一致性较好。
目前麻醉指南[22]将脑缺氧通常定义为相对于基线下降20%或rcSO2绝对值为50%。本研究表明,当INVOS 5100C的rcSO2测量值下降达到了20%的相对下降阈值时,EGOS-600、MNIR-P100、BRS-1分别有78.1%、94.7%、76.1%的受试者未达到此标准;当INVOS 5100C的rcSO2测量值下降达到50%的绝对阈值时,EGOS-600、MNIR-P100、BRS-1分别有52.9%、54.6%、54.3%的受试者未达到该标准。结果表明当外界环境导致rcSO2下降时,INVOS 5100C能更早地监测到rcSO2下降,灵敏度更佳。而采用rcSO2为50%的绝对阈值作为缺氧标准,3种国产仪器反映脑缺氧的发生率很接近;而当INVOS 5 100C的rcSO2测量值未达到此缺氧标准时,其余3种国产仪器也同样未达到,这说明以rcSO2为50%的绝对阈值作为缺氧标准时,4种仪器的rcSO2测量值反映脑缺氧具有良好的特异性。
本研究仍存在不足:①受限于试验条件,未直接采集动脉和静脉血来计算加权饱和度,以此作为“金标准”与rcSO2值进行对比研究;②受试者均为20岁左右的男性,而老年、婴幼儿和女性人群在高原环境rcSO2的检测结果可能存在一定的差异;③本研究采用模拟的海拔高度,未能反映实际高原条件下温差和湿度等因素对仪器使用的影响,但能反映在手术室等恒温、封闭环境下的使用,未来我们将会进一步测试仪器在高原室外的使用情况,为其在高海拔地区的应用提供理论依据;④所有仪器在模拟高海拔环境下使用的时间只有数小时,不能反映实际工作中仪器长时间使用的状态。
综上所述,4种脑氧仪在4 500 m高海拔环境下对rcSO2监测都具有一定的实用价值,以rcSO2为50%的绝对值为脑缺氧判断标准更具特异性,在反映脑缺氧的敏感性上,INVOS 5100C可能比其他3种仪器更好。4种仪器在4 500 m高原环境下长期使用的稳定性如何还需进一步研究。
| [1] |
高钰琪, 黄庆愿, 刘福玉, 等. 促进高原习服措施的研究进展[J]. 解放军预防医学杂志, 2002, 20(4): 306-309. GAO Y Q, HUANG Q Q, LIU F Y, et al. Research progress on measures to promote acclimatization at high altitude[J]. J Prev Med Chin, 2002, 20(4): 306-309. |
| [2] |
吴世政. 高原脑科学研究进展[J]. 高原医学杂志, 2019, 29(1): 47-53. DOI: CNKI:SUN:GYYZ.0.2019-01-010. WU S Z. Research progress of high altitude brain[J]. J High Alt Med, 2019, 29(1): 47-53. DOI: CNKI:SUN:GYYZ.0.2019-01-010. |
| [3] |
廉国锋, 李锏, 罗勇军, 等. 高原脑水肿发病机制及防治研究进展[J]. 人民军医, 2020, 63(4): 343-346, 357. DOI: CNKI:SUN:RMJZ.0.2020-04-013. LIAN G F, LI J, LUO Y J, et al. Research progress on the pathogenesis and prevention of high altitude cerebral edema[J]. People Mil Surg, 2020, 63(4): 343-346, 357. DOI: CNKI:SUN:RMJZ.0.2020-04-013. |
| [4] |
IMRAY C H, CLARKE T, FORSTER P J, et al. Carbon dioxide contributes to the beneficial effect of pressurization in a portable hyperbaric chamber at high altitude[J]. Clin Sci (Lond), 2001, 100(2): 151-157. |
| [5] |
HADOLT I, LITSCHER G. Noninvasive assessment of cerebral oxygenation during high altitude trekking in the Nepal Himalayas (2850-5600 m)[J]. Neurol Res, 2003, 25(2): 183-188. |
| [6] |
邱宇, 戚思华. 无创脑氧饱和度监测技术的研究现状[J]. 现代医学, 2019, 47(8): 1045-1048. DOI: CNKI:SUN:TDYX.0.2019-08-034. QIU Y, QI S H. Research status of non-invasive monitoring technology of cerebral oxygen saturation[J]. Mod Med J, 2019, 47(8): 1045-1048. DOI: CNKI:SUN:TDYX.0.2019-08-034. |
| [7] |
刘强, 韩如泉. 脑氧饱和度监测方法及其应用进展[J]. 国际麻醉学与复苏杂志, 2018, 39(3): 234-238. LIU Q, HAN R Q. Advanes in cerebral oxygen saturation monitoring and its application[J]. Int J Anesthesiol Resusc, 2018, 39(3): 234-238. |
| [8] |
BICKLER P E, FEINER J R, ROLLINS M D. Factors affecting the performance of 5 cerebral oximeters during hypoxia in healthy volunteers[J]. Anesth Analg, 2013, 117(4): 813-823. |
| [9] |
SHAH N, TRIVEDI N K, CLACK S L, et al. Impact of hypoxemia on the performance of cerebral oximeter in volunteer subjects[J]. J Neurosurg Anesthesiol, 2000, 12(3): 201-209. |
| [10] |
MURKIN J M, ADAMS S J, NOVICK R J, et al. Monitoring brain oxygen saturation during coronary bypass surgery: a randomized, prospective study[J]. Anesth Analg, 2007, 104(1): 51-58. |
| [11] |
LA COUR A, GREISEN G, HYTTEL-SORENSEN S. In vivo validation of cerebral near-infrared spectroscopy: a review[J]. Neurophotonics, 2018, 5(4): 040901. |
| [12] |
BENNI P B, MACLEOD D, IKEDA K, et al. A validation method for near-infrared spectroscopy based tissue oximeters for cerebral and somatic tissue oxygen saturation measurements[J]. J Clin Monit Comput, 2018, 32(2): 269-284. |
| [13] |
BLAND J M, ALTMAN D G. Applying the right statistics: analyses of measurement studies[J]. Ultrasound Obstet Gynecol, 2003, 22(1): 85-93. |
| [14] |
陆梦洁, 刘玉秀, 缪华章, 等. Bland-Altman一致性评价的样本含量估计[J]. 中国卫生统计, 2015, 32(3): 537-539. LU M J, LIU Y X, MIAO H Z, et al. Estimation of sample size in Bland-Altman consistency evaluation[J]. Chin J Heal Stat, 2015, 32(3): 537-539. |
| [15] |
屈仁超. 光电传感器响应时间的准确测量方法[J]. 电子质量, 2014(4): 64-66. QU R C. Accurate measurement of photoelectric sensor response time[J]. Electron Qual, 2014(4): 64-66. |
| [16] |
TOMLIN K L, NEITENBACH A M, BORG U. Detection of critical cerebral desaturation thresholds by three regional oximeters during hypoxia: a pilot study in healthy volunteers[J]. BMC Anesthesiol, 2017, 17(1): 6. |
| [17] |
GERKE O. Reporting standards for a bland-Altman agreement analysis: a review of methodological reviews[J]. Diagnostics (Basel), 2020, 10(5): E334. |
| [18] |
向小燕. 浅谈高原环境对医疗设备的影响[J]. 西藏医药, 2020, 41(4): 150-151. DOI: CNKI:SUN:YLZB.0.2003-10-036. XIANG X Y. Effects of medical equipment in plateau environment[J]. Tibet Med, 2020, 41(4): 150-151. DOI: CNKI:SUN:YLZB.0.2003-10-036. |
| [19] |
阿祥仁, 赵生秀, 赵文君. 我国高原地区POCT临床应用的现况[J]. 中华检验医学杂志, 2014, 37(11): 812-814. A X R, ZHAO S X, ZHAO W J. Clinical application of point-of-care testing in plateau region of China[J]. Chin J Lab Med, 2014, 37(11): 812-814. |
| [20] |
KUSAKA T, ISOBE K, NAGANO K, et al. Quantification of cerebral oxygenation by full-spectrum near-infrared spectroscopy using a two-point method[J]. Comp Biochem Physiol A Mol Integr Physiol, 2002, 132(1): 121-132. |
| [21] |
AINSLIE P N, OGOH S. Regulation of cerebral blood flow in mammals during chronic hypoxia: a matter of balance[J]. Exp Physiol, 2010, 95(2): 251-262. |
| [22] |
于布为, 王国林, 邓小明, 等. 临床麻醉监测指南中国-麻醉学指南与专家共识[M]. 2017版. 北京: 人民卫生出版社, 2017: 168-169. YU B W, WANG G L, DENG X M, et al. Clinical anesthesia monitoring guidelines: chinese anesthesiology guidelines and expert consensus[M]. 2017. Beijing: People's Medical Publishing House, 2017: 168-169. |




