心脏肿瘤中转移性恶性肿瘤最常见,即使在大的心脏中心,原发性心脏肿瘤也少见,尸检系列中原发性心脏肿瘤的发生率为0.02%,其中约75%为良性[1-2]。黏液瘤是原发性良性心脏肿瘤中最常见类型,约占成人良性心脏肿瘤的50%[3],多数发生在左心房,右心房黏液瘤约占心房黏液瘤的7.89%[4]~20%[5]。心脏肿瘤在不同的腔室有其各自不同的特点,分腔室研究具有重大意义。关于右心房肿瘤的大宗报道国内外少见,多为个案报道。因心脏肿瘤总体发病率低,目前尚无合适的循证治疗指南。本文回顾性分析了2009年1月至2021年1月我院心血管外科收治的64例右心房肿瘤患者的临床特点、诊断、外科治疗经验及效果。
1 资料与方法 1.1 患者一般资料本研究纳入了2009年1月至2021年1月收入我院心血管外科的64例右心房占位患者,年龄5~79(47.0±16.4)岁,男性27例(42.2%),女性37例(57.8%)。64例患者中,手术治疗并获得病理学诊断53例,其中右心房黏液瘤36例,其他类型良性右心房占位8例,恶性右心房肿瘤9例;未手术者11例,其中6例临床怀疑右心房黏液瘤可能性大,因患者自身原因放弃手术,5例临床高度怀疑恶性右心房肿瘤或转移瘤未予手术。肿瘤类型见表 1。
| 肿瘤类型 | 例数(%) | 男/女(例) |
| 黏液瘤 | 36(56.2) | 14/22 |
| 怀疑黏液瘤 | 6(9.4) | 6/0 |
| 脂肪瘤 | 3(4.7) | 1/2 |
| 乳头状弹力纤维瘤 | 2(3.1) | 1/1 |
| 海绵状血管瘤 | 1(1.6) | 0/1 |
| 肉芽肿性血管瘤 | 1(1.6) | 1/0 |
| 静脉内平滑肌瘤病 | 1(1.6) | 0/1 |
| 血管肉瘤 | 4(6.3) | 0/4 |
| 低度恶性血管内皮细胞瘤 | 1(1.6) | 0/1 |
| 上皮样血管内皮细胞瘤 | 2(3.1) | 1/1 |
| 恶性孤立性纤维瘤 | 1(1.6) | 1/0 |
| 横纹肌肉瘤 | 1(1.6) | 1/0 |
| 其他恶性肿瘤 | 5(7.8) | 1/4 |
| 总计 | 64 | 27/37 |
以下为本组患者的影像学表现及部分少见类型的病理学资料。
黏液瘤心脏超声(36例):均质或不均质,液化者可见透声暗区,增强或等回声,结构较疏松,活动度大(瘤体小且蒂宽者活动度小),边界清,可呈分叶状,部分病例见血供。常见肿瘤随着心脏收缩舒张经三尖瓣瓣口往返于右心房及右心室之间,造成三尖瓣不同程度梗阻,三尖瓣舒张期流速增快;CT呈低密度影,形态规则或表面不规整,可伴有混杂密度影(钙化、出血、液化、坏死、纤维化等)。肿瘤外观见图 1。

|
| 图 1 右心房黏液瘤(A)、右心房脂肪瘤(B)和静脉内平滑肌瘤病(C)的术中外观所见 |
脂肪瘤心脏超声(3例):增强回声,界限清,宽基底部;CT呈低密度影,3例CT值分别为:-88、-110、-100 HU。肿瘤外观见图 1。
乳头状弹力纤维瘤心脏超声(2例):等回声,结构疏松,活动度较大;CT呈稍低密度影,1例CT值为40 HU,中度强化。
海绵状血管瘤心脏超声(1例):形态规则,界限清,蒂位于房间隔,活动度较大,大小约5.3 cm×3.4 cm,梗阻上腔静脉口;CT肿块密度均匀,CT值约50 HU,增强扫描见少许斑片状强化。
肉芽肿性血管瘤心脏超声(1例):强回声,直径约1.0 cm,位于房隔中下部(术中发现位于下腔静脉瓣上),轻微摆动;肿瘤呈囊实性,切面灰白色。
恶性孤立性纤维瘤心脏超声(1例):形态不规则,界限不清;CT肿块密度不均,内见结节状钙化灶;病理见肿块呈灰白灰红色,质硬,附有包膜,内有钙化灶,梭形细胞肿瘤伴广泛玻璃样变性,大量异形巨核细胞浸润,部分区域见黏液。
上皮样血管内皮细胞瘤心脏超声(2例):稍强回声,形态不规则,内部回声不均质,活动度小,与心房壁关系密切。CT呈低密度,明显强化,见丰富血管影;肿瘤切面呈黄白兼红褐色,伴多灶性出血、坏死。
低度恶性血管内皮细胞瘤心脏超声(1例):增强回声,欠均质,与右心房壁界限不清,无活动性,大量心包积液;病理见大量异形梭形细胞。
血管肉瘤(4例):界限不清,宽基底,活动度小,心包积液;CT呈低密度影,不规则,侵犯右心房壁,不均匀强化。
1.2 方法 1.2.1 手术方法所有患者均在体外循环辅助下完成肿瘤摘除,多数采取胸部正中切口心脏停搏方式,个别患者经右胸前外侧切口或在心脏不停跳下摘除肿瘤。手术过程避免不必要的搬动、碰触心脏,尽早阻断主动脉,心脏灌停后再游离并阻断上下腔静脉,降低肿瘤脱落栓塞风险。选择经上腔静脉插管,一方面避免经右心耳插管可能造成瘤体破碎,另一方面对于肿瘤造成上腔静脉开口狭窄的病例,预留更多的空间以备上腔静脉加宽之需。对于肿瘤延伸至下腔静脉口以远,或肿瘤经下腔静脉来源的病例,经单根上腔静脉或经上腔静脉和股静脉转流常引流不充分,流量不足,则快速降温,在心脏不停跳下,加大心内吸引,迅速摘除下腔静脉内的瘤体后予下腔静脉插管,恢复流量,SvO2>80%开始复温。对合并肺栓塞的病例,尽量靠近无名静脉置入上腔静脉引流管,中低温低流量下作肺动脉切口取出瘤栓。以上操作难度大时可选择短暂深低温停循环。
良性肿瘤主要为黏液瘤,尽可能切除肿瘤蒂部附着处心内膜及周围1.0~1.5 cm正常心肌组织,必要时以补片修补房间隔或房壁。摘除肿瘤后用大量的生理盐水冲洗心腔,氩气刀适当灼烧蒂部附着处,以降低种植复发概率。肿瘤附着于三尖瓣瓣体者,剥离后如造成瓣叶较大面积缺失,可选择自体心包片或牛心包补片修补。肿瘤梗阻三尖瓣瓣口,大多不影响瓣叶结构,而造成瓣环扩张,可予三尖瓣环缩成形或置入合适的三尖瓣成形环。撤离体外循环前常规经食道超声探查有无多发或残余瘤体,探查三尖瓣的对合及反流情况,上、下腔静脉有无残余梗阻。
恶性肿瘤患者以保证手术安全为基础,尽可能扩大切除范围,以自体心包片或人工材料修复心房壁、血管壁及瓣膜,不可盲目追求所谓“根治切除”而造成不可控制的大出血、损伤重要结构或转机时间过长。
1.2.2 观察指标总结64例右心房肿瘤患者的肿瘤类型特征、年龄分布、性别比例、临床表现、术前合并症、手术死亡率、术后并发症、复发及转移情况等。
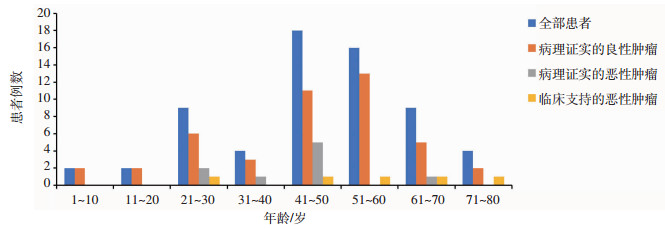
2 结果 2.1 年龄分布及临床特点本组64例患者年龄分布见图 2;总体良性肿瘤占比78.1%,恶性肿瘤占比21.9%;手术组良性肿瘤占比83.0%,恶性肿瘤占比17.0%。获得病理学诊断的患者中,黏液瘤占良性肿瘤的67.9%,血管肉瘤占恶性肿瘤的44.4%。良、恶性肿瘤患者年龄均集中在41~60岁区间,均更倾向于发生在女性患者。最常见的临床症状前三位依次为疲乏(53.1%)、胸闷胸痛或心前区不适感(26.6%)、面部或下肢水肿(9.4%),其他临床表现还有咳嗽咳痰、咯血、晕厥、发热、贫血、腹痛等,15.6%的患者无明显症状,仅于体检时发现。术前合并症情况:房颤/房扑5例(7.8%),肺栓塞3例(4.7%),脑梗1例(1.6%)。
|
| 图 2 64例右心房肿瘤患者年龄分布 |
2.2 手术结果及随访情况
总体住院死亡率为3.1%(2例),手术患者的住院死亡率为1.9%(1例)。2例死亡患者分别为:1例恶性右心房肿瘤患者术前死亡;1例右心房血管肉瘤患者术后第2天死于低心排综合征。术后无其他患者发生严重器官功能衰竭、严重感染、再次开胸、新发栓塞等事件。
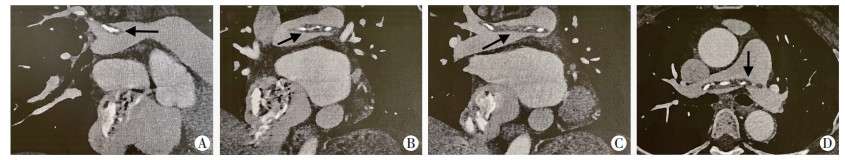
手术治疗的良性肿瘤患者多预后良好。1例海绵状血管瘤患者肿瘤摘除后术中经食道超声探查上腔静脉口流速超过1.5 m/s,测中心静脉压25 mmHg,予再次阻断主动脉,以牛心包补片加宽上腔静脉近端,患者恢复良好。1例右心房黏液瘤患者,术前CT提示肺栓塞(图 3),手术残留下腔静脉远端(约右肾静脉汇入层面至双侧髂静脉区)瘤栓无法取出,予抗凝治疗。1例右心房脂肪瘤患者术前为房扑心律,肿瘤与上腔静脉入口、窦房结区、主动脉后壁关系密切,剥离后以牛心包补片修补右心房顶及上腔静脉侧壁,术后患者反复发作快心室率房扑并伴有临床症状,观察2月后无改善,于心内科行经导管射频消融术。1例静脉内平滑肌瘤病合并房间隔缺损患者,同期先行全子宫、双侧附件、盆腔包块切除术,继之胸部正中切口开胸,分别作下腔静脉起始部、右心房、肺动脉切口,因肿瘤质地较坚韧,表面附有内皮或内膜,小心分离并拖拽出全长肿瘤条索(图 1),术后随访三尖瓣轻至中度反流。1例右心房脂肪瘤及2例右心房黏液瘤患者术后随访三尖瓣中至重度反流,三尖瓣反流压差均在30~40 mmHg间,综合评估目前尚不需再次手术干预。转移性复发2例。其中1例为36岁女性患者,初发为右心房黏液瘤,心脏CT肿块内可见增粗扭曲血管影,术后3年发现左心房内占位,直径约3.2 cm×2.2 cm,黏液瘤可能性大,患者目前尚未接受再次手术的治疗建议。另1例同为女性黏液瘤患者,无家族史,21岁时外院行左心房黏液瘤切除及二尖瓣机械瓣置换术,25岁时于我科接受第二次手术,术中见两处肿块,右心房内肿块蒂部位于右心房后下侧壁,右心室内肿块蒂部位于右心室游离壁,27岁时于随访中发现左心房内复发,并于我科接受第三次手术切除。其所有肿块病理结果均为黏液瘤。末次心脏手术同年,此患者于我院整形科行全身皮肤多处包块切除术,病理检查均考虑黏液瘤。目前患者恢复良好。
|
| A、B、C、D:不同切面右心房占位及从肺动脉分叉处至右肺上叶尖后段肺动脉分支的充盈缺损(箭头示栓塞) 图 3 右心房黏液瘤合并肺栓塞的CT影像学表现 |
恶性肿瘤患者总体预后不良。本组手术治疗的9例恶性右心房肿瘤患者,1例术后早期死亡,余患者无手术早期严重并发症。6例行完整切除的患者在术后半月到2年7个月间发现转移灶,最常见的转移部位为肺,其次为肝、骨;其中同时伴有心脏原位复发者2例。1例右心房血管瘤部分区域恶变——血管肉瘤,患者行姑息性切除手术,生存至1年后失访。1例病理结果为未分化肉瘤或横纹肌肉瘤患者右心房右心室多处肿块,最大者位于三尖瓣隔瓣上,摘除后以自体心包片修补隔瓣,术后在院复查三尖瓣轻到中度反流,患者因自身原因拒绝后续治疗。
3 讨论右心系统肿瘤的恶性比例高于左心系统,在本研究中原发性良性肿瘤仍占据右心房肿瘤的较大比例,因门诊收治患者入外科病区时已排除一部分转移瘤和无手术意愿、无手术机会的恶性肿瘤患者,可能对本研究的肿瘤构成比造成一定影响。黏液瘤发生在右心房少见,但仍是良性右心房肿瘤中最常见的类型,其发生自心内膜下瘤前体细胞,组织学上包含了多角形细胞和多潜能间叶细胞[6-7]。约10%有家族史并为常染色体显性遗传[8]:Carney’s综合征——一种神经内分泌心脏综合征,其特征为:①家族性复发性黏液瘤;②色素性皮肤病变,神经鞘瘤和多发性复发性皮肤黏膜黏液瘤;③内分泌功能亢进和肿瘤[5]。本组1例年轻女性患者多次复发,且多发皮肤黏膜黏液瘤,但无明确家族史,无神经内分泌系统病变。右心房黏液瘤较小时常无临床症状,患者常于体检或治疗其他疾病时偶然发现,出现临床症状者瘤体通常已较大,在本组接受手术的患者中,瘤体最大径超过5.0 cm的占比63.9%。临床表现常为非特异性全身症状,可能系全身性栓塞细胞碎片或白细胞介素-6造成的炎症反应引起[8-9]。本组黏液瘤患者有1例术前发生了肺栓塞,1例有短暂晕厥史。目前普遍认为其一经确诊即应考虑手术,以避免栓塞、血流动力学障碍等严重并发症发生,尽早手术同样可以保护右心功能、阻止右心扩张及肺动脉高压的进展,从而也保护了三尖瓣的功能及窦性心律的维持。右心房黏液瘤的蒂部最常位于房间隔特别是卵圆窝处,也可位于右心房的任何位置如冠状静脉窦附近、下腔静脉口附近、右心房壁,少数位于三尖瓣瓣叶或瓣环上。其复发被认为与肿瘤多生长点、手术的不完全切除、肿瘤碎片的播散种植、家族性黏液瘤、异常的DNA倍体等有关,文献报道的心脏黏液瘤复发率为1%[10],本组右心房黏液瘤复发率为5.6%,均为异位复发。尽管目前对其具体的切除范围有争议,我们仍在不损伤重要结构的前提下尽可能切除肿瘤附着处心内膜及周围一部分正常心肌组织,以期降低原位复发风险。
脂肪瘤在良性心脏肿瘤中发生率仅次于黏液瘤[11],由成熟脂肪细胞构成,且含有周围结缔组织成分,常有完整包膜,倾向生长于右心房及左心室[3]。脂肪瘤放射密度低,CT值约-50~-150 HU,可帮助术前鉴别。心内脂肪瘤较小时常无症状,生长较大时可导致心律失常或心脏流入道、流出道梗阻[12],有症状者考虑手术切除。乳头状弹力纤维瘤常见于老年患者,肿瘤主要累及瓣膜,倾向于发生在左心系统,体积通常较小,质脆,易发生肿瘤部分脱落或附着的血栓脱落而引起栓塞,遂建议发现即应手术,本组的两例分别为76岁及79岁,肿瘤直径均在2.0~3.5 cm间,紧邻三尖瓣。心脏血管瘤的发病率很低,约占原发心脏肿瘤的2.8%,多生长于心室,其特征为血管内皮细胞良性增殖,冠状动脉CT血管造影约有1/3的患者可呈现特异性肿瘤染色现象(tumor blush)[13]。海绵状血管瘤常发生于心外膜,其次为心内膜,也可位于心瓣膜上,位于心内的海绵状血管瘤常见于右心系统[14],其特征是薄壁而扩张的血管[15]。肉芽肿性血管瘤又称化脓性肉芽肿、毛细血管扩张性肉芽肿,发生在心脏的报道极少,本组的这例患者入院前一年因发热咳嗽诊断为肺结核并予抗结核治疗,入院前2周再次出现发热,行心脏超声检查发现右心房占位,二者是否有关系目前尚不清楚。
上皮样血管内皮细胞瘤一般发生在肝、肺、四肢的皮肤及软组织,发生于心脏极罕见,好发于右心房[16],低度恶性,有潜在转移能力。血管内皮细胞瘤分为血管肉瘤和中间型(低度恶性),血管肉瘤是最常见的原发恶性心脏肿瘤亚型,约占其1/3[2],常生长于右心房室沟并侵及右心房壁及心包,可表现为心包积液致心包填塞、腔静脉梗阻或右心衰等相关症状,不经治疗的生存期仅6到9月[17]。恶性心脏肿瘤仍是目前治疗的难题,当没有转移或仅存在有限转移时,完整的切除是改善预后的唯一积极影响因素,可延长中位生存期[18-19]。因右心系统肉瘤早期常无症状或仅表现为非特异性症状,待发现时肿瘤常已较大,且右心系统肉瘤更易发生远处转移,给手术完整切除带来困难[20-21]。即使行完整切除,绝大多数患者仍复发转移而死亡。恶性心脏肿瘤总体的中位生存期约在6到18个月[3, 22],OLIVEIRA等[23]报道的大宗原发恶性心脏肿瘤系列中位生存期为10个月,且心脏肉瘤的生存期更短。对合适的患者采取手术、放化疗、免疫疗法等综合治疗有希望延长患者生存期[24]。本组手术治疗的恶性心脏肿瘤除1例术后早期失访的患者外,62.5%的患者生存期超过10个月;术后有3例接受了放化疗或免疫治疗,生存期超过1年者2例,其中1例恶性孤立性纤维瘤患者生存期超过4年,因例数少,且本组患者均未接受术前新辅助化疗,尚不足以证明综合治疗可显著延长生存期。
综上,本研究右心房肿瘤中良性肿瘤的比例高于恶性,以黏液瘤最多见。良性右心房肿瘤手术效果良好,即使复发,再次手术治疗仍为首选并安全有效。恶性肿瘤患者是否手术治疗,需权衡手术风险及获益,谨慎选择,目的为改善血流动力学、临床症状。
| [1] |
HOFFMEIER A, SINDERMANN J R, SCHELD H H, et al. Cardiac tumors: diagnosis and surgical treatment[J]. Dtsch Arztebl Int, 2014, 111(12): 205-211. |
| [2] |
MCALLISTER H, FENOGLIO J. Tumors of the cardiovascular system[J]. Atlas of tumor pathology, 1978, 1-20. |
| [3] |
BUSSANI R, CASTRICHINI M, RESTIVO L, et al. Cardiac tumors: diagnosis, prognosis, and treatment[J]. Curr Cardiol Rep, 2020, 22(12): 169. |
| [4] |
LI H, GUO H, XIONG H, et al. Clinical features and surgical results of right atrial myxoma[J]. J Card Surg, 2016, 31(1): 15-17. |
| [5] |
SHETTY ROY A N, RADIN M, SARABI D, et al. Familial recurrent atrial myxoma: Carney's complex[J]. Clin Cardiol, 2011, 34(2): 83-86. |
| [6] |
PUCCI A, GAGLIARDOTTO P, ZANINI C, et al. Histopathologic and clinical characterization of cardiac myxoma: Review of 53 cases from a single institution[J]. Am Heart J, 2000, 140(1): 134-138. |
| [7] |
KODAMA H, HIROTANI T, SUZUKI Y, et al. Cardiomyogenic differentiation in cardiac myxoma expressing lineage-specific transcription factors[J]. Am J Pathol, 2002, 161(2): 381-389. |
| [8] |
SAHITYA V, ANANDAM G, SHASTRY S. Right atrial myxoma in a 65-year-old female: a rare presentation[J]. Med J Dr D Y Patil Vidyapeeth, 2018, 11(6): 551. |
| [9] |
YOKOMURO H, YOSHIHARA K, WATANABE Y, et al. The variations in the immunologic features and interleukin-6 levels for the surgical treatment of cardiac myxomas[J]. Surg Today, 2007, 37(9): 750-753. |
| [10] |
BURKE A, TAVORA F. The 2015 WHO classification of tumors of the heart and pericardium[J]. J Thorac Oncol, 2016, 11(4): 441-452. |
| [11] |
KOSHY A N, KOSHY G, HARDIKAR A A. Intracardiac lipoma arising from the papillary muscle[J]. J Card Surg, 2011, 26(1): 65-66. |
| [12] |
SCHREPFER S, DEUSE T, DETTER C, et al. Successful resection of a symptomatic right ventricular lipoma[J]. Ann Thorac Surg, 2003, 76(4): 1305-1307. |
| [13] |
LI W, TENG P, XU H, et al. Cardiac Hemangioma: A Comprehensive Analysis of 200 Cases[J]. Ann Thorac Surg, 2015, 99(6): 2246-2252. |
| [14] |
杨秋蓝, 唐兵, 周晓辉, 等. 心脏海绵状血管瘤的临床表现及外科手术疗效分析[J]. 中华心血管病杂志, 2017, 45(9): 786-790. YANG Q L, TANG B, ZHOU X H, et al. Clinical features and surgical treatment effect of patients with cardiac cavernous hemangioma[J]. Chin J Cardiol, 2017, 45(9): 786-790. |
| [15] |
UNGER E, COSTIC J, LAUB G. Giant cardiac cavernous hemangioma[J]. Ann Thorac Surg, 2015, 100(1): 322-325. |
| [16] |
赵丽红, 王金山, 蒋萍, 等. 心脏和肺上皮样血管内皮细胞瘤一例[J]. 中华肿瘤杂志, 2015, 37(4): 265. ZHAO L H, WANG J S, JIANG P, et al. A case of cardiac and pulmonary epithelioid hemangioendothelioma[J]. Chin J Oncol, 2015, 37(4): 265. |
| [17] |
HERRMANN M A, SHANKERMAN R A, EDWARDS W D, et al. Primary cardiac angiosarcoma: a clinicopathologic study of six cases[J]. J Thorac Cardiovasc Surg, 1992, 103(4): 655-664. |
| [18] |
GALIUT L. The EAE textbook of echocardiography/[M]// The EAE textbook of echocardiography. 1st edition. Oxford University Press, 2011.
|
| [19] |
SIMPSON L, KUMAR S K, OKUNO S H, et al. Malignant primary cardiac tumors: review of a single institutionexperience[J]. Cancer, 2008, 112(11): 2440-2446. |
| [20] |
BOUMA W, LEXIS C P, WILLEMS T P, et al. Successful surgical excision of primary right atrial angiosarcoma[J]. J Cardiothorac Surg, 2011, 6: 47. |
| [21] |
RAMLAWI B, LEJA M J, ABU SALEH W K, et al. Surgical treatment of primary cardiac sarcomas: review of a single-institutionexperience[J]. Ann Thorac Surg, 2016, 101(2): 698-702. |
| [22] |
张羽冠, 沙悦, 程午樱, 等. 以咯血首发右心房血管肉瘤1例[J]. 协和医学杂志, 2014, 5(2): 217-220. DOI: 10.3969/j.issn.1674-9081.2014.02.020. YANG Y G, SHA Y, CHENG W Y, et al. One case report of right atrial angiosarcoma with hemopthsis as first symptom[J]. Med J Peking Union Med Coll Hosp, DOI: 10.3969/j.issn.1674-9081.2014.02.020. |
| [23] |
OLIVEIRA G H, AL-KINDI S G, HOIMES C, et al. Cha- racteristics and survival of malignant cardiac tumors: a 40-year analysis of >500 patients[J]. Circulation, 2015, 132(25): 2395-2402. |
| [24] |
KAKIZAKIA S, TAKAGIB H, HOSAKAC Y. Cardiac angiosarcoma responding to multidisciplinary treatment[J]. Int J Cardiol, 1997, 62(3): 273-275. |




