2. 400038 重庆,陆军军医大学(第三军医大学)基础医学院: 教学实验中心
2. Teaching and Experimental Center, College of Basic Medical Sciences, Army Medical University (Third Military Medical University), Chongqing, 400038, China
瘙痒是一种能引起抓挠欲望的、不愉快的主观感觉。瘙痒是特异性皮炎、湿疹等皮肤病的主要症状之一,也常见于慢性肾衰竭、胆汁淤积、肿瘤、血液病及艾滋病等多种系统性疾病患者[1]。虽然瘙痒引起的抓挠能帮助机体及时有效地减轻或缓解症状,在生理上具有积极的保护作用,但是持续的长时间抓挠会导致皮损和感染,严重影响患者的生活质量。然而目前临床上针对多数类型的瘙痒尚缺乏有效的治疗药物和手段。其原因是对于瘙痒的相关机制、特别是中枢神经机制了解甚少[2]。瘙痒的相关研究在过去较长时间内一直进展缓慢,其中部分可归因于缺乏可靠而敏感的瘙痒动物模型,特别是不同动物对不同致痒剂的瘙痒行为表现似乎存在较大差异,而相关研究对此未给予足够重视。Sprague-Dawley(SD)大鼠作为一种常用的实验动物,其广泛用于各种感觉(如疼痛)神经机制的研究[3],但是迄今关于啮齿类动物如SD大鼠瘙痒模型中不同致痒剂的作用效果的研究报道尚少,已有研究采用的致痒剂种类单一。目前针对大鼠仅报道5-羟色胺皮内注射是诱导急性瘙痒模型较为理想的药物。然而,磷酸组胺一直被认为是人类瘙痒的主要介质,在许多动物模型中都有广泛的应用,在大鼠瘙痒模型中作用如何尚不清楚。因此,本研究采用组胺依赖和非组胺依赖性两类致痒剂,对比检测大鼠在不同种类和不同剂量下诱导致痒的搔抓程度,分析注射部位的感觉神经末梢活动和肥大细胞数量的变化,评价其瘙痒程度。以期为快速建立SD大鼠的瘙痒模型提供重要实验证据,为后续进一步研究瘙痒相关机制并寻找开发有效的抗瘙痒治疗药物提供可靠的模型依据。
1 材料与方法 1.1 实验动物选用3~4月龄的健康雄性SD大鼠240只(陆军军医大学实验动物中心提供)。大鼠于实验前驯养至少3 d,实验前2 d将动物颈部或脸颊(药物注射区)的毛发剃除,所有动物给予自由进食和饮水,饲养环境保持12 h循环光照。
1.2 致痒剂的种类、注射剂量和部位选择两类致痒剂,包括组胺依赖和非组胺依赖性致痒剂。组胺依赖性致痒剂主要包括磷酸组胺(H7250,Sigma公司产品)和化合物48/80(C2313,Sigma公司产品)。非组胺依赖类致痒剂主要包括5-羟色胺(H9523,Sigma公司产品)、氯喹(C6628,Sigma公司产品)和内皮素-1(HY-P0202,MCE公司产品)。上述致痒剂均采用生理盐水配制。注射浓度的设定依据文献[2]和预实验,具体注射浓度见表 1。采用皮内注射,每次注射50 μL,分别选择颈部或脸颊。以生理盐水组(n=40)作为对照。
| 致痒剂类别名称 | 低浓度 | 中浓度 | 高浓度 | |
| 组胺依赖类致痒剂 | ||||
| 磷酸组胺(mmol/L) | 32.5 | 325 | 812.5 | |
| 化合物48/80(mmol/L) | 13 | 65 | 130 | |
| 非组胺依赖类致痒剂 | ||||
| 5-羟色胺(mmol/L) | 5 | 10 | 20 | |
| 氯喹(mmol/L) | 7.7 | 77 | 770 | |
| 内皮素-1(μmol/L) | 2 | 20 | 50 | |
1.3 抓挠行为的检测和分析
采用后肢磁环结合行为记录箱系统,在需要注射致痒剂的同侧后肢套上磁环,SD大鼠放入行为记录箱中预适应15 min,皮内注射致痒剂后,立即将动物放入行为记录箱中记录30 min内的行为变化,结果使用labchart软件记录。如出现抓挠行为则后肢磁环即感应环绕的铜线产生感应电流。感应电流使用差分放大器滤波(3~100 Hz)放大(100×;型号3500,美国A-M System公司) 后,使用生理记录系统(采样频率1 000 Hz;Powerlab 16/35, 澳大利亚AD Instuments公司)记录。记录的数据采用实验室编写的分析软件分析,抓挠和行走、跳跃等运动都会被记录,但是实验室编写的分析软件设定以下原则:①后肢连续运动事件中连续两次的运动最少间隔时间为20 ms, 最长间隔时间为250 ms, ②分析至少连续4次后肢运动事件,其他后爪运动(如行走、跳跃)大多被排除在这些标准之外。在实验过程中同时用高速摄像机拍摄抓挠行为,两个方法获得的结果进行比较具有明显相关性。以一次发作为单位计算,即从后肢抬起接触到致痒剂注射部位开始,到后肢放回到地面或口中为止,整个过程当做一次抓挠,统计抓挠次数。
1.4 致痒区感觉神经末梢电活动记录为了快速观察致痒剂的诱导效果,采用各组致痒剂高浓度皮内注射10 min后,大鼠麻醉后记录局部注射区域中皮肤的感觉神经末梢电活动的变化。采用RM6240E多道生理信号采集处理系统(成都仪器厂)的方法,将记录电极的正极和负极倾斜45°插入注射部位皮内。记录通道模式为生物电,采集频率为10 kHz,扫描速度为20 ms/div(计算机显示波形的扫描速度表示水平方向一个大格代表 20 ms),灵敏度为50 μV,时间常数为0.02 s,滤波频率为3 kHz。共记录15 min电活动。
1.5 致痒区皮下组织肥大细胞染色采用甲苯胺蓝染色的方法,观察各组致痒剂高浓度皮内注射10 min后,剪取少许致痒区皮下结缔组织,均匀地铺在载玻片上,空气中晾干,用0.5%甲苯胺蓝染色1 min,自来水冲洗干净后使用二甲苯透明封片。镜下拍照,图像分析肥大细胞的数量和形态变化。
1.6 统计学分析采用SPSS25.0统计学软件进行分析,大鼠抓挠次数、电活动的峰谷差值、局部电位频率、肥大细胞数量以x±s表示,采用单因素方差分析和两两之间的LSD多重比较。
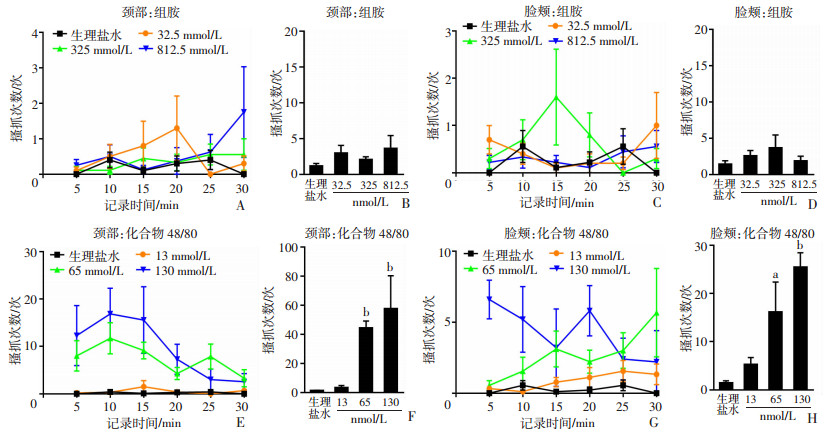
2 结果 2.1 各组抓挠行为分析在组胺依赖性致痒剂各组中,磷酸组胺3个不同浓度(32.5、325、812.5 mmol/L)注射后颈部和脸颊注射区大鼠30 min(每隔5 min分析)的抓挠次数与生理盐水组相比差异无统计学意义(P>0.05,图 1A~D)。中高浓度(65、130 mmol/L)化合物48/80注射后颈部和脸颊注射区大鼠30 min(每隔5 min分析)的抓挠次数较生理盐水组明显上升(P<0.05,图 1E~H),而低浓度(13 mmol/L)化合物48/80注射后颈部和脸颊注射区大鼠30 min总的抓挠次数(每隔5 min分析)与生理盐水组相比差异无统计学意义(P>0.05,图 1E~H)。
|
| A、B:颈部注射磷酸组胺;C、D:脸颊注射磷酸组胺;E、F:颈部注射化合物48/80;G、H:脸颊注射化合物48/80; A、C、E、G: 30 min内不同时间的抓挠次数; B、D、F、H: 总抓挠次数; a:P<0.05,b:P<0.01,与生理盐水组比较 图 1 组胺依赖性致痒剂组在颈部和脸颊注射后大鼠抓挠次数分析(n=40,x±s) |
在非组胺依赖性致痒剂各组中,5-羟色胺3个不同浓度(5、10、20 mmol/L)注射后颈部和脸颊注射区大鼠30 min总的抓挠次数(每隔5 min分析)与生理盐水组相比都明显增加(P<0.05,图 2A~D)。中高浓度(77、770 mmol/L)氯喹注射后颈部和脸颊注射区大鼠30 min总的抓挠次数(每隔5 min分析)较生理盐水组明显上升(P<0.05,图 2E~H),而低浓度(7.7 mmol/L) 氯喹注射后颈部和脸颊注射区大鼠30 min总的抓挠次数(每隔5 min分析)与生理盐水组相比差异无统计学意义(P>0.05,图 2E~H)。中高浓度(20、50 μmol/L) 内皮素-1注射后颈部和脸颊注射区大鼠30 min总的抓挠次数(每隔5 min分析)较生理盐水组明显上升(P<0.05,图 2I~L),而低浓度(2 μmol/L)内皮素-1注射后颈部和脸颊注射区大鼠30 min总的抓挠次数(每隔5 min分析)与生理盐水组相比差异无统计学意义(P>0.05,图 2I~L)。

|
| A、B:颈部注射5-羟色胺;C、D:脸颊注射5-羟色胺;E、F:颈部注射氯喹;G、H:脸颊注射氯喹;I、J:颈部注射内皮素-1;K、L:脸颊注射内皮素-1;A、C、E、G、I、K:30 min内不同时间的抓挠次数;B、D、F、H、J、L:总抓挠次数;a:P<0.05,b:P<0.01,与生理盐水组比较 图 2 非组胺依赖性致痒剂组在颈部和脸颊注射后大鼠的抓挠次数分析(n=40,x±s) |
2.2 各组致痒区感觉神经末梢放电活动变化
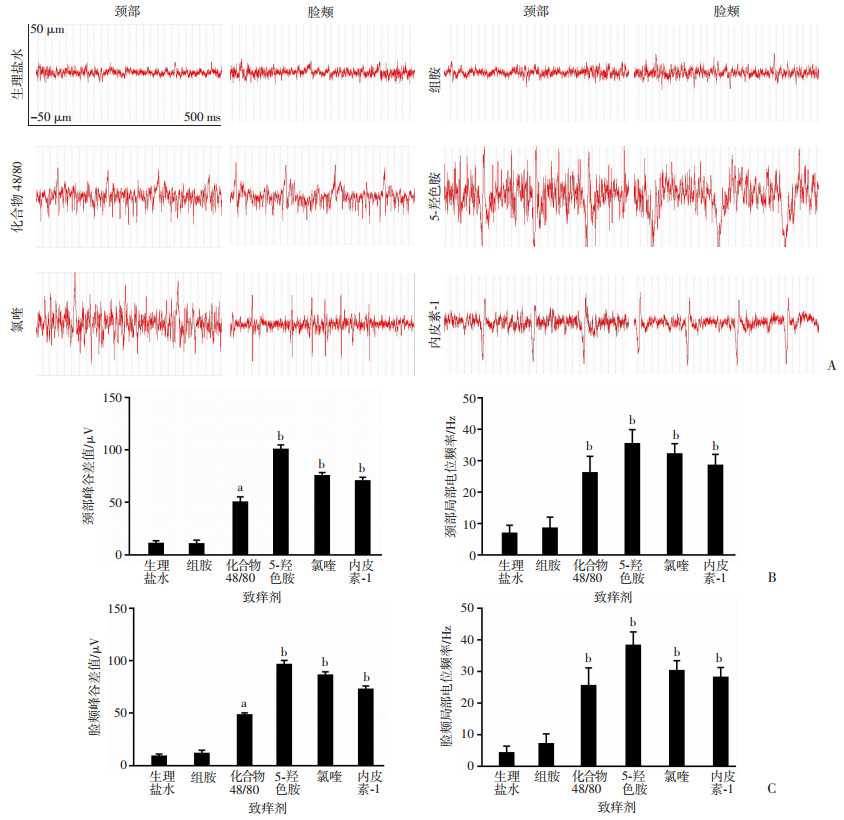
组胺依赖类致痒剂磷酸组胺(812.5 mmol/L)在颈部和脸颊注射区记录到感觉神经末梢电活动波振幅高低变化平缓,峰谷差值仅10 μV,周期性规律性簇发放电较少,局部电位频率较低,与生理盐水组比较差异无统计学意义(P>0.05,图 3A~C)。而化合物48/80(130 mmol/L)在颈部和脸颊注射区记录到感觉神经末梢电活动波振幅增大,峰谷差值>60 μV,呈现周期性规律性簇发放电,局部电位频率明显增多,与生理盐水组比较差异有统计意义(P<0.05,图 3A~C)。
|
| A:颈部和脸颊注射高浓度致痒剂后感觉神经末梢电活动的记录;B:颈部感觉神经末梢电活动峰谷差值和局部电位频率分析;C:脸颊感觉神经末梢电活动峰谷差值和局部电位频率分析;a:P<0.05,b:P<0.01,与生理盐水组比较 图 3 组胺依赖和非组胺依赖类致痒剂组在颈部和脸颊注射后皮下感觉神经末梢电活动的统计分析(n=40,x±s) |
非组胺依赖性致痒剂5-羟色胺(20 mmol/L)、氯喹(770 mmol/L)、内皮素-1(50 μmol/L)均记录到与化合物48/80相似的效应(P<0.05,图 3A~C)。
2.3 致痒区皮下组织肥大细胞分布变化组胺依赖性致痒剂磷酸组胺(812.5 mmol/L) 在颈部和脸颊注射区皮下组织肥大细胞数目较少,与生理盐水相比两者无显著差异(P>0.05,图 4),仅散在分布于组织中及小血管旁。然而组胺依赖性致痒剂化合物48/80(130 mmol/L)、非组胺依赖性致痒剂5-羟色胺(20 mmol/L)、氯喹(770 mmol/L)、内皮素-1(50 μmol/L)在颈部和脸颊注射区皮下组织肥大细胞数目明显增多,与生理盐水组相比差异有统计意义(P<0.05,图 4),多聚集分布于小血管周围,在5-羟色胺颈部注射区皮下可见肥大细胞周边深蓝着色区,提示可能出现脱颗粒现象。

|
| A:甲苯胺蓝染色观察注射高浓度不同致痒剂后肥大细胞形态;B:颈部注射高浓度致痒剂后肥大细胞数目分析;C:脸颊注射高浓度致痒剂后肥大细胞数目分析;a:P<0.05,b:P<0.01,与生理盐水组比较 图 4 不同致痒剂在颈部和脸颊注射后皮下组织中肥大细胞形态及分布(n=40,x±s) |
3 讨论
瘙痒是一种不愉快的多维度的复杂感受或反应,然而目前临床上对大部分瘙痒症状缺乏有效的诊断和治疗方法,对痒觉的生理、病理过程亦不清楚,一个重要的原因是缺乏标准的瘙痒动物模型[5, 8]。颈部和脸颊的皮下组织丰富,对致痒剂敏感性较其他部位好。因此,本研究选这两个区域作为瘙痒建模区[9],同时便于记录到动物后肢的抓挠行为。既往研究动物瘙痒行为主要采用两类方法量化:一是采用摄像机拍摄记录一段时间内动物的全部动作行为,依据录像回放进行抓挠次数统计,这种方法不仅耗时,而且不能观察到潜在被掩盖的抓挠[6]。二是在动物后肢埋置小磁铁,将动物放在四周环绕圆形线圈的观察笼中,通过磁感应电流记录抓挠,但是这种方法需要有创手术,小磁铁的埋置过程可能会并发局部感染、动物不适等,影响抓挠,记录的抓挠次数不具有客观性[7]。本实验采用在注射致痒剂的同侧大鼠后肢套上磁环,磁环与后肢搔抓动作同步运动引发观察笼外壁环绕的铜线产生感应电流,经生理记录系统滤波放大存储后自动记录,由软件对搔抓行为进行离线判读统计。这样既避免了录像回放中的主观判断,又避免了手术创伤,增加了数据分析的客观性,是一种可靠的建模方法。
组胺是较早发现的瘙痒介导物质之一,也是研究最普遍的致痒剂,一直被认为是人类瘙痒的主要介质,已有研究显示组胺引起小鼠的抓挠行为[4]。本研究观察到在颈部和脸颊皮内注射812.5 mmol/L磷酸组胺却不能使大鼠出现对注射部位的抓挠反应。然而,化合物48/80作为组胺依赖性致痒剂,在浓度为65、130 mmol/L时能够诱发大鼠的剂量依赖性抓挠行为。由于磷酸组胺本身不能诱发大鼠的抓挠行为,注射化合物48/80诱导大鼠的抓挠行为并不是通过促进组胺释放发挥作用,推测是通过非组胺依赖机制产生,可能是通过肥大细胞脱颗粒以及肥大细胞独立通路介导的[10],具体的作用机制有待进一步研究。
非组胺依赖的致痒物质包括5-羟色胺、氯喹、内皮素-1等。本研究观察到在颈部和脸颊皮内注射5-羟色胺都可引起大鼠的抓挠反应,与既往的动物实验结果一致[11]。但在人类,皮内注射5-羟色胺仅引起轻微瘙痒。研究证实5-羟色胺虽可促进组胺释放,但其诱导的抓挠行为是通过非组胺依赖机制产生的;大鼠主要是通过5-羟色胺2型受体引起抓挠行为[12]。本研究发现77、770 mmol/L氯喹亦可使大鼠出现对注射部位的抓挠反应。既往研究报道氯喹注射到皮肤可激活Mrgprs家族成员中痒相关的MrgprA3受体[13],但MrgprA3在细胞内的信号传导机制还不清楚。本研究还证实,内皮素-1在2 μmol/L时不引起大鼠的抓挠行为,随着浓度的增加大鼠的抓挠行为逐渐明显。有研究提示,内皮素-1可由皮肤中的肥大细胞、内皮细胞和角质形成细胞产生,是一种强效的瘙痒原,痒相关的ETA受体可介导内皮素-1诱发抓挠[14]。
由于大鼠瘙痒模型中不同致痒剂浓度的设定报道较少,主要参考MU等[2]研究的小鼠致痒剂注射低浓度。其中氯喹是以10倍递增,5-羟色胺则以2倍递增,本研究的目的是建立瘙痒模型,但预实验显示,磷酸组胺和内皮素-1的浓度剂量如按照10倍浓度梯度递增时,高浓度注射区域则出现皮肤溃烂,可导致疼痛发生,将干扰对瘙痒模型的评判。为避免二者叠加,将高浓度下降变为中浓度的2.5倍。化合物48/80浓度梯度递增5倍时也出现皮肤溃烂现象,因此,将高浓度下降变为中浓度的2倍。
大脑感受到瘙痒的过程是由位于真皮乳头层中的瘙痒感受器传导。研究显示痒觉感受器分布于游离神经末梢表面,可以特异性结合不同的致痒因子,产生电信号,从而传递神经冲动[15]。本研究在大鼠颈部和脸颊皮内注射高浓度组胺类和非组胺类致痒剂后,记录到局部感觉神经末梢的电位频率显著增强,其中5-羟色胺注射后电活动峰谷差值较大,提示外周应用5-羟色胺激发的皮肤神经放电涉及瘙痒相关反应较多。但大鼠注射磷酸组胺后电活动的峰谷差值和局部电位频率与生理盐水组相比无明显变化,进一步表明磷酸组胺未引起大鼠瘙痒。此结果与瘙痒-抓挠反应的行为学结果一致。
研究认为瘙痒的发生与肥大细胞脱颗粒相关,如变应性的、物理的、精神的等刺激均导致使肥大细胞释放出致痒相关物质[16]。肥大细胞有很多生理活性,常沿小血管和淋巴管分布,其颗粒内含有嗜酸性粒细胞趋化因子和肝素等,在炎症及免疫应答方面具有重要作用,可引起血管通透性增高、充血、痛和痒[17]。本研究显示,与生理盐水比较,化合物48/80、氯喹、内皮素-1均导致注射区皮下的组织肥大细胞数目上升,分析其原因:①可能是接受刺激后肥大细胞合成颗粒功能增强,染色后显示颗粒数目增多;②可能是血液等相邻部位组织迁移过来,导致聚集分布从而引起皮肤的炎症反应。5-羟色胺导致注射区皮下组织肥大细胞聚集于小血管周围,数目显著增多,并观察到肥大细胞周边脱颗粒现象;而注射磷酸组胺后肥大细胞散在分布,数量没有明显增多,提示磷酸组胺不是大鼠的理想致痒剂。肥大细胞的检测结果进一步支持了本研究的行为学结果。
综上所述,本研究结果为研究瘙痒的神经机制及探讨瘙痒治疗途径供了重要的动物模型资料。组胺依赖性和非组胺依赖性的痒觉神经通路目前尚不清楚,本研究也为采用啮齿类动物进一步探讨中枢神经系统中瘙痒信息的加工奠定了基础。
| [1] |
杨雁, 唐宗湘. 痒觉信号通路与相关受体研究进展[J]. 生物化学与生物物理进展, 2013, 40(3): 209-215. YANG Y, TANG Z X. Research progress of itch signal pathways and related receptors[J]. Prog Biochem Biophys, 2013, 40(3): 209-215. |
| [2] |
MU D, DENG J, LIU K F, et al. A central neural circuit for itch sensation[J]. Science, 2017, 357(6352): 695-699. |
| [3] |
CHA M, LEE K, WON J S, et al. Manganese-enhanced magnetic resonance imaging of the spinal cord in rats with formalin-induced pain[J]. Neurosci Res, 2019, 149: 14-21. |
| [4] |
KLEIN A, CARSTENS M I, CARSTENS E. Facial injections of pruritogens or algogens elicit distinct behavior responses in rats and excite overlapping populations of primary sensory and trigeminal subnucleus caudalis neurons[J]. J Neurophysiol, 2011, 106(3): 1078-1088. |
| [5] |
AKIYAMA T, CARSTENS E. Neural processing of itch[J]. Neuroscience, 2013, 250: 697-714. |
| [6] |
SAKAI K, AKIYAMA T. New insights into the mechanisms behind mechanical itch[J]. Exp Dermatol, 2020, 29(8): 680-686. |
| [7] |
DONG X T, DONG X Z. Peripheral and central mechanisms of itch[J]. Neuron, 2018, 98(3): 482-494. |
| [8] |
聂红, 付凯, 林娟, 等. 瘙痒的神经机制及其动物模型[J]. 协和医学杂志, 2011, 2(4): 370-374. NIE H, FU K, LIN J, et al. Neuromechanism of itch and its animal rhodels[J]. Med J Peking Union Med Coll Hosp, 2011, 2(4): 370-374. |
| [9] |
LAY M, DONG X Z. Neural mechanisms of itch[J]. Annu Rev Neurosci, 2020, 43: 187-205. |
| [10] |
WANG F, YANG T B, KIM B S. The return of the mast cell: new roles in neuroimmol/Lune itch biology[J]. J Invest Dermatol, 2020, 140(5): 945-951. |
| [11] |
HAN L, DONG X Z. Itch mechanisms and circuits[J]. Annu Rev Biophys, 2014, 43: 331-355. |
| [12] |
MOCHIZUKI H, KAKIGI R. Itch and brain[J]. J Dermatol, 2015, 42(8): 761-767. |
| [13] |
CARSTENS E, AKIYAMA T. Central mechanisms of itch[J]. Curr Probl Dermatol, 2016, 50: 11-17. |
| [14] |
LIU X, MIAO X H, LIU T. More than scratching the surface: recent progress in brain mechanisms underlying itch and scratch[J]. Neurosci Bull, 2020, 36(1): 85-88. |
| [15] |
FENG J, LUO J L, YANG P, et al. Piezo2 channel-Merkel cell signaling modulates the conversion of touch to itch[J]. Science, 2018, 360(6388): 530-533. |
| [16] |
GREEN D P, LIMJUNYAWONG N, GOUR N, et al. A mast-cell-specific receptor mediates neurogenic inflammol/Lation and pain[J]. Neuron, 2019, 101(3): 412-420.e3. |
| [17] |
MEIXIONG J, ANDERSON M, LIMJUNYAWONG N, et al. Activation of mast-cell-expressed mas-related G-protein-coupled receptors drives non-histaminergic itch[J]. Immol/Lunity, 2019, 50(5): 1163-1171.e5. |




