蜱属于蛛形纲、蜱螨亚纲、寄型目、蜱总科,包括硬蜱科、软蜱科和纳蜱科,世界已知约1 000余种,其中硬蜱约占80%,软蜱约占20%。我国记录的硬蜱科有120余种,软蜱科10种[1]。不同蜱种的分布与气候、地势、土壤、植被和宿主等多种因素有关。大多数蜱的宿主非常广泛,并可侵袭人类,在流行病学上有重要意义。蜱的危害性包括直接危害和传播疾病。直接危害是蜱在钉刺吸血时可造成局部充血、水肿、急性炎症反应,还可引起继发性感染。蜱传播的病原体是人和家畜众多疾病的重要来源,还包括一些严重危害人类健康的疾病。已知蜱可携带83种病毒、14种细菌、17种回归热螺旋体、32种原虫,所致疾病大多为重要的感染性疾病和人兽(畜、禽)共患病[2],因此蜱传疾病的研究具有重大的兽医学、医学及经济学价值。甘肃省河西走廊地区属于半荒漠、荒漠草原、戈壁荒漠区,这里不仅自然环境复杂多样,存在着适合多种病原体生存和流行的多种动物宿主和适宜的地理景观,而且也是重要的交通枢纽,人员流动交往密集且复杂,但有关新发虫媒传染病研究较少。以往有学者在河西走廊地区进行调查发现:调查点内不仅蜱种丰富,而且人群、家畜被蜱叮咬的现象普遍,甚至有些家庭深受其害[3]。但人们对蜱的危害及传播的相关疾病并不清楚,有些出现不适反应甚至疾病也搞不清楚是什么原因。为了解甘肃河西走廊地区蜱携带病原体种类,我们在河西走廊沿线地区进行相关调查,现报告如下:
1 材料与方法 1.1 调查时间与地点2020年3月及9月,分别两次在河西走廊沿线进行现场调查及标本采集。调查点为武威、张掖、酒泉及嘉峪关。武威调查点为天祝旦马乡县土塔村;张掖调查点为乌江镇敬依村;酒泉调查点为酒泉市肃州区银达镇西坝村;嘉峪关调查点为新城镇移民村。所选调查点均为农牧区,农田均为多年由戈壁荒滩及盐碱地改造而成,村庄及农田周围多为戈壁荒滩,属于半荒漠及半荒漠草地地区。
1.2 标本的采集布旗法采集游离蜱:布旗由60 cm×100 cm白绒布制成,采集人员身着防护衣帽在草地或荒漠中、灌木丛等可行走的兽道上边走边拖拉布旗,每行走20~30 m检查布旗,用镊子收集布旗两面黏附的蜱,同时注意收集采集人员衣、裤、帽上的蜱。家畜动物体表采用捡蜱法:深入走访村民,进行仔细摸排,检查动物的颈、耳背、股内侧等部位,收集寄生的蜱。圈舍内蜱标本采集:直接用镊子收集地面及墙缝等地爬行的游离蜱。所有采集的蜱标本装入透气并有一定湿度的标本管中保存,带回实验室分类鉴定。
1.3 蜱标本中病原体DNA的提取蜱标本带回实验室,显微镜下进行形态学分类鉴定[1, 4-5]:以检索表为依据,观察蜱标本的假头部基部形状、背面是否覆盖有盾板、肛沟位置、气门板形状、有无眼等形态特征,进行形态学鉴定,整理并记录。鉴定完毕的蜱标本用75%酒精浸泡20 min进行杀灭及体表消毒,用无菌滤纸吸干,再用生理盐水,漂洗3次,用无菌滤纸吸干蜱体表水分后备用。取单只、未吸血成年蜱置EP管中,加入提取缓冲液200 μL,研磨器充分研磨后置沸水中煮10 min,使用TIANGEN公司DNA提取试剂盒(离心柱型)提取病原体DNA,具体操作按照说明书进行。
1.4 病原体扩增巢式PCR法扩增Q热病原体(贝氏柯克斯体,Coxiella burnetii,C. burnetii)、野兔热病原体(土拉弗菌,Francisella tularensis,F. tularensis)、莱姆病病原体(莱姆病螺旋体,Borrelia burgdorferi,B. burgdorferi)目的病原体DNA片段。Q热病原体针对病原体的23S rRNA基因序列,引物及扩增条件参考文献[6]进行。莱姆病病原体针对病原体5S~23S rRNA基因间隔区进行扩增[7]。土拉弗菌针对病原体fopA基因扩增[8]。检测所用引物及扩增条件详见表 1。
| 病原体 | 引物名称 | 序列(5′-3′) | 扩增条件 |
| 土拉 | FNA8L | CGAGGAGTCTCAATGTACTAAGGTTTGCCC | 95 ℃ 3 min,95 ℃ 15 s,55 ℃ 15 s72 ℃ 30 s,35个循环,72 ℃ 10 min |
| FNA2L | CACCATTATCCTGGATATTACCAGTGTCAT | ||
| 弗菌 | FNA7L | CTTGAGTCTTATGTTTCGGCATGTGAATAG | |
| FNA1L | CCAACTAATTGGTTGTACTGTACAGCGAAG | ||
| C1 | TCCGGTTGGATAGGTGTTGGATT | 94 ℃ 5 min,94 ℃ 30 s,64 ℃ 30 s 72 ℃ 30 s,30个循环,72 ℃ 10 min | |
| C4 | GCGCGGATAAATTTAAATTC | ||
| 贝氏柯克斯体 | 23S IVSF | CTTTAAAGAAAGCCTAATAG | 94 ℃ 3 min,94 ℃ 60 s,55 ℃ 60s,72 ℃ 60 s,30个循环,72 ℃ 5 min |
| 23S IVS R | TTACT TTATGTCAGCATTCG | ||
| IVSF | TCACTGGTCGAGTCGTC | ||
| IVS R | ATTCGCACTTCTGATACC | ||
| 莱姆病螺旋体 | 23S3 | CGACCTTCTTCGCCTTAAAGC | 96 ℃ 2 min,94 ℃ 30 s,55 ℃ 30s,72 ℃ 40 s,30个循环,72 ℃ 5 min |
| 23Sa | TAAGCTGACTAATACTAATTACCC | ||
| primer 1 | CTGCGAGTTCGCGGGAGA | 96 ℃ 2 min,94 ℃ 30 s,59 ℃ 30s,72 ℃ 40 s,30个循环,72 ℃ 5 min | |
| primer 2 | TCCTAGGCATTCACCATA |
1.5 病原体基因型别分析
对莱姆病病原体检测阳性的标本进行基因分型,采用RFLP法[7]:用限制性内切酶Mse Ⅰ (10 000 U/mL; New England Biolabs) 于37 ℃酶切9 h,酶切后65 ℃灭活20 min,酶切产物进行电泳分离片段。土拉弗菌检测阳性标本,采用C1/C4引物进行扩增区分亚种[8-9],反应条件为:94 ℃ 5 min,94 ℃ 30 s,64 ℃ 30 s 72 ℃ 30 s,30个循环。
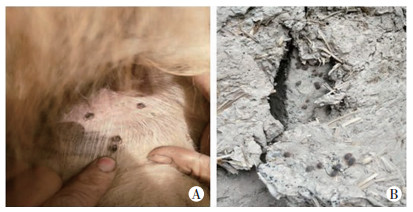
2 结果 2.1 蜱标本采集情况河西4个调查点共采集3个蜱种约5 000余只蜱,其中2 123只为成蜱,未吸血蜱。2 123只蜱在不同采样点的分布见表 2。其中,亚东璃眼蜱(Hyalomma asiaticum),采自农户野外放养的骆驼体表(图 1A),草原革蜱(Dermacentor nuttalli) 采自骆驼体表及野外拖蜱获得;波斯锐缘蜱(Argas persicus)采自农户家中圈舍(图 1B)。
| 蜱标本采集点 | 蜱种(只) | 合计 | ||
| 亚东璃眼蜱 | 波斯锐缘蜱 | 草原革蜱 | ||
| 张掖 | 55 | 742 | 43 | 840 |
| 武威 | 256 | … | 135 | 391 |
| 酒泉 | 503 | … | … | 503 |
| 嘉峪关 | … | … | 389 | 389 |
| 合计 | 814 | 742 | 567 | 2 123 |
|
| A:野外放养的骆驼;B:农户圈舍 图 1 蜱标本采集现场 |
2.2 蜱内莱姆病螺旋体感染情况及其基因型
2 123只蜱中,共计有54只检测阳性,阳性率2.54%,其中亚东璃眼蜱43只,草原革蜱11只,波斯锐缘蜱中未检出。54份阳性标本中48份标本成功分型。阳性标本使用Mse Ⅰ酶切进行基因型别判定,共产生3种片段大小(bp)不同组合的酶切带型,其中属于Borrelia garinii (B. garinii)基因型的两种:107,95,51、107,57,51,38;属于Borrelia afzelii (B. afzelii)基因型一种:107,68,51,20。48份标本中37份属于B. garinii基因型,占77.08%,11份为B. afzelii基因型,不同蜱种不同病原体检测结果见表 3。莱姆病螺旋体基因型别的分布见表 4。
| 蜱种 | 检测阳性数(只) | 合计 | ||
| 莱姆病螺旋体 | 土拉弗菌 | Q热柯克斯体 | ||
| 亚东璃眼蜱 | 43 | 18 | 62 | 123 |
| 草原革蜱 | 11 | 5 | 36 | 52 |
| 波斯锐缘蜱 | — | 9 | 24 | 33 |
| 合计 | 54 | 32 | 122 | 208 |
| 基因型 | 酶切片段组合(bp) | 蜱种(只) | 合计 | |
| 亚东璃眼蜱 | 草原革蜱 | |||
| B. garinii | 107,95,51 | 26 | 3 | 29 |
| 107,57,51,38 | 6 | 2 | 8 | |
| B. afzelii | 107,68,51,20 | 7 | 4 | 11 |
| 合计 | 39 | 9 | 48 | |
2.3 蜱内土拉弗菌感染情况及病原体基因型
共检测到阳性标本32只,阳性率为1.51%,其中亚东璃眼蜱18只,波斯锐缘蜱中5只,草原革蜱9只。32只阳性标本经分型判定均属于土拉弗菌B亚种(表 2)。
2.4 蜱体内Q热柯克斯体检测结果共检测到阳性标本122只,阳性率为4.61%,其中亚东璃眼蜱62只,草原革蜱36只,波斯锐缘蜱24只(表 3)。
2.5 复合感染情况共检测到15只来自野外放养骆驼体表的亚东璃眼蜱存在复合感染的现象,复合感染率为0.71%,其中10只为土拉弗氏菌与Q热柯克斯体共感染,5只为莱姆病螺旋体与Q热柯克斯体共感染。
3 讨论甘肃省地处青藏高原、蒙新高原和黄土高原的交汇处,全境分为六个不同的自然景观区,地形地貌多样,气候变化明显,动物种类繁多。本研究以河西走廊半荒漠、荒漠草原、戈壁荒漠区为调查地区,采集不同生境下的蜱标本进行研究。调查发现,调查点内的媒介蜱种有:亚东璃眼蜱、草原革蜱及波斯锐缘蜱。其中亚东璃眼蜱采自野外放养的骆驼体表,草原革蜱采自野外及野外放养的骆驼体表,这两种蜱在家养的牲畜及其圈舍内未发现,这一结果与三十年前康新民[10]等的调查结果一致;波斯锐缘蜱只是在农户的圈舍内发现,野外环境下未采集到。这与不同蜱种的生活习性有关,但其是否会有宿主选择偏好目前并不清楚,今后需进一步研究。
研究发现,调查区域内蜱携带有莱姆病螺旋体、土拉弗菌及Q热柯克斯体,其中莱姆病螺旋体基因型别为致病基因型,土拉弗菌亦属于致病类型(B亚种),Q热柯克斯体属于感染性极强的病原体,但由于此类疾病在我国并非法定报告传染病,人们对此类疾病了解较少,因此当地人群中是否存在患者目前尚不清楚,今后开展血清流行病学调查将可能了解此类疾病在人群中感染的情况。值得一提的是,本研究将首次在张掖发现的波斯锐缘蜱[3]纳入检测,发现土拉弗菌及Q热柯克斯体DNA目的片段,该蜱种是否只是携带上述病原体,能否作为这两种病原体传播媒介尚需做传播动力学实验加以验证,今后在调查点内针对该蜱种进行详细的流行病学调查十分有必要。
蜱携带和传播的病原体种类数量繁多,且其在自然界中宿主动物分布广泛、流行环节多样,这就使得几种蜱传疾病可以共存于同一疫源地,甚至一种蜱或一只蜱可同时携带多种病原体,这些因素都会增加宿主动物及人类感染的机会[11-13]。本研究发现在野外放养的骆驼身上至少有两种蜱,同时从15只亚东璃眼蜱体内检测到两种病原体的DNA,这也提示我们,当地居民们可能会有复合感染的可能,尤其是对从事剪驼毛的牧民们。今后详细进行相关调查,掌握可能有的媒介蜱种及其所携带的病原体种类对于防控此类疾病至关重要。
| [1] |
刘增加, 罗芳. 西北地区重要医学动物与疾病[M]. 北京: 军事医学科学出版社, 2013: 688-745. LIU Z J, LUO F. Important medical animals and diseases in Northwest China[M]. Beijing: Military Medical Science Press, 2013: 688-745. |
| [2] |
SHI J, HU Z, DENG F, et al. Tick-borne viruses[J]. Virol Sin, 2018, 33(1): 21-43. |
| [3] |
王和平, 甘军, 李璐, 等. 甘肃河西地区蜱类初步调查[J]. 中华卫生杀虫药械, 2018, 24(4): 288-290. WANG H P, GAN J, LI L, et al. Preliminary investigation on ticks in Hexi region of Gansu Province[J]. Chin J Hyg Insect Equip, 2018, 24(4): 288-290. |
| [4] |
陆宝麟, 吴厚永. 中国重要医学昆虫分类与鉴别[M]. 郑州: 河南科学技术出版社, 2003: 652-679. LU B L, WU H Y. Classification and identification of important medical insects in China[M]. Zhengzhou: Henan Science and Technology Press, 2003: 652-679. |
| [5] |
刘增加. 中国西北地区病媒生物物种名录[M]. 北京: 军事医学科学出版社, 2011: 193-204. LIU Z J. List of Vector Species in Northwest China[M]. Beijing: Military Medical Science Press, 2011: 193-204. |
| [6] |
陈荣, 温博海, 张雪, 等. 套式PCR和DNA探针技术检测Q热立克次体[J]. 中国人兽共患病杂志, 2001, 17(1): 28-30, 44. CHEN R, WEN B H, ZHANG X, et al. Detection of Coxiella burnetti by nested PCR and DNA probe[J]. Chin J Zoonoses, 2001, 17(1): 28-30, 44. |
| [7] |
LIVERIS D, WORMSER G P, NOWAKOWSKI J, et al. Molecular typing of Borrelia burgdorferi from Lyme disease patients by PCR-restriction fragment length polymorphism analysis[J]. J Clin Microbiol, 1996, 34(5): 1306-1309. |
| [8] |
FULOP M, LESLIE D, TITBALL R. A rapid, highly sensitive method for the detection of Francisella tularensis in clinical samples using the polymerase chain reaction[J]. Am J Trop Med Hyg, 1996, 54(4): 364-366. |
| [9] |
DE LA PUENTE-REDONDO V A, DEL BLANCO N G, GUTIÉRREZ-MARTÍN C B, et al. Comparison of different PCR approaches for typing of Francisella tularensis strains[J]. J Clin Microbiol, 2000, 38(3): 1016-1022. |
| [10] |
康新民, 朱道宏, 王红红, 等. 甘肃河西三地区骆驼寄生蜱调查[J]. 中国兽医科技, 1991(4): 19-20. KANG X M, ZHU D H, WANG H H, et al. Investigation of camel parasitic ticks in three areas of Hexi, Gansu[J]. Chin Vet Sci Tech, 1991(4): 19-20. |
| [11] |
周磊. 内蒙古林区媒介携带病原体的调查研究[D]北京: 军事医学科学院, 2017. ZHOU L. Investigation of pathogens carried by vectors in Inner Mongolia forest area[D] Beijing: Academy of Military Medical Sciences, 2017. |
| [12] |
赵俊伟, 王环宇, 王英. 中国蜱传病原体分布研究概况[J]. 中国媒介生物学及控制杂志, 2012, 23(5): 445-448. ZHAO J W, WANG H Y, WANG Y. Regional distribution profiles of tick-borne pathogens in China[J]. Chin J Vector Biol Control, 2012, 23(5): 445-448. |
| [13] |
于志军, 刘敬泽. 蜱传疾病及其媒介蜱类研究进展[J]. 应用昆虫学报, 2015, 52(5): 1072-1081. YU Z J, LIU J Z. Progress in research on tick-borne diseases and vector ticks[J]. Chin J Appl Entomol, 2015, 52(5): 1072-1081. |




