2. 401332 重庆,重庆市医药高等专科学校
2. Chongqing Medical and Pharmaceutical College, Chongqing, 401332, China
白内障超声乳化手术是全世界治疗白内障的首选手术方式[1]。经过几十年的发展,白内障超声乳化手术比以往任何时候都更加安全和高效,可以为白内障患者带来良好的术后视觉质量,同时并发症发生率极低[2]。然而,由于术中前房稳定性不佳引起的阻塞后浪涌(post-occlusion surge,POS)仍然可能造成术中后囊破裂等不良后果[3-4]。特别是对于硬核白内障手术,POS可能存在处理硬核晶体的最后一块核块时发生后囊破裂,导致玻璃体涌出、玻璃体牵拉视网膜、残留的核块掉入玻璃体腔等严重并发症。因此前房稳定性对于硬核白内障超声乳化手术有至关重要的作用。
既往研究发现传统的白内障超声乳化手术时,重力控制液流系统的灌注压由灌注瓶高决定,灌注速度无法适应超乳抽吸速度的变化,导致前房稳定性较差、眼内压波动较大。过高的眼压不仅引起眼部不适,还可导致眼部血流灌注降低、青光眼视神经损伤加速和术后角膜水肿[5]。
本课题组既往报道在原发性闭角型青光眼患者白内障超声乳化手术中,主动液流控制系统相对于传统重力控制液流系统而言,具有更高的手术效率,更快的术后视力恢复速度,更轻的术后角膜水肿程度[6],但在硬核白内障患者的手术中应用主动液流控制系统,是否能够在手术效率和术后早期视力恢复等方面更加优于传统重力液流灌注系统,目前尚不清楚。因此,本研究拟对Centurion Vision System两种不同液流控制系统在硬核白内障超声乳化手术中的效率及术后早期角膜水肿程度、视力恢复程度进行对比研究, 以明确主动液流控制系统对硬核白内障手术患者的超声乳化手术效率。
1 资料与方法 1.1 研究对象本研究为前瞻性随机对照研究。研究对象为2020年1月至2020年12月就诊于陆军军医大学第一附属医院眼科,施行白内障超声乳化吸除联合人工晶体植入手术的老年性白内障患者60例(60只眼)。
纳入标准:(1)年龄≥65岁;(2)临床诊断为老年性白内障;(3)术眼晶状体核硬度按照LOCS Ⅱ分级系统均属N Ⅳ级,每例患者仅入选1只眼;(4)使用Centurion Vision System视觉系统超声乳化仪(Alcon Laboratories, Inc.)行白内障超声乳化吸除联合人工晶状体植入术。
排除标准:(1)合并其他眼部疾病(如角膜变性、圆锥角膜、Fuchs内皮营养不良等角膜病变、假性囊膜剥脱综合征、青光眼、眼底疾病、晶状体半脱位、葡萄膜炎等)或眼外伤;(2)术眼曾进行过其他内眼手术;(3)术前内皮细胞计数小于1 500 /mm2;(4)合并严重的全身疾病(未控制的糖尿病、严重的心血管问题、出血和凝血障碍、慢性阻塞性肺疾病等)不能耐受手术者。
采用随机数字表法将60例(60只眼)患者分成2组,主动控制液流系统组:术中应用主动控制液流系统行白内障超声乳化吸除联合人工晶体植入手术30例(30眼);重力控制液流系统组:术中应用重力控制液流系统行白内障超声乳化吸除联合人工晶体植入手术30例(30眼)。本研究经本院伦理委员会审核批准(KY2020168),患者及家属已签署知情同意书。
1.2 方法 1.2.1 术前检查最佳矫正远视力(best corrected distance visual acuity,CDVA)由综合验光仪(RT-5100,日本尼德克)主观验光结合插片完成。眼轴长度、前房深度、角膜曲率采用IOL Master(IOLMaster 500,德国蔡司)测量。中央角膜厚度由Sirius眼前节分析仪(Sirius,意大利CSO)测量完成。角膜内皮细胞计数采用非接触式镜检显微镜(SP 3000P,Topcon Medical Systems,Inc)测量。晶体混浊程度分级依据为Lens Opacities Classification System Ⅱ (LOCS Ⅱ)。
1.2.2 手术参数两种液流灌注系统均使用Centurion Vision System视觉系统超声乳化仪(Alcon Laboratories, Inc.)及0.9 mm 45°Intrepid Balanced超声乳化针头和0.9 mm Intrepid Ultra针头套管。主动液流控制组术中眼压设定为55 mmHg,重力控制系统组术中的瓶高距离术眼的水平面为90 cm,相当于术中眼压设定为67.67 mmHg(1 mmHg=1.33 cmH2O)。
收集自动显示在Centurion系统界面上的每例患者手术效率参数,手术参数包括累计释放能量(cumulative dissipated energy, CDE)、总超声乳化时间(ultrasound total time,UTT)、扭动能量振幅(torsional amplitude, TA)、扭动超声使用时间(torsion use time, TUT)、抽吸时间(aspiration time, AT)、液流使用量(fluid use, FU)。
1.2.3 手术方法所有手术由同一名经验丰富的医师完成。详细手术过程同文献[6]。
1.2.4 术后随访术后第1天记录包括裸眼远视力(uncorrected distance visual acuity,UDVA)、Sirius眼前节分析仪测量角膜中央厚度、裂隙灯显微镜下所观察的中央角膜水肿程度。中央角膜水肿等级评分标准如下:0=完全没有可见角膜混浊和角膜厚度增加;1/2=切口部位的轻微角膜混浊和轻微角膜增厚;1=角膜轻度混浊和增厚,面积小于角膜总面积的25%,无角膜后弹力层褶皱,虹膜纹理清晰;2=角膜中度混浊和增厚,面积超过角膜总面积25%,几乎无角膜后弹力层褶皱,虹膜纹理欠清晰;3=角膜重度混浊和增厚,面积超过角膜总面积的50%,角膜后弹力层明显褶皱,虹膜纹理模糊[7]。
1.2.5 统计学方法使用SPSS 25.0统计学软件进行描述性统计和差异性分析。UDVA及CDVA均转化为标准化最小分辨角对数(logarithm of minimum angle of resolution,logMAR)视力进行统计分析。采用独立样本t检验及Mann-Whitney U检验对符合正态分布(采用x±s表示)和不符合正态分布[采用中位数(范围)表示]的计量资料进行组间差异性检验,包括视力、角膜中央厚度、角膜内皮细胞计数及平均角膜水肿等级评分等。采用χ2检验对计数资料进行组间差异性检验,包括性别分布、术后第1天不同角膜水肿等级评分的患者比例。以P < 0.05为差异有统计学意义。
2 结果 2.1 基本资料共纳入患者60例(60只眼),其中女性21例(21只眼),男性39例(39只眼)。年龄69~91(80.43±5.84)岁。主控组30例(30只眼),重力组30例(30只眼)。术前两组患者的年龄、性别、最佳矫正远视力、中央角膜厚度、角膜内皮细胞计数差异均无统计学意义(P>0.05)。见表 1。
| 组别 | n | 年龄/岁 | 性别(男/女) | 最佳矫正远视力(logMAR) | 中央角膜厚度/μm | 角膜内皮细胞计数/个·mm-2 |
| 主控组 | 30 | 80.03±6.61 | 19/11 | 0.77±0.19 | 532.93±40.00 | 2 473.04±473.59 |
| 重力组 | 30 | 80.83±5.05 | 20/10 | 0.76±0.19 | 526.40±34.86 | 2 544.56±475.57 |
| t/χ2值 | -0.527 | 0.073 | -0.027 | 0.674 | -0.584 | |
| P值 | 0.600 | 0.787 | 0.978 | 0.503 | 0.562 |
2.2 两组术中效率参数对比
主控组的CDE、UTT、TUT、AT、FU均显著少于重力组(P < 0.05)。但两组之间TA差异无统计学意义。见表 2。
| 组别 | n | 累计释放能量 | 总超声乳化时间/s | 扭动能量振幅 | 扭动超声使用时间/s | 抽吸时间/s | 液流使用量/mL |
| 主控组 | 30 | 14.90(7.70~25.10) | 90.50(41.00~176.00) | 67.85(46.70~89.90) | 34.50(18.00~77.00) | 214.70±10.17 | 69.50±1.84 |
| 重力组 | 30 | 21.50(10.30~34.10) | 126.00(77.00~197.00) | 72.00(53.50~99.10) | 48.50(21.00~99.00) | 340.77±10.51 | 80.57±2.34 |
| 检验量 | U=223.50 | U=199.50 | U=334.00 | U=260.50 | t=-8.62 | t=-3.71 | |
| P值 | 0.001 | < 0.001 | 0.080 | 0.005 | < 0.001 | < 0.001 |
2.3 两组患者术后第1天视力、CCT变化及中央角膜水肿程度对比
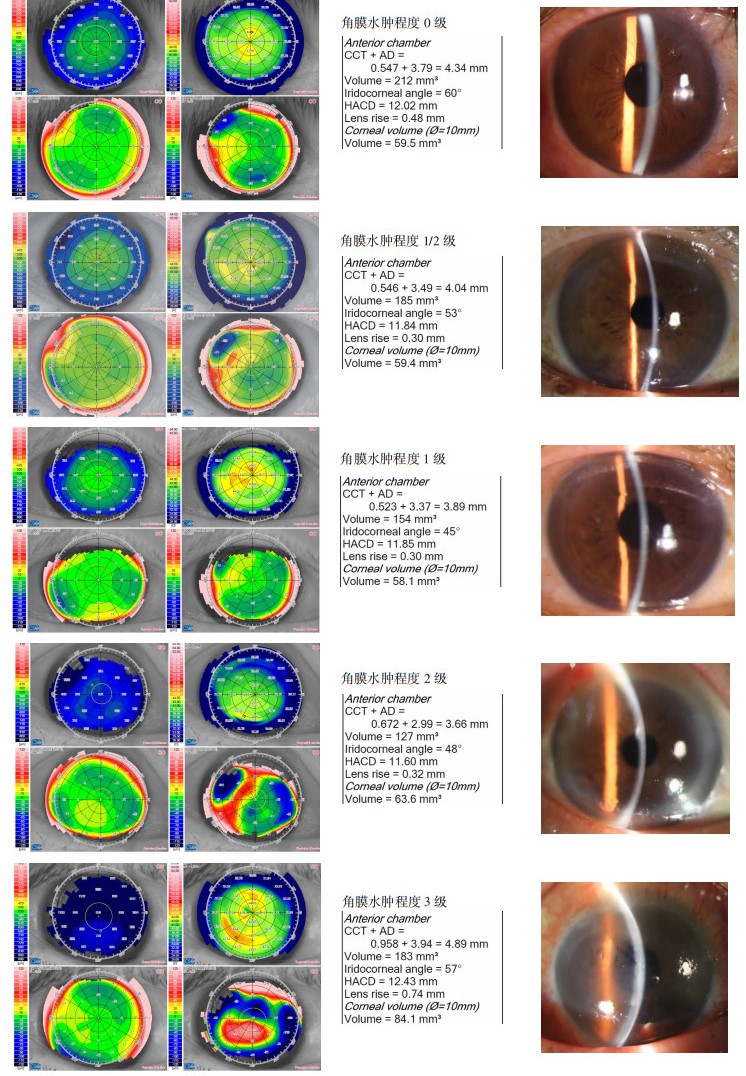
如表 3所示,术后第1天两组病例CCT差异均无统计学意义(P=0.060)。术后1 d主控组CCT增加幅度显著低于重力组(P=0.006)。主控组裸眼远视力显著优于重力组(P=0.005),主控组平均角膜水肿等级显著低于重力组(P < 0.001)。使用角膜地形图及前节照相记录不同程度中央角膜水肿分级,并对主动控制液流组和重力控制液流组患者术后第1天角膜水肿程度百分比进行统计,结果显示术后第1天角膜水肿0级、1/2级的百分比两组间无明显差异;主控组角膜水肿1级的百分比显著高于重力组,而在角膜水肿2级和3级中,主控组显著低于重力组(图 1)。
| 组别 | n | 中央角膜厚度/μm | △中央角膜厚度(%) | 裸眼远视力(logMAR) | 平均角膜水肿等级 | 中央角膜水肿等级评分 | |||
| 0 | 1/2 | 1 | 2或3 | ||||||
| 主控组 | 30 | 567.00±31.21 | 6.65±5.21 | 0.31±0.12 | 1.00±0.56 | 2(6.7) | 4(13.3) | 21(70.0) | 3(10.0) |
| 重力组 | 30 | 582.53±41.65 | 10.91±6.34 | 0.42±0.17 | 1.52±0.78 | 1(3.3) | 3(10.0) | 1(36.7) | 15(50.0) |
| 检验值 | t=-1.91 | t=-2.84 | t=-2.89 | t=-2.95 | N/a | N/a | χ2=6.70 | χ2=11.43 | |
| P值 | 0.060 | 0.006 | 0.005 | < 0.001 | 1.000 | 1.000 | 0.010 | 0.001 | |
|
| 左:角膜地形图;中:中央角膜厚度;右:角膜水肿的裂隙灯前节照相 图 1 角膜水肿不同程度分级的地形图及前节照相 |
2.4 两组患者手术并发症
60例入组患者术中无1例出现后囊破裂、玻璃体丢失、人工晶体未植入、眼内出血等并发症。
3 讨论超声乳化新技术的发展虽然已经极大地改善了常规白内障手术的疗效[8],然而硬核白内障手术仍然是白内障手术医师面临的挑战。因为随着核硬度的增加,术中需要的超声能量更多,超声时间更长,可能导致角膜内皮细胞丢失、术后角膜水肿、术后早期视力恢复欠佳[9]。据报道白内障超声乳化手术内皮细胞损失率可在4%~25%[10]。白内障超声乳化手术过程中有许多可能导致角膜内皮细胞功能损伤的因素,包括超声能量释放较多、超声乳化时间较长、局部温度增加、液流灌注的冲刷、碎核的碰撞以及术后的炎症反应等[11]。在上述因素中,导致术后角膜内皮细胞丢失的最重要因素为手术中所用超声乳化能量值过多[12]。除了术中所用超声乳化能量值以外,导致白内障术后角膜内皮细胞丢失的另一主要因素就是手术时间[13]。由此可见手术效率是白内障超声乳化手术术后效果的决定性因素之一。Centurion超声乳化仪已被证明其出色的前房稳定性可以提高术后临床效果以及术中效率[14]。因此本研究的目的之一就是比较使用Centurion超声乳化仪的两种不同超声乳化液流控制系统进行硬核白内障手术的术中超声能量使用量及手术时间的差异。
本研究结果显示,主动控制液流组的CDE、UTT、TUT、AT和FU均明显低于重力控制液流系统组。与重力控制液流组相比,主动控制液流组术中总CDE减少约30.6%,与其他文献的报道结果相似,SOLOMON等[15]学者的研究报道了主动控制液流组相对于重力控制液流组的CDE减少了40%;另外,CHEN等[14]报道了主动控制液流组相对于重力控制液流组的CDE的差异为38%。本研究结果同时显示,在UTT、TUT、AT 3个时间参数方面,主动控制液流组均显著低于重力控制液流组,也与其他文献报道结果一致[15],由此可见对于硬核白内障应用主动控制液流系统,可以明显降低手术时间。综上所述,主动控制液流相对于重力液流系统在硬核白内障超声乳化手术中拥有更低能量的输出、更少的手术时间,即更高的手术效率。在超声乳化手术过程中,术中前房稳定性是决定手术效率的重要因素之一。而前房稳定性受多种因素的影响,其中最主要的原因是由于术中抽吸和灌注流速的变化不同步导致前房的波动,主动控制液流系统可以很好地动态平衡术中抽吸和灌注流速[15],在抽吸过快时,自动正压增加灌注流量,更快速地补充了前房液流,更好地维持了前房压力。在既往的报告中,与重力控制液流系统相比,Centurion主动控制液流系统术中出现POS较少,前房稳定性更好[16]。我们推测这正是主动控制液流组手术效率高于重力控制液流组的主要原因。
大量研究表明术后中央角膜厚度和中央角膜水肿程度是评估术源性角膜内皮细胞功能损伤的有效指标[17]。研究结果显示术后第1天主动控制液流组CCT增加幅度、中央角膜水肿程度以及重度中央角膜水肿患者比例均显著低于重力控制液流组,由此证明主动控制液流组病例拥有更少的术中能量使用和更短的手术时间,会使角膜内皮损伤更少以及角膜水肿程度更低,这和其他研究结果一致[18]。
术后第1天主动控制液流组裸眼远视力显著优于重力控制液流组。尽管无法确定术中效率与术后视力恢复的直接联系,但可以推测正是由于Centurion主动控制液流系统术中前房更稳定,术中眼内压波动更小,术中超声乳化针头阻塞后的浪涌更少,超声能量使用和更短的超声时间更少,从而使角膜内皮细胞损伤的程度相对于传统的重力控制液流系统而言,得到了极大的降低,术后视力恢复速度也更快。
还应指出的是,虽然既往有少量关于主动控制液流系统和重力控制液流系统的研究[7],但其研究均采用了不同的超声乳化系统(Centurion Vision System和Infiniti Vision System)和不同的超声乳化针头(Intrepid balance针头和Kelman针头),而本研究两组病例均是基于Centurion Vision System和Intrepid balance针头同一系统,因此本研究结果可能更具有临床代表意义。
本研究的局限性包括随访时间较短,未纳入术后远期随访指标,例如术后角膜水肿恢复时间、术后黄斑水肿情况等。同时,本研究样本量较少,理想情况下,应该进行大规模的前瞻性随机研究,以更好地评估主动控制液流系统超声乳化技术的相对安全性和有效性。
综上所述,本研究结果显示,相对于传统重力控制液流系统,Centurion Vision System主动控制液流系统更好的前房稳定性使得在硬核白内障手术中CDE释放更少,超声乳化时间更短,液流使用量更少,具有更高的手术效率。Centurion Vision System主动控制液流系统超声乳化手术的高效率使得硬核白内障患者术后早期角膜水肿程度更轻,角膜厚度变化更小,术后早期视力恢复更快。
| [1] |
DAVIDORF J M. Femtosecond versus (gold) standard phacoemulsification[J]. J Cataract Refract Surg, 2015, 41(5): 1124. |
| [2] |
韩钰, 王军. 微小切口白内障手术新进展[J]. 中华眼科杂志, 2012, 48(4): 369-373. HAN Y, WANG J. New progresses in micro-incision cataract surgery[J]. Chin J Ophthalmol, 2012, 48(4): 369-373. |
| [3] |
GEORGESCU D, KUO A F, KINARD K I, et al. A fluidics comparison of Alcon Infiniti, Bausch & Lomb Stellaris, and Advanced Medical Optics Signature phacoemulsification machines[J]. Am J Ophthalmol, 2008, 145(6): 1014-1017. |
| [4] |
GEORGESCU D, PAYNE M, OLSON R J. Objective measurement of postocclusion surge during phacoemulsification in human eye-bank eyes[J]. Am J Ophthalmol, 2007, 143(3): 437-440. |
| [5] |
MALIK P K, DEWAN T, PATIDAR A K, et al. Effect of IOP based infusion system with and without balanced phaco tip on cumulative dissipated energy and estimated fluid usage in comparison to gravity fed infusion in torsional phacoemulsification[J]. Eye Vis (Lond), 2017, 4: 22. |
| [6] |
谢晶, 徐江宁, 刘美芳, 等. 主动控制液流系统应用于原发性闭角型青光眼白内障超声乳化术的临床研究[J]. 第三军医大学学报, 2020, 42(21): 2141-2147. XIE J, XU J N, LIU M F, et al. Application of active-fluidic pressure control phacoemulsification system for primary angle-closure glaucoma with cataract: reports of 24 cases[J]. J Third Mil Med Univ, 2020, 42(21): 2141-2147. |
| [7] |
CHRISTAKIS P G, BRAGA-MELE R M. Intraoperative performance and postoperative outcome comparison of longitudinal, torsional, and transversal phacoemulsification machines[J]. J Cataract Refract Surg, 2012, 38(2): 234-241. |
| [8] |
HAN Y K, MILLER K M. Heat production: Longitudinal versus torsional phacoemulsification[J]. J Cataract Refract Surg, 2009, 35(10): 1799-1805. |
| [9] |
FOSTER G J L, ALLEN Q B, AYRES B D, et al. Phacoemulsification of the rock-hard dense nuclear cataract: options and recommendations[J]. J Cataract Refract Surg, 2018, 44(7): 905-916. |
| [10] |
MENCUCCI R, PONCHIETTI C, VIRGILI G, et al. Corneal endothelial damage after cataract surgery: microincision versus standard technique[J]. J Cataract Refract Surg, 2006, 32(8): 1351-1354. |
| [11] |
NIXON D R. Preoperative cataract grading by Scheimpflug imaging and effect on operative fluidics and phacoemulsification energy[J]. J Cataract Refract Surg, 2010, 36(2): 242-246. |
| [12] |
CHO Y K, CHANG H S, KIM M S. Risk factors for endothelial cell loss after phacoemulsification: comparison in different anterior chamber depth groups[J]. Korean J Ophthalmol, 2010, 24(1): 10-15. |
| [13] |
DICK H B, KOHNEN T, JACOBI F K, et al. Long-term endothelial cell loss following phacoemulsification through a temporal clear corneal incision[J]. J Cataract Refract Surg, 1996, 22(1): 63-71. |
| [14] |
CHEN M, ANDERSON E, HILL G, et al. Comparison of cumulative dissipated energy between the Infiniti and Centurion phacoemulsification systems[J]. Clin Ophthalmol, 2015, 9: 1367-1372. |
| [15] |
SOLOMON K D, LORENTE R, FANNEY D, et al. Clinical study using a new phacoemulsification system with surgical intraocular pressure control[J]. J Cataract Refract Surg, 2016, 42(4): 542-549. |
| [16] |
SHARIF-KASHANI P, FANNEY D, INJEV V. Comparison of occlusion break responses and vacuum rise times of phacoemulsification systems[J]. BMC Ophthalmol, 2014, 14: 96. |
| [17] |
REUSCHEL A, BOGATSCH H, BARTH T, et al. Comparison of endothelial changes and power settings between torsional and longitudinal phacoemulsification[J]. J Cataract Refract Surg, 2010, 36(11): 1855-1861. |
| [18] |
HO J W, AFSHARI N A. Advances in cataract surgery: preserving the corneal endothelium[J]. Curr Opin Ophthalmol, 2015, 26(1): 22-27. |




