口腔鳞状细胞癌(oral squamous cell carcinoma, OSCC)是一种多发头颈部恶性肿瘤,为东南亚地区常见的恶性肿瘤,全世界每年新增的OSCC病例多达30万余例[1]。虽近十年来恶性肿瘤的生物治疗、靶向治疗有了突破,然而OSCC患者主要还是依靠手术、放疗、化疗等传统治疗,总体5年的生存率仍只有50%左右[2]。因而,治疗OSCC的关键还在于探索更有效的、新的预后因子。
MED是一种进化保守的多蛋白,为所有细胞生长及生存基础[3]。真核生物中,mRNA转录依赖RNA聚合酶Ⅱ,它受不同的分子调控,如MED亚单位、一般转录因子和染色质[4]。迄今为止,转录机械功能障碍已被证明可导致细胞发育、增殖和分化异常,甚至诱发癌症[5]。在恶性肿瘤细胞中,特定基因的激活往往致转录异常[6]。到目前为止,约有30个MED亚单位在人类基因组中被证实[7]。近期研究显示,MED多个亚单位参与了多种癌症发生,如前列腺癌、结肠癌、乳腺癌、肺癌等[8]。到目前为止,许多亚单位已经在人类基因中发生突变或在癌症中出现特异性表达。其中,MED1、MED28、MED12、CDK8和Cyclin C在恶性肿瘤发生机制中的作用得到了充分的证实。而其中,有学者研究了MED28在恶性肿瘤内皮细胞中的表达[9],MED28在乳腺癌中表达增加,同时MED28可以通过表皮生长因子(epidermal growth factor, EGF)上调诱导人乳腺癌细胞金属蛋白酶(MMP2)的表达[10]。与影像学相结合,MED亚单位作为一种新的恶性肿瘤的诊断和预后标志物广泛应用于临床肿瘤学,为开发新的抗癌靶点和分子靶向治疗提供了可靠的依据[11]。这些研究表明,MED28可以作为恶性肿瘤的预后预测因子,其高表达可能预测疾病相关死亡的更大风险。
本课题组前期通过生物信息学分析显示,33个MED亚单位在TCGA-HNSC的OSCC亚组中的表达与预后相关,其中,MED28的功能是最有潜在预后价值的[12]。因而本研究拟分析MED28在本院OSCC患者中的表达水平及其与预后的关系,为OSCC的治疗和预后预测提供理论依据。
1 资料与方法 1.1 一般资料选取2015年1月至2020年6月首次在我院口腔颌面外科就诊住院手术的OSCC患者142例(发病部位在口腔、舌、唇、颊、腭、牙龈、口咽等),包括91例癌旁组织标本,术后病理结果均为口腔鳞状细胞癌,癌旁组织经HE染色证实无癌细胞浸润,取得病理结果前未接受手术、放化疗及其他抗肿瘤治疗,能够定期取得电话或者微信随访,确诊之日为随访开始时间,终止事件因肿瘤而死亡,排除非肿瘤的相关死亡。患者中男性89例,女性53例;年龄26~82(58.96±12.08)岁;有吸烟史者65例;TNM分期:Ⅰ期21例、Ⅱ期53例、Ⅲ期42例、Ⅳ期26例;有淋巴结转移44例。本研究经陆军军医大学第二附属医院医学伦理委员会批准(2019-研第108-01)。
1.2 方法 1.2.1 临床石蜡样本组织切片收集OSCC患者相关信息,选取患者癌组织和癌旁组织的蜡块,并切片。
1.2.2 临床石蜡样本组织免疫组化染色使用Roche全自动免疫组化染色法(仪器型号:Benchmark Ultra,生产商:Roche),首先将临床石蜡样本组织连续切片,置于切片架上,放入72 ℃医用烘干箱中,烘烤8 min,随后放入EZ prep液体,脱蜡4 min,水合处理使用梯度乙醇溶液,再以CC1 (含Tris缓冲液,pH8.5)行抗原修复,滴加3%的过氧化氢于切片上,孵育30 min。反复用磷酸盐缓冲液(PBS)洗涤。加100 μL抑制剂,再加油膜LCS,36 ℃孵育4 min。滴加一抗(MED28抗体,1 ∶150)孵育32 min。使用PBS洗涤3次,每次约5 min。滴加二抗,36 ℃恒温孵箱孵育4 min,再用PBS洗涤3次,随后,依次使用DAB显色,并用苏木精Ⅱ称染12 min,返蓝4 min,取出切片,用含有清洗剂的清水涮洗1 min,梯度乙醇脱水,最后用过二甲苯、中性树胶进行封片。根据染色强度和阳性细胞率,结果采用综合判定法。染色强度:棕褐色3分,棕黄色2分,淡黄色1分,无着色0分;阳性细胞率以阳性细胞数≥75%、51%~74%、26%~50%、10%~25%及<10%,分别计4分、3分、2分、1分、0分;最终得分为2个得分相乘结果,阳性结果为大于2分者,否则判为阴性。根据142例癌组织切片的最终得分平均值,将得分≤平均值的设为MED28低表达组,高于平均值的设为MED28高表达组。2名资深病理医师用盲法独立评估所有切片。
1.3 统计学分析采用SPSS 23.0进行统计分析。癌组织、癌旁组织中MED28表达对比进行卡方检验,运用Logistics回归分析MED28表达与OSCC病理特征的关系,Kaplan-Meier法对患者随访的生存情况进行分析,Log-rank检验比较生存率,并以COX回归模型分析预后的影响因素;P < 0.05为差异具有统计学意义。
2 结果 2.1 OSCC患者MED28的表达与临床病理特征的关系本研究共纳入142例OSCC患者,其中91例为符合病理学研究的癌旁正常组织。免疫组化结果显示,MED28在OSCC患者癌组织中呈阳性表达(图 1)。根据免疫组化染色评分结果,发现MED28在癌组织中的表达明显高于癌旁组织(P < 0.01,表 1)。142例癌组织切片免疫组化染色的最终得分平均值为4.12分,MED28低表达组73例(切片最终得分≤4.12),MED28高表达组69例(切片最终得分>4.12分),两组淋巴结转移差异有统计学意义(P < 0.001,表 2)。通过Logistics回归分析,发现MED28表达与吸烟、淋巴结转移相关(P < 0.05,表 3)。

|
| 患者1和患者2的癌组织中MED28均为阳性表达,即切片最终得分>2分;而两患者的癌旁组织中MED28均为阴性表达,即切片最终得分≤2分 图 1 MED28在癌组织及癌旁组织中的表达比较 |
| 组织类型 | 总数(n) | MED28的表达 | |
| 阳性 | 阴性 | ||
| 癌组织 | 142 | 103 | 39 |
| 癌旁组织 | 91 | 17 | 74 |
| χ2值 | 64.40 | ||
| P值 | < 0.001 | ||
| 临床特征 | 总数(n) | MED28的表达 | χ2值 | P值 | |
| 低表达(n=73) | 高表达(n=69) | ||||
| 性别 | |||||
| 男 | 89 | 47(52.8) | 42(47.2) | 0.187 | 0.665 |
| 女 | 53 | 26(49.1) | 27(50.9) | ||
| 年龄 | |||||
| < 60岁 | 66 | 31(47.0) | 35(53.0) | 0.973 | 0.324 |
| ≥60岁 | 76 | 42(55.3) | 34(44.7) | ||
| 肿瘤大小 | |||||
| < 3 cm | 43 | 24(55.8) | 19(44.2) | 0.479 | 0.489 |
| ≥3 cm | 99 | 49(49.5) | 50(50.5) | ||
| 分化程度 | |||||
| 高分化 | 47 | 25(53.2) | 22(46.8) | 0.998 | 0.607 |
| 中分化 | 65 | 35(53.8) | 30(46.2) | ||
| 低分化 | 30 | 13(43.3) | 17(56.7) | ||
| 吸烟 | |||||
| 未吸烟 | 77 | 45(58.4) | 32(41.6) | 3.331 | 0.068 |
| 吸烟 | 65 | 28(43.1) | 37(56.9) | ||
| TNM分期 | |||||
| Ⅰ~Ⅱ期 | 74 | 37(50.0) | 37(50.0) | 0.123 | 0.726 |
| Ⅲ~Ⅳ期 | 68 | 36(52.9) | 32(47.1) | ||
| 淋巴结转移 | |||||
| 未转移 | 98 | 64(65.3) | 34(34.7) | 24.454 | < 0.001 |
| 转移 | 44 | 9(20.5) | 35(79.5) | ||
| 临床特征 | β | SE | Wald | P值 | OR(95%CI) |
| 性别 | 0.294 | 0.412 | 0.507 | 0.476 | 1.341(0.598~3.009) |
| 年龄分级 | -0.172 | 0.405 | 0.180 | 0.672 | 0.842(0.381~1.862) |
| 肿瘤大小 | 0.285 | 0.532 | 0.287 | 0.592 | 1.330(0.469~3.769) |
| 中分化(vs高分化) | -0.044 | 0.450 | 0.010 | 0.922 | 0.957(0.397~2.309) |
| 低分化(vs高分化) | 0.241 | 0.542 | 0.199 | 0.656 | 1.273(0.440~3.680) |
| 吸烟 | 1.008 | 0.414 | 5.931 | 0.015 | 2.740(1.217~6.167) |
| TNM分期 | -0.364 | 0.497 | 0.538 | 0.463 | 0.695(0.262~1.839) |
| 淋巴结转移 | 2.268 | 0.476 | 22.677 | < 0.001 | 9.659(3.798~24.563) |
2.2 OSCC患者MED28的表达与预后的关系
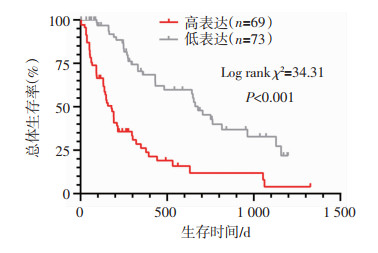
Kaplan-Meier生存分析结果显示MED28的表达与OSCC患者总体生存时间(OS)显著相关,MED28高表达组总体生存时间显著低于低表达组(P < 0.01,图 2)。多因素与预后的关系采用COX回归分析,发现MED28高表达组的死亡风险是低表达组的5.301倍,同时男性和吸烟者的预后较差(P < 0.05,表 4)。
|
| 图 2 MED28的表达与OSCC患者生存期的关系 |
| 临床特征 | β | SE | Wald | P值 | HR(95%CI) |
| 性别 | -0.748 | 0.261 | 8.228 | 0.004 | 0.474(0.284~0.789) |
| 年龄分级 | 0.206 | 0.238 | 0.749 | 0.387 | 1.229(0.770~1.961) |
| 肿瘤大小 | 0.472 | 0.304 | 2.410 | 0.121 | 1.603(0.884~2.907) |
| 中分化(vs高分化) | 0.098 | 0.267 | 0.134 | 0.714 | 1.103(0.653~1.861) |
| 低分化(vs高分化) | -0.029 | 0.309 | 0.009 | 0.924 | 0.971(0.530~1.779) |
| 吸烟 | 0.761 | 0.230 | 10.943 | 0.001 | 2.140(1.363~3.358) |
| TNM分期 | -0.301 | 0.270 | 1.243 | 0.265 | 0.740(0.436~1.256) |
| 淋巴结转移 | -0.327 | 0.275 | 1.409 | 0.235 | 0.721(0.421~1.237) |
| MED28表达 | 1.668 | 0.280 | 35.431 | < 0.001 | 5.301(3.061~9.181) |
3 讨论
OSCC是头颈部常见的恶性肿瘤之一,其发病率和死亡率呈上升趋势,已成为全球性的公共卫生问题。传统的治疗方法,不论是放疗还是根治性的手术,都会致患者的咀嚼功能下降,甚至张口受限。严重时,这些治疗还会损毁患者的外观和发音,造成巨大的精神心理障碍[13]。因此,靶向治疗、生物治疗等治疗方法越来越受到重视。虽然近年来治疗方法有所改进,但5年生存率仍然没有明显提高。因此,寻找新的预测基因和治疗靶点是提高OSCC患者5年生存率的关键所在[14]。
近年来,MED亚基在mRNA转录中的重要调控作用受到越来越多的关注和研究,MED亚基异常表达引起的转录功能障碍已被证实可诱导多种癌症[15]的发生。有研究发现,通过抑制MED28的表达可以抑制MMP2的表达,而过表达MED28可增强MMP2的表达和细胞迁移[16]。此项研究提示MED28可能是影响乳腺癌患者生存率的一个新的独立预后指标[17]。同时,浸润性导管癌和导管原位癌中MED28蛋白的表达水平明显高于非恶性腺癌的导管上皮细胞。MED28与结肠癌、肺癌、前列腺癌的发生发展也密切相关[18],与OSCC的关系有待进一步探讨。
在对我院口腔颌面外科142例OSCC患者的研究中,证实了MED28在OSCC组织中的表达水平明显高于癌旁组织,且其表达水平与吸烟、淋巴结转移相关。生存分析显示,MED28高表达患者的预后较低表达者差(P < 0.01)。多因素与预后的关系采用COX回归分析,发现MED28高表达组的死亡风险明显高于MED28低表达组,同时男性和吸烟者的预后较差,这可能与男性吸烟者较女性多有关,而吸烟已列为口腔癌的诱因之一。MED28的表达与OSCC的关系与乳腺癌、前列腺癌的结果一致,但与肺癌有所不同。可能的原因是MED亚单位属于激素受体所必需的共激活因子,其中前列腺癌和乳腺癌都是激素性的,而肺癌是非激素性的[19]。
本研究证实了MED28的表达与OSCC患者的预后直接相关,且与患者吸烟状况、淋巴结转移有关,可作为OSCC患者肿瘤进展情况与预后判断的重要指标,为潜在的诊断标志物和治疗靶点。但关于MED28在OSCC中的具体作用机制还有待进一步研究,且因标本数量少,随访时间短,其远期的影响和相关性尚待观察。
| [1] |
ALLEN B L, TAATJES D J. The mediator complex: a central integrator of transcription[J]. Nat Rev Mol Cell Biol, 2015, 16(3): 155-166. DOI:10.1038/nrm3951 |
| [2] |
ROBINSON P J, TRNKA M J, BUSHNELL D A, et al. Structure of a complete mediator-RNA polymerase Ⅱ pre-initiation complex[J]. Cell, 2016, 166(6): 1411-1422. DOI:10.1016/j.cell.2016.08.050 |
| [3] |
CLARK A D, OLDENBROEK M, BOYER T G. Mediator kinase module and human tumorigenesis[J]. Crit Rev Biochem Mol Biol, 2015, 50(5): 393-426. DOI:10.3109/10409238.2015.1064854 |
| [4] |
SCHIANO C, CASAMASSIMI A, RIENZO M, et al. Involvement of Mediator complex in malignancy[J]. Biochim Biophys Acta, 2014, 1845(1): 66-83. DOI:10.1016/j.bbcan.2013.12.001 |
| [5] |
SHAIKHIBRAHIM Z, OFFERMANN A, HALBACH R, et al. Clinical and molecular implications of MED15 in head and neck squamous cell carcinoma[J]. Am J Pathol, 2015, 185(4): 1114-1122. DOI:10.1016/j.ajpath.2014.12.010 |
| [6] |
SCHMITZ S, MACHIELS J P. Molecular biology of squamous cell carcinoma of the head and neck: relevance and therapeutic implications[J]. Expert Rev Anticancer Ther, 2010, 10(9): 1471-1484. DOI:10.1586/era.10.115 |
| [7] |
PURAM S V, TIROSH I, PARIKH A S, et al. Single-cell transcriptomic analysis of primary and metastatic tumor ecosystems in head and neck cancer[J]. Cell, 2017, 171(7): 1611-1624. DOI:10.1016/j.cell.2017.10.044 |
| [8] |
YUAN H T, YAN M, ZHANG G X, et al. CancerSEA: a cancer single-cell state atlas[J]. Nucleic Acids Res, 2019, 47(D1): D900-D908. DOI:10.1093/nar/gky939 |
| [9] |
MONTOJO J, ZUBERI K, RODRIGUEZ H, et al. GeneMANIA: Fast gene network construction and function prediction for Cytoscape[J]. F1000Res, 2014, 3: 153. DOI:10.12688/f1000research.4572.1 |
| [10] |
DE ANDRADE N P, RODRIGUES M F S D, RODINI C O, et al. Cancer stem cell, cytokeratins and epithelial to mesenchymal transition markers expression in oral squamous cell carcinoma derived from ortothopic xenoimplantation of CD44 high cells[J]. Pathol-Res Pract, 2017, 213(3): 235-244. DOI:10.1016/j.prp.2016.12.009 |
| [11] |
LEE M, JI H, FURUTA Y, et al. p120-catenin regulates REST and CoREST, and modulates mouse embryonic stem cell differentiation[J]. J Cell Sci, 2014, 127(pt 18): 4037-4051. DOI:10.1242/jcs.151944 |
| [12] |
XIANG Z, ZHOU S, LIANG S, et al. RCOR1 directly binds to MED28 and weakens its inducing effect on cancer stem cell-like activity of oral cavity squamous cell carcinoma cells[J]. J Oral Pathol Med, 2020, 49(8): 741-750. DOI:10.1111/jop.13022 |
| [13] |
CHO J, CHOI J S, LEE J H, et al. MED28 over-expression shortens the cell cycle and induces genomic instability[J]. Int J Mol Sci, 2019, 20(7): 1746. DOI:10.3390/ijms20071746 |
| [14] |
HUANG C Y, HSIEH N T, LI C I, et al. MED28 regulates epithelial-mesenchymal transition through NFκB in human breast cancer cells[J]. J Cell Physiol, 2017, 232(6): 1337-1345. DOI:10.1002/jcp.25610 |
| [15] |
HUANG C Y, CHOU Y H, HSIEH N T, et al. MED28 re-gulates MEK1-dependent cellular migration in human breast cancer cells[J]. J Cell Physiol, 2012, 227(12): 3820-3827. DOI:10.1002/jcp.24093 |
| [16] |
LEE M F, HSIEH N T, HUANG C Y, et al. All Trans-retinoic acid mediates MED28/HMG box-containing protein 1 (HBP1)/β-catenin signaling in human colorectal cancer cells[J]. J Cell Physiol, 2016, 231(8): 1796-1803. DOI:10.1002/jcp.25285 |
| [17] |
HSIEH N T, HUANG C Y, LI C C, et al. MED28 and forkhead box M1 (FOXM1) mediate matrix metalloproteinase 2 (MMP2)-dependent cellular migration in human nonsmall cell lung cancer (NSCLC) cells[J]. J Cell Physiol, 2019, 234(7): 11265-11275. DOI:10.1002/jcp.27784 |
| [18] |
LI L, WALSH R M, WAGH V, et al. Mediator subunit Med28 is essential for mouse peri-implantation development and pluripotency[J]. PLoS ONE, 2015, 10(10): e0140192. DOI:10.1371/journal.pone.0140192 |
| [19] |
YAO H L, GOLDMAN D C, FAN G, et al. The corepressor Rcor1 is essential for normal myeloerythroid lineage differentiation[J]. Stem Cells, 2015, 33(11): 3304-3314. DOI:10.1002/stem.2086 |




