2. 300070 天津,天津医科大学研究生院;
3. 300193 天津,天津医药集团研究院有限公司
2. Graduate School of Tianjin Medical University, Tianjin, 300070;
3. Tianjin Pharmaceutical Group Research Institute Co., Ltd, Tianjin, 300193, China
直接口服抗凝药(direct oral anticoagulants, DOACs)是近年来研制开发的一类口服抗凝药,由于其优于华法林的药代动力学性质和安全性,被广泛地应用于心房颤动所致脑卒中的预防,以及手术后肺栓塞、深静脉血栓和动脉血栓的预防[1-2]。DOACs作为抗凝药物,服用后会导致凝血指标改变,从而影响临床上一些凝血敏感指标的检测,有时会出现假阳性的结果。当服用DOACs的患者需要检测相关指标时,为排除DOACs的干扰不得不采取停药的措施,而停药后患者凝血功能发生改变,容易造成血栓形成的风险,因此,寻找一种或一类药物,有效清除血浆内DOACs的影响,显得尤为重要。
DOAC-Stop是澳大利亚Haematex Research公司研制开发的药物,用于清除血浆中所有类型的DOACs。据报道,DOAC-Stop能够有效清除包括达比加群酯、阿哌沙班和利伐沙班等在内的绝大多数DOACs,而对血浆的凝血功能无显著影响。知非沙班是天津药物研究院自主研发的新型口服FXa抑制剂,前期实验已证实其与利伐沙班类似,具有显著的抑制动静脉血栓作用[3-4]。知非沙班作为最新开发的DOACs,DOAC-Stop对它的清除作用尚不清楚。本研究采用离体和在体实验,使用DOAC-Stop处理含知非沙班的血浆,观察其对知非沙班的清除效果。
1 材料与方法 1.1 药品及试剂知非沙班由天津药物研究院创新药研究中心提供,批号:Y-121225;DOAC-Stop由澳大利亚Haematex Research公司提供,批号:475-1-P1;S-2765由北京艾德豪克国际技术有限公司生产,批号:170306;RVV-X为日本Sekisui Diagnostics GmbH公司产品,批号:41985101;凝血酶原时间(prothrombin time, PT)测定试剂盒为美德太平洋科技有限公司产品,批号:011710A;活化部分凝血酶时间(activated partial thrombopastin time, APTT)测定试剂盒为美德太平洋科技有限公司产品,批号:021708A。
1.2 仪器Rayto RT-6100酶标仪为深圳雷杜生命科学股份有限公司产品;LG-PABER型凝血因子分析仪为北京世帝科学仪器公司产品;高效液相色谱仪为美国沃特世公司产品;Sartorius电子分析天平为北京赛多利斯天平有限公司产品;LD5-2A离心机为北京医用离心机厂产品。
1.3 实验动物及饲养环境Beagle犬,雄性,体质量10~12 kg,辽宁省沈阳康平实验动物研究所提供,许可证号SCXK(辽)2014-0003;Wistar大鼠,雌雄兼用,体质量220~250 g,北京维通利华实验动物技术有限公司提供,动物生产许可证号SCXK(京)2016-0011,在温度22℃、相对湿度60%、光照/黑暗12 h/12 h条件下饲养。
1.4 不同浓度知非沙班对离体给药血浆PT、APTT与FXa活性的影响雄性健康Beagle犬3只,每只犬股静脉采血8 mL,3.8%枸橼酸钠抗凝(血∶抗凝剂=1∶9),3 000 r/min离心10 min,取血浆,分为4等份,每份900 μL,分别设置为对照组和知非沙班低、中、高剂量组,对照组加入100 μL知非沙班溶剂(DMSO),知非沙班低、中、高剂量组分别加入100 μL 0.01、0.10、1.00 mg/mL的知非沙班,充分混匀后进行PT、APTT和凝血因子Xa(FXa)活性检测,PT和APTT采用试剂盒法按照说明书方法操作。FXa活性采用生色底物法检测[5-7],方法为:取40 μL血浆,加入10 μL含1 mg/mL的凝血酶抑制剂水蛭素和50 μL 800 μmol/L的S-2765,室温下孵育5 min,然后加入50 μL 200 mU的RVV-X开始反应,在酶标仪405 nm处于反应起始与反应后5 min各测定光密度值[D(405)]1次,2次光密度值差值除以反应时间,即得FXa活性。
1.5 不同剂量DOAC-Stop对知非沙班离体给药的清除作用雄性健康Beagle犬3只,每只犬股静脉分批采血40 mL,3.8%枸橼酸钠抗凝(血∶抗凝剂=1∶9),3 000 r/min离心10 min,取血浆,分为12等份,每份900 μL,分别设置为对照组、DOAC-Stop 1/512、1/256、1/128、1/64、1/32、1/16、1/8、1/4、1/2、1 minitabs/mL组、知非沙班组。对照组加入100 μL知非沙班溶剂(DMSO),知非沙班组加入100 μL 0.1 mg/mL的知非沙班,对照组和知非沙班组不加入DOAC-Stop,仅进行相应的离心处理,DOAC-Stop 1/512~1 minitabs/mL组均加入100 μL 0.1 mg/mL的知非沙班,然后分别加入1/512、1/256、1/128、1/64、1/32、1/16、1/8、1/4、1/2、1 minitabs的DOAC-Stop(1片DOAC-Stop为1 minitab),充分混悬5 min,常温3 000 r/min离心10 min,取上清备用。试剂盒法检测PT与APTT,生色底物法检测FXa活性。高效液相法检测血浆内知非沙班的浓度,采用华谱Unitary C18色谱柱,流动相A为乙腈,流动相B为水,等度洗脱10 min(A∶B=40∶60),流速1.0 mL/min,柱温35 ℃,检测波长250 nm,进样量10 μL。
1.6 不同剂量知非沙班在体给药对血浆PT、APTT和FXa活性的影响健康Wistar大鼠24只,雌雄各半,按照体质量分为对照组,知非沙班低、中、高剂量组,每组6只。其中对照组大鼠灌胃给予相应体积的溶剂(含0.5%吐温80的聚乙二醇甘油酯),知非沙班低、中、高剂量组分别灌胃给予3、10、30 mg/kg的知非沙班。给药1.5 h后,各组大鼠水合氯醛(0.36 g/kg, ip)麻醉,腹主动脉插管采血,3.8%枸橼酸钠抗凝(全血∶抗凝剂=9∶1),3 000 r/min离心10 min后取血浆,用于PT、APTT和FXa活性的检测,检测方法同离体实验部分。
1.7 DOAC-Stop对知非沙班在体给药的清除作用健康Wistar大鼠24只,雌雄各半,按照体质量分为对照组、知非沙班组、DOAC-Stop对照组、知非沙班+DOAC-Stop组,每组6只。其中对照组和DOAC-Stop对照组大鼠灌胃给予相应体积的溶剂(含0.5%吐温80的聚乙二醇甘油酯),知非沙班组和知非沙班+DOAC-Stop组均灌胃给予30 mg/kg的知非沙班。给药1.5 h后,各组大鼠水合氯醛麻醉采血取血浆,方法同上,其中对照组和知非沙班组仅进行相应的离心处理,DOAC-Stop对照组和知非沙班+DOAC-Stop组均在1 mL血浆内加入1片DOAC-Stop,充分混匀5 min后,3 000 r/min离心取上清。PT、APTT、FXa活性及知非沙班浓度检测方法同上。
1.8 统计学分析采用SPSS 20.0统计软件,计量资料以x±s表示,组间比较用单因素方差分析,方差齐者用LSD检验,方差不齐者用Dunnett-t检验,P < 0.05为差异有统计学意义。
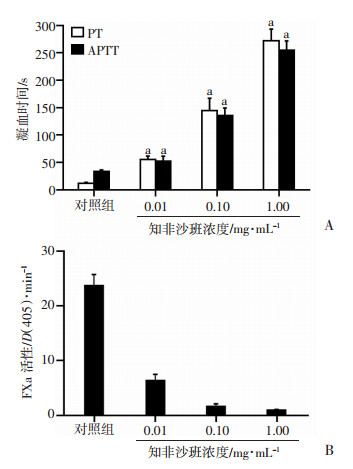
2 结果 2.1 不同浓度知非沙班离体给药对血浆PT、APTT和FXa活性的影响犬血浆的PT和APTT分别为11.8 s和33.4 s,加入0.01、0.10、1.00 mg/mL知非沙班后,凝固时间均显著延长,且存在一定的剂量依赖性,与对照组比较,PT分别延长了372.0%(P < 0.001)、1 125.4%(P < 0.001)、2 205.1%(P < 0.001),APTT分别延长了55.7%(P < 0.05)、307.2%(P < 0.001)、664.4%(P < 0.001),见图 1A。
|
|
a: P < 0.001,与对照组比较 A: 血浆PT和APTT;B: 血浆FXa活性 图 1 不同浓度知非沙班离体给药对血浆PT、APTT和FXa活性的影响 |
犬血浆的FXa活性为23.7,加入0.01、0.10、1.00 mg/mL知非沙班后,FXa活性剂量依赖性降低,与对照组比较,FXa活性分别降低了73.0%(P < 0.001)、93.2%(P < 0.001)、95.8%(P < 0.001),见图 1B。
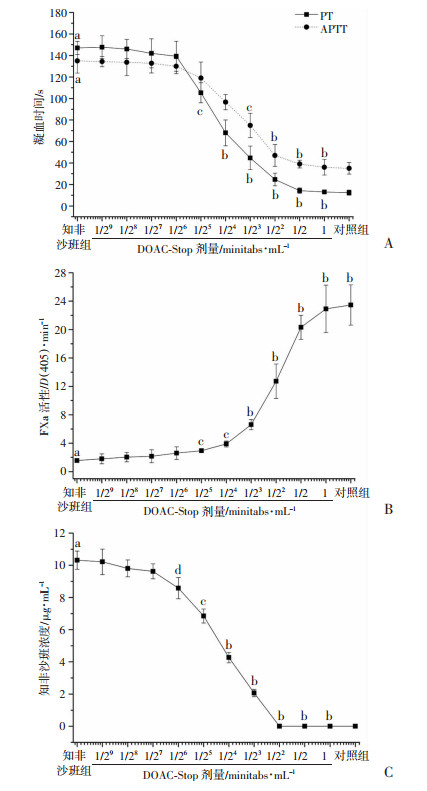
2.2 不同剂量DOAC-Stop对知非沙班离体给药的清除作用犬血浆内加入0.1 mg/mL的知非沙班后,PT和APTT均显著延长(12.4 vs 147.0 s, P < 0.001;35.0 vs 135.1 s, P < 0.001);含知非沙班的血浆使用不同剂量DOAC-Stop处理后,PT和APTT均显著降低,且具有剂量依赖性,与知非沙班组比较,DOAC-Stop 1/512、1/256、1/128、1/64、1/32、1/16、1/8、1/4、1/2、1 minitabs组PT分别降低了-0.5%(P>0.05)、0.7%(P>0.05)、3.4%(P>0.05)、5.2%(P>0.05)、28.4% (P < 0.01)、53.7% (P < 0.001)、69.6%(P < 0.001)、83.2% (P < 0.001)、90.3%(P < 0.001)、91.2%(P < 0.001),APTT分别降低了0.5%(P>0.05)、1.0%(P>0.05)、1.7%(P>0.05)、3.7%(P>0.05)、11.9%(P < 0.01)、28.4%(P < 0.001)、44.4%(P < 0.001)、65.2%(P < 0.001)、71.1%(P < 0.001)、73.3%(P < 0.001),见图 2A。
|
|
a: P < 0.001,与对照组比较;b: P < 0.001,c: P < 0.01,d: P < 0.05,与知非沙班组比较 A: 血浆PT和APTT;B: 血浆FXa活性;C: 血药浓度 图 2 不同剂量DOAC-Stop对知非沙班离体给药的影响 |
犬血浆内加入0.1 mg/mL的知非沙班后,FXa活性显著降低(23.5 vs 1.6, P < 0.01);加入知非沙班的血浆使用不同剂量DOAC-Stop处理后,FXa活性剂量依赖性地升高,与知非沙班组比较,DOAC-Stop 1/512、1/256、1/128、1/64、1/32、1/16、1/8、1/4、1/2、1 minitabs组FXa活性分别升高了14.9%(P>0.05)、29.7%(P>0.05)、38.3%(P>0.05)、66.1%(P>0.05)、87.6%(P < 0.01)、148.4%(P < 0.001)、321.8%(P < 0.001)、712.2%(P < 0.001)、1 196.3%(P < 0.001)、1 362.0%(P < 0.001),见图 2B。
对照组血浆内无知非沙班检出,加入0.1 mg/mL知非沙班后,知非沙班血浆内的浓度为10.3 μg/mL;加入知非沙班的血浆使用不同剂量DOAC-Stop处理后,知非沙班浓度呈剂量依赖性的降低,与知非沙班组比较,DOAC-Stop 1/512、1/256、1/128、1/64、1/32、1/16、1/8 minitabs组分别降低了1.0%(P>0.05)、4.9%(P>0.05)、6.7%(P>0.05)、16.8%(P < 0.05)、33.6%(P < 0.01)、58.6%(P < 0.001)、80.0%(P < 0.001),DOAC-Stop 1/4、1/2、1 minitabs组均未检出知非沙班(P < 0.001),见图 2C。
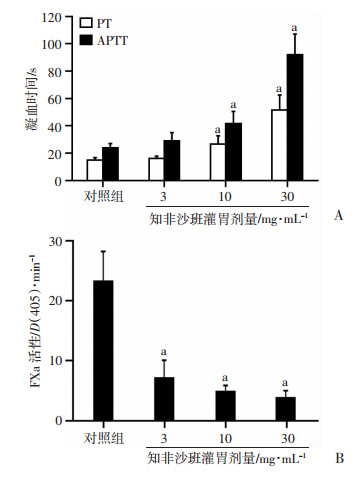
2.3 不同剂量知非沙班在体给药对血浆PT、APTT和FXa活性的影响大鼠血浆的PT和APTT分别为14.8 s和24.0 s,灌胃给予3、10、30 mg/kg知非沙班后,凝固时间均显著延长,且存在一定的剂量依赖性,与对照组相比较,PT分别延长了8.8%(P>0.05)、81.1%(P < 0.001)、248.0%(P < 0.001),APTT分别延长了20.8%(P>0.05)、73.8%(P < 0.001)、283.3%(P < 0.001),见图 3A。
|
|
a: P < 0.001,与对照组比较 A: 血浆PT和APTT;B: 血浆FXa活性 图 3 不同剂量知非沙班在体给药对血浆PT、APTT和FXa活性的影响 |
大鼠血浆的FXa活性为23.2,灌胃给予3、10、30 mg/kg知非沙班后,FXa活性剂量依赖性降低,与对照组比较,FXa活性分别降低了69.4%(P < 0.001)、78.9%(P < 0.001)、83.6%(P < 0.001),见图 3B。
2.4 DOAC-Stop对知非沙班在体给药的清除作用大鼠血浆使用DOAC-Stop处理后,PT和APTT均无显著性变化(15.0 vs 14.0 s, 24.9 vs 26.0 s, P>0.05)。大鼠灌胃给予30 mg/kg知非沙班后,PT和APTT均显著延长(15.0 vs 27.3 s, P < 0.001;24.9 vs 41.3 s, P < 0.001),知非沙班给药组大鼠血浆使用DOAC-Stop处理后,PT与APTT均显著缩短(27.3 vs 16.3 s, P < 0.001;41.3 vs 31.1 s, P < 0.01),见图 4A。

|
|
a: P < 0.001,与对照组比较;b: P < 0.001,c:P < 0.01,与知非沙班组比较 A: 血浆PT和APTT;B: 血浆FXa活性;C: 血药浓度 图 4 DOAC-Stop对知非沙班在体给药的影响 |
正常大鼠血浆使用DOAC-Stop处理后,FXa活性无显著变化(22.7 vs 21.2, P>0.05)。大鼠灌胃给予30 mg/kg知非沙班后,FXa活性显著降低(22.7 vs 5.2, P < 0.001),灌胃给予知非沙班大鼠血浆使用DOAC-Stop处理后,FXa活性显著恢复(5.2 vs 9.6, P < 0.001),见图 4B。
对照组和DOAC-Stop对照组血浆内均无知非沙班的存在。大鼠灌胃给予知非沙班1.5 h后,血浆内知非沙班的浓度为4.6 μg/mL,使用DOAC-Stop处理5 min后,血浆内知非沙班完全被清除,未检出知非沙班存在(P < 0.001),见图 4C。
3 讨论DOACs是继华法林后应用最广泛的口服抗凝药物,作为抗凝药物,对凝血指标的影响不容忽视,同时,该类药物缺乏特异性拮抗剂,在发生严重出血或需要紧急手术时无法消除其抗凝活性。针对DOACs的特异性拮抗剂目前正在开发当中,但在实验室检测中目前尚未广泛使用。Idarucizumab是德国勃林格殷格翰公司研制针对达比加群酯的特异性拮抗剂,在离体血浆实验中,它可以有效中和达比加群酯的抗凝效果,但它的拮抗效果仅针对达比加群酯,而对口服FXa抑制剂无效[8-9]。Andaxanet alpha是美国波特兰制药公司研制的FXa抑制剂拮抗剂,它是一个重组凝血因子Xa(FXa)诱导分子,可以竞争性地抑制直接或间接FXa抑制剂如利伐沙班、阿哌沙班等的抗凝活性[10-11]。Ciraparantag是美国Perosphere公司研制的“通用型”抗凝药物拮抗剂,据称可以逆转DOACs和大多数其他种类抗凝药物[12]。Andaxanet alpha和Ciraparantag目前均处于临床阶段,且在使用过程中需要根据DOACs的浓度计算准确用药剂量,过量使用可能会导致促凝血或产生免疫原性,因而均不利于常规实验检测使用[13]。
DOAC-Stop是根据活性炭的吸附功能研制开发的药物,用于清除血浆中所有类型的DOACs[14]。EXNER等[13]的研究结果表明:DOAC-Stop可以将血浆内的达比加群酯、阿哌沙班、利伐沙班和依杜沙班彻底清除,使得血浆凝固指标无显著的影响,从而避免系统性红斑狼疮抗凝检测的假阳性结果。在临床检测中,DOACs的存在可以对血栓形成测试(如抗凝、蛋白S、蛋白C活性等)造成影响,为避免该类药物对检测结果的影响,有时不得不停止药物的服用。DOAC-Stop通过简单有效的吸附作用,可以很好地消除DOACs的影响,从而使得患者不必停药,降低血栓产生的风险[15]。此外,JACQUEMIN等[16]通过测定药物浓度、PT、APTT等,发现DOAC-Stop对达比加群酯的吸附作用可以达到和idarucizumab的中和作用相同的效果,进而使得服用达比加群酯的患者可以接受常规凝血指标检测。
尽管DOAC-Stop对DOACs均有较好的清除效果,但对于不同的DOACs,其清除效果也不尽相同,EXNER等[17]的研究表明,相对于利伐沙班和阿哌沙班,它对达比加群酯和依度沙班的清除更加彻底,因此,对于新出现的DOAC,有必要研究DOAC-Stop针对它的清除效果。知非沙班是国内首个口服FXa抑制剂,和利伐沙班、阿哌沙班等均属于DOACs,DOAC-Stop对它的清除作用尚不明确。本研究采用离体和在体两种给药途径,观察DOAC-Stop对知非沙班的清除作用。结果表明:无论离体还是在体给药,DOAC-Stop均能缩短由知非沙班所致的PT、APTT的延长,恢复FXa的活性,高效液相结果显示,经DOAC-Stop处理后,直接加入或口服吸收知非沙班的动物血浆内,均未见知非沙班的检出,表明DOAC-Stop对知非沙班有很好的清除作用。在日后临床应用中,如服用知非沙班的患者需要进行常规凝血指标或其他敏感指标检查时,为排除药物对测试结果的影响,可先使用DOAC-Stop对患者血浆进行处理,从而得出更加准确客观的结果。
DOAC-Stop作为广谱DOACs清除药物,关键在于其强大的吸附作用。根据开发者的资料表明:DOAC-Stop能够清除与DOACs分子量接近的所有小分子药物,但对静脉注射而非口服的抗凝药物包括阿加曲班、抑肽酶、鱼精蛋白、水蛭素类、多粘菌素和相关阳离子药物清除效果不佳。尽管如此,DOAC-Stop的出现为服用DOACs的患者进行常规检查提供有效的帮助,使DOACs的使用更加方便,从而提高服药者的用药依从性,值得在临床和实验室检测中推广和使用。
利益冲突声明 本研究与天津医药集团研究院有限公司不存在利益冲突
| [1] |
YEH C H, FREDENBURGH J C, WEITZ J I. Oral direct factor Xa inhibitors[J]. Circ Res, 2012, 111(8): 1069-1078. |
| [2] |
MACKMAN N, BERGMEIER W, STOUFFER G A, et al. Therapeutic strategies for thrombosis: new targets and approaches[J]. Nat Rev Drug Discov, 2020, 19(5): 333-352. |
| [3] |
QIU X M, ZHOU J J, WANG W T, et al. Effect of a new inhibitor of factor Xa zifaxaban, on thrombosis in the inferior vena cava in rabbits[J]. J Thromb Thrombolysis, 2019, 47(1): 80-86. |
| [4] |
QIU X M, WANG W T, ZHAO Z Y, et al. Pre-clinical pharmacodynamic study of a novel oral factor Xa inhibitor zifaxaban[J]. Eur J Pharmacol, 2018, 836: 50-56. |
| [5] |
IWATSUKI Y, SATO T, MORITANI Y, et al. Biochemical and pharmacological profile of darexaban, an oral direct factor Xa inhibitor[J]. Eur J Pharmacol, 2011, 673(1/2/3): 49-55. |
| [6] |
HU X, XIAO Y, YU C, et al. Characterization of a novel selective factor Xa inhibitor, DJT06001, which reduces Thrombus formation with low risk of bleeding[J]. Eur J Pharmacol, 2018, 825: 85-91. |
| [7] |
HE K, LUETTGEN J M, ZHANG D, et al. Preclinical pharmacokinetics and pharmacodynamics of apixaban, a potent and selective factor Xa inhibitor[J]. Eur J Drug Metab Pharmacokinet, 2011, 36(3): 129-139. |
| [8] |
RODRIGUES A O, DAVID C, FERREIRA J J, et al. The incidence of thrombotic events with idarucizumab and andexanet alfa: a systematic review and meta-analysis[J]. Thromb Res, 2020, 196: 291-296. |
| [9] |
RAWAL A, ARDESHNA D, MINHAS S, et al. Current status of oral anticoagulant reversal strategies: a review[J]. Ann Transl Med, 2019, 7(17): 411. |
| [10] |
KAATZ S, BHANSALI H, GIBBS J, et al. Reversing factor Xa inhibitors—clinical utility of andexanet alfa[J]. J Blood Med, 2017, 8: 141-149. |
| [11] |
NAFEE T, ASLAM A, CHI G, et al. Andexanet Alfa for the reversal of anticoagulant activity in patients treated with direct and indirect factor Xa inhibitors[J]. Expert Rev Cardiovasc Ther, 2017, 15(4): 237-245. |
| [12] |
ALMEGREN M. Reversal of direct oral anticoagulants[J]. Vasc Health Risk Manag, 2017, 13: 287-292. |
| [13] |
EXNER T, MICHALOPOULOS N, PEARCE J, et al. Simple method for removing DOACs from plasma samples[J]. Thromb Res, 2018, 163: 117-122. |
| [14] |
EXNER T, AHUJA M, ELLWOOD L. Effect of an activated charcoal product (DOAC StopTM) intended for extracting DOACs on various other APTT-prolonging anticoagulants[J]. Clin Chem Lab Med, 2019, 57(5): 690-696. |
| [15] |
FAVRESSE J, LARDINOIS B, SABOR L, et al. Evaluation of the DOAC-stopⓇ procedure to overcome the effect of DOACs on several thrombophilia screening tests[J]. TH Open, 2018, 2(2): e202-e209. |
| [16] |
JACQUEMIN M, TOELEN J, FEYEN L, et al. The adsorption of dabigatran is as efficient as addition of idarucizumab to neutralize the drug in routine coagulation assays[J]. Int J Lab Hematol, 2018, 40(4): 442-447. |
| [17] |
EXNER T, RIGANO J, FAVALORO E J. The effect of DOACs on laboratory tests and their removal by activated carbon to limit interference in functional assays[J]. Int J Lab Hematol, 2020, 42(Suppl 1): 41-48. |




