糖尿病(diabetes mellitus,DM)是严重影响人类健康的重大慢病,与非糖尿病人群相比,糖尿病患者因肿瘤、心脑血管事件、痴呆等并发症相关死亡风险显著提高[1-3]。将血糖控制在合适水平是减少糖尿病相关并发症的关键[4]。连续血糖监测(continuous glucose monitoring,CGM)可以提供连续、全面、可靠的全天血糖波动情况[5],但其高昂的费用和长时间穿戴的不适感限制了其广泛使用。糖化血红蛋白(HbA1c)与24 h平均葡萄糖水平(24 hour mean glucose, 24 h MBG)具有良好的相关性[6],目前已经作为估算24 h MBG的重要临床指标[7]。然而在贫血、妊娠、血液透析、急慢性失血等情况下,由于红细胞寿命缩短、血红蛋白结构改变以及血红蛋白与葡萄糖结合率异常等因素,导致HbA1c并不能反映真实血糖水平[8-10]。作为2型糖尿病诊断试验的口服葡萄糖耐量试验(oral glucose tolerance test, OGTT),可以用于评估胰岛功能和血糖特征[11],其与HbA1c、24 h MBG同样具有良好的相关性[12-13]。因此,本研究拟建立一种通过OGTT试验估算全天平均血糖的数学模型。
1 资料与方法 1.1 一般资料病历资料均来源于2014年1月至2017年12月于本科住院治疗的2型糖尿病患者36例。所有患者在住院期间行72 h动态血糖监测,并满足以下入组标准:①年龄≥18周岁,性别不限;②既往已诊断的糖尿病患者及新诊断的糖尿病患者[符合1999年世界卫生组织(WHO)糖尿病诊断标准:空腹血糖(fasting plasma glucose, FPG)≥7.0 mmol/L,或糖负荷后2 h血糖(2 h post plasma glucose, 2h PPG)≥11.1 mmol/L][14];③既往及血糖监测期间未使用过降糖药物;④住院期间行OGTT试验。排除标准:①1型糖尿病患者;②肝脏功能损害(ALT或者AST≥正常值上限3倍以上);③肾功能损害[肾小球滤过率<90 mL/(min·1.73 m2)];④贫血(既往明确诊断目前接受治疗的以及入院查Hb、RBC提示贫血的患者);⑤妊娠或哺乳期妇女;⑥糖尿病急性并发症者(糖尿病酮症酸中毒、高血糖高渗状态等);⑦有消化吸收功能障碍及其他内分泌疾病者;⑧ 2周内有脑梗死、心肌梗死、重大外伤或手术等应激状态;血糖监测及OGTT期间采取生酮饮食(尿酮体阳性)或地中海饮食结构。本研究遵循赫尔辛基宣言及药物临床试验质量管理规范(GCP)指导原则,已通过本院伦理委员会审查同意(医研伦审号2021-13)。
1.2 方法本研究为回顾性分析,通过电子病历系统采集所有研究对象的相关资料,包括姓名、性别、年龄、吸烟史、饮酒史、糖尿病史、体质指数[BMI=体质量(kg)/身高(m2)]、空腹血糖、OGTT 2 h血糖、糖化血红蛋白、血红蛋白、肌酐、尿素氮、总胆固醇、甘油三酯、高密度脂蛋白、低密度脂蛋白、总胆红素、谷丙转氨酶、谷草转氨酶,通过美敦力动态血糖系统收集自监测起共计3 d平均血糖。
1.2.1 动态血糖监测采用动态血糖监测仪(MiniMed系统,美敦力公司,美国)进行连续3 d的血糖监测。系统主要由感应器、血糖监测器、信息提取器和软件分析系统组成,检测范围为2.2~22.2 mmol/L。由统一的专科医生操作,专用注射器将探头插入腹部皮下。探头传感器包括半透膜、葡萄糖氧化酶和微电极3层,组织间液中的葡萄糖与氧化酶反应生成电信号,检测器每隔10 s从探头接受1次来自组织间液的电信号,将5 min的值平均后储存,同时每天至少输入4次指端血糖值进行校正,监测72 h后用信息提取器与计算机连接下载数据,通过仪器专用软件进行分析得出每日平均血糖和总平均血糖。
1.2.2 OGTT试验入院期间进行,试验前3~7 d内未使用糖皮质激素、避孕药、噻嗪类利尿剂、磺胺类药物、水杨酸钠等影响血糖的药物[11],每天进食碳水化合物> 250 g,受试者夜间禁食10~14 h,第2天早晨8:00之前空腹静脉抽血后,取82.5 g一水葡萄糖粉(dextrose monohydrate, C6H12O6.H2O)溶于300 mL温开水内,5 min内服完,从饮用第1口开始计时,于2 h采集静脉血标本送检,采用己糖激酶(HK)法分别测定空腹血糖(FPG)和糖负荷后2 h血糖(2 h PPG)。
1.3 通过OGTT估算全天平均血糖数学模型的建立 1.3.1 OGTT试验平均血糖估计模型构建参照常规OGTT试验特征血糖反应曲线形态(图 1A),将血糖反应曲线认为是随时间变化曲线函数y=f(x),y为OGTT试验后在时间x对应的血糖值。曲线下面积则表示血糖的累积值,可通过每一时间点对应的血糖值的积分函数表示,即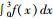
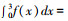


|
| A: OGTT试验特征血糖反应曲线; B: 24 h血糖累积曲线上图:理想化全天血糖波动曲线。将日间基线血糖认为是恒定水平,忽略进食后餐后血糖增高及下降曲线;下图:模型计算用日间血糖基线及餐后血糖波动图。在简化图基础上将不同时间段基线及餐后血糖结合 图 1 应用OGTT估算全天平均血糖示意图 |
1.3.2 全天平均血糖估计模型构建
应用上述构建估算平均血糖的方法,将每次进食后的3 h内血糖波动曲线可以近似用进食后2 h静脉血糖水平代替,即可将每日血糖累积曲线表示成为图 1B中第1张图。因为每日进食3餐,餐后血糖波动范围共9 h,因此,可以将空腹血糖与餐后血糖变化结合到一起,进而形成图 1B中第2张图的形态。从而得出计算全天平均血糖的计算公式:24 h平均血糖
本研究采用动态血糖仪软件设置,为避免不同佩戴时间导致初始血糖波动对全天平均血糖计算的影响,依据动态血糖仪平均血糖计算的方法[6],采用血糖监测期间第2天00:00至第4天00:00连续2 d全天血糖监测情况,每日288个点血糖测量值,2 d共计576个点血糖测量值,分别计算出每日24 h平均血糖值MBG,后通过采用平均值法估算24 h平均血糖。
1.4 统计学分析计量资料用x±s或中位数(四分位数:第25至第75百分位数)表示,计数资料用频数(构成比)表示。使用Spearman相关系数分析评估了OGTT估计全天平均血糖与HbA1c、24 h MBG之间的相关性。进行线性回归建模以估计OGTT估算平均血糖(MBGOGTT),以及MBGOGTT联合HbA1c与24 h MBG之间的关系。采用SPSS 23.0统计软件进行处理,检验水准α=0.05。
1.5 模型验证纳入住院治疗并满足纳入标准的2021年2月至2021年4月于大坪医院高血压内分泌科住院治疗的18例已行CGM监测和OGTT的糖尿病患者对该模型进行外部验证。采用一种几何意义清晰、计算简单、分辨率与灵敏度较高的曲线拟合优度指标RNL[15]评估该模型的拟合程度,其中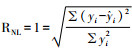
共纳入资料完整的合格病例36例,其中男性13例,年龄(62.9±13.1)岁,平均糖尿病病程6.7年,平均HbA1c为7.3%。应用OGTT试验所得血糖估计全天平均血糖为(9.66±3.34)mmol/L,应用动态血糖监测仪计算24 h MBG为[(9.40±2.67)mmol/L,表 1]。
| 年龄/岁 | 男性 | 糖尿病病程/年 | 空腹血糖/mmol·L-1 | 餐后2 h血糖/mmol·L-1 | HbA1c(%) | 收缩压/mmHg |
| 62.9±13.1 | 13(36.1) | 3.5[0.0,10.8] | 6.97±2.86 | 14.15±5.54 | 7.3±2.2 | 129±20 |
| 舒张压/mmHg | BMI/kg·m-2 | Hb/g·L-1 | 肌酐/μmol·L-1 | TC/mmol·L-1 | TG/mmol·L-1 | |
| 75±15 | 23.1±5.5 | 122.1±30.2 | 69.9±19.6 | 4.29±1.40 | 1.57±1.12 | |
| HDL-c/mmol·L-1 | LDL-c/mmol·L-1 | AST/U·L-1 | ALT/U·L-1 | MBGOGTT/mmol·L-1 | 24 h MBG/mmol·L-1 | |
| 1.11±0.43 | 2.75±1.17 | 26.7±23.7 | 25.3±28.2 | 9.66±3.34 | 9.40±2.67 | |
2.2 OGTT估计平均血糖与HbA1c、24 h MBG的相关性
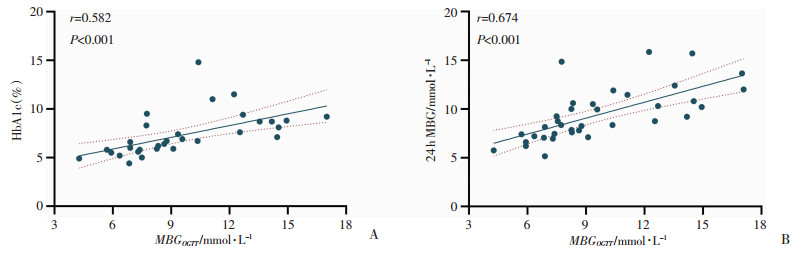
OGTT估计平均血糖与HbA1c、24 h MBG均具有较好的相关性,相关系数分别为0.582、0.674(P<0.001,图 2)。应用线性回归模型分析,建立应用OGTT估计的平均血糖反映24 h动态血糖的模型:24 h MBGmmol/L=4.166+0.545×MBGOGTT, (R=0.674,P<0.001)。为进一步提高估计的准确度,将HbA1c纳入回归分析,进而得到如下估计动态血糖的模型:24 h MBGmmol/L=1.797+0.359×MBGOGTT+0.565×HbA1c(R=0.768,P<0.001)。
|
| A:MBGOGTT与HbA1c相关性;B:MBGOGTT与24 h MBG相关性 图 2 OGTT估计平均血糖(MBGOGTT)与HbA1c、24 h MBG相关性 |
2.3 预测模型的验证
在上述数学模型基础上,进一步选取2021年2月至2021年4月于大坪医院高血压内分泌科住院治疗的18例未使用过降糖药物的糖尿病患者进行外部验证,其中年龄、BMI、收缩压、舒张压、糖尿病病程、血肌酐与试验模型相比差异均无统计学意义(表 2)。拟合优度指标RNL=0.816,表明模型与24 h血糖监测得到的平均血糖值拟合度较高,有较好的评估患者平均血糖的能力。
| 年龄/岁 | 男性 | 糖尿病病程/年 | 空腹血糖/mmol·L-1 | 餐后2 h血糖/mmol·L-1 | HbA1c(%) | 收缩压/mmHg |
| 60.9±9.9 | 9(56.3) | 3.0 [1.8,10.0] | 6.62±1.62 | 19.61±4.12 | 9.32±2.43 | 126±14 |
| 舒张压/mmHg | BMI/kg·m-2 | Hb/g·L-1 | 肌酐/μmol·L-1 | TC/mmol·L-1 | TG/mmol·L-1 | |
| 74±12 | 23.8±3.65 | 137.8±23.3 | 63.76±19.68 | 4.09±1.00 | 1.41±0.71 | |
| HDL-c/mmol·L-1 | LDL-c/mmol·L-1 | AST/U·L-1 | ALT/U·L-1 | MBGOGTT/mmol·L-1 | 24 h MBG/mmol·L-1 | |
| 1.12±0.23 | 2.78±0.83 | 25.3±15.1 | 26.9±16.8 | 11.49±1.83 | 9.91±2.02 | |
3 讨论
CGM可提供连续、全面、可靠的全天血糖信息,但其相对较高的治疗费用及对日常生活的影响限制了其广泛应用。既往国内外研究多将HbA1c作为估计全天平均血糖的指标[16-18],因其与动态血糖监测估计的全天平均血糖具有良好的相关性,同时其可作为预测糖尿病患者远期并发症和心血管事件的风险。但HbA1c反映的是过去2~3个月的平均血糖水平,因此对于调整治疗后的疗效评估存在“延迟效应”[19]。此外,HbA1c诸多因素可以造成糖化血红蛋白值出现假性升高和降低[19-21]。同时有研究表明HbA1c存在与血糖状态无关的个体差异,在空腹血糖匹配状态下,非裔美国人HbA1c普遍比白人偏高,因此依据HbA1c预测平均血糖水平与监测血糖存在显著差异[22-23]。在上述情况下,利用HbA1c估算的全天平均血糖指导降糖方案的制订,尤其对门诊患者的居家自我血糖控制是非常不利的。
OGTT试验是目前常用的糖尿病诊断试验,也可作为评估患者胰岛功能的一项检查,应用广泛。空腹血糖作为糖尿病最常用的检测指标,反映患者在非刺激状态下达到稳态时的血糖水平。正常人日常餐后2 h血糖会降至空腹水平[7]表示机体在餐后2 h后葡萄糖摄入、肝糖原输出与消耗之间达到平衡。糖尿病患者餐后2 h近似于达到高糖平衡状态(没有降糖干预情况下)。本研究假设以OGTT 2 h的点血糖作为餐后3 h内的平均血糖,建立表达式, 得到以OGTT估算的平均血糖,其与实际全天平均血糖相关性较高,故可以用来建立模型估计全天平均血糖。鉴于中国人膳食习惯以碳水化合物饮食为主(碳水化合物占50%~60%),故糖耐量试验中血糖上升曲线与日常饮食后血糖上升曲线虽不完全相等,其波型及到达波峰时间类似。国内外多项研究均已证实OGTT试验的空腹血糖、负荷后2 h血糖,与HbA1c、24 h日平均血糖之间存在显著相关[6, 13]。同时,ABDUL-GHANI等[24]在1项对624名非糖尿病受试者进行的3年半的随访研究中证明,尽管糖化血红蛋白是2型糖尿病风险的一个重要预测因子,但与负荷后血糖相比,其预测能力较弱,糖化血红蛋白与胰岛素敏感性和β细胞功能的相关性不如负荷后2 h血糖精确。本研究通过观察OGTT试验血糖反应曲线形态,应用数学相关原理与方法,成功构建估计全天平均血糖的数学模型,其与应用动态血糖监测计算的全天平均血糖水平之间显著相关,具有较准确的预测作用。为兼顾血糖的即时、慢性状态特征,本研究进一步将HbA1c纳入评估模型,成功建立联合OGTT试验、HbA1c评估动态血糖的数学模型,其与24 h平均血糖相关性与准确性进一步提高。
本模型根据糖耐量试验判断患者平均血糖,避免了动态血糖监测的长期性、复杂性和不适感,在门诊就可以完成对患者血糖的评估,联合HbA1c可以同时反映既往与即时血糖情况,平均血糖水平同时可间接反映不同个体高血糖状态对胰岛β细胞的糖毒性大小,可以进一步指导临床及时干预和治疗方案的调整。
本研究的局限性在于,因所有入组患者需完善3 d动态血糖监测,纳入研究样本量较少;为回顾性研究,后续工作可在新入院患者及门诊患者中,广泛开展相关血糖预测进行验证。本研究入组人群为未使用降糖药物的2型糖尿病患者,以便对未能完全掌握全天血糖情况的患者进行药物指导。对于降糖药物对预测模型潜在影响,拟在后续研究工作中进一步探索;生酮饮食、地中海饮食不在此次研究考虑范围内,也属于本研究的局限性之一。
综上,本研究通过对OGTT血糖曲线进行理论分析,成功构建估算全天平均血糖的数学模型,并在改进模型中通过引入HbA1c效应,兼顾急、慢性血糖波动对平均血糖的影响,经外部验证,该模型拟合效果较好,可作为简便、经济的平均血糖估计方法,为评估糖尿病患者近期血糖控制情况提供了新的方法。
| [1] |
ZHOU X H, QIAO Q, ZETHELIUS B, et al. Diabetes, prediabetes and cancer mortality[J]. Diabetologia, 2010, 53(9): 1867-1876. |
| [2] |
CRANE P K, WALKER R, HUBBARD R A, et al. Glucose levels and risk of dementia[J]. N Engl J Med, 2013, 369(6): 540-548. |
| [3] |
CAI X Y, ZHANG Y L, LI M J, et al. Association between prediabetes and risk of all cause mortality and cardiovascular disease: updated meta-analysis[J]. Br Med J, 2020, 370: m2297. |
| [4] |
CHAMBERLAIN J J, RHINEHART A S, SHAEFER C F JR, et al. Diagnosis and management of diabetes: synopsis of the 2016 american diabetes association standards of medical care in diabetes[J]. Ann Intern Med, 2016, 164(8): 542-552. |
| [5] |
ZHOU J, LI H, RAN X W, et al. Reference values for continuous glucose monitoring in Chinese subjects[J]. Diabetes Care, 2009, 32(7): 1188-1193. |
| [6] |
ZHOU J, MO Y F, LI H, et al. Relationship between HbA1c and continuous glucose monitoring in Chinese population: a multicenter study[J]. PLoS ONE, 2013, 8(12): e83827. |
| [7] |
中华医学会糖尿病学分会. 中国2型糖尿病防治指南(2020年版)[J]. 中华内分泌代谢杂志, 2021, 37(4): 311-398. Diabetes Branch of Chinese Medical Association. Guideline for the prevention and treatment of type 2 diabetes mellitus in China (2020 edition)[J]. Chin J Endocrinol Metab, 2021, 37(4): 311-398. |
| [8] |
GALINDO R J, BECK R W, SCIOSCIA M F, et al. Glycemic monitoring and management in advanced chronic kidney disease[J]. Endocr Rev, 2020, 41(5): 756-774. |
| [9] |
BOMHOLT T, ADRIAN T, NØRGAARD K, et al. The use of HbA1c, glycated albumin and continuous glucose monitoring to assess glucose control in the chronic kidney disease population including dialysis[J]. Nephron, 2021, 145(1): 14-19. |
| [10] |
BLOOMGARDEN Z, HANDELSMAN Y. How does CKD affect HbA1c?[J]. J Diabetes, 2018, 10(4): 270. |
| [11] |
No ne. Classification and diagnosis of diabetes mellitus and other categories of glucose intolerance[J]. Diabetes, 1979, 28(12): 1039-1057. DOI: 10.100210470862092.d0101.
|
| [12] |
ITO C, MAEDA R, ISHIDA S, et al. Correlation among fasting plasma glucose, two-hour plasma glucose levels in OGTT and HbA1c[J]. Diabetes Res Clin Pract, 2000, 50(3): 225-230. |
| [13] |
储小宏, 赵广碧, 贾丽, 等. HbA1c与口服葡萄糖耐量试验血糖及平均血糖相关性研究[J]. 安徽医药, 2013, 17(11): 1911-1912. CHU X H, ZHAO G B, JIA L, et al. Study on the correlation between HbA1c and blood glucose and mean blood glucose in oral glucose tolerance test[J]. Anhui Med Pharm J, 2013, 17(11): 1911-1912. |
| [14] |
American Diabetes Association. 2. Classification and diagnosis of diabetes: Standards of medical care in diabetes-2021[J]. Diabetes Care, 2021, 44(suppl 1): S15-S33. |
| [15] |
张世强. 曲线回归的拟合优度指标的探讨[J]. 中国卫生统计, 2002, 19(1): 9-11. ZHANG S Q. Approach on the fitting optimization index of curve regression[J]. Chin J Heal Stat, 2002, 19(1): 9-11. |
| [16] |
NATHAN D M, KUENEN J, BORG R, et al. Translating the A1C assay into estimated average glucose values[J]. Diabetes Care, 2008, 31(8): 1473-1478. |
| [17] |
SVENDSEN P A, LAURITZEN T, SØEGAARD U, et al. Glycosylated haemoglobin and steady-state mean blood glucose concentration in Type 1 (insulin-dependent) diabetes[J]. Diabetologia, 1982, 23(5): 403-405. |
| [18] |
International Expert Committee. International expert committee report on the role of the A1C assay in the diagnosis of diabetes[J]. Diabetes Care, 2009, 32(7): 1327-1334. |
| [19] |
中华医学会糖尿病学分会. 中国血糖监测临床应用指南(2015年版)[J]. 糖尿病天地(临床), 2016, 10(5): 205-218. Diabetes Branch of Chinese Medical Association. Clinical guidelines for blood glucose monitoring in China (2015)[J]. Diabetes World, 2016, 10(5): 205-218. |
| [20] |
KANG S H, JUNG D J, CHOI E W, et al. HbA1c levels are associated with chronic kidney disease in a non-diabetic adult population: a nationwide survey (KNHANES 2011-2013)[J]. PLoS ONE, 2015, 10(12): e0145827. |
| [21] |
吴菲. 糖化血红蛋白检测的影响因素[J]. 世界最新医学信息文摘, 2016, 16(66): 162, 164. WU F. The influencing factors of glycated hemoglobin[J]. World Latest Med Inf, 2016, 16(66): 162, 164. |
| [22] |
SELVIN E, STEFFES M W, BALLANTYNE C M, et al. Racial differences in glycemic markers: a cross-sectional analysis of community-based data[J]. Ann Intern Med, 2011, 154(5): 303-309. |
| [23] |
KIRK J K, D'AGOSTINO R B Jr, BELL R A, et al. Disparities in HbA1c levels between african-american and non-hispanic white adults with diabetes: a meta-analysis[J]. Diabetes Care, 2006, 29(9): 2130-2136. |
| [24] |
ABDUL-GHANI M A, ABDUL-GHANI T, MÜLLER G, et al. Role of glycated hemoglobin in the prediction of future risk of T2DM[J]. J Clin Endocrinol Metab, 2011, 96(8): 2596-2600. |




