胃癌(gastric cancer,GC)是我国最为常见的消化系统恶性肿瘤,肿瘤转移是胃癌患者不良预后的关键因素,究其原因是GC转移发生、发展的相关机制尚未完全阐明。表观稳态的失衡是维持肿瘤细胞恶性生物学行为的重要因素,RNA的动态化学修饰是表观调控的前沿领域。N6-甲基腺嘌呤N6-Methyladenosine(m6A)真核细胞中发现最早,丰度最高的RNA修饰方式[1-2]。m6A修饰参与基因表达调控中的多个环节,如RNA剪切,成熟,出核,翻译及降解,从而影响多种生理、病理进程,如胚胎发育,代谢稳态维持和肿瘤发生、发展[3]。m6A修饰酶的异常表达在胃肠道肿瘤发生、发展中的作用已有报道,但m6A是否参与胃癌转移尚不完全清楚。
m6A修饰的动态平衡由3大调控元件控制:编码器(Writer),主要指m6A转甲基转移酶复合物,包含核心催化酶METTL3(Methyltransferase-3),位点识别辅助蛋白METTL14(Methyltransferase-14),支架蛋白WTAP(Wilms tumor 1-associated protein)等;消码器(Eraser),m6A去甲基化酶,包括经典的FTO及ALKBH5(AlkB family member 5);读码器(Reader),主要由YTHDF1-3(YTH domain family1-3),YTHDC1/2(YTH domain-containing 1/2)和IGF2BPs构成。目前已有文献报道编码器和读码器在胃癌当中的作用,如METTL3通过m6A修饰调节HDGF(Hepatoma-derived growth factor)的表达进而维持胃癌细胞的糖酵解能力[4];YTHDF1通过提升FZD7(Frizzled7)翻译效率促进胃癌发生[5]。而消码器在胃癌中的作用仍未清楚阐述。FTO作为去甲基化酶不仅催化m6A去甲基化,还参与m6Am、m1A等去甲基化进程[6-7],ALKBH5相对于FTO,在底物的选择上更专一,仅催化去除m6A上的甲基,进而影响mRNA的剪接、稳定和翻译[8-9]。因此本研究重点探索ALKBH5作为m6A去甲基化酶在胃癌侵袭、转移中的作用及潜在调控机制。
Wnt信号通路是1条在生物进化过程中高度保守的通路,它参与调节多种细胞进程,如细胞增殖,分化,迁移以及干性维持。Wnt信号通路的异常激活可以促进一系列重要癌基因如MYC、c-Met的异常表达,进而驱动肿瘤的发生、发展[10-11]。有研究报道,METTL14的缺失可以通过抑制m6A修饰进而激活Wnt/PI3K-Akt信号,最终导致胃癌细胞的增殖以及侵袭[12]。但是在胃癌模型中,ALKBH5与Wnt信号通路之间的关系尚不清楚。本研究旨在探索m6A去甲基化酶ALKBH5是否通过刺激Wnt信号通路的激活参与到胃癌的恶性生物学行为的调控。
1 材料与方法 1.1 实验材料 1.1.1 主要试剂与仪器包括:ALKBH5抗体,DDK标签抗体,HA标签抗体(日本MBL公司),FTO抗体,c-Met抗体,METTL3抗体,tubulin抗体,GAPDH抗体,IgG抗体(美国Proteintech公司),MYC抗体,β-catenin抗体(美国Cell signaling technology公司),山羊抗鼠抗体,山羊抗兔抗体(北京中杉金桥生物技术公司),ALKBH5小发夹RNA,METTL3小发夹RNA,β-catenin质粒,METTL3质粒,ALKBH5质粒,GAPDH,MYC,CD44,c-Met PCR引物(上海生工生物工程有限公司),1640培养基,DMEM-高糖培养基,opti-MEM培养基,胎牛血清,Lipofectamine3000,青链霉素混合液(100×美国Gibco公司),Transwell小室(美国Corning公司),protein A /G-beads (美国Thermo公司),PCR反转录及定量扩增试剂(日本TAKARA公司),4%组织固定液,结晶紫染料,Western blot配胶试剂盒(上海碧云天公司),Western blot电泳槽,凝胶电泳成像仪(美国Bio-Rad公司), 5% CO2细胞培养箱,酶标仪(美国Thermo公司)等。
1.1.2 细胞与动物人正常胃黏膜上皮细胞GES-1,胃癌细胞(SGC-7901,MGC-803,BGC-823,HGC-27),人胚胎肾细胞HEK-293T购自中国科学院上海细胞库,胃癌细胞XNYY-0422由西南医院病理科赠送。BALB/C Nude小鼠由陆军特色医学中心实验动物中心提供。
1.2 方法 1.2.1 细胞培养GES-1、SGC-7901、MGC-803、BGC-823、HGC-27细胞用含1%双抗,10%胎牛血清的1640培养基培养,HEK293T用含1%双抗、10%胎牛血清的DMEM高糖培养基培养。培养条件为:5% CO2,37 ℃恒温孵箱。每日观察,隔日换液,细胞汇合度85%~95%时传代。
1.2.2 包装病毒及慢病毒感染将HEK-293T细胞传代至皿内,待细胞汇合度达到70%左右进行病毒包备,8 h后换液,24 h后收取上清,换入新鲜培养基,收取3次上清后浓缩病毒,准备病毒感染;将MGC-803,XNYY-0422传代至12孔板内,待细胞生长到50%左右行病毒感染,从-80 ℃冰箱取出浓缩的ALKBH5sh1、sh2、METTL3sh1、sh2病毒,过表达ALKBH5病毒和阴性对照病毒,冰上解冻。准备7只灭菌EP管,1管用于配置700含10%胎牛血清的DMEM高糖培养基与0.7 μL Polybrene混合液,分装至6只EP管内,各管90 μL,各管内分别加入10 μL ALKBH5 sh1、sh2、METTL3sh1、sh2病毒,过表达ALKBH5病毒和阴性对照病毒,混匀。弃12孔板内上清,各孔加入100 μL含病毒的混合液,孵箱培养,期间观察细胞形态,8 h后换入新鲜培养液,待汇合度达到80%~90%时传代至10 cm皿继续培养,细胞贴壁后行嘌呤霉素筛选。
1.2.3 过表达质粒转染将HEK-293T细胞传代至6孔板内,待细胞汇合度达到70%左右时进行质粒转染。准备8只灭菌的EP管,8只管内均加入125 μL Opti-MEM,其中4管内分别加入3、6、7.5、9 μL PEI,轻柔混匀,静置5 min;另4只EP管内分别加入1 μg HA-β-catenin,1 μg HA-β-catenin+1 μg Flag-METTL3,1 μg HA-β-catenin+1 μg Flag-METTL3+0.5 μg Flag-ALKBH5,1 μg HA-β-catenin+1 μg Flag-METTL3+1 μg Flag-ALKBH5轻柔混匀;将含有PEI的Opti-MEM培养基以前后对应的方式加入到包含质粒的混合液中,混合后静置10 min,加入HEK-293T细胞内,孵箱培养,8 h后换液,待细胞汇合度95%时收集细胞部分提蛋白行Western blot实验,部分行免疫共沉淀实验。
1.2.4 Western blot实验提取待实验细胞蛋白,检测蛋白表达水平。电泳恒压60 V/30 min, 120 V/1 h;转膜:250 mA/1 h 10 min;封闭:含5%奶粉的PBST溶液;一抗孵育4 ℃摇床过夜;二抗孵育室温摇床1 h;曝光显影。
1.2.5 Transwell小室迁移与侵袭实验共计4组细胞,MGC-803野生型细胞系,MGC-803敲低ALKBH5细胞系,XNYY-0422野生型细胞系,XNYY-0422过表达ALKBH5细胞系;四组细胞均饥饿处理24 h,后消化,离心,PBS洗涤细胞1次去除残留血清,用无血清培养基重悬细胞,计数,MGC-803 1×104个/100 μL;XNYY-0422 1×104个/100 μL,加入到Transwell小室上室,下室加入700 μL含20%胎牛血清DMEM高糖培养基,迁移实验上下室中间聚碳酸酯膜无处理,侵袭实验聚碳酸酯膜上层铺基质胶。孵箱培养24 h后固定,染色,风干后显微镜下拍照。
1.2.6 实时荧光定量PCR(quantitative Real-time PCR,qRT-PCR)利用TRIzol提取RNA后行反转录得到放线菌素处理后的MGC-803野生型和敲低ALKBH5细胞的cDNA产物,后以cDNA为模板扩增GAPDH、CD44、MYC和c-Met,qPCR程序为:95 ℃ 30 s;95 ℃ 5 s,60 ℃ 34 s,72 ℃ 15 s,共40个循环;95 ℃ 15 s,60 ℃ 1 min,95 ℃ 15 s。后根据c(T)值计算CD44,MYC和c-Met的相对表达量。
1.2.7 小鼠胃原位种植与转移模型准备SGC-7901胃腺癌细胞系,使用PBS将细胞稀释至2×107个/mL。小鼠麻醉后行体表消毒,于腹部开1 cm小口,将小鼠胃轻柔取出,使用胰岛素针吸取50 μL细胞悬液,注入胃浆膜层下,注意防止细胞悬液从进针口渗出,体外观察无悬液渗漏后放回体内,缝合伤口。期间观察触摸是否形成肿瘤,2~3个月后处死小鼠,探查腹部脏器,拍照取证,取原发灶和转移灶胃癌细胞行下一步实验。
1.3 统计学分析采用SPSS 20.0统计软件,数据采用x±s表示。TCGA数据库生存分析采用Log-rank检验,HR>1表示危险因素;Transwell小室迁移与侵袭实验采用独立样本t检验。检验水准α=0.05。
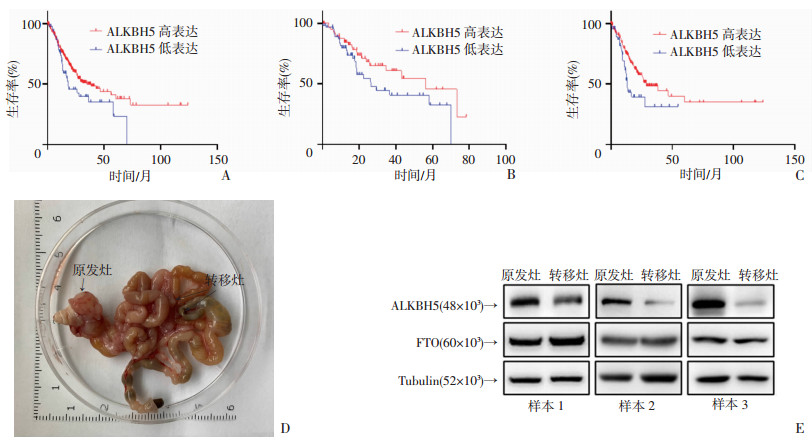
2 结果 2.1 ALKBH5低表达提示胃癌不良预后和远处转移为明确ALKBH5是否与胃癌不良预后有关,我们通过人类癌症基因库(the cancer genome atlas, TCGA)对371例胃癌患者进行ALKBH5差异表达相关的总体生存期分析,发现ALKBH5低表达提示更短的生存期(HR=1.485,P < 0.0340);与此同时,我们筛选出134例Ⅱ级胃癌和218例Ⅲ级胃癌进行生存分析,也得到相同的结果(HR=1.623,P=0.0861;HR=1.749,P=0.0163,图 1)。通过构建胃癌原位种植和转移小鼠模型,获得原发灶及转移灶肿瘤细胞,提取蛋白进行Western blot检测,发现相对原发灶的胃癌细胞,转移灶中的FTO蛋白相对原发灶无明显差异,但ALKBH5蛋白表达水平更低(图 1)。以上结果提示:①ALKBH5低表达与胃癌不良预后相关;②ALKBH5的低表达可能与胃癌细胞高侵袭转移特性相关。
|
| A: TCGA-Whole生存分析;B:TCGA-Grade Ⅱ生存分析;C:TCGA-Grade Ⅲ生存分析; D: 胃癌原位种植及转移小鼠模型;E:原发灶及转移灶FTO和ALKBH5蛋白表达的Wester blot结果 图 1 ALKBH5表达降低与胃癌转移及不良预后密切相关 |
2.2 ALKBH5敲低/过表达细胞系构建及验证
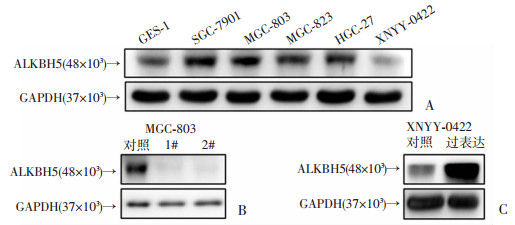
通过分析人正常胃黏膜细胞(GES-1),胃癌细胞株SGC-7901,MGC-803,BGC-823,HGC-27,XNYY-0422的ALKBH5的蛋白表达水平,发现在胃癌细胞MGC-803中,ALKBH5的表达水平相对较高,XNYY-0422中ALKBH5表达水平相对较低(图 2A),因此我们分别选择MGC-803构建ALKBH5敲低细胞株,XNYY-0422构建过表达细胞株,通过Western blot验证2株敲低的MGC-803及1株过表达的XNYY-0422细胞株构建成功(图 2B、C)。
|
| A:人正常胃黏膜细胞及胃癌细胞株ALKBH5蛋白表达的western blot结果;B:MGC-803 ALKBH5敲低细胞株ALKBH5蛋白表达的Werter blot结果;C:XNYY-0422 ALKBH5过表达细胞株ALKBH5蛋白表达的western blot结果 图 2 ALKBH5敲低/过表达细胞系构建及验证 |
2.3 ALKBH5的表达抑制胃癌细胞迁移和侵袭
应用Transwell实验观察敲低和过表达ALKBH5对胃癌细胞迁移和侵袭是否产生影响。结果提示:相对于对照组的MGC-803细胞,敲低ALKBH5的MGC-803细胞迁移和侵袭能力显著增强(P < 0.000 1,P < 0.000 1);在XNYY-0422细胞当中,过表达ALKBH5时细胞的迁移和侵袭能力减弱(P < 0.000 1;P < 0.000 1,图 3)。以上结果表明:ALKBH5表达下调可以促进胃癌细胞的迁移和侵袭能力。

|
| A:AGC-803细胞;B:XNYY-0422细胞 a: P < 0.01,与对照组比较 图 3 ALKBH5抑制胃癌细胞的运动侵袭能力 (结晶紫染色×200) |
2.4 ALKBH5表达下调促进Wnt下游基因表达
Wnt信号通路的激活是维持胃癌高侵袭转移特性的关键分子生物学事件。ALKBH5作为经典的m6A去甲基化酶,是否影响Wnt信号通路的转导?通过比较对照组与敲低ALKBH5的MGC-803细胞系Wnt下游的靶基因表达情况,结果显示Wnt下游MYC与c-MET蛋白表达在敲低细胞系中表达增加(图 4)。与此同时,METTL3作为公认的m6A核心甲基转移酶是否也参与Wnt信号通路的调节?我们通过构建敲低METTL3的MGC-803细胞系,发现当敲低METTL3时,Wnt下游MYC和c-MET表达出现抑制(图 4)。以上结果提示:ALKBH5可能通过发挥其m6A消码器的作用参与调节Wnt信号通路下游基因表达。

|
| 图 4 ALKBH5和METTL3敲低Wnt信号下游基因表达的变化 |
2.5 Wnt下游分子RNA m6A修饰位点预测
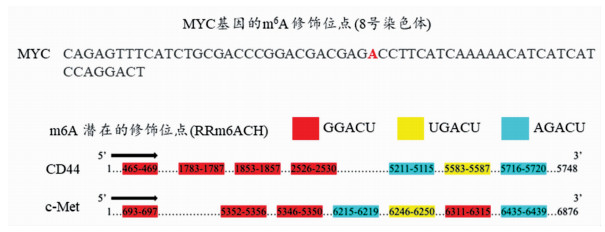
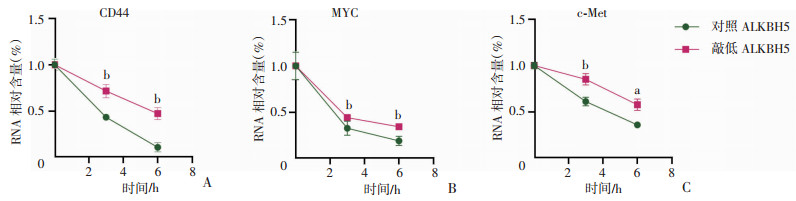
mRNA发生m6A修饰依赖于m6A修饰酶对底物的识别,那么Wnt信号通路下游的效应分子是否存在m6A修饰位点?我们运用m6A修饰位点预测网站m6AVAR(http://m6Avar.renlab.org/index.html)发现了基于m6A交联免疫共沉淀法(m6A cross-linking immunoprecipitation,m6A-CLIP)测序数据中MYC基因的m6A修饰位点13,其具体位点见图 5。同时基于m6A修饰位点的序列特征(RRACH,R=),我们发现CD44和c-Met上具备多个潜在的m6A修饰位点(图 5)。以上结果提示Wnt下游关键效应分子MYC,CD44和c-Met可能受到RNA去甲基化酶ALKBH5的调节。m6A修饰通常通过影响mRNA稳定性参与基因表达调控,通过放线菌素抑制RNA合成结合qRT-PCR实验,我们发现敲低ALKBH5可显著延长MYC,CD44和c-Met的mRNA半衰期(图 6)。上述结果表明ALKBH5可能通过去除Wnt下游靶基因MYC,CD44和c-Met mRNA上的m6A修饰维持其稳定性,促进基因表达。
|
| 图 5 MYC基因的m6A修饰位点及CD44和c-Met上潜在的m6A修饰位点 |
|
| A:CD44;B:MYC;C:c-Met a: P < 0.05, b: P < 0.01, 与对照ALKBH5比较 图 6 放线菌素加入后MYC、CD44和c-Met mRNA含量的变化 |
3 讨论
胃癌是人类第5大常见肿瘤,也是最为常见的消化系统肿瘤,死亡病例数排第3位。胃癌起病隐匿,早期无特异的临床表现,大部分患者在首次确诊时已是中晚期,患者常常因此错过最佳治疗期[14]。因此,寻找到新的胃癌生物标志物和治疗靶点迫在眉睫。
m6A修饰已被证实在肿瘤发生和进展中起至关重要的作用,因此,m6A相关修饰酶是否可以作为肿瘤诊断标志物以及针对m6A修饰酶的抗肿瘤治疗策略是否有良好的临床运用前景亟须阐明。ALKBH5作为m6A去甲基化酶,已被证实在非小细胞肺癌[15],胶质瘤[16]、肝癌[17]、胰腺癌[18]发生和进展中起重要作用。本研究基于TCGA数据库行生信分析发现ALKBH5的低表达与胃癌不良预后相关,同时构建小鼠胃原位种植及转移模型证实ALKBH5低表达与胃癌远处转移相关,通过Transwell小室迁移与侵袭实验确认ALKBH5能够抑制胃癌细胞的侵袭转移,提示ALKBH5是胃癌进展中的抑癌因素。那么ALKBH5是如何参与调节胃癌进展的?文献[19]报道在胶质瘤中,ALKBH5可以去除SOX2转录子上的m6A修饰,上调SOX2的表达,激活Wnt信号,从而导致胶质瘤替莫唑胺(temozolomide,TMZ)耐药的发生;而在胰腺导管细胞癌中,ALKBH5可以通过m6A修饰Wnt抑制因子-1(Wnt inhibitory factor-1,WIF-1)的方式,激活WIF-1,下调Wnt信号,进而抑制胰腺癌细胞的增殖最终发挥其抑癌效应[20]。这些研究结果提示,ALKBH5表达失调,在不同肿瘤的恶性生物学行为中充当不同的角色,同时也说明ALKBH5-Wnt轴在肿瘤进展中发挥重要的调控作用。
在胃癌中,Wnt信号通路通常存在持续异常的激活并促进胃癌的进展[21]。文献[22-24]报道在多种类型肿瘤中,Wnt下游β-catenin、MYC、c-Met受到m6A修饰酶METTL3和IGF2BPs的调节。这些在胃癌中m6A修饰关键酶的过度激活或者缺失通常会介导Wnt信号通路下游基因表达异常。我们依托m6AVAR网站预测Wnt下游MYC、CD44和c-Met受m6A修饰的位点,同时基于mRNA半衰期实验,证明在胃癌细胞中,这些基因的表达也受到m6A去甲基化酶ALKBH5的调控。据此,我们的研究证明ALKBH5表达丢失介导的m6A修饰失衡可以导致Wnt信号下游分子的异常上调,可能是导致胃癌转移的潜在机制。结合胰腺癌中ALKBH5通过调控Wnt上游WIF-1表达进而发挥其抑癌效应,提示ALKBH5表达缺失导致的m6A修饰上调对于Wnt信号激活是明确的,m6A修饰的增加是促癌因素;但是,ZHANG等[12]报道在胃癌进展中,METTL14敲低介导m6A修饰的下调激活Wnt信号通路,提示m6A修饰的增加是抑癌因素。我们认为可能有以下原因:①m6A修饰水平的高低与编码器和消码器相关,但这种修饰发挥其转录调控的功能更多的基于读码器的作用;②ALKBH5缺失激活Wnt信号可能具备疾病依赖性,如何筛选出以m6A异常修饰作为主导调控方式的肿瘤亚型值得深入研究。
m6A修饰作为最常见的RNA修饰方式,广泛存在于转录产物mRNA上并影响其表达,是目前肿瘤表观靶向研究领域的热点。本研究基于临床实际问题,胃癌的高侵袭转移特性,发现m6A去甲基化酶ALKBH5表达的缺失可以显著促进胃癌细胞的迁移和侵袭能力;机制研究层面,我们初步探讨了ALKBH5可能通过去甲基化修饰Wnt信号通路下游关键基因MYC,CD44和c-Met,促进其mRNA稳定性及蛋白表达。下一步我们将继续探索ALKBH5-Wnt轴的转录调控机制,同时明确读码器YTHDF1-3,YTHDC1/2在该调控轴中的作用,为探索胃癌转移的发生、发展机制以及通过靶向m6A的表观治疗策略,提供新的认识和研究思路。
| [1] |
MEYER K D, SALETORE Y, ZUMBO P, et al. Comprehensive analysis of mRNA methylation reveals enrichment in 3' UTRs and near stop codons[J]. Cell, 2012, 149(7): 1635-1646. DOI:10.1016/j.cell.2012.05.003 |
| [2] |
ROUNDTREE I A, EVANS M E, PAN T, et al. Dynamic RNA modifications in gene expression regulation[J]. Cell, 2017, 169(7): 1187-1200. DOI:10.1016/j.cell.2017.05.045 |
| [3] |
LEE Y, CHOE J, PARK O H, et al. Molecular mechanisms driving mRNA degradation by m6A modification[J]. Trends Genet, 2020, 36(3): 177-188. DOI:10.1016/j.tig.2019.12.007 |
| [4] |
WANG Q, CHEN C, DING Q Q, et al. METTL3-mediated m6A modification of HDGF mRNA promotes gastric cancer progression and has prognostic significance[J]. Gut, 2020, 69(7): 1193-1205. DOI:10.1136/gutjnl-2019-319639 |
| [5] |
PI J N, WANG W, JI M, et al. YTHDF1 promotes gastric carcinogenesis by controlling translation of FZD7[J]. Cancer Res, 2020, canres.0066.2020. DOI:10.1158/0008-5472.can-20-0066 |
| [6] |
MAUER J, LUO X B, BLANJOIE A, et al. Reversible methylation of m6Am in the 5' cap controls mRNA stability[J]. Nature, 2017, 541(7637): 371-375. DOI:10.1038/nature21022 |
| [7] |
WEI J B, LIU F G, LU Z K, et al. Differential m6A, m6Am, and m1A demethylation mediated by fto in the cell nucleus and cytoplasm[J]. Mol Cell, 2018, 71(6): 973-985. DOI:10.1016/j.molcel.2018.08.011 |
| [8] |
TANG C, KLUKOVICH R, PENG H Y, et al. ALKBH5-dependent m6A demethylation controls splicing and stability of long 3'-UTR mRNAs in male germ cells[J]. Proc Natl Acad Sci USA, 2018, 115(2): E325-E333. DOI:10.1073/pnas.1717794115 |
| [9] |
ZHENG G Q, DAHL J A, NIU Y M, et al. ALKBH5 is a mammalian RNA demethylase that impacts RNA metabolism and mouse fertility[J]. Mol Cell, 2013, 49(1): 18-29. DOI:10.1016/j.molcel.2012.10.015 |
| [10] |
SCHOLZ B A, SUMIDA N, DE LIMA C D M, et al. WNT signaling and AHCTF1 promote oncogenic MYC expression through super-enhancer-mediated gene gating[J]. Nat Genet, 2019, 51(12): 1723-1731. DOI:10.1038/s41588-019-0535-3 |
| [11] |
HAN B, YAN S J, WEI S S, et al. YTHDF1-mediated translation amplifies Wnt-driven intestinal stemness[J]. EMBO Rep, 2020, 21(4): e49229. DOI:10.15252/embr.201949229 |
| [12] |
ZHANG C, ZHANG M Q, GE S, et al. Reduced m6A modifi cation predicts malignant phenotypes and augmented Wnt/PI3K-Akt signaling in gastric cancer[J]. Cancer Med, 2019, 8(10): 4766-4781. DOI:10.1002/cam4.2360 |
| [13] |
KE S D, ALEMU E A, MERTENS C, et al. A majority of m6A residues are in the last exons, allowing the potential for 3' UTR regulation[J]. Genes Dev, 2015, 29(19): 2037-2053. DOI:10.1101/gad.269415.115 |
| [14] |
RAWLA P, BARSOUK A. Epidemiology of gastric cancer: global trends, risk factors and prevention[J]. Przeglad Gastroenterol, 2019, 14(1): 26-38. DOI:10.5114/pg.2018.80001 |
| [15] |
JIN D, GUO J W, WU Y, et al. m6A demethylase ALKBH5 inhibits tumor growth and metastasis by reducing YTHDFs-mediated YAP expression and inhibiting miR-107/LATS2-mediated YAP activity in NSCLC[J]. Mol Cancer, 2020, 19(1): 40. DOI:10.1186/s12943-020-01161-1 |
| [16] |
ZHANG S C, ZHAO B S, ZHOU A D, et al. m6 A demethylase ALKBH5 maintains tumorigenicity of glioblastoma stem-like cells by sustaining FOXM1 expression and cell proliferation program[J]. Cancer Cell, 2017, 31(4): 591-606. DOI:10.1016/j.ccell.2017.02.013 |
| [17] |
CHEN M N, WEI L, LAW C T, et al. RNA N6-methyladenosine methyltransferase-like 3 promotes liver cancer progression through YTHDF2-dependent posttranscriptional silencing of SOCS2[J]. Hepatol Baltim Md, 2018, 67(6): 2254-2270. DOI:10.1002/hep.29683 |
| [18] |
GUO X Y, LI K, JIANG W L, et al. RNA demethylase ALKBH5 prevents pancreatic cancer progression by posttranscriptional activation of PER1 in an m6A-YTHDF2-dependent manner[J]. Mol Cancer, 2020, 19(1): 91. DOI:10.1186/s12943-020-01158-w |
| [19] |
LIU B Y, ZHOU J, WANG C Y, et al. LncRNA SOX2OT promotes temozolomide resistance by elevating SOX2 expression via ALKBH5-mediated epigenetic regulation in glioblastoma[J]. Cell Death Dis, 2020, 11(5): 384. DOI:10.1038/s41419-020-2540-y |
| [20] |
TANG B, YANG Y H, KANG M, et al. m6A demethylase ALKBH5 inhibits pancreatic cancer tumorigenesis by decreasing WIF-1 RNA methylation and mediating Wnt signaling[J]. Mol Cancer, 2020, 19(1): 3. DOI:10.1186/s12943-019-1128-6 |
| [21] |
刘洪伟, 梅基雄. 双氢青蒿素通过Wnt/β-catenin信号通路抑制胃癌细胞的增殖和侵袭[J]. 第三军医大学学报, 2018, 40(5): 387-394. LIU H W, MEI J X. Dihydroartemisinin inhibits proliferation and invasion in human gastric cancer cells through suppression of Wnt/β-catenin signaling pathways[J]. J Third Mil Med Univ, 2018, 40(5): 387-394. DOI:10.16016/j.1000-5404.201710089 |
| [22] |
LIU L, WANG J, SUN G F, et al. m6A mRNA methylation regulates CTNNB1 to promote the proliferation of hepato blastoma[J]. Mol Cancer, 2019, 18(1): 188. DOI:10.1186/s12943-019-1119-7 |
| [23] |
HUANG H L, WENG H Y, SUN W J, et al. Recognition of RNA N6-methyladenosine by IGF2BP proteins enhances mRNA stability and translation[J]. Nat Cell Biol, 2018, 20(3): 285-295. DOI:10.1038/s41556-018-0045-z |
| [24] |
LUO G Y, XU W W, ZHAO Y P, et al. RNA m6A methylation regulates uveal melanoma cell proliferation, migration, and invasion by targeting c-Met[J]. J Cell Physiol, 2020, 235(10): 7107-7119. DOI:10.1002/jcp.29608 |




