阿尔茨海默病(Alzheimer’s disease, AD)是中老年常见神经系统退行性疾病,也是痴呆发生的最常见原因[1]。AD的致病原因和发病机制目前还不清楚,缺乏有效干预措施[2]。脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)在AD发生、发展过程中的作用越来越受到重视[3]。BDNF首先是以脑源性神经营养因子前体蛋白(precursor of brain-derived neurothrophic factor,proBDNF)的形式由细胞合成和分泌。proBDNF裂解后产生脑源性神经营养因子前肽(BDNF propeptide,pBDNF)和成熟BDNF(mature BDNF,mBDNF)。BDNF能起到促进细胞增殖、分化和存活,促进长时程增强(long-term potentiation, LTP),促进突触生长、突触传递以及可塑性的作用,改善AD鼠的认知功能[4-5],而proBDNF能够加剧AD鼠脑内β淀粉样蛋白(Aβ)沉积[6],抑制海马神经元增殖,促进细胞凋亡,降低突触可塑性,从而降低小鼠的学习与记忆功能[7]。近期研究表明:在AD患者的海马标本中,pBDNF水平是健康人的16倍,而pBDNF/BDNF比值是健康人的30倍;pBDNF能够与Aβ蛋白一起在AD的发生、发展中发挥协同毒性作用[8]。但有关pBDNF在AD发病中的作用及机制尚不明确,因此,本研究采用AD鼠海马注射携带pBDNF基因的腺相关病毒基因整合载体(AAV-pBDNF),观察内源性pBDNF对AD鼠学习与记忆功能以及海马突触后致密蛋白-95(postsynaptic density protein 95,PSD-95)表达的影响。
1 材料与方法 1.1 实验动物与分组采用阿尔茨海默病模型转基因小鼠为实验动物,购自江苏集萃药康生物科技有限公司(APPswePS1dE9,18只,雄性,4月龄,体质量28~32 g),饲养于本院实验动物中心。当AD鼠长至6月龄时,采用抛硬币法随机分为空载体对照组、AAV-pBDNF组、AAV-pBDNF+ p75NTR抗体组,每组6只。空载体对照组右侧海马注射AAV-GFP(2 μL,1×1012 vg/mL,和元生物,中国),pBDNF组右侧海马注射AAV-pBDNF(2 μL,1×1012 vg/mL,和元生物,中国),pBDNF+p75NTR抗体组右侧海马注射AAV-pBDNF(2 μL,1×1012 vg/mL)和p75NTR抗体(2 μL,10 μg/mL,Alomone,以色列)。AAV-pBDNF和AAV-GFP血清型皆为AAV8,对神经系统靶向性强。
1.2 右侧海马药物注射6%水合氯醛腹腔注射麻醉小鼠,固定于立体定位仪,头部剃毛,从小鼠头部中缝处剪开皮肤,把囟门作为中心点,坐标点的定位坐标值为:前后-1.75 mm,右侧旁开2.3 mm。然后用小电钻在颅骨上钻1个小孔。再次定位后穿刺1.5 mm深,此时针尖到达右侧海马部位,采用微量注射器以0.5 μL/mL的速度进行注射。注射完毕后针头停留5 min再缓慢拔针,防止注射药物溢出。缝皮、固定,手术之后安静放置,注意保暖,观察30 min,小鼠没有异常后,1只/笼继续饲养。
1.3 水迷宫实验检测AD鼠的学习记忆功能所有小鼠于海马注射4周后进行Morris水迷宫实验。将圆形游泳池分为4个象限,在第3象限内放置1个20 cm高的平台,加入自来水至水面约高于平台2 cm。小鼠先学习训练5 d:将小鼠从1、2、4象限分别3次放入游泳池中,若小鼠在1 min内找到平台,并在平台上停留>3 s,则系统自动停止录像;若1 min后仍没找到平台,则引导它停留在平台上10 s;接下来另外2个象限重复实验。到第6天时,撤去平台,记录小鼠在第3象限内的时间和穿越平台的次数。
1.4 免疫荧光检测AAV-pBDNF在AD鼠脑内转染情况水迷宫检测完毕后,次日处死小鼠并取材,右侧半脑组织用于免疫组化,左侧半脑组织用于Western blot实验。右侧半脑组织固定、脱水后冰冻切片,每片约35 μm。每组动物分别取2组脑片,清洗、打孔、封闭。然后其中1组脑片加入鼠来源NeuN抗体(1 ∶500,Abcam,英国),另1组脑片加入鼠来源GFAP抗体(1 ∶1 000,Abcam,英国),4 ℃过夜。PBST清洗脑片后加入Cy3鼠来源抗体(1 ∶500,Abcam,英国),37 ℃孵箱避光孵育1 h。贴片,荧光显微镜下拍照,观察AAV-pBDNF的转染情况。
1.5 Western blot检测AD鼠脑内PSD-95表达水平取左侧半脑组织,裂解、取上清,制成样本后放入冰箱保存待用。免疫印迹法跑电泳,转膜后牛奶封闭1 h,一抗4 ℃过夜,加一抗为兔来源PSD-95抗体(1 ∶500,CST,美国)和小鼠来源β-actin(1 ∶1 000,Sigma,美国)。再加二抗为兔来源IRDye 800CW荧光抗体和小鼠来源IRDye 800CW(1 ∶1 000,LI-COR,美国)。再加二抗避光室温1 h。洗膜后显影,Image J软件计算各个目的条带的灰度值,用PSD-95/β-actin值来表示PSD-95的相对蛋白表达量。
1.6 统计学分析采用GraphPad Prism 8.0统计与制图,所有计量资料以x±s表示,水迷宫实验前5 d各组之间的游泳速度比较应用双因素方差分析,其他指标:两组间比较采用独立样本t检验, 多组间比较采用单因素方差分析。检验水准:α=0.05。
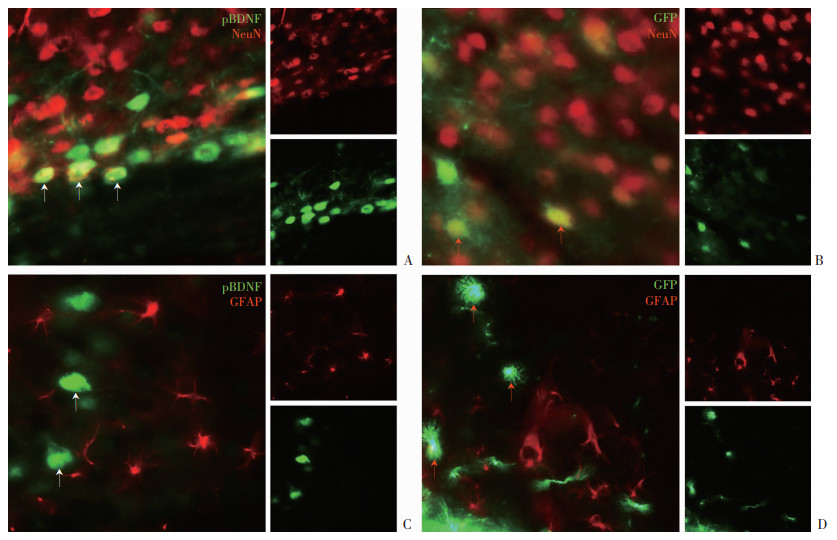
2 结果 2.1 AAV-pBDNF在AD鼠脑内转染情况免疫荧光检测结果发现:AAV-pBDNF和AAV-GFP集中表达于神经元内,而胶质细胞内未见pBDNF或者GFP表达(图 1)。
|
|
白色箭头示pBDNF阳性细胞; 红色箭头示GFP阳性细胞 A: pBDNF与NeuN共染; B: CFP与NeuN共染; C: pBDNF与GFAP共染; D: GFP与GFAP共染 图 1 AAV-pBDNF在AD鼠脑内转染情况(×40) |
2.2 AAV-pBDNF对AD鼠学习记忆能力的影响
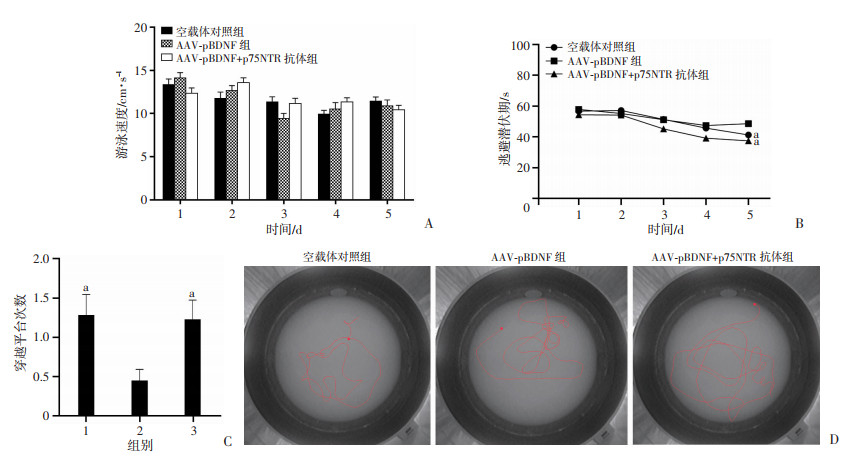
水迷宫实验结果显示:在水迷宫实验前5 d,同1 d内各组小鼠的运动速度无明显差异。第5天时,对照组(P=0.004 5,F=4.054)与AAV-pBDNF+p75NTR抗体组(P=0.002 4,F=4.504)的逃避潜伏期均较第1天有明显下降,而pBDNF组AD鼠的逃避潜伏期虽然也较第1天有所缩短,但差异无统计学意义。在空间探索实验中,AAV-pBDNF组AD小鼠穿越平台次数较其余两组少(P=0.020 1,F=4.225),而AAV-pBDNF+p75NTR抗体组小鼠平台穿越次数与对照组相比无明显差异(图 2)。
|
|
a : P<0.05, 与AAV-pBDNF组比较 A: 各组小鼠的游泳速度; B: 各组小鼠找到平台的潜伏期; C: 各组小鼠穿越平台次数﹐1:空载体对照组; 2:AAV-pBDNF组; 3:AAV-pBDNF+p75NTR抗体组; D: 各组小鼠游泳轨迹图 图 2 AAV-pBDNF对AD鼠学习记忆能力的影响 |
2.3 AAV-pBDNF对AD鼠脑内PSD-95表达的影响
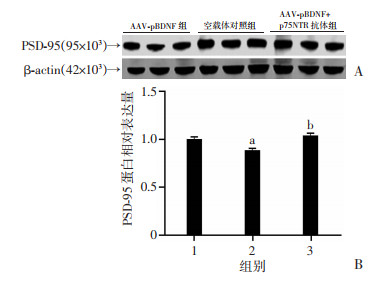
Western blot检测结果显示:AAV-pBDNF组PSD-95表达量低于对照组和pBDNF+p75NTR抗体组(P < 0.05),而AAV-pBDNF+p75NTR抗体组PSD-95表达量与对照组比较差异无统计学意义(图 3)。
|
| A : Western blot检测; B: 半定量分析1 : 空载体对照组; 2:AAV-pBDNF组; 3:AAV-pBDNF+p75NTR抗体组; a: P<0.05, 与对照组比较; b: P<0.01, 与AAV-pBDNF组比较 图 3 AAV-pBDNF对AD小鼠PSD-95表达的影响 |
3 讨论
BDNF是神经营养因子家族中重要的一员,BDNF首先是以前体蛋白proBDNF的形式由细胞合成和分泌,proBDNF在细胞内被弗林酶、前体蛋白转化酶,或者被分泌到细胞外并被血浆纤维溶酶和基质金属蛋白酶-9等蛋白裂解酶裂解,释放出pBDNF和mBDNF,pBDNF、proBDNF、mBDNF三者共同存在于中枢神经系统中[9-10]。在生理状态下,海马部位pBDNF与mBDNF等摩尔存在,但含量比proBDNF高10倍以上[11]。pBDNF分子质量约为17×103,是proBDNF的N端片段[12]。既往认为pBDNF只是参与BDNF的修饰及转运,其本身无生物学活性且很快被降解,近年的研究表明proBDNF裂解后产生的pBDNF本身有着重要作用[1]。Met-pBDNF可改变神经元形态,抑制培养海马神经元生长锥;Val-pBDNF促进海马长时程抑制,而Met-pBDNF抑制海马长时程抑制;Val-pBDNF还可抑制短粗树突的生长,降低树突棘数量[13]。临床研究表明重度抑郁症患者脑脊液内pBDNF水平降低,尤其是男性患者下降更为明显[14-15], 同时还发现Met-pBDNF可以降解树突棘进而减少海马神经元的突触形成,从而改变了恐惧消退的路径[16]。在1项尸检研究中发现:抑郁症患者的顶叶皮层中mBDNF水平较低,而pBDNF水平较高[17]。说明pBDNF参与了神经精神疾病的发生、发展。
本研究采用转基因AD鼠海马注射携带pBDNF基因的腺相关病毒基因整合载体(AAV-pBDNF),免疫组化结果表明:AAV-pBDNF集中表达于神经元内,而胶质细胞内未见pBDNF,说明AAV-pBDNF在神经元成功转染。水迷宫实验结果表明:海马注射AAV-pBDNF及p75NTR抗体对AD鼠的运动速度无明显影响。海马注射AAV-pBDNF后AD鼠学习及记忆能力均明显下降,而海马同时注射AAV-pBDNF和p75NTR抗体(中和p75NTR受体)后,AD鼠学习及记忆能力与对照组比较无明显差异,说明pBDNF可能通过p75NTR信号通路降低AD鼠的学习记忆能力。
PSD-95是兴奋性突触后致密区核心构架蛋白,具有调节、聚合受体,稳定突触连接结构以及传导膜受体信号的作用,主要参与调控突触可塑性及皮质和海马神经元长时程增强效应(LTP),在记忆形成和信息传递中发挥重要的调控作用[10, 18-19]。本研究结果表明:AD鼠海马注射AAV-pBDNF后AD鼠脑内PSD-95含量较AAV-GFP组降低,提示其神经突触后兴奋性传递水平下降,pBDNF使PSD-95表达下降,提示这也许是AD鼠学习记忆功能下降的原因之一。而海马同时注射AAV-pBDNF和p75NTR抗体后,PSD-95含量与对照组无明显差异,说明p75NTR抗体中和p75NTR后能够拮抗pBDNF的作用,pBDNF可能通过p75NTR信号通路降低PSD-95的表达。
本研究结果显示:AD鼠海马注射AAV-pBDNF后穿越平台次数减少、逃避潜伏期无明显缩短、学习记忆能力下降、PSD-95的表达降低,而p75NTR抗体能够拮抗AAV-pBDNF上述作用,说明pBDNF可能通过p75NTR信号通路降低PSD-95的表达,导致AD鼠的学习记忆能力下降。本研究初步发现BDNF代谢过程中产生的pBDNF可能参与了AD的发病,为进一步了解pBDNF在神经精神疾病中的作用提供参考。但本研究仍然存在一定的局限性。例如,p75NTR抗体可能还通过阻断其他信号通路来促进AD鼠的学习记忆功能与PSD-95表达;p75NTR是否作为pBDNF主要受体传导信号,影响其功能;AD鼠突触可塑性功能的变化还需要更多的实验进行验证。因此,在未来的研究中,可以进一步研究pBDNF对AD鼠脑内其他蛋白表达以及神经功能的影响,以及p75NTR具体是如何调控pBDNF作用的。
| [1] |
许曼玉, 许志强. 不同形态脑源性神经营养因子与阿尔茨海默病关系研究进展[J]. 重庆医学, 2019, 48(6): 1025-1028. XU M Y, XU Z Q. Research progress on the relationship between different forms of brain-derived neurotrophic factors and Alzheimer's disease[J]. Chongqing Med, 2019, 48(6): 1025-1028. |
| [2] |
JOE E, RINGMAN J M. Cognitive symptoms of Alzheimer's disease: clinical management and prevention[J]. BMJ Clin Res Ed, 2019, 367: l6217. DOI:10.1136/bmj.l6217 |
| [3] |
FOLTRAN R B, DIAZ S L. BDNF isoforms: a round trip ticket between neurogenesis and serotonin?[J]. J Neurochem, 2016, 138(2): 204-221. DOI:10.1111/jnc.13658 |
| [4] |
HARWARD S C, HEDRICK N G, HALL C E, et al. Autocrine BDNF-TrkB signalling within a single dendritic spine[J]. Nature, 2016, 538(7623): 99-103. DOI:10.1038/nature19766 |
| [5] |
KUIPERS S D, TRENTANI A, TIRON A, et al. BDNF-induced LTP is associated with rapid Arc/Arg3.1-dependent enhancement in adult hippocampal neurogenesis[J]. Sci Rep, 2016, 6: 21222. DOI:10.1038/srep21222 |
| [6] |
CHEN J, ZHANG T, JIAO S, et al. proBDNF accelerates brain amyloid-β deposition and learning and memory impairment in APPswePS1dE9 transgenic mice[J]. J Alzheimers Dis, 2017, 59(3): 941-949. DOI:10.3233/jad-161191 |
| [7] |
CHEN J, LI C R, YANG H, et al. proBDNF attenuates hippocampal neurogenesis and induces learning and memory deficits in aged mice[J]. Neurotox Res, 2016, 29(1): 47-53. DOI:10.1007/s12640-015-9568-2 |
| [8] |
LIM J Y, REIGHARD C P, CROWTHER D C. The pro-domains of neurotrophins, including BDNF, are linked to Alzheimer's disease through a toxic synergy with Aβ[J]. Hum Mol Genet, 2015, 24(14): 3929-3938. DOI:10.1093/hmg/ddv130 |
| [9] |
GUO J, JI Y, DING Y, et al. BDNF pro-peptide regulates dendritic spines via caspase-3[J]. Cell Death Dis, 2016, 7: e2264. DOI:10.1038/cddis.2016.166 |
| [10] |
许曼玉, 陈甲, 许志强. AAV-proBDNF对阿尔茨海默病鼠海马DCX阳性细胞数及PSD-95表达的影响[J]. 第三军医大学学报, 2019, 41(2): 95-99. XU M Y, CHEN J, XU Z Q. Effects of AAV-proBDNF on hippocampal DCX positive cells and PSD-95 expression in Alzheimer's disease mice[J]. J Third Mil Med Univ, 2019, 41(2): 95-99. DOI:10.16016/j.1000-5404.201808088 |
| [11] |
ANASTASIA A, DEINHARDT K, CHAO M V, et al. Val66Met polymorphism of BDNF alters prodomain structure to induce neuronal growth cone retraction[J]. Nat Commun, 2013, 4: 2490. DOI:10.1038/ncomms3490 |
| [12] |
HASHIMOTO K. Regulation of brain-derived neurotrophic factor (BDNF) and its precursor proBDNF in the brain by serotonin[J]. Eur Arch Psychiatry Clin Neurosci, 2016, 266(3): 195-197. DOI:10.1007/s00406-016-0682-9 |
| [13] |
ZANIN J P, UNSAIN N, ANASTASIA A. Growth factors and hormones pro-peptides: the unexpected adventures of the BDNF prodomain[J]. J Neurochem, 2017, 141(3): 330-340. DOI:10.1111/jnc.13993 |
| [14] |
KOJIMA M, MATSUI K, MIZUI T. BDNF pro-peptide: physiological mechanisms and implications for depression[J]. Cell Tissue Res, 2019, 377(1): 73-79. DOI:10.1007/s00441-019-03034-6 |
| [15] |
MIZUI T, HATTORI K, ISHIWATA S, et al. Cerebrospinal fluid BDNF pro-peptide levels in major depressive disorder and schizophrenia[J]. J Psychiatr Res, 2019, 113: 190-198. DOI:10.1016/j.jpsychires.2019.03.024 |
| [16] |
GIZA J I, KIM J, MEYER H C, et al. The BDNF Val66Met prodomain disassembles dendritic spines altering fear extinction circuitry and behavior[J]. Neuron, 2018, 99(1): 163-178. DOI:10.1016/j.neuron.2018.05.024 |
| [17] |
YANG B, REN Q, ZHANG J C, et al. Altered expression of BDNF, BDNF pro-peptide and their precursor proBDNF in brain and liver tissues from psychiatric disorders: rethinking the brain-liver axis[J]. Transl Psychiatry, 2017, 7(5): e1128. DOI:10.1038/tp.2017.95 |
| [18] |
LISEK M, FERENC B, STUDZIAN M, et al. Glutamate deregulation in ketamine-induced psychosis-A potential role of PSD95, NMDA receptor and PMCA interaction[J]. Front Cell Neurosci, 2017, 11: 181. DOI:10.3389/fncel.2017.00181 |
| [19] |
HORGUSLUOGLU-MOLOCH E, NHO K, RISACHER S L, et al. Targeted neurogenesis pathway-based gene analysis identifies ADORA2A associated with hippocampal volume in mild cognitive impairment and Alzheimer's disease[J]. Neurobiol Aging, 2017, 60: 92-103. DOI:10.1016/j.neurobiolaging.2017.08.010 |




