2. 402160 重庆,重庆医科大学附属永川医院:中心实验室
2. Laboratory Center, Yongchuan Hospital, Chongqing Medical University, Chongqing, 402160, China
骨质疏松性椎体压缩骨折(osteoporotic vertebral compression fracture,OVCF)是骨质疏松性骨折中最常见的骨折[1-2]。经皮穿刺椎体成形术(percutaneous vertebroplasty,PVP)是一种有效的治疗OVCF的术式[3-5]。虽然目前广泛采用的填充材料为聚甲基丙烯酸甲酯(polymethylmethacrylate,PMMA)[6],但它也存在诸多不足,如强度太高易引发临近椎体骨折,放热温度太高灼伤周围组织以及缺乏生物活性,同时,骨水泥与骨界面可发生骨的吸收导致骨水泥漂浮而削弱了填充物对椎体的强化[7-8]。因此,探索新型的填充物势在必行。我科自2018年1月开始在PVP手术中使用含PMMA和磷酸钙骨水泥(calcium phosphate cement,CPC)的混合骨水泥,取得了较好的临床疗效。本研究通过回顾性研究比较混合材料(PMMA ∶CPC=1 ∶1)与单一材料(PMMA)治疗OVCF的临床疗效,为混合骨水泥的临床应用提供依据。
1 资料与方法 1.1 研究设计采用回顾性研究,收集2018年1-8月在我科因OVCF而行PVP手术,2年期随访资料较完整的病例,随访至2020年10月。所有手术由同一组手术医师共同完成。男性12例,女性57例,年龄55~80岁。其中36例填充物为混合材料(PMMA ∶CPC=1 ∶1),设为混合组;33例填充物为单纯的PMMA,设为PMMA组,填充物的选择由主治医师向患者及家属沟通后,由患者及家属自行决定。本研究通过本院医学伦理委员会审批(2018年科伦审49号)。两组患者对诊疗过程充分了解,并签署相关医疗同意书。
1.2 纳入标准和排除标准 1.2.1 纳入标准① 经MRI检查诊断为OVCF(单一节段),并且年龄在55岁以上;②双能骨密度检测:-4.5≤T值<-2.5;③胸腰段(胸10至腰2)椎体骨折;④受伤后2周内的新鲜骨折;⑤患者无重大心脑血管疾病,无沟通障碍;⑥根据中国骨质疏松性骨折诊疗指南[9],具备PVP手术指征的患者。
1.2.2 排除标准① 累及中柱或者后柱的不稳定的椎体骨折;②肿瘤、感染等原因造成的病理性骨折;③开放性骨折或伴有腰背部严重软组织开放伤;④压缩骨折时伴有神经损伤,出现肢体感觉、运动功能障碍或尿便障碍;⑤既往因疾病或创伤遗留肢体功能障碍、尿便功能障碍;⑥胸腰段骨折同时伴有骨盆或(和)下肢骨折;⑦患有精神类疾病或不具备完全民事行为能力。
1.3 手术方法经椎弓根入路PVP简要手术过程如下:①患者取俯卧位,C臂X光机定位后常规消毒、铺巾;②于病变椎体双侧椎弓根附近予以1%利多卡因局部浸润麻醉;③在C臂X光机透视监视下经皮穿刺,通过椎弓根放置工作通道。术中C臂X光机透视病变椎体压缩明显,术中穿刺证实椎体骨质疏松严重。将单一骨水泥(PMMA,泰科瑞,生产批号:AB5909)或者混合骨水泥(PMMA ∶CPC=1 ∶1)(CPC,瑞邦骨泰,生产批号:B2001013)与固化液混合,使其粘稠呈牙膏状,在C臂X光机透视监视下注入骨水泥至病变椎体,注意观察骨水泥是否有渗漏,待骨水泥凝固后拔出工作通道。手术切口予以局部碘伏消毒,外盖无菌敷料。
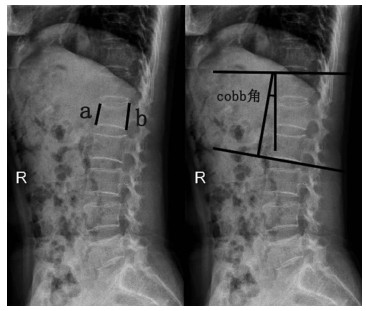
1.4 评价指标统计患者术前,术后2 d、1个月、6个月和2年的资料。评价指标:①一般情况:年龄、性别、骨密度、骨折椎体水平以及围手术期指标(手术时间、术中出血量、骨水泥注入量);②临床疗效指标:Oswestry功能障碍指数问卷表(Oswestry disability index,ODI)和疼痛视觉模拟量表(visual analog scale,VAS);③并发症[术后2年的临近椎体骨折发生率、骨水泥渗漏率(骨水泥发生渗漏例数/总例数×100%)];④放射学指标:椎体矢状指数[压缩椎体前后壁高度比值(anterior vertebral height,AVH)=a/b]和cobb角(图 1)。所有测量数据由2名主治医师测定,并取平均值,量表计算出总分。
|
| 图 1 椎体矢状指数和cobb角的测量方法 |
1.5 统计学分析
采用SPSS 26.0统计软件。采用x±s描述符合正态分布方差齐性的连续性资料,组间比较采用独立样本t检验。连续性变量采用重复测量方差分析比较各时间点组内差异。分类变量采用例和百分比表示,组间比较采用χ2检验或Fisher精确检验。P<0.05为差异具有统计学意义。
2 结果 2.1 患者的一般情况两组患者年龄、性别、骨密度、骨折椎体水平、手术时间、术中出血量以及骨水泥的注入量比较,差异无统计学意义(表 1)。
| 项目 | 混合组(n=36) | PMMA组(n=33) | P |
| 年龄/岁 | 69.3±6.0 | 66.7±6.1 | 0.115 |
| 性别(男/女) | 6/30 | 6/27 | 0.788 |
| 骨密度T值 | -2.9±1.0 | -3.0±0.3 | 0.580 |
| 骨折水平 | |||
| T10 | 3 | 2 | 1.000 |
| T11 | 4 | 3 | 1.000 |
| T12 | 10 | 9 | 0.963 |
| L1 | 12 | 13 | 0.601 |
| L2 | 7 | 6 | 0.893 |
| 手术时间/min | 47.6±8.1 | 49.1±10.9 | 0.534 |
| 出血量/mL | 5.3±2.5 | 4.4±1.5 | 0.089 |
| 骨水泥注入量/mL | 4.5±1.2 | 4.5±0.8 | 0.996 |
2.2 临床疗效指标
混合组和PMMA组患者术后2 d、1个月、6个月、2年的疼痛VAS评分以及术后1个月、6个月、2年ODI评分均下降,差异具有统计学意义(P<0.05),但同一时间点两组比较差异无统计学意义(表 2)。
| 评分指标 | 混合组(n=36) | PMMA组(n=33) | P |
| VAS评分 | |||
| 术前 | 8.0±1.2 | 7.8±1.2 | 0.479 |
| 术后2 d | 3.1±1.3 | 3.4±1.1 | 0.344 |
| 术后1个月 | 2.3±0.6 | 2.5±0.8 | 0.257 |
| 术后6个月 | 1.6±0.5 | 1.8±0.5 | 0.109 |
| 术后2年 | 1.3±0.7 | 1.5±0.6 | 0.142 |
| F | 225.518 | 234.627 | |
| P | <0.05 | <0.05 | |
| ODI评分 | |||
| 术前 | 74.7±4.6 | 75.0±3.8 | 0.814 |
| 术后1个月 | 25.2±11.0 | 26.4±8.3 | 0.617 |
| 术后6个月 | 25.4±8.4 | 26.1±7.8 | 0.723 |
| 术后2年 | 24.4±5.9 | 26.1±7.4 | 0.289 |
| F | 854.343 | 626.365 | |
| P | <0.05 | <0.05 |
2.3 并发症
通过对术后2 d的病椎的CT检测,发现混合组的骨水泥渗漏率[27.8%(10/36)]高于PMMA组[15.1%(5/33)],但差异无统计学意义(P=0.204)。大部分渗漏发生在椎间盘或者椎体前缘,未发生椎管渗漏和肺栓塞,且渗漏都无临床症状发生。而在临近椎体骨折发生方面,术后2年的随访结果显示:混合组的发生率为11.1%(4/36),低于PMMA组的30.3%(10/33),差异具有统计学意义(P=0.048)。
2.4 放射学指标通过术后X线片测量病椎的后凸畸形指标(椎体矢状指数和cobb角)。与PMMA组相比,混合组术后2 d、1个月、6个月、2年的椎体矢状指数和cobb角差异均无统计学意义。在不同时间点两组椎体矢状指数的变化趋势差异无统计学意义,但cobb角的变化趋势差异有统计学意义(P < 0.05)。同时,椎体矢状指数和cobb角的测量都显示术后2 d的后凸畸形与术前相比有改善,但后期随访发现这种改变并没有持续存在(表 3)。表明两种填充物都能较好地强化椎体,避免后凸畸形的加重。
| 指标 | 混合组(n=36) | PMMA组(n=33) | P |
| 椎体矢状指数 | |||
| 术前 | 0.68±0.13 | 0.66±0.11 | 0.810 |
| 术后2 d | 0.71±0.09 | 0.70±0.12 | 0.941 |
| 术后1个月 | 0.68±0.12 | 0.66±0.12 | 0.437 |
| 术后6个月 | 0.68±0.13 | 0.66±0.09 | 0.585 |
| 术后2年 | 0.68±0.11 | 0.65±0.10 | 0.459 |
| F | 1.100 | 2.126 | |
| P | 0.363 | 0.086 | |
| Cobb角/° | |||
| 术前 | 13.6±7.1 | 14.4±7.2 | 0.650 |
| 术后2 d | 12.7±6.4 | 13.2±7.1 | 0.767 |
| 术后1个月 | 14.7±6.9 | 14.2±7.7 | 0.771 |
| 术后6个月 | 14.4±6.9 | 14.9±7.7 | 0.754 |
| 术后2年 | 14.8±7.1 | 14.3±8.0 | 0.808 |
| F | 8.549 | 3.352 | |
| P | <0.05 | 0.044 |
2.5 典型病例
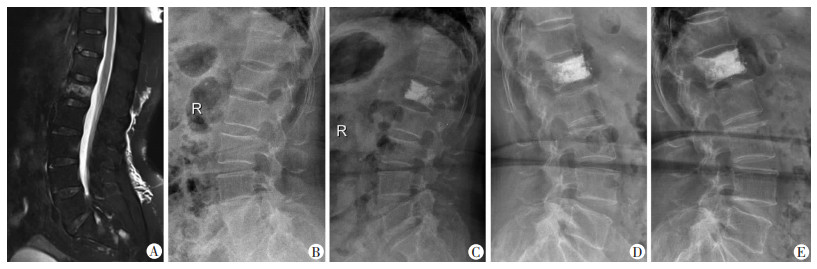
病例1:女性患者,60岁,诊断为腰1椎体骨质疏松压缩性骨折、重度骨质疏松症,采用混合骨水泥(PMMA/CPC)行PVP。图 2为术前MRI、X线片以及术后1个月、6个月、2年的X线片,随访完整,未出现骨水泥渗漏以及后凸畸形。
|
| A:术前MRI(T2压脂);B:术前X线片;C:术后1个月X线片;D:术后6个月X线片;E:术后2年X线片 图 2 腰1椎体骨质疏松压缩性骨折患者术前MRI及术前、术后X线片表现 |
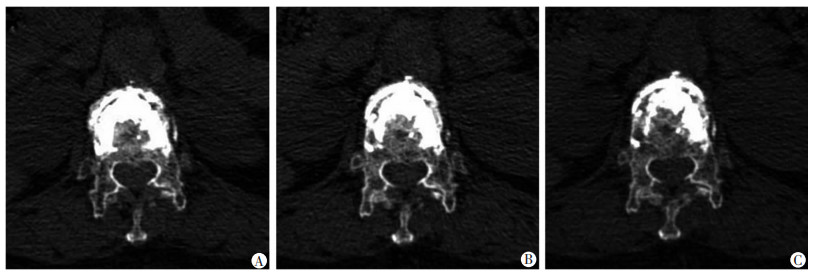
病例2:女性患者,70岁,诊断为胸12椎体骨质疏松压缩性骨折、重度骨质疏松症,采用混合骨水泥(PMMA/CPC)行PVP,图 3为术后1个月、6个月、2年的CT检查,随访完整,可见部分填充物已部分被骨组织吸收替代。
|
| A:术后1个月CT,可见混合骨水泥与周围骨组织有良好的相容性;B:术后6个月CT,可见混合骨水泥与周围骨组织有良好的相容性,并可见部分填充物的吸收;C:术后2年CT,可见混合骨水泥在椎体内稳定存在,组织相容性良好,明显可见部分填充物的吸收 图 3 胸12椎体骨质疏松压缩性骨折患者术后CT表现 |
3 讨论
OVCF是老年人群急性和慢性背痛的常见原因,症状性和无症状性OVCF均可导致严重的脊柱畸形、功能受限、肺损害和生活质量下降,且可进一步增加椎体骨折和死亡风险[10]。目前采用PMMA作为填充材料的PVP手术是公认的治疗OVCF的手术方式,但PMMA的生物力学研究表明其刚度值比松质骨高7~10倍[11],因此临近节段椎体骨折的风险比远节椎体骨折的风险高3倍[12-13]。可吸收的填充材料CPC具有良好的骨传导性、生物相容性,且能在体温下逐渐凝固[14-15],自1993年被提出来后,引起了骨科医师的广泛关注[16]。相关研究已证明CPC在OVCF中的应用是安全有效的[17-18]。但CPC的力学性能欠佳,在弯曲、牵引或剪切力作用下容易发生破坏,因此它在OVCF中的应用存在限制[19]。已有个案报道了单纯采用CPC治疗OVCF出现了骨水泥塌陷[19]。因此两者都不是理想的填充物。
有体外和体内动物实验的相关研究发现混合骨水泥(PMMA/CPC)的优点比较突出[20-21]。首先,混合骨水泥的生物力学性能较好。大鼠椎体的动物研究发现:PMMA与CPC以1 ∶1比例混合后的骨水泥,抗压强度较CPC提高约120%,与1 ∶2、2 ∶1相比较,凝固温度低,固化时间合理,具备合理的空隙率和满意的生物相容性,能有效克服单一材料缺点[22]。且不同配比的混合骨水泥的生物力学研究发现:1 ∶1、2 ∶1、3 ∶1混合的CPC/PMMA骨水泥综合性能更佳,拥有更好的生物安全性、生物力学性能和组织相容性[23]。同时在羊的椎体实验中发现:PMMA与CPC形成的混合骨水泥具有较好的骨痂形成能力和抗压强度[24]。其次,混合骨水泥更有利于成骨。研究表明成骨细胞生长所需要的最低孔径为70 μm,将70 μm以上的孔径称为细胞生长的“有效孔径”[25];而电镜微观观察得知混合骨水泥(PMMA ∶CPC=1 ∶1)的微观结构与CPC相似,孔径在100~300 μm分布最多,满足了骨组织生长的“有效孔径”,因此该配比的混合骨水泥的微观结构更有利于骨生长[22]。在兔桡骨缺损模型上的研究已表明CPC的存在能显著提高PMMA骨水泥的成骨[26]。
但是目前关于PMMA/CPC的混合骨水泥的临床研究较少。WANG等[27]通过临床研究指出矿化胶原改性骨水泥(PMMA/Ⅰ型胶原和羟基磷灰石)与单纯的PMMA都能较好地改善患者的症状及生活质量,且改性骨水泥可使临近椎体的骨折发生率从13.3%降低到2%。姜文康等[28]的临床研究发现含有羟基磷灰石的PMMA具有更好的生物学特性,但在降低邻椎骨折的发生方面还具有争议。两者都指出PMMA/CPC的混合物具有重要的临床意义,但在降低临椎骨折的发生方面还需要更多的临床验证。同时,上述的生物力学以及动物研究显示PMMA与CPC以1 ∶1比例混合的填充物具有更适中的抗压强度和成骨效果,但已有研究未阐述混合的具体比例。本课题组已进行了不同比例的混合骨水泥的研究,目前的初步结果显示1 ∶1比例的混合骨水泥凝固时间较适中,安全性相对较高。因此,本研究首先比较了固定比例(1 ∶1)的PMMA/CPC与PMMA的临床疗效。通过2年的随访发现,混合骨水泥和PMMA都能较好地减轻患者疼痛以及改善功能,明显提高患者的生活质量,具有同等的临床疗效,证明混合骨水泥在PVP手术中的应用是安全有效的。同时,本研究在随访中还发现混合骨水泥与周围骨组织具有良好的组织相容性,术后6个月行CT检查,可见混合填充物已被周围的骨组织吸收、替代,这可能与CPC体内特性密切相关,CPC能被缓慢吸收且被新骨所替代,同时体积不会减少[29]。但影响CPC的降解吸收速度的因素较多,包括不同材料的混合、粉液比以及孔隙率等[30],因此混合骨水泥中CPC何时才能完全吸收且被骨组织替代还需要长时间的随访观察。最重要的是,本研究发现混合组邻近椎体骨折的发生率(11.1%)低于PMMA组(30.3%),差异具有统计学意义(P=0.048),因此混合骨水泥在减少临椎骨折的发生发面具有重要的临床意义。
骨水泥渗漏是PVP手术的主要并发症,骨水泥进入椎管将引起脊髓损伤,甚至进入周围血管引起肺栓塞,但是大部分骨水泥渗漏并不会造成上述严重的并发症[31-32]。渗漏与多种因素有关,其中骨折损伤程度、骨水泥黏度、术者的手术经验是主要因素[33]。已有研究发现PMMA的渗漏率为41%~59.7%[34],而本研究的PMMA组渗漏率为15.1%,远低于文献中报道的比例;上述两项关于混合骨水泥的临床研究报道显示其渗漏率分别为8%和6.7%[27-28],而本研究混合组的渗漏率为27.8%,渗漏率偏高。分析原因:首先,可能是混合骨水泥的凝固时间相对较长,研究表明CPC的凝固时间较PMMA长[35],而混合填充物的凝固时间介于PMMA与CPC之间,较PMMA长,而且与混合比例密切相关,因此渗漏的风险也就相对较高;其次,混合填充物的最佳推注时机需要手术经验的积累才能掌握,存在一定的学习曲线,这也可能是渗漏偏高的原因。但统计学分析发现两组之间比较差异无统计学意义(P=0.204),且渗漏并未出现严重的并发症,因此,混合骨水泥的临床应用是安全可靠的。为了减少混合骨水泥的渗漏,可采取缓慢推注的方式,也可以采取分批次推注的方式。首次推注后,如发现渗漏的风险大时,可适当暂停推注,待首批骨水泥稍凝固后再继续注入。
为更好地比较两种填充物对后凸畸形的影响,本研究采用了椎体矢状指数和cobb角进行分析。两种指标的数据显示混合组和PMMA组组间比较差异无统计学意义,术后2年与术前相比差异也无统计学意义,因此两组患者的后凸畸形都无明显改变,表明两种填充材料都能强化椎体,避免后凸畸形的发生。本研究还通过重复测量方差分析发现:在不同时间点,两组椎体矢状指数的变化趋势差异无统计学意义,但cobb角的变化趋势有差异(P < 0.05),说明cobb角在随访中的变化较大,但2年的随访发现后凸畸形并没有明显变化,可能是因为两种指标的测量差异引起。椎体矢状指数为椎体前后壁高度比值,患者前屈后伸的体位改变对其影响较小;而cobb角为头侧端椎上缘的垂线与尾侧端椎下缘垂线的夹角,体位的变化对其影响较大,且患者在摄片时可因腰背部疼痛出现前屈或后伸的保护体位,因此这两种指标用于病椎后凸畸形的检测,cobb角不如椎体矢状指数精确。本研究在术后2 d的放射检查中还发现两组骨水泥都一定程度上纠正了后凸畸形,但这可能与骨水泥注入量有关,两组的注入剂量都为4.5 mL左右,对病椎的填充都很充分,因此术后近期结果显示后凸有一定的改善,而长期的随访发现这种改变并没有持续。
综上所述,本研究结果显示混合骨水泥(PMMA ∶CPC= 1 ∶1)与PMMA在PVP手术中的应用都能较好地减轻患者的疼痛和改善功能,并强化椎体,避免后凸畸形进一步加重,且部分混合填充物能被骨组织吸收替代,所以混合骨水泥在PVP中的应用是安全有效的。最重要的是,混合骨水泥比PMMA更能降低再发骨折的发生率,因此混合骨水泥具有更好的临床价值。但本研究纳入的病例较少,随访时间较短,仍需要长时间、多中心和大样本的随机对照研究进一步验证该结论。且本研究只比较了1 ∶1比例的混合骨水泥和PMMA的临床疗效,还需要进行更多比例的混合骨水泥的研究,以寻求最佳比例的混合骨水泥。
| [1] |
HE Z, ZHAI Q, HU M, et al. Bone cements for percutaneous vertebroplasty and balloon kyphoplasty: Current status and future developments[J]. J Orthop Translat, 2015, 3(1): 1-11. DOI:10.1016/j.jot.2014.11.002 |
| [2] |
KIM M J, LINDSEY D P, HANNIBAL M, et al. Vertebroplasty versus kyphoplasty: biomechanical behavior under repetitive loading conditions[J]. Spine (Phila Pa 1976), 2006, 31(18): 2079-2084. DOI:10.1097/01.brs.0000231714.15876.76 |
| [3] |
LU Q F, LIU C, WANG D S, et al. Biomechanical evaluation of calcium phosphate-based nanocomposite versus polymethylmethacrylate cement for percutaneous kyphoplasty[J]. Spine J, 2019, 19(11): 1871-1884. DOI:10.1016/j.spinee.2019.06.007 |
| [4] |
ZHU R S, KAN S L, NING G Z, et al. Which is the best treatment of osteoporotic vertebral compression fractures: balloon kyphoplasty, percutaneous vertebroplasty, or non-surgical treatment? A Bayesian network meta-analysis[J]. Osteoporos Int, 2019, 30(2): 287-298. DOI:10.1007/s00198-018-4804-2 |
| [5] |
GARFIN S R, YUAN H A, REILEY M A. New technologies in spine: kyphoplasty and vertebroplasty for the treatment of painful osteoporotic compression fractures[J]. Spine (Phila Pa 1976), 2001, 26(14): 1511-1515. DOI:10.1097/00007632-200107150-00002 |
| [6] |
LIEBERMAN I H, TOGAWA D, KAYANJA M M. Vertebroplasty and kyphoplasty: filler materials[J]. Spine J, 2005, 5(6 Suppl): 305S-316S. DOI:10.1016/j.spinee.2005.02.020 |
| [7] |
BELKOFF S M, MOLLOY S. Temperature measurement during polymerization of polymethylmethacrylate cement used for vertebroplasty[J]. Spine (Phila Pa 1976), 2003, 28(14): 1555-1559. |
| [8] |
KLAZEN C A, LOHLE P N, DE VRIES J, et al. Vertebroplasty versus conservative treatment in acute osteoporotic vertebral compression fractures (Vertos Ⅱ): an open-label randomised trial[J]. Lancet, 2010, 376(9746): 1085-1092. DOI:10.1016/S0140-6736(10)60954-3 |
| [9] |
邱贵兴, 裴福兴, 胡侦明, 等. 中国骨质疏松性骨折诊疗指南——骨质疏松性骨折诊断及治疗原则[J]. 黑龙江科学, 2018, 9(2): 85-88, 95. QIU G X, PEI F X, HU Z M, et al. Guide to diagnosis and treatment of osteoporotic fracture in China——osteoporotic fracture diagnosis and treatment principles[J]. Heilongjiang Sci, 2018, 9(2): 85-88, 95. |
| [10] |
LAU E, ONG K, KURTZ S, et al. Mortality following the diagnosis of a vertebral compression fracture in the Medicare population[J]. J Bone Joint Surg Am, 2008, 90(7): 1479-1486. DOI:10.2106/jbjs.g.00675 |
| [11] |
BOGER A, HEINI P, WINDOLF M, et al. Adjacent vertebral failure after vertebroplasty: a biomechanical study of low-modulus PMMA cement[J]. Eur Spine J, 2007, 16(12): 2118-2125. DOI:10.1007/s00586-007-0473-0 |
| [12] |
LIN D S, HAO J M, LI L, et al. Effect of bone cement volume fraction on adjacent vertebral fractures after unilateral percutaneous kyphoplasty[J]. Clin Spine Surg, 2017, 30(3): E270-E275. DOI:10.1097/BSD.0000000000000204 |
| [13] |
TAYLOR R S, TAYLOR R J, FRITZELL P. Balloon kyphoplasty and vertebroplasty for vertebral compression fractures: a comparative systematic review of efficacy and safety[J]. Spine (Phila Pa 1976), 2006, 31(23): 2747-2755. DOI:10.1097/01.brs.0000244639.71656.7d |
| [14] |
LARSSON S, HANNINK G. Injectable bone-graft substitutes: current products, their characteristics and indications, and new developments[J]. Injury, 2011, 42(Suppl 2): S30-S34. DOI:10.1016/j.injury.2011.06.013 |
| [15] |
BURGUERA E F, XU H H, WEIR M D. Injectable and rapid-setting calcium phosphate bone cement with dicalcium phosphate dihydrate[J]. J Biomed Mater Res B Appl Biomater, 2006, 77(1): 126-134. DOI:10.1002/jbm.b.30403 |
| [16] |
NAKANO M, HIRANO N, MATSUURA K, et al. Percutaneous transpedicular vertebroplasty with calcium phosphate cement in the treatment of osteoporotic vertebral compression and burst fractures[J]. J Neurosurg, 2002, 97(3 suppl): 287-293. DOI:10.3171/spi.2002.97.3.0287 |
| [17] |
NAKANO M, HIRANO N, ZUKAWA M, et al. Vertebroplasty using calcium phosphate cement for osteoporotic vertebral fractures: study of outcomes at a minimum follow-up of two years[J]. Asian Spine J, 2012, 6(1): 34-42. DOI:10.4184/asj.2012.6.1.34 |
| [18] |
RYU K S, SHIM J H, HEO H Y, et al. Therapeutic efficacy of injectable calcium phosphate cement in osteoporotic vertebral compression fractures: prospective nonrandomized controlled study at 6-month follow-up[J]. World Neurosurg, 2010, 73(4): 408-411. DOI:10.1016/j.wneu.2010.01.006 |
| [19] |
YOSHⅡ T, UEKI H, KATO T, et al. Severe kyphotic deformity resulting from collapses of cemented and adjacent vertebrae following percutaneous vertebroplasty using calcium phosphate cement. A case report[J]. Skeletal Radiol, 2014, 43(10): 1477-1480. DOI:10.1007/s00256-014-1912-8 |
| [20] |
AGHYARIAN S, RODRIGUEZ L C, CHARI J, et al. Characterization of a new composite PMMA-HA/Brushite bone cement for spinal augmentation[J]. J Biomater Appl, 2014, 29(5): 688-698. DOI:10.1177/0885328214544770 |
| [21] |
AGHYARIAN S, HU X B, LIEBERMAN I H, et al. Two novel high performing composite PMMA-CaP cements for vertebroplasty: an ex vivo animal study[J]. J Mech Behav Biomed Mater, 2015, 50: 290-298. DOI:10.1016/j.jmbbm.2015.06.022 |
| [22] |
包利, 唐海, 王炳强, 等. CPC/PMMA双向骨水泥性能及生物相容性的初步研究[J]. 中国骨质疏松杂志, 2012, 18(5): 420-424. BAO L, TANG H, WANG B Q, et al. Preliminary study on properties and biocompatibility of CPC/PMMA dual-phase bone cement[J]. Chin J Osteoporos, 2012, 18(5): 420-424. DOI:10.3969/j.issn.1006-7108.2012.05.006 |
| [23] |
YANG J, ZHANG K R, ZHANG S, et al. Preparation of calcium phosphate cement and polymethyl methacrylate for biological composite bone cements[J]. Med Sci Monit, 2015, 21: 1162-1172. DOI:10.12659/MSM.893845 |
| [24] |
KOMANG-AGUNG I S, HYDRAVIANTO L, SINDRAWATI O, et al. Effect of polymethylmethacrylate-hydroxyapatite composites on callus formation and compressive strength in goat vertebral body[J]. Malays Orthop J, 2018, 12(3): 6-13. DOI:10.5704/moj.1811.002 |
| [25] |
ADACHI T, OSAKO Y, TANAKA M, et al. Framework for optimal design of porous scaffold microstructure by computational simulation of bone regeneration[J]. Biomaterials, 2006, 27(21): 3964-3972. DOI:10.1016/j.biomaterials.2006.02.039 |
| [26] |
ZHANG X, KANG T, LIANG P Q, et al. Biological activity of an injectable biphasic calcium phosphate/PMMA bone cement for induced osteogensis in rabbit model[J]. Macromol Biosci, 2018, 18(3): 1700331. DOI:10.1002/mabi.201700331 |
| [27] |
WANG X, KOU J M, YUE Y, et al. Clinical outcome comparison of polymethylmethacrylate bone cement with and without mineralized collagen modification for osteoporotic vertebral compression fractures[J]. Medicine (Madr), 2018, 97(37): e12204. DOI:10.1097/md.0000000000012204 |
| [28] |
姜文康, 耿伟, 许莹莹, 等. 矿化胶原改性骨水泥在骨质疏松性椎体压缩骨折中的应用[J]. 中国组织工程研究, 2020, 24(15): 2381-2386. JIANG W K, GENG W, XU Y Y, et al. Application of mineralized collagen modified bone cement in the treatment of osteoporotic vertebral compression fractures[J]. Chin J Tissue Eng Res, 2020, 24(15): 2381-2386. DOI:10.3969/j.issn.2095-4344.2603 |
| [29] |
ZHANG J T, LIU W Z, SCHNITZLER V, et al. Calcium phosphate cements for bone substitution: chemistry, handling and mechanical properties[J]. Acta Biomater, 2014, 10(3): 1035-1049. DOI:10.1016/j.actbio.2013.11.001 |
| [30] |
GALOVICH L A, PEREZ-HIGUERAS A, ALTONAGA J R, et al. Biomechanical, histological and histomorphometric analyses of calcium phosphate cement compared to PMMA for vertebral augmentation in a validated animal model[J]. Eur Spine J, 2011, 20(Suppl 3): 376-382. DOI:10.1007/s00586-011-1905-4 |
| [31] |
DE LACERDA SCHICKERT S, PINTO J C, JANSEN J, et al. Tough and injectable fiber reinforced calcium phosphate cement as an alternative to polymethylmethacrylate cement for vertebral augmentation: a biomechanical study[J]. Biomater Sci, 2020, 8(15): 4239-4250. DOI:10.1039/d0bm00413h |
| [32] |
LIN B J, LI C C, MA H I. Intradural cement leakage after percutaneous vertebroplasty[J]. Turk Neurosurg, 2015, 25(6): 940-942. DOI:10.5137/1019-5149.JTN.11079-14.1 |
| [33] |
赵敏超, 武汉. 骨水泥材料在椎体成形术中的研究进展[J]. 医学综述, 2018, 24(17): 3409-3413, 3418. ZHAO M C, WU H. Research progress of bone cement in vertebroplasty[J]. Med Recapitul, 2018, 24(17): 3409-3413, 3418. DOI:10.3969/j.issn.1006-2084.2018.17.016 |
| [34] |
ZHAN Y, JIANG J, LIAO H, et al. Risk factors for cement leakage after vertebroplasty or kyphoplasty: a meta-analysis of published evidence[J]. World Neurosurg, 2017, 101: 633-642. DOI:10.1016/j.wneu.2017.01.124 |
| [35] |
MAESTRETTI G, CREMER C, OTTEN P, et al. Prospective study of standalone balloon kyphoplasty with calcium phosphate cement augmentation in traumatic fractures[J]. Eur Spine J, 2007, 16(5): 601-610. DOI:10.1007/s00586-006-0258-x |




