肾母细胞瘤(wilms tumor,WT)起源于肾脏胚胎组织,是儿童最常见的肾脏肿瘤,约占儿童肾脏肿瘤的90%[1]。近年来,随着手术、化疗、放疗等多学科合作和个体化治疗技术的提升,整体生存率可达90%以上[2]。但肿瘤复发仍出现在一些低风险患儿中,因此亟待更加准确的分期和分层改善这部分患儿的预后。从1969年开始,通过多机构试验对不同的治疗策略进行评估,已经确定了WT患儿的几个预后因素,其中一个重要的预后因素是局部区域淋巴结的受累[3-4]。越来越多的学者对淋巴结相关因素进行研究,发现不仅仅是淋巴结受累对患儿预后有影响,淋巴结取样与患儿的预后也有一定相关性[5-9]。因此,本研究旨在探究淋巴结受累及淋巴结取样对肾母细胞瘤患儿预后的影响,并确定分期所需要的最少淋巴结取样数量。
1 对象与方法 1.1 研究设计与对象本研究是项回顾性队列研究,收集2010年1月至2019年12月期间在重庆医科大学附属儿童医院泌尿外科规范化诊治的肾脏恶性肿瘤173例患儿的临床资料,男性81例,女性92例,年龄1个月至13岁,发病中位年龄为2岁。收集信息包括:性别、肿瘤组织学、淋巴结取样数量、淋巴结组织学、术前化疗及患儿预后情况。根据是否有淋巴结受累将患儿分为淋巴结受累组和淋巴结未受累组,比较两组患儿的5年无事件生存率(event-free survival,EFS)。根据淋巴结取样数量的不同,探究淋巴结取样数量对淋巴结阳性率的影响,同时比较不同取样数量患儿的5年EFS。本研究已获得重庆医科大学附属儿童医院医学研究伦理委员会审查批准(2020年伦审第255号)。
1.2 诊断标准及治疗方案入组患儿均由重庆医科大学病理科根据术后病理组织学确诊,根据肿瘤病理组织学类型分为预后良好型(favorable histology,FH)与预后不良型(unfavorable histology,uFH)。治疗方案采用美国国家肾母细胞瘤研究组(National Wilms Tumor Study,NWTS) 推荐方案,对于能一期行肿瘤切除术的患儿均一期手术,术前评估一期手术难度较大的患儿先行术前化疗,待肿瘤缩小后再行手术。手术方式为患肾根治术及淋巴结活检,采用经腹腔入路暴露患肾及肿瘤,完整切除瘤体、残肾、输尿管等。淋巴结活检范围包括肾周淋巴结、下腔静脉旁淋巴结、腹主动脉旁淋巴结、肠系膜淋巴结,不行广泛淋巴结清扫[10]。所有患儿均由重庆医科大学附属儿童医院泌尿外科正高医师主刀完成手术。分期采用NWTS的分期系统[12]。术后根据患儿肿瘤组织学类型及分期行辅助放化疗,化疗方案参照NWTS-5方案[11]。
1.3 纳入排除标准纳入标准:①在我院完成手术及术后放化疗;②术后病理组织学检查证实为肾母细胞瘤;③术前无远处转移。排除标准:①治疗中失访;②双侧发病。
1.4 随访采用门诊、住院、电话、微信、信件等方式随访。定期进行体格检查,随访血常规、生化、B超、X线、CT等指标。随访起始日为术后第1天,随访截至2020年6月1日。随访指标为5年无事件生存时间,事件定义为进入治疗后出现复发、转移、进展、死亡。
1.5 统计学分析利用SPSS统计软件对数据进行分析,利用Kaplan-Meier生存函数描述淋巴结受累及淋巴结取样数量对患儿5年EFS的影响,采用Log-rank检验比较组间患儿的生存率差异。Pearson χ2检验用于分类变量的比较。
2 结果 2.1 肾母细胞瘤患儿的一般特征共有173例WT患儿纳入本研究,纳入研究患儿的性别、分期、病理类型、术前化疗情况、淋巴结取样数量以及淋巴结受累情况详见表 1。
| 特征 | 例数 | 百分比(%) |
| 性别 | ||
| 男 | 81 | 46.8 |
| 女 | 92 | 53.2 |
| 临床分期 | ||
| Ⅰ期 | 57 | 32.9 |
| Ⅱ期 | 74 | 42.8 |
| Ⅲ期 | 42 | 24.3 |
| 病理类型 | ||
| FH型 | 133 | 76.9 |
| uFH型 | 40 | 23.1 |
| 是否术前化疗 | ||
| 是 | 69 | 39.9 |
| 否 | 104 | 60.1 |
| 淋巴结取样数量 | ||
| 0 | 20 | 11.6 |
| 1~3 | 71 | 41.0 |
| 4~6 | 41 | 23.7 |
| 7~9 | 25 | 14.5 |
| 10~ | 16 | 9.2 |
| 淋巴结受累 | ||
| 否 | 150 | 86.7 |
| 是 | 23 | 13.3 |
2.2 淋巴结受累对WT患儿预后的影响
淋巴结受累患儿与未受累患儿的5年EFS分别为56.19%与81.27%(P<0.000 1)。在不同病理类型的亚组中,淋巴结受累对uFH患儿预后(25.00% vs 71.13%,P=0.000 2)的影响明显大于FH患儿(73.33% vs 84.16%,P=0.091 8,图 1)。

|
| A:总体患儿;B:uFH患儿;C:FH患儿 图 1 淋巴结受累对WT患儿预后的影响 |
2.3 淋巴结取样数量与淋巴结阳性率的关系
淋巴结受累患儿的取样数量中位数为8(2~24)个,淋巴结未受累患儿的取样数量中位数为3(0~19)个。图 2总结了淋巴结受累患儿的百分比与淋巴结取样数量间的关系。淋巴结阳性率随淋巴结取样数量的增加而增加(P<0.000 1)。当淋巴结取样数量为7~9个时,有38.46%患儿发现有淋巴结受累。但当淋巴结取样数量超过10个时,发现阳性淋巴结的概率并没有明显增加(P=0.826 0)。取样的淋巴结数量与疾病分期有关:14.0%的Ⅰ期患儿及12.2%的Ⅱ期患儿采集至少7个淋巴结,而Ⅲ期患儿为57.1%(P<0.000 1)。FH患儿与uFH患儿淋巴结的取样数量差异无统计学意义(P=0.839 0)。淋巴结取样数量与患儿是否术前化疗无显著关联(P=0.621 0)。

|
| 图 2 淋巴结取样数量对WT患儿淋巴结阳性率的影响 |
2.4 淋巴结取样数量对WT患儿预后的影响
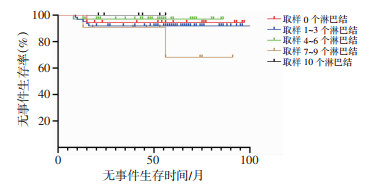
为了排除肿瘤淋巴结浸润对预后的干扰,我们排除了队列中的Ⅲ期患儿。在Ⅰ期和Ⅱ期患儿中,淋巴结取样数量与WT患儿的5年EFS无显著关联(P=0.479 0,图 3)。
|
| 图 3 WT患儿淋巴结取样数量对预后的影响 |
3 讨论
本研究证实了先前的报道:淋巴结受累对WT患儿的预后有显著影响[13]。然而淋巴结受累对uFH患儿预后的影响明显大于FH患儿。这表明目前的后续辅助治疗对由于淋巴结受累而归为Ⅲ期的FH患儿是有效的,在这些患儿中,淋巴结取样提供了分期的重要依据,使其得到了适当的后续放化疗。而在uFH患儿中,肿瘤的组织学类型对患儿预后的影响更大,后续治疗的强度可能不足。
由于肾母细胞瘤对后续放化疗的高敏感性,广泛的淋巴结清扫并不会显著提高患儿的预后,反而会增加不必要的术后并发症[14]。但近年来多个权威机构(如NWTS小组、中国小儿肿瘤专业委员会等)研究发现,在肿瘤切除时未能取样淋巴结与肿瘤复发率的升高相关[15-17]。这是由于部分低分期患儿中存在隐匿性的淋巴结转移,导致这部分患儿未得到正确的分期从而导致后续辅助治疗强度不足[18]。因此为确保患儿术后的准确分期,需确定淋巴结的最少取样数量。本研究发现在一定范围内,随着淋巴结取样数量的增加,发现阳性淋巴结的概率会随之增加,当至少取样7个淋巴结时,发现阳性淋巴结的概率更大。但没有必要无限制的增加淋巴结的取样数量,当淋巴结取样超过10个以后,淋巴结的阳性率并没有明显提高。同时,本研究在Ⅰ、Ⅱ期患儿中并未得到淋巴结取样数量对患儿的预后有显著影响的结论,反而淋巴结取样越多的患儿EFS可能更低,这可能是外科医生在高风险的患儿(如肿瘤更大、肿瘤破溃、淋巴结阳性)中倾向性地取样更多的淋巴结。
淋巴结受累的位置是影响肾母细胞瘤患儿预后的关键因素之一,肾门淋巴结受累的概率明显高于其他位置,且肾门淋巴结受累的患儿较其他区域淋巴结受累的患儿具有更好的预后[19]。遗憾的是由于部分病例对于淋巴结受累的位置并未描述,本研究未分析淋巴结受累位置对预后的影响。同时肾母细胞瘤患儿的预后是受患儿年龄、肿瘤质量、16q和1p杂合性丢失、淋巴结受累等因素影响,本研究未进行这些因素的多因素分析,所以这也是本研究的局限之处。
总之,淋巴结受累对肾母细胞瘤患儿的预后是有显著影响的,虽然淋巴结取样数量不能预测患儿的预后,但它与淋巴结的阳性率显著相关,在术中进行淋巴结取样时,需至少取样7个淋巴结以满足术后分期的准确性。而外科医生应该更加重视术中淋巴结的规范化取样,设计更多前瞻性研究来明确淋巴结相关因素(淋巴结受累、淋巴结受累位置、淋巴结取样数量、淋巴结密度等)对WT患儿预后的影响。
| [1] |
DAVIDOFF A M. Wilms' tumor[J]. Curr Opin Pediatr, 2009, 21(3): 357-364. DOI:10.1097/mop.0b013e32832b323a |
| [2] |
COTTON C A, PETERSON S, NORKOOL P A, et al. Early and late mortality after diagnosis of Wilms tumor[J]. J Clin Oncol, 2009, 27(8): 1304-1309. DOI:10.1200/jco.2008.18.6981 |
| [3] |
BRESLOW N, SHARPLES K, BECKWITH J B, et al. Prognostic factors in nonmetastatic, favorable histology Wilms' tumor. Results of the third national Wilms' tumor study[J]. Cancer, 1991, 68(11): 1245-1353. DOI:10.1002/1097-0142(19911201)68:112345:aid-cncr2820681103>3.0.co;2-t |
| [4] |
SHAMBERGER R C, GUTHRIE K A, RITCHEY M L, et al. Surgery-related factors and local recurrence of Wilms tumor in national wilms tumor study 4[J]. Ann Surg, 1999, 229(2): 292-297. DOI:10.1097/00000658-199902000-00019 |
| [5] |
AMIT M, TAM S, BOONSRIPITAYANON M, et al. Association of lymph node density with survival of patients with papillary thyroid cancer[J]. JAMA Otolaryngol Head Neck Surg, 2018, 144(2): 108. DOI:10.1001/jamaoto.2017.2416 |
| [6] |
YOU H S, YANG J, LIU Q Q, et al. The impact of the lymph node density on overall survival in patients with Wilms' tumor: a SEER analysis[J]. Cancer Manag Res, 2018, 10: 671-677. DOI:10.2147/cmar.s163514 |
| [7] |
PAN Z Y, BU Q T, YOU H S, et al. Determining the optimal cutoff point for lymph node density and its impact on overall survival in children with Wilms' tumor[J]. Cancer Manag Res, 2019, 11: 759-766. DOI:10.2147/cmar.s190138 |
| [8] |
WALKER J P, JOHNSON J S, EGUCHI M M, et al. Factors affecting lymph node sampling patterns and the impact on survival of lymph node density in patients with Wilms tumor: a Surveillance, Epidemiology, and End Result (SEER) database review[J]. J Pediatr Urol, 2020, 16(1): 81-88. DOI:10.1016/j.jpurol.2019.10.030 |
| [9] |
LEAPE L L, BRESLOW N E, BISHOP H C. The surgical treatment of Wilms' tumor: results of the National Wilms' Tumor Study[J]. Ann Surg, 1978, 187(4): 351-356. DOI:10.1097/00000658-197804000-00001 |
| [10] |
METZGER M L, DOME J S. Current therapy for Wilms' tumor[J]. Oncologist, 2005, 10(10): 815-826. DOI:10.1634/theoncologist.10-10-815 |
| [11] |
KO E Y, RITCHEY M L. Current management of Wilms' tumor in children[J]. J Pediatr Urol, 2009, 5(1): 56-65. DOI:10.1016/j.jpurol.2008.08.007 |
| [12] |
DOME J S, GRAF N, GELLER J I, et al. Advances in wilms tumor treatment and biology: progress through international collaboration[J]. J Clin Oncol, 2015, 33(27): 2999-3007. DOI:10.1200/jco.2015.62.1888 |
| [13] |
JEREB B, TOURNADE M F, LEMERLE J, et al. Lymph node invasion and prognosis in nephroblastoma[J]. Cancer, 1980, 45(7): 1632-1636. DOI:10.1002/1097-0142(19800401)45:71632:aid-cncr2820450719>3.0.co;2-f |
| [14] |
GODZINSKI J, DEKRAKER J, GRAF N, et al. Is the number of lymph nodes sampled at Wilms tumour nephrectomy predictive for detection of the regional extension of the disease[J]. Pediatr Blood Cancer, 2004, 43(4): 329. |
| [15] |
ZHUGE Y, CHEUNG M C, YANG R L, et al. Improved survival with lymph node sampling in wilms tumor[J]. J Surg Res, 2011, 167(2): e199-e203. DOI:10.1016/j.jss.2010.12.026 |
| [16] |
LEAPE L L, BRESLOW N E, BISHOP H C. The surgical treatment of Wilms' tumor: results of the National Wilms' Tumor Study[J]. Ann Surg, 1978, 187(4): 351-356. DOI:10.1097/00000658-197804000-00001 |
| [17] |
RAVAL M V, BILIMORIA K Y, BENTREM D J, et al. Nodal evaluation in Wilms' tumors: analysis of the national cancer data base[J]. Ann Surg, 2010, 251(3): 559-565. DOI:10.1097/sla.0b013e3181cc95d7 |
| [18] |
KIERAN K, ANDERSON J R, DOME J S, et al. Lymph node involvement in Wilms tumor: results from National Wilms Tumor Studies 4 and 5[J]. J Pediatr Surg, 2012, 47(4): 700-706. DOI:10.1016/j.jpedsurg.2011.08.017 |
| [19] |
BIEMANN OTHERSEN H Jr, DELORIMER A, HRABOVSKY E, et al. Surgical evaluation of lymph node metastases in Wilms' tumor[J]. J Pediatr Surg, 1990, 25(3): 330-331. DOI:10.1016/0022-3468(90)90079-o |




