头痛和前庭症状都是神经内科常见的症状,偏头痛的终生患病率为16%,眩晕终生患病率为7%,实际上有3.2%的人群会同时发生[1]。研究发现偏头痛较其他原发性头痛疾病更常合并发作性前庭症状或前庭疾病(如良性阵发性位置性眩晕、前庭神经炎、梅尼埃病等)[2]。虽然近年来国际头痛协会及国际眩晕协会共同提出前庭性偏头痛的概念并制定了诊断标准,但是目前该标准仍置于国际头痛分类第3版(International Classification of Headache Disorders, 3rd edition, ICHD-3)附录中[3]。
前庭症状与偏头痛的关系是复杂的,远超出前庭性偏头痛的诊断概念[4-5]。目前关于偏头痛伴随头晕或眩晕作为相关症状的研究较少,也没有报告偏头痛与前庭症状发生的时间关系,这会影响前庭症状与偏头痛发生的相关性的机制研究。前庭症状也是偏头痛预防性药物如抗高血压和抗惊厥药物的常见副作用,充分了解前庭症状与偏头痛的关系,对治疗有指导作用。
因此,本研究分析前庭症状在发作性偏头痛、慢性偏头痛、紧张型头痛患者中的患病率,研究前庭症状与偏头痛特征之间的相关性,探讨前庭症状在偏头痛中的临床应用价值,为进一步了解偏头痛的发病机制提供临床依据。
1 资料与方法 1.1 研究对象连续性纳入2019年1-12月首次就诊于重庆医科大学附属第一医院神经内科头痛门诊,以头痛为主诉的患者。本研究方案获重庆医科大学附属第一医院伦理委员会批准(2014-13号),所有患者在参与研究前被告知研究目的并获得知情同意。
1.2 纳入及排除标准根据ICHD-3偏头痛及紧张型头痛(严格版)诊断标准,纳入偏头痛及紧张型头痛患者;前庭症状标准指巴拉尼协会前庭症状分类[5]所描述的所有类别的前庭症状,包括内在性眩晕,外在性眩晕,位置、视觉、头部运动等诱发的眩晕以及头晕伴有恶心。排除标准包括:①年龄小于16岁;②头痛发病年龄大于60岁;③其他原发性头痛;④合并其他继发性头痛疾病(如高血压、中风、癫痫、精神疾病、头部外伤、肿瘤、鼻窦炎等);⑤妊娠;⑥合并其他前庭疾病(如前庭性偏头痛、前庭神经炎、良性阵发性位置性眩晕、梅尼埃病、前庭阵发症等)。
1.3 方法每位患者在神经科医师指导下完成半结构型问卷调查,问卷内容包括3个部分:①人口统计学(个人情况及家族史);②头痛情况,包括头痛发病年龄、病程、诱因、持续时间、发作频率(每月发作天数)、严重程度(数字疼痛量表评分1~10分)、伴随症状及止痛药使用情况;③前庭症状情况,包括发病年龄、病程、发作频率、与头痛发作的时间关系(3种记录方式:总是、偶尔、从不)[6]。将纳入患者分为3组:发作性偏头痛组、慢性偏头痛组(头痛≥15 d/月,偏头痛样头痛发作≥8 d/月,持续3个月)及紧张型头痛组。
1.4 统计学方法采用SPSS 22.0统计软件,连续型变量表示为x±s,单因素方差分析用于评估3组之间的差异,分类变量表示为频率分布[例(%)],使用χ2检验评估组间差异,出现样本量小于40时,用Fisher精确检验,所有统计分析为双侧检验,P < 0.05为差异有统计学意义。
2 结果 2.1 一般情况研究期间共有685位头痛患者就诊,排除数据收录不完整的19例,诊断不清楚的15例,再根据排除标准排除227例,共424例纳入研究分组,女性患者占比75%(318/424), 年龄16~83(43.45±14.17)岁。其中发作性偏头痛222例(52.4%),慢性偏头痛174例(41.0%),紧张型头痛28例(6.6%)。
2.2 发作性偏头痛、慢性偏头痛、紧张型头痛患者的临床特点发作性偏头痛、慢性偏头痛与紧张型头痛3组患者基本情况见表 1。慢性偏头痛与紧张型头痛就诊年龄大于发作性偏头痛(P < 0.05),但是性别比例差异无统计学意义。紧张型头痛的头痛程度以轻度为主,偏头痛以中度-重度头痛为主。前庭症状在偏头痛组与紧张型头痛组中的占比分别为25.3%(100/396)和3.6%(1/28),在偏头痛组中,慢性偏头痛患者的前庭症状占比及止痛药使用明显多于发作性偏头痛组(P < 0.05)。
| 基本资料 | 发作性偏头痛组(n=222) | 慢性偏头痛组(n=174) | 紧张型头痛组(n=28) |
| 年龄/岁 | 40.09±13.16 | 47.10±14.38a | 47.39±14.38a |
| 女性 | 163(73.4) | 137(78.7) | 18(64.3) |
| 家族史 | |||
| 头痛家族史 | 151(68.0)b | 121(69.5)b | 5(17.9) |
| 前庭症状家族史 | 70(31.5)b | 46(26.4)b | 0(0) |
| 头痛特点 | |||
| 单侧 | 85(38.3)b | 66(37.9)b | 5(17.9) |
| 搏动性 | 69(31.1)b | 50(28.7)b | 0(0) |
| 活动后加重 | 141(63.5)b | 125(71.8)b | 0(0) |
| 头痛程度 | |||
| 0~3分 | 9(4.1)b | 5(2.9)b | 20(71.4) |
| 4~6分 | 113(50.9)b | 85(48.9)b | 8(28.6) |
| 7~10分 | 100(45.0)b | 84(48.3)b | 0(0) |
| 伴随症状 | |||
| 恶心 | 110(49.5)b | 91(52.3)b | 0(0) |
| 呕吐 | 55(24.8)b | 39(22.4)b | 0(0) |
| 畏声 | 96(43.2)b | 80(46.0)b | 1(3.6) |
| 畏光 | 62(27.9)b | 43(24.7)b | 0(0) |
| 恶心或呕吐 | 114(51.4)b | 96(55.2)b | 0(0) |
| 畏光和畏声 | 47(21.2)b | 32(18.4)b | 0(0) |
| 前庭症状 | 46(20.7)b | 54(31.0)ab | 1(3.6) |
| 止痛药使用 | 149(67.1)b | 138(79.3)ab | 0(0) |
| a: P < 0.05, 与发作性偏头痛比较;b:P < 0.05,与紧张型头痛比较 | |||
2.3 不同头痛频率发作性偏头痛患者头痛特点及伴随症状
将发作性偏头痛患者根据头痛频率分为低频组(≤1 d/月)、中频组(2~8 d/月)及高频组(9~14 d/月),发现中频组人数125例(56.3%),3组在年龄、性别比例、家族史、前庭症状及头痛、前庭症状(发病年龄及病程)上差异均无统计学意义,但在头痛特点(单侧、搏动性、活动后加重)及伴随症状上中频组最典型,尤其对比低频组有统计学差异(P < 0.05)。在低频组头痛程度以中度为主(43例,72.9%),而在中频及高频组头痛程度以重度为主(P < 0.05)。并且发现随着头痛频率的增加,止痛药使用也在增加(表 2)。
| 临床资料 | 低频组(n=59) | 中频组(n=125) | 高频组(n=38) |
| 年龄/岁 | 41.98±13.82 | 39.24±12.59 | 39.94±13.99 |
| 女性 | 44(74.6) | 94(75.2) | 25(65.8) |
| 家族史 | |||
| 头痛家族史 | 36(61.0) | 88(70.4) | 27(71.1) |
| 前庭症状家族史 | 21(35.6) | 38(30.4) | 11(28.9) |
| 头痛发病年龄/岁 | 30.15±11.30 | 28.46±11.03 | 28.66±14.27 |
| 头痛病程/年 | 11.78±10.36 | 11.24±9.16 | 11.45±11.57 |
| 前庭症状发病年龄/岁 | 38.50±15.37 | 33.57±12.80 | 32.00±13.93 |
| 前庭症状病程/年 | 5.16±6.53 | 7.48±8.07 | 9.29±10.36 |
| 头痛特点 | |||
| 单侧 | 17(28.8) | 58(46.4)ab | 10(26.3) |
| 搏动性 | 10(16.9) | 49(39.2)a | 10(26.3) |
| 活动后加重 | 31(52.5) | 88(70.4)a | 22(57.9) |
| 头痛程度评分 | |||
| 0~3分 | 3(5.1) | 5(4.0) | 1(2.6) |
| 4~6分 | 43(72.9) | 54(44.8)a | 16(42.1)a |
| 7~10分 | 13(22.0) | 66(51.2)a | 21(55.3)a |
| 伴随症状 | |||
| 恶心 | 22(37.3) | 73(58.4)a | 15(39.5) |
| 呕吐 | 9(15.3) | 37(29.6)a | 9(23.7) |
| 畏声 | 18(30.5) | 61(48.8)a | 17(44.7) |
| 畏光 | 10(16.9) | 40(32.0)a | 12(31.6) |
| 恶心或呕吐 | 23(39.0) | 74(59.2)a | 17(44.7) |
| 畏光和畏声 | 7(11.9) | 31(24.8)a | 9(23.7) |
| 前庭症状 | 16(27.1) | 23(18.4) | 7(18.4) |
| 止痛药使用情况 | 36(61.0) | 84(67.2) | 29(76.3) |
| a: P < 0.05, 与低频组比较;b:P < 0.05,与高频组比较 | |||
2.4 不同头痛频率慢性偏头痛患者的临床特点
进一步将慢性偏头痛患者根据头痛频率分成两组:非持续性头痛组(15~29 d/月)及持续性头痛组(30 d/月),两组间在人口统计学、家族史、临床特点、前庭症状及止痛药的使用上差异均无统计学意义(表 3)。
| 临床资料 | 非持续性头痛组(n=65) | 持续性头痛组(n=109) |
| 年龄/岁 | 46.40±12.34 | 47.53±12.76 |
| 女性 | 50(76.9) | 87(79.8) |
| 家族史 | ||
| 头痛家族史 | 48(73.8) | 72(66.1) |
| 前庭症状家族史 | 19(29.2) | 27(24.8) |
| 头痛发病年龄/岁 | 30.31±12.34 | 31.50±11.52 |
| 头痛病程/年 | 15.92±10.32 | 16.03±12.43 |
| 前庭症状发病年龄/岁 | 33.71±10.46 | 37.33±11.39 |
| 前庭症状病程/年 | 10.33±9.73 | 12.36±8.92 |
| 头痛特点 | ||
| 单侧 | 23(35.4) | 43(39.4) |
| 搏动性 | 19(29.2) | 31(28.4) |
| 活动后加重 | 50(76.9) | 75(68.8) |
| 头痛程度评分 | ||
| 0~3分 | 0(0.0) | 5(4.9) |
| 4~6分 | 34(52.3) | 51(46.9) |
| 7~10分 | 31(47.7) | 53(48.6) |
| 伴随症状 | ||
| 恶心 | 34(52.3) | 57(52.3) |
| 呕吐 | 15(23.1) | 24(22.0) |
| 畏声 | 30(46.2) | 50(45.9) |
| 畏光 | 17(26.2) | 26(23.9) |
| 恶心或呕吐 | 37(56.9) | 59(54.1) |
| 畏光和畏声 | 13(20.0) | 19(17.4) |
| 前庭症状 | 21(32.3) | 33 (30.3) |
| 止痛药使用情况 | 51(78.5) | 87(79.8) |
2.5 前庭症状分类比较
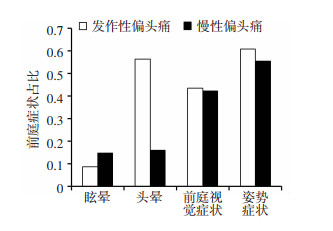
对100例有前庭症状的偏头痛患者前庭症状进行分类。发现眩晕在发作性偏头痛及慢性偏头痛两组中占比最小(8.7%、14.1%),而头晕及姿势症状占比最高,其次是前庭视觉症状(41.2%、40.9%),但四类前庭症状在两组偏头痛之间差异无统计学意义(图 1)。
|
| 图 1 偏头痛中前庭症状的分类对比 |
2.6 各头痛频率组前庭症状与头痛发生时间的关系
根据头痛频率分别列出每组前庭症状与头痛发生的时间关系,发现前庭症状在低频组(≤1 d/月)患者中与头痛分开发作的占比最高(68.8%,P < 0.05),而随着头痛频率的增加,与头痛同时发作的频率也逐渐增高,尤其是在慢性偏头痛中占比明显高于低频组(P < 0.05,表 4)。
| 前庭症状与头痛发生时间关系 | ≤1 d/月(n=16) | 2~8 d/月(n=23) | 9~14 d/月(n=7) | 15~29 d/月(n=21) | 30 d/月(n=33) |
| 从不 | 11(68.8) | 8(34.8)a | 1(14.3)a | 3(14.3)a | 6(18.2)a |
| 偶尔 | 2(12.5) | 5(21.7) | 2(28.6) | 6(28.6) | 8(24.2) |
| 经常 | 3(18.8) | 10(43.4) | 4(57.1) | 12(57.1)a | 19(57.6)a |
| a: P < 0.05, 与≤1 d/月比较 | |||||
进一步分析前庭症状与头痛发生的时间关系是否有1个界限点,根据头痛频率分为4组(< 8 d/月、8~14 d/月、15~29 d/月、30 d/月),观察前庭症状在各组中占比情况,发现头痛频率 < 8 d/月的患者,头痛与前庭症状分开发作的占比最高(19例,51.4%),而两者同时发作的频率最低(11例,29.7%),以上两种情况与头痛频率≥8 d/月的3组比较差异均有统计学意义。当头痛与前庭症状同时发作时,随着头痛频率的增加,头晕病程逐渐增长(P < 0.05)。对比头痛频率 < 8 d/月的患者,持续性头痛组的患者头痛病程明显较长(P < 0.05,表 5)。
| 前庭症状与头痛发生时间的关系 | < 8 d/月(n=37) | 8~14 d/月(n=9) | 15~29 d/月(n=21) | 30 d/月(n=33) |
| 从不 | 19(51.4) | 1(15.4)a | 3(14.3)a | 6(18.2)a |
| 家族史 | ||||
| 头痛家族史 | 12(63.2) | 1(100.0) | 2(66.7) | 3(50.0) |
| 前庭症状家族史 | 8(42.1) | 0(0.0) | 2(66.7) | 2(33.3) |
| 头痛发病年龄/岁 | 33.20±14.89 | 31.00 | 37.67±11.03 | 37.33±12.11 |
| 头痛病程/年 | 15.58±10.67 | 13.00 | 17.33±9.16 | 20.00±8.58 |
| 前庭症状发病年龄/岁 | 39.04±16.32 | 39.00 | 37.67±12.51 | 39.17±13.92 |
| 前庭症状病程/年 | 5.63±6.64 | 5.00 | 9.33±7.91 | 8.17±11.26 |
| 偶尔 | 7(18.9) | 2(23.1) | 6(28.6) | 8(24.2) |
| 家族史 | ||||
| 头痛家族史 | 3(42.9) | 1(50.0) | 4(66.7) | 5(62.5) |
| 前庭症状家族史 | 2(28.6) | 1(50.0) | 3(50.0) | 4(50.0) |
| 头痛发病年龄/岁 | 30.00±4.54 | 28.95±13.54 | 25.5±5.54 | 30.25±13.42 |
| 头痛病程/年 | 11.50±6.36 | 11.50±5.47 | 18.50±7.36 | 16.13±11.58 |
| 前庭症状发病年龄/岁 | 33.50±4.54 | 33.00±5.66 | 39.17±9.03 | 37.75±12.82 |
| 前庭症状病程/年 | 5.50±7.64 | 7.50±8.32 | 6.67±5.64 | 8.63±5.26 |
| 经常 | 11(29.7) | 6(58.3)a | 12(57.1)a | 19(57.6)a |
| 家族史 | ||||
| 头痛家族史 | 6(54.5) | 4(66.7) | 7(58.3) | 10(52.6) |
| 前庭症状家族史 | 4(36.4) | 2(33.3) | 4(33.3) | 5(26.3) |
| 头痛发病年龄/岁 | 27.71±6.36 | 28.95±8.67 | 26.65±10.03 | 28.63±10.31 |
| 头痛病程/年 | 9.43±10.65 | 12.40±9.32 | 13.92±9.16 | 20.05±9.43a |
| 前庭症状发病年龄/岁 | 30.86±11.02 | 31.01±9.24 | 28.75±11.51 | 33.42±11.18 |
| 前庭症状病程/年 | 4.38±2.83 | 10.69±9.59a | 11.66±6.91a | 15.79±10.35a |
| a: P < 0.05, 与 < 8 d/月比较 | ||||
3 讨论
前庭症状和偏头痛之间的相关性在之前的研究中已经得到证实[5, 7],前期研究显示,有10%的偏头痛患者符合前庭性偏头痛的诊断标准[8]。另一项基于临床的研究发现,72%的偏头痛患者报告头晕是偏头痛发作的相关症状[9]。最近一项Meta分析中也阐述前庭症状与偏头痛的关系,但是仍然没有明确的结论[7]。
既往研究发现,在偏头痛患者中,头晕或眩晕的患病率为12%~72%[4, 9],但是均未排除前庭性偏头痛。为进一步分析前庭症状与头痛的关系,本研究中未纳入前庭性偏头痛患者,结果仍然支持偏头痛和前庭症状之间存在联系。当患者表现出头痛慢性化时,这种联系的频率更高,与前面的研究相一致[4-5]。而前庭性偏头痛的诊断标准并没有考虑偏头痛慢性化的情况[3], 并且关于这方面的研究探讨也很少,前庭症状与头痛的相关性还需要进一步探讨。
在药物临床试验中,新药治疗发作性偏头痛的头痛频率选择各有不同,有的选择头痛频率在3~8 d/月[10],有的1~6 d/月[11],也有的2~8 d/月[12],该选取哪段头痛频率组进行治疗,临床上仍没给出充分的研究证据。本研究发现,头痛频率在2~8 d/月患者约占56.3%,而这一组患者的头痛特点以及伴随症状最为典型,如果选取这组患者执行相应的药物临床试验,在观察治疗效果时会更加明显,比选取其他频率组的患者更有临床研究价值。
慢性偏头痛在全球的患病率为0.9%~5.0%,每年约有2.5%的发作性偏头痛向慢性偏头痛转换[13]。研究发现发作性偏头痛在高频(9~14 d/月)发展成慢性偏头痛的机率最大[14], 但是,当偏头痛慢性化后,是否因头痛频率的差异而出现临床特征的差异研究较少,而在本研究中,根据头痛频率分为两组,发现15~29 d/月与持续性天天痛(30 d/月)两组间的临床特征没有明显差异,这说明当偏头痛出现慢性化后,慢性和发作性不仅仅只局限于天数的差别,还反映了更深刻的病理生理差异。
本研究将前庭症状与头痛发生的时间关系分成3组,发现随着头痛频率的增加,前庭症状与头痛同时发作的频率增加;在进一步调整头痛频率分组时,找到了一个分界点(头痛频率为8 d/月),这个界值点前后前庭症状与头痛发生的时间关系有明显差异,但是头痛频率在8~29 d/月与持续性天天痛之间无明显差异,这可能与偏头痛慢性化的临界值有关。
偏头痛慢性化从1994年被提出, 到2004年国际头痛协会(IHS)分类委员会公布了包括偏头痛在内的一系列头痛疾病的诊断,至2018年,慢性偏头痛在头痛频率上一致认为是头痛≥15 d/月,偏头痛样头痛发作≥8 d/月,持续3个月[3, 15]。然而,最近的研究提出将头痛频率≥8 d/月作为慢性偏头痛的诊断标准[16],本研究也显示8 d是一个警示点,前庭症状是否与皮肤触痛一样是偏头痛慢性化的一个标志,还需要基础研究加以证实。
本研究的诊断标准是根据国际头痛分类第3版,该诊断标准对年龄没有特殊限制,此外,本研究纳入小于18岁的患者(发作性偏头痛和慢性偏头痛分别有6人和5人)均符合诊断标准,不影响研究结果。本院头痛门诊中紧张型头痛患者占比为6.6%,与2002年LIPTON团队[17]对偏头痛和紧张型头痛进行诊断分类的研究结果一致,提示基于人群研究紧张型头痛患病率较高,但基于头痛门诊研究中紧张型头痛占比显著低于偏头痛,符合紧张型头痛为轻中度头痛,患者就诊率较低的特点。
偏头痛患者常被证实有前庭功能的异常,但是对于前庭性偏头痛、脑干先兆型偏头痛、良性复发性眩晕中的前庭症状与偏头痛的机制仍然不清楚,而本研究中,除外这些疾病后的偏头痛患者群中前庭症状与偏头痛的发生机制是否又是独立的呢?既往研究认为偏头痛患者前庭症状的病因可能与三叉神经和前庭通路重叠有关[18];我们前期的动物实验发现慢性偏头痛动物模型中出现前庭损伤的行为学表现,并且前庭损伤的发展与痛觉过敏的发展趋势相一致,同时我们观察到慢性偏头痛大鼠模型前庭传入终末器官的结构得以保留[19];此外,在慢性偏头痛动物模型中三叉神经脊束核和前庭神经核部位的神经元活化,进一步研究发现慢性偏头痛模型诱导大鼠三叉神经核活化主要是三叉神经脊束核介导的前庭神经核的活化[19],这些研究提示慢性偏头痛相关前庭功能损伤可能是由于偏头痛慢性化过程中三叉神经血管系统的激活进而引起前庭神经核的活化。偏头痛神经递质在前庭神经元活动的调节中发挥作用[20],进一步敲定大鼠三叉神经节部位CGRP可以缓解前庭功能的损伤,提示抗CGRP治疗在慢性偏头痛相关前庭症状中具有重要作用[19]。基于目前研究的限制性,我们只能作此初步的探讨,还需要设计更深层次的研究探索前庭症状在偏头痛中的发生机制。
综上所述,前庭症状在偏头痛患者中很常见,特别是在慢性偏头痛患者中出现频率高,这提示前庭症状可能与偏头痛的慢性化有关。由于本研究的病例资料只来源于我科门诊,样本量有限,结果可能存在偏倚,需开展多中心、大样本量的临床研究数据证实;此外,还需在今后的研究中利用偏头痛动物模型,研究前庭症状与头痛发生关系的病理生理机制。
| [1] |
NEUHAUSER H K, RADTKE A, VON BREVERN M, et al. Migrainous vertigo: prevalence and impact on quality of life[J]. Neurology, 2006, 67(6): 1028-1033. DOI:10.1212/01.wnl.0000237539.09942.06 |
| [2] |
PYYKKÖ I, PYYKKÖ N, MANCHAIAH V. Vestibular drop attacks in Ménière's disease and its association with migraine[J]. Eur Arch Oto-Rhino-Laryngol, 2020, 277(7): 1907-1916. DOI:10.1007/s00405-020-05890-3 |
| [3] |
OLESEN J. Problem areas in the International Classification of Headache Disorders, 3rd edition (beta)[J]. Cephalalgia, 2014, 34(14): 1193-1199. DOI:10.1177/0333102414534327 |
| [4] |
CALHOUN A H, FORD S, PRUITT A P, et al. The point prevalence of dizziness or Vertigo in migraine: and factors that influence presentation[J]. Headache, 2011, 51(9): 1388-1392. DOI:10.1111/j.1526-4610.2011.01970.x |
| [5] |
CARVALHO G F, VIANNA-BELL F H, FLORENCIO L L, et al. Presence of vestibular symptoms and related disability in migraine with and without aura and chronic migraine[J]. Cephalalgia, 2019, 39(1): 29-37. DOI:10.1177/0333102418769948 |
| [6] |
ZHANG Y X, KONG Q T, CHEN J J, et al. International Classification of Headache Disorders 3rd edition beta-based field testing of vestibular migraine in China: Demographic, clinical characteristics, audiometric findings and diagnosis statues[J]. Cephalalgia, 2016, 36(3): 240-248. DOI:10.1177/0333102415587704 |
| [7] |
ILJAZI A, ASHINA H, LIPTON R B, et al. Dizziness and Vertigo during the prodromal phase and headache phase of migraine: a systematic review and meta-analysis[J]. Cephalalgia, 2020, 40(10): 1095-1103. DOI:10.1177/0333102420921855 |
| [8] |
CHO S J, KIM B K, KIM B S, et al. Vestibular migraine in multicenter neurology clinics according to the appendix criteria in the third beta edition of the International Classification of Headache Disorders[J]. Cephalalgia, 2016, 36(5): 454-462. DOI:10.1177/0333102415597890 |
| [9] |
KELMAN L, TANIS D. The relationship between migraine pain and other associated symptoms[J]. Cephalalgia, 2006, 26(5): 548-553. DOI:10.1111/j.1468-2982.2006.01075.x |
| [10] |
KNIEVEL K, BUCHANAN A S, LOMBARD L, et al. Lasmiditan for the acute treatment of migraine: Subgroup analyses by prior response to triptans[J]. Cephalalgia, 2020, 40(1): 19-27. DOI:10.1177/0333102419889350 |
| [11] |
SARACCO M G, ALLAIS G, TULLO V, et al. Efficacy of frovatriptan and other triptans in the treatment of acute migraine of normal weight and obese subjects: a review of randomized studies[J]. Neurol Sci, 2014, 35(1): 115-119. DOI:10.1007/s10072-014-1752-2 |
| [12] |
TEPPER S J, DODICK D W, SCHMIDT P C, et al. Efficacy of ADAM zolmitriptan for the acute treatment of difficult-to-treat migraine headaches[J]. Headache, 2019, 59(4): 509-517. DOI:10.1111/head.13482 |
| [13] |
NATOLI J L, MANACK A, DEAN B, et al. Global prevalence of chronic migraine: a systematic review[J]. Cephalalgia, 2010, 30(5): 599-609. DOI:10.1111/j.1468-2982.2009.01941.x |
| [14] |
BIGAL M E, SERRANO D, BUSE D, et al. Acute migraine medications and evolution from episodic to chronic migraine: a longitudinal population-based study[J]. Headache, 2008, 48(8): 1157-1168. DOI:10.1111/j.1526-4610.2008.01217.x |
| [15] |
Headache Classification Committee of the International Headache Society. The International Classification of Headache Disorders, 3rd edition (beta version)[J]. Cephalalgia, 2013, 33(9): 629-808. DOI:10.1177/0333102413485658 |
| [16] |
CHALMER M A, HANSEN T F, LEBEDEVA E R, et al. Proposed new diagnostic criteria for chronic migraine[J]. Cephalalgia, 2020, 40(4): 399-406. DOI:10.1177/0333102419877171 |
| [17] |
LIPTON R B, CADY R K, STEWART W F, et al. Diagnostic lessons from the spectrum study[J]. Neurology, 2002, 58(9 suppl 6): S27-S31. DOI:10.1212/wnl.58.9_suppl_6.s27 |
| [18] |
FURMAN J M, MARCUS D A, BALABAN C D. Vestibular migraine: clinical aspects and pathophysiology[J]. Lancet Neurol, 2013, 12(7): 706-715. DOI:10.1016/s1474-4422(13)70107-8 |
| [19] |
ZHANG Y, ZHANG Y X, TIAN K, et al. Calcitonin gene-related peptide facilitates sensitization of the vestibular nucleus in a rat model of chronic migraine[J]. J Headache Pain, 2020, 21(1): 1-15. DOI:10.1186/s10194-020-01145-y |
| [20] |
LEMPERT T, NEUHAUSER H. Migrainous Vertigo[J]. Neurol Clin, 2005, 23(3): 715-730. DOI:10.1016/j.ncl.2005.01.003 |




