2. 510280 广州,南方医科大学第二临床医学院
2. Second School of Clinical Medicine, Southern Medical University, Guangzhou, Guangdong Province, 510280, China
随着人口老龄化与生活方式的变化,糖尿病患病人数显著增加,中国糖尿病患病率也从1980年的0.67% 迅速增加到2013年的10.4%[1]。糖尿病肾脏疾病(diabetic kidney disease,DKD)是糖尿病最主要的微血管并发症之一,是目前引起终末期肾病的首要原因,给患者、家庭及社会带来沉重的经济负担[2]。国外报道2型糖尿病患者中DKD的患病率为20%~40%[3]。本研究旨在通过现况调查,探究重庆市2型糖尿病患者并发DKD的现状,比较城乡社区DKD患病情况,并对DKD的危险因素进行分析,为城乡社区制订针对性的DKD防治策略和干预措施提供参考。
1 资料与方法 1.1 研究对象来源于“2型糖尿病多种危险因素多中心临床干预与评价”课题[4]的基线调查研究。2019年3-7月,采用分层整群随机抽样的方法,将重庆市主城9区的社区分成城市社区和农村社区两层,随机抽取7个城市社区和5个农村社区,然后在每个社区卫生服务机构随机抽取数量相同的符合纳入排除标准的2型糖尿病患者。纳入标准:①年龄35~75岁;②符合1999年WHO糖尿病诊断标准[5];③在社区卫生服务机构进行基本公共卫生服务常规管理的2型糖尿病患者。排除标准:①1型糖尿病、特殊类型糖尿病、妊娠糖尿病和糖尿病合并妊娠,继发性糖尿病患者;②存在感染、严重的急慢性疾病等;③其他原因导致的蛋白尿,如急慢性肾炎、过敏性紫癜性肾炎、狼疮性肾炎等,或出现活动性尿沉渣(红细胞、白细胞、细胞管型等);④急性心梗、脑梗发作并住院或急性心衰发作并住院治疗3个月内;⑤恶性肿瘤等。
本研究分析的是DKD患病率,样本量估计采用抽样公式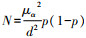
由经过课题组专业培训合格的医护人员完成本次研究,研究内容主要包括问卷调查、体格检测和实验室检查。
1.2.1 问卷调查以面对面询问的方式,收集患者性别、年龄、文化程度、月收入、病程、吸烟史和用药史等人口学信息。
1.2.2 体格检测采用标准仪器设备现场测量获取患者身高、体质量、腰围、臀围、血压等信息;每个检测项目由2名调查员完成,1名负责测量,另1名协助测量并记录;体格检测前休息10 min,血压检测时取坐位,排空膀胱,统一使用水银血压计测量左上臂;所有检测项目测量2次取平均值。
1.2.3 实验室检查空腹10 h,于右臂肘正中静脉抽取静脉血液4管,共14 mL,分别检测空腹血糖(FBG)、糖化血红蛋白(HbA1c)、总胆固醇(TC)、甘油三酯(TG)、低密度脂蛋白(LDL)、高密度脂蛋白(HDL)、尿酸(UA)、空腹C肽(C-P)、胰岛素(INS)等指标,留取中段晨尿液5 mL检测尿肌酐(UCr)、尿白蛋白(Alb),并计算尿白蛋白/尿肌酐比值(UACR)。1、3个月后分别再次复查UCr、Alb。
1.3 诊断标准 1.3.1 糖尿病诊断标准采用1999年WHO糖尿病诊断标准[5],即典型糖尿病症状(多饮、多尿、多食、体质量下降);加上随机血糖水平≥11.1 mmol/L;或FBG水平≥7.0 mmol/L;或葡萄糖负荷后2 h血糖≥11.1 mmol/L。其中,随机血糖指不考虑上次用餐时间,1 d中任意时间的血糖;空腹状态要求至少8 h没有进食热量。
1.3.2 糖尿病肾脏疾病根据《中国糖尿病肾脏疾病防治临床指南》[8]标准,以尿白蛋白/尿肌酐比值(urinary albumin/creatinine ratio,UACR)高于30 mg/g持续超过3个月作为诊断标准。
1.4 糖尿病综合控制目标的相关指标定义根据《中国2型糖尿病防治指南(2017年版)》[5]标准,FBG控制达标是指FBG≤7.0 mmol/L;HbA1c控制达标是指HbA1c < 7.0%;成年人血压控制达标是指 < 130/80 mmHg,老年人血压控制目标放宽至 < 150/90 mmHg;TC控制达标是指TC < 4.5 mmol/L;TG控制达标是指TG < 1.7 mmol/L;HDL控制达标是指男性HDL > 1.0 mmol/L, 女性HDL>1.3 mmol/L;LDL控制达标是指未合并动脉粥样硬化性心血管疾病时LDL < 2.6 mmol/L,合并动脉粥样硬化性心血管疾病时LDL < 1.8 mmol/L。
1.5 质量控制本次调查研究的人员由陆军军医大学第一附属医院内分泌科临床医师、各社区医院临床医师及护士组成,调查前中国疾控中心课题组相关专家对所有参与人员进行统一培训,统一诊断标准及数据记录形式,问卷调查通过统一设计的结构化问卷进行调查,相关血尿样本通过冷链运输方式送至济南金域医学检验有限公司实验室集中检测。
1.6 统计学分析采用SPSS 20.0统计软件进行数据处理,符合正态分布的计量资料以x±s表示,两组间比较采用独立样本t检验,非正态分布的计量资料以M(P25, P75)表示,两组间比较采用秩和检验, 计数资料以例数(%)表示,采用χ2检验或Fisher确切概率法比较,DKD的危险因素采用非条件多因素Logistic回归分析,自变量入选采用前进法。
2 结果 2.1 调查结果本研究共调查重庆市主城区2型糖尿病患者792例,其中57例因资料不完整而被剔除,最终入组735例,有效调查率92.8%。5个农村社区入组301例,7个城市社区共入组434例。各年龄组(35~44岁、45~54岁、55~64岁和65~75岁)占比分别为3.0%、15.2%、36.9%和44.9%(表 1)。
| 项目 | 总体(n=735) | 农村(n=301) | 城市(n=434) | P值 |
| 男性 | 331(45.0) | 134(44.5) | 196(45.2) | 0.934 |
| 年龄/岁 | 62.1±8.2 | 61.4±8.5 | 62.6±7.9 | 0.042 |
| 35~44 | 22(3.0) | 10(3.3) | 12(2.8) | |
| 45~54 | 112(15.2) | 59(19.6) | 53(12.2) | |
| 55~64 | 271(36.9) | 109(36.2) | 162(37.3) | |
| 65~75 | 330(44.9) | 123(40.9) | 207(47.7) | |
| 文化程度 | < 0.001 | |||
| 小学及以下 | 263(35.8) | 168(55.8) | 95(21.9) | |
| 初中 | 282(38.4) | 99(32.9) | 183(42.2) | |
| 高中及中职 | 130(17.7) | 29(9.6) | 101(23.3) | |
| 大学及以上 | 60(8.2) | 5(1.7) | 55(12.7) | |
| 吸烟 | 145(19.7) | 67(22.3) | 78(18.0) | 0.151 |
| 月收入/元 | 2 000(900, 3 000) | 1 000(200, 2 000) | 3 000(2 000, 4 000) | < 0.001 |
| SBP/mmHg | 136.7±19.8 | 141.0±21.8 | 133.8±17.7 | < 0.001 |
| DBP/mmHg | 82.0±11.6 | 85.8±12.5 | 79.5±10.2 | < 0.001 |
| 身高/m | 1.59±0.09 | 1.58±0.09 | 1.59±0.09 | 0.134 |
| 体质量/kg | 63.2±11.0 | 62.4±11.0 | 63.8±10.9 | 0.084 |
| BMI/kg·m-2 | 25.1±3.8 | 25.0±3.9 | 25.2±3.7 | 0.368 |
| 腰围/cm | 88.4±9.3 | 89.0±8.5 | 88.0±9.8 | 0.050 |
| 臀围/cm | 95.4±8.0 | 95.1±6.7 | 95.6±8.7 | 0.158 |
| 腰臀比(WHR) | 0.93±0.09 | 0.94±0.06 | 0.92±0.10 | < 0.001 |
| 服用ACEI或ARB类药物 | 87(11.8) | 32(10.6) | 55(12.7) | 0.269 |
| 病程/年 | 8.2±6.5 | 6.6±5.7 | 9.3±6.8 | < 0.001 |
| FBG/mmol·L-1 | 8.7±3.3 | 9.4±3.7 | 8.2±2.9 | < 0.001 |
| HbA1c(%) | 7.9±1.8 | 8.2±1.9 | 7.7±1.7 | < 0.001 |
| C-P/ng·mL-1 | 2.2±1.0 | 2.2±1.1 | 2.1±0.9 | 0.231 |
| INS/ng·mL-1 | 6.8(4.4,11.1) | 6.2(3.8,9.4) | 7.6(4.9,11.9) | < 0.001 |
| Alb/mg·L-1 | 19.9(7.6,47.1) | 24.2(9.0,56.2) | 17.9(6.6,44.3) | 0.009 |
| UCr/μmol·L-1 | 11 302.1(7 683.5,15 881.0) | 10 545.9(7 259.0,15 396.6) | 12 077.3(8 029.5,16 202.4) | 0.010 |
| UACR/mg·g-1 | 14.9(6.0,39.2) | 20.0(9.0,46.1) | 12.8(4.9,33.6) | < 0.001 |
| TG/mmol·L-1 | 1.5(1.1,2.3) | 1.7(1.2,2.7) | 1.5(1.1,2.2) | 0.001 |
| TC/mmol·L-1 | 5.2±1.3 | 5.4±1.4 | 5.1±1.1 | 0.006 |
| HDL/mmol·L-1 | 1.6±0.6 | 1.6±0.5 | 1.5±0.6 | 0.030 |
| LDL/mmol·L-1 | 2.6±0.8 | 2.6±0.7 | 2.6±0.8 | 0.870 |
| UA/μmol·L-1 | 330.4±93.4 | 314.7±94.8 | 341.2±90.9 | < 0.001 |
2.2 城乡社区2型糖尿病患者人口学特征及体格检测比较
农村社区和城市社区2型糖尿病患者男女比例无统计学差异(表 1)。年龄方面,城市社区糖尿病患者年龄显著大于农村社区(P < 0.05)。文化程度方面,农村社区和城市社区存在明显差异(P < 0.001), 其中农村社区以小学及以下学历为主(55.8%),大学及以上学历仅占1.7%,城市社区以初中学历为主(42.2%),大学及以上学历占12.7%。家庭月收入方面,城市社区月收入显著高于农村社区(P < 0.001)。血压方面,农村社区的收缩压(SBP)和舒张压(DBP)均显著高于城市社区(P < 0.001)。病程方面,农村社区显著低于城市社区(P < 0.001)。农村社区腰臀比(WHR)显著高于城市社区(P < 0.001)。在吸烟、身高、体质量、BMI、腰围、臀围、ACEI或ARB类药物服药史等方面农村社区和城市社区均未见明显差异。
2.3 城乡社区2型糖尿病患者代谢指标比较农村社区和城市社区2型糖尿病患者在多项代谢指标方面均存在统计学差异(表 1),其中在FBG、HbA1c、Alb、UACR、TG、TC和HDL等指标方面农村社区显著高于城市社区(P < 0.05),INS、UCr和UA等指标农村社区显著低于城市社区(P < 0.05),而C-P和LDL等指标未见统计学差异。
2.4 糖尿病综合控制目标达标情况分析重庆市主城区2型糖尿病患者血糖控制较差,血脂控制水平差异性较大(表 2)。以性别亚组分析发现,男性的TC和HDL控制达标率均显著高于女性(P < 0.001),其余均未见明显性别差异。以区域亚组分析发现,农村社区在FBG、HbA1c、血压和TG控制达标率方面均显著低于城市社区(P < 0.05),其余未见明显区域差异,提示农村社区糖尿病综合控制情况明显差于城市社区。
| 指标 | 总达标数 | 性别 | 区域 | |||||
| 男性 | 女性 | P值 | 农村 | 城市 | P值 | |||
| FBG | 260(35.4) | 115(34.8) | 145(35.8) | 0.788 | 84(27.9) | 176(40.6) | < 0.001 | |
| HbA1c | 289(39.3) | 126(38.2) | 163(40.2) | 0.569 | 97(32.2) | 192(44.2) | 0.001 | |
| 血压 | 372(50.6) | 168(50.9) | 204(50.4) | 0.884 | 112(37.2) | 260(59.9) | < 0.001 | |
| TC | 207(28.2) | 116(35.2) | 91(22.5) | < 0.001 | 74(24.6) | 133(30.6) | 0.072 | |
| TG | 415(56.5) | 197(59.7) | 218(53.8) | 0.110 | 148(49.2) | 267(61.5) | 0.001 | |
| HDL | 641(87.2) | 306(92.7) | 335(82.7) | < 0.001 | 270(89.7) | 371(85.5) | 0.092 | |
| LDL | 395(53.7) | 185(56.1) | 210(51.9) | 0.255 | 161(53.5) | 234(53.9) | 0.909 | |
| BMI | 285(38.8) | 126(38.2) | 159(39.3) | 0.735 | 116(38.5) | 169(38.9) | 0.912 | |
2.5 城乡社区DKD患病率比较
重庆市主城区农村社区2型糖尿病患者的DKD患病率显著高于城市社区(P < 0.001,表 3)。≥65岁年龄组患病率远高于 < 65岁年龄组(P < 0.01)。在农村社区和城市社区中,≥65岁年龄组患病率均显著高于 < 65岁年龄组(P < 0.05)。DKD患病率未见性别差异。
| 项目 | DM | DKD | 农村 | 城市 | P值 | |||
| DM | DKD | DM | DKD | |||||
| 总体 | 735 | 230(31.3) | 301 | 108(35.9) | 434 | 122(28.1) | 0.003 | |
| 性别 | ||||||||
| 男性 | 330 | 101(30.6) | 134 | 49(36.6) | 196 | 52(26.5) | 0.052 | |
| 女性 | 405 | 129(31.9) | 167 | 59(35.3) | 238 | 70(29.4) | 0.208 | |
| P值 | 0.717 | 0.824 | 0.506 | |||||
| 年龄 | ||||||||
| < 65岁 | 405 | 107(26.4) | 178 | 55(30.9) | 227 | 52(22.9) | 0.070 | |
| ≥65岁 | 330 | 123(37.3) | 123 | 53(43.1) | 207 | 70(33.8) | 0.092 | |
| P值 | 0.002 | 0.030 | 0.012 | |||||
| DM: 糖尿病 | ||||||||
2.6 DKD影响因素的Logistic回归分析
采用非条件多因素Logistic回归分析,将调查区域、性别、年龄、文化程度、吸烟、月收入、SBP、DBP、BMI、WHR、服用ACEI或ARB类药物、病程、FBG、HbA1c、C-P、INS、TG、TC、HDL、LDL及UA作为自变量,将DKD作为因变量,采用前进法进行分析,纳入标准为0.05,排除标准为0.10。先对所有患者进行Logistic回归分析,而后分别对农村社区患者和城市社区患者进行Logistic回归分析,比较危险因素的差异。赋值见表 4。
| 变量 | 赋值 | |||
| 0 | 1 | 2 | 3 | |
| 调查区域 | 城市 | 农村 | ||
| 性别 | 女 | 男 | ||
| 年龄/岁 | < 65 | ≥65 | ||
| 文化程度 | 小学及以下 | 初中 | 高中或中职 | 大学及以上 |
| 吸烟 | 否 | 是 | ||
| 月收入/元 | < 2 000 | < 3 000 | < 4 000 | ≥4 000 |
| SBP/mmHg | < 140 | ≥140 | ||
| DBP/mmHg | < 90 | ≥90 | ||
| BMI/kg·m-2 | < 18.5 | < 24 | < 28 | ≥28 |
| WHR | ||||
| 男 | < 0.9 | ≥0.9 | ||
| 女 | < 0.8 | ≥0.8 | ||
| 服用ACEI或ARB类药物 | 否 | 是 | ||
| 病程/年 | < 10 | ≥10 | ||
| FBG/mmol·L-1 | ≤7.0 | >7.0 | ||
| HbA1c(%) | < 7.0 | ≥7.0 | ||
| C-P/ng·mL-1 | < 4.4 | ≥4.4 | ||
| INS/ng·mL-1 | < 24.9 | ≥24.9 | ||
| TG/mmol·L-1 | < 1.7 | ≥1.7 | ||
| TC/mmol·L-1 | < 4.5 | ≥4.5 | ||
| HDL/mmol·L-1 | ||||
| 男 | >1 | ≤1 | ||
| 女 | >1.3 | ≤1.3 | ||
| LDL/mmol·L-1 | < 2.6 | ≥2.6 | ||
| UA/μmol·L-1 | ||||
| 男 | < 428 | ≥428 | ||
| 女 | < 357 | ≥357 | ||
| DKD | 否 | 是 | ||
结果显示,年龄(OR=1.715,95%CI:1.213~2.425)、SBP(OR=2.360,95%CI:1.668~3.339)、病程(OR=1.664,95%CI:1.156~2.397)、HbA1c(OR= 2.343,95%CI:1.615~3.400)、TG(OR=1.738,95%CI:1.226~2.463)、TC(OR=1.521,95%CI:1.027~2.254)和UA(OR=1.988,95%CI:1.354~2.921)是DKD的独立危险因素(表 5),服用ACEI或ARB类药物(OR=0.356,95%CI:0.199~0.638)是保护因素。按照区域进行亚组分析,结果显示SBP(OR=2.393,95%CI:1.429~4.006)、病程(OR=2.471,95%CI:1.294~4.719)和TG(OR=1.988,95%CI:1.198~3.300)是农村社区DKD的独立危险因素,服用ACEI或ARB类药物(OR=0.163,95%CI:0.057~0.464)是其保护因素;城市社区的危险因素包括年龄(OR=1.682,95%CI:1.062~2.664)、SBP(OR=2.201,95%CI:1.393~3.478)、病程(OR=1.644,95%CI:1.038~2.602)、HbA1c(OR=2.844,95%CI:1.746~4.632)和UA(OR=2.182,95%CI:1.338~3.558)。
| 变量 | β | S.E | Wals检验 | P值 | OR值 | 95%CI | |
| 下限 | 上限 | ||||||
| 总体 | |||||||
| 年龄 | 0.540 | 0.177 | 9.325 | 0.002 | 1.715 | 1.213 | 2.425 |
| SBP | 0.859 | 0.177 | 23.530 | 0.000 | 2.360 | 1.668 | 3.339 |
| 服用ACEI或ARB类药物 | -1.032 | 0.298 | 12.026 | 0.001 | 0.356 | 0.199 | 0.638 |
| 病程 | 0.510 | 0.186 | 7.490 | 0.006 | 1.664 | 1.156 | 2.397 |
| HbA1c | 0.852 | 0.190 | 20.121 | 0.000 | 2.343 | 1.615 | 3.400 |
| TG | 0.553 | 0.178 | 9.649 | 0.002 | 1.738 | 1.226 | 2.463 |
| TC | 0.420 | 0.201 | 4.373 | 0.037 | 1.521 | 1.027 | 2.254 |
| UA | 0.687 | 0.196 | 12.272 | 0.000 | 1.988 | 1.354 | 2.921 |
| 农村 | |||||||
| SBP | 0.872 | 0.263 | 11.015 | 0.001 | 2.393 | 1.429 | 4.006 |
| 服用ACEI或ARB类药物 | -1.815 | 0.535 | 11.524 | 0.001 | 0.163 | 0.057 | 0.464 |
| 病程 | 0.905 | 0.330 | 7.509 | 0.006 | 2.471 | 1.294 | 4.719 |
| TG | 0.687 | 0.259 | 7.062 | 0.008 | 1.988 | 1.198 | 3.300 |
| 城市 | |||||||
| 年龄 | 0.520 | 0.235 | 4.918 | 0.027 | 1.682 | 1.062 | 2.664 |
| SBP | 0.789 | 0.233 | 11.417 | 0.001 | 2.201 | 1.393 | 3.478 |
| 病程 | 0.497 | 0.234 | 4.497 | 0.034 | 1.644 | 1.038 | 2.602 |
| HbA1c | 1.045 | 0.249 | 17.627 | 0.000 | 2.844 | 1.746 | 4.632 |
| UA | 0.780 | 0.250 | 9.775 | 0.002 | 2.182 | 1.338 | 3.558 |
3 讨论
DKD是糖尿病主要的并发症之一,是引起终末期肾病的首要原因。目前多数研究以城市患者为对象,研究结果不能代表广大农村或郊区患者情况。本研究对重庆市主城区城乡2型糖尿病患者DKD患病率及危险因素进行比较研究。
本研究发现重庆市主城区DKD患病率为31.3%,高于全国平均患病率(21.8%),但低于西部地区平均患病率(41.3%)[9],也低于国内一些城市[10-11]。按性别分组分析显示,DKD患病率未见明显性别差异。按年龄分组分析显示,≥65岁年龄组DKD患病率均显著高于 < 65岁年龄组,提示老年糖尿病群体是DKD发病高危人群,应重点关注并及时做好疾病筛查和健康教育。DUAN等[6-7]研究发现农村社区糖尿病患者中DKD患病率(35.5%)显著高于城市社区(23.0%),本研究进一步证实了这种城乡差异,其中重庆主城区农村社区DKD患病率为35.9%,与DUAN等[6]研究一致,但高于上海郊区(27.9%)[12]。重庆主城区城市社区DKD患病率28.1%,高于郑州城市社区(23.0%)[7],也高于其他城市[13-14]。
城乡社区在多项指标方面均存在统计学差异,其中农村社区在年龄、文化程度、月收入等人口学指标,UCr、UA等代谢指标和FBG、HbA1c、血压、TG等达标率方面显著低于城市社区,而在SBP、DBP、WHR等体格检测指标和FBG、HbA1c、Alb、TG、TC、HDL等代谢指标方面均显著高于城市社区,说明相比于城市社区,农村社区2型糖尿病患者受教育程度低、经济情况差、代谢指标异常、糖尿病综合控制水平欠佳,这些可能是导致农村社区DKD患病率显著高于城市社区的主要原因。
与众多研究[7, 10-12, 15]类似,多因素Logistic回归分析显示:年龄、SBP、病程、HbA1c、TG、TC、UA都是2型糖尿病患者DKD患病的独立危险因素,服用ACEI或ARB类药物是保护性因素。对比农村社区和城市社区的危险因素发现,SBP和病程是城乡共同且重要的危险因素,说明严格的血压控制、重视长病程糖尿病患者DKD的筛查和健康管理,对于农村社区和城市社区预防DKD都具有重要的临床意义。本研究发现农村社区糖尿病病程显著少于城市社区,但DKD患病率却显著高于城市社区, 这是因为病程对农村社区的影响(OR=2.471)大于对城市社区的影响(OR=1.644),同时城乡DKD患病率的不同是年龄、病程、血压、HbA1c等多种危险因素共同作用的结果,城市社区在多项人口学特征、体格检测和代谢指标等方面均显著优于农村社区。除SBP和病程之外,农村社区更应重点控制高甘油三酯等高脂血症,而城市社区则更应强化HbA1c等指标的血糖控制,重视老龄患者等高危人群DKD的筛查和健康管理,注意纠正高尿酸血症。根据对所有患者的Logistic回归分析,结果显示:服用ACEI/ARB类药物是DKD的保护性因素(OR=0.356,95%CI:0.199~0.638),提示重庆地区患者应适时加强ACEI/ARB类药物的使用。虽然在分别对城乡患者进行Logistic回归分析后发现,服用ACEI/ARB类药物是农村社区DKD的保护性因素(OR=0.163,95%CI:0.057~0.464),而非城市社区的保护性因素,但考虑到城乡之间ACEI/ARB的使用无明显差异,因此不足以说明农村地区居民更应加强ACEI/ARB类药物使用而城市社区不用。
中国老龄人口数量不断增加,到2022年左右中国将进入老龄社会。本研究发现老龄(≥65岁)和长病程(>10年)都将增加糖尿病患者DKD的患病危险(OR=1.715,OR=1.664),提示必须重视老龄人群和长病程人群的DKD筛查和健康管理。2型糖尿病患者容易并发高血压[16],并使肾病的发生和进展风险明显增加,而严格的血压控制可以降低DKD发生的风险[17]。本研究显示SBP是DKD患病的危险因素,因此严格控制血压对于延缓2型糖尿病患者的肾损害具有重要的临床意义。多项临床研究表明,肾素-血管紧张素-醛固酮系统(RAAS)抑制剂(ACEI或ARB)在DKD的进展中扮演着重要的作用,RAAS抑制剂能显著降低糖尿病患者的尿蛋白和血压[18],并且降尿蛋白作用独立于降压作用[19],同时可降低糖尿病患者尿蛋白升高的风险[20-21],以及终末期肾脏疾病发展和全因死亡的风险[22]。本研究也进一步证实服用ACEI或ARB类药物是DKD的保护因素(OR=0.356)。据英国糖尿病前瞻性研究(UKPDS)表明严格控制血糖能够延缓蛋白尿的发生,减少DKD的发生和延缓其进展[23],而长期高血糖将导致系统性的微血管损伤[24]。本研究也显示HbA1c是DKD患病的重要危险因素(OR=2.343)。但本研究中FBG未被纳入危险因素,可能原因是FBG代表及时的血糖情况且波动较大,难以正确反映患者的血糖控制情况,而HbA1c代表患者2~3个月血糖波动的情况,因此在DKD的防治工作中应重点关注HbA1c控制水平。研究显示TG始终作为蛋白尿的独立决定因素出现[25],TG和TC异常与eGFR降低和发生ESRD风险均显著相关[26-27],而降血脂药物可以延缓2型糖尿病患者微量蛋白尿的进展[28]。本研究结果也显示TG和TC是DKD的独立危险因素(OR=1.738),为防止DKD的发生发展仍需严格控制血脂。UA可通过激活RASS诱导血管内皮细胞功能失调和氧化应激进而导致肾脏损伤[29],临床研究表明血清UA浓度的增加与新发蛋白尿和eGFR降低密切相关[30]。本研究也证实UA将会导致2型糖尿病患者DKD患病风险的增加(OR=1.988)。
本研究存在一些局限性。首先,本研究对DKD的诊断依据尿微量白蛋白与尿肌酐比值,未考虑eGFR等指标,可能低估了肾脏疾病的患病率,对危险因素分析也可能产生影响[15];其次,虽然根据患病率调查的样本量估计,本研究样本量满足要求,但相较于重庆市人口仍然比较少,这可能对结果产生影响;再则,本研究为横断面研究,无法确切推论相关危险因素与DKD的因果关系;最后,本研究没有纳入饮食、运动、民族等混杂因素,而相关因素可能会对DKD产生影响。后期我们将进一步扩大样本量,开展前瞻性研究进一步论证相关危险因素的影响。
综上所述,重庆主城区社区2型糖尿病患者的DKD患病率偏高,年龄、血压、病程、HbA1c、TG、TC、UA等因素可能会增加2型糖尿病患者并发DKD的风险, 服用ACEI或ARB类药物会降低该风险。城乡在患病率及危险因素方面均有差异,提示我们应该在2型糖尿病患者中进行DKD的疾病筛查和早期干预,并针对城乡差异分别指定防治措施。
| [1] |
JIA W, WENG J, ZHU D, et al. Standards of medical care for type 2 diabetes in China 2019[J]. Diabetes Metab Res Rev, 2019, 35(6): e3158. DOI:10.1002/dmrr.3158 |
| [2] |
KDOQI. Clinical practice guidelines and clinical practice recommendations for diabetes and chronic kidney disease[J]. Am J Kidney Dis, 2007, 49(2 Suppl 2): S12-S154. DOI:10.1053/j.ajkd.2006.12.005 |
| [3] |
GHEITH O, FAROUK N, NAMPOORY N, et al. Diabetic kidney disease: world wide difference of prevalence and risk factors[J]. J Nephropharmacol, 2016, 5(1): 49-56. |
| [4] |
WANG Q, ZHANG X, FANG L, et al. Prevalence, awareness, treatment and control of diabetes mellitus among middle-aged and elderly people in a rural Chinese population: A cross-sectional study[J]. PLoS ONE, 2018, 13(6): e198343. DOI:10.1371/journal.pone.0198343 |
| [5] |
中华医学会糖尿病学分会. 中国2型糖尿病防治指南(2017年版)[J]. 中国实用内科杂志, 2018, 38(4): 292-344. Diabetes Mellitus Branch of Chinese Medical Association. Guidelines for the prevention and control of type 2 diabetes in China (2017 Edition)[J]. Chin J Pract Intern Med, 2018, 38(4): 292-344. DOI:10.19538/j.nk2018040108 |
| [6] |
DUAN J Y, WANG C J, LIU D W, et al. Prevalence and risk factors of chronic kidney disease and diabetic kidney disease in Chinese rural residents: a cross-sectional survey[J]. Sci Rep, 2019, 9(1): 10408. DOI:10.1038/s41598-019-46857-7 |
| [7] |
DUAN J Y, DUAN G C, WANG C J, et al. Prevalence and risk factors of chronic kidney disease and diabetic kidney disease in a central Chinese urban population: a cross-sectional survey[J]. BMC Nephrol, 2020, 21(1): 115. DOI:10.1186/s12882-020-01761-5 |
| [8] |
中华医学会糖尿病学分会微血管并发症学组. 中国糖尿病肾脏疾病防治临床指南[J]. 中华糖尿病杂志, 2019, 11(1): 15-28. Microvascular Complications Group of Diabetes Mellitus Branch of Chinese Medical Association. Chinese clinical practice guideline of diabetic kidney disease[J]. Chin J Diabetes Mellit, 2019, 11(1): 15-28. DOI:10.3760/cma.j.issn.1674-5809.2019.01.004 |
| [9] |
ZHANG X X, KONG J, YUN K. Prevalence of diabetic nephropathy among patients with type 2 diabetes mellitus in China: a meta-analysis of observational studies[J]. J Diabetes Res, 2020, 2020: 2315607. DOI:10.1155/2020/2315607 |
| [10] |
LOU J Q, JING L M, YANG H, et al. Risk factors for diabetic nephropathy complications in community patients with type 2 diabetes mellitus in Shanghai: Logistic regression and classification tree model analysis[J]. Int J Health Plann Manage, 2019, 34(3): 1013-1024. DOI:10.1002/hpm.2871 |
| [11] |
李小勇, 沈鹏, 林鸿波, 等. 宁波社区2型糖尿病患者发生糖尿病肾病危险因素调查[J]. 浙江大学学报(医学版), 2018, 47(2): 163-168. LI X Y, SHEN P, LIN H B, et al. A community-based survey on risk factors of type 2 diabetic kidney disease in Ningbo, China[J]. J Zhejiang Univ(Med Sci), 2018, 47(2): 163-168. DOI:10.3785/j.issn.1008-9292.2018.04.09 |
| [12] |
许嵘, 钟一红, 陈波, 等. 上海市郊区2型糖尿病患者肾脏疾病及其危险因素研究[J]. 中华内科杂志, 2012, 51(1): 18-23. XU R, ZHONG Y H, CHEN B, et al. The prevalence and risk factors of kidney disease in type 2 diabetic patients in rural Shanghai[J]. Chin J Intern Med, 2012, 51(1): 18-23. DOI:10.3760/cma.j.issn.0578-1426.2012.01.005 |
| [13] |
柯箫韵, 翟海龙, 黄飞. 黄石社区2型糖尿病肾病患病率调查及其相关因素研究[J]. 中国全科医学, 2013, 16(12): 1373-1375. KE X Y, ZHAI H L, HUANG F. A epidemiological survey on the incidence of type 2 diabetic nephropathy and its related risk factors in Huangshi community[J]. Chin Gen Pract, 2013, 16(12): 1373-1375. DOI:10.3969/j.issn.1007-9572.2013.04.091 |
| [14] |
邢桂红, 屈丹, 周红, 等. 2型糖尿病患者糖尿病肾病患病率及其相关因素分析[J]. 中国慢性病预防与控制, 2009, 17(6): 599-600, 603. XING G H, QU D, ZHOU H, et al. The prevalence of diabetic nephropathy and its associated factors in type 2 diabetes patients living in the center area of Benxi City during 2008-2009[J]. Chin J Prev Control Chronic Non-Commun Dis, 2009, 17(6): 599-600, 603. |
| [15] |
RETNAKARAN R, CULL C A, THORNE K I, et al. Risk factors for renal dysfunction in type 2 diabetes: U.K. Prospective Diabetes Study 74[J]. Diabetes, 2006, 55(6): 1832-1839. DOI:10.2337/db05-1620 |
| [16] |
WU A Y, TAN C B, ENG P H, et al. Microalbuminuria prevalence study in hypertensive patients with type 2 diabetes mellitus in Singapore[J]. Singapore Med J, 2006, 47(4): 315-320. |
| [17] |
RADCLIFFE N J, SEAH J M, CLARKE M, et al. Clinical predictive factors in diabetic kidney disease progression[J]. J Diabetes Investig, 2017, 8(1): 6-18. DOI:10.1111/jdi.12533 |
| [18] |
PARVING H H, LEHNERT H, BROCHNER-MORTENSEN J, et al. The effect of irbesartan on the development of diabetic nephropathy in patients with type 2 diabetes[J]. N Engl J Med, 2001, 345(12): 870-878. DOI:10.1056/NEJMoa011489 |
| [19] |
RUGGENENTI P, PERNA A, GANEVA M, et al. Impact of blood pressure control and angiotensin-converting enzyme inhibitor therapy on new-onset microalbuminuria in type 2 diabetes: a post hoc analysis of the BENEDICT trial[J]. J Am Soc Nephrol, 2006, 17(12): 3472-3481. DOI:10.1681/ASN.2006060560 |
| [20] |
PATEL A, ADVANCE COLLABORATIVE GROUP, MACMAHON S, et al. Effects of a fixed combination of perindopril and indapamide on macrovascular and microvascular outcomes in patients with type 2 diabetes mellitus (the ADVANCE trial): a randomised controlled trial[J]. Lancet, 2007, 370(9590): 829-840. DOI:10.1016/S0140-6736(07)61303-8 |
| [21] |
HALLER H, ITO S, IZZO J L, et al. Olmesartan for the delay or prevention of microalbuminuria in type 2 diabetes[J]. N Engl J Med, 2011, 364(10): 907-917. DOI:10.1056/nejmoa1007994 |
| [22] |
LEWIS E J, HUNSICKER L G, CLARKE W R, et al. Renoprotective effect of the angiotensin-receptor antagonist irbesartan in patients with nephropathy due to type 2 diabetes[J]. N Engl J Med, 2001, 345(12): 851-860. DOI:10.1056/NEJMoa011303 |
| [23] |
STRATTON I M, CULL C A, ADLER A I, et al. Additive effects of glycaemia and blood pressure exposure on risk of complications in type 2 diabetes: a prospective observational study (UKPDS 75)[J]. Diabetologia, 2006, 49(8): 1761-1769. DOI:10.1007/s00125-006-0297-1 |
| [24] |
HIRSCH I B, BROWNLEE M. Beyond hemoglobin A1c: need for additional markers of risk for diabetic microvascular complications[J]. JAMA, 2010, 303(22): 2291-2292. DOI:10.1001/jama.2010.785 |
| [25] |
RETNAKARAN R, CULL C A, THORNE K I, et al. Risk factors for renal dysfunction in type 2 diabetes: U.K. Prospective Diabetes Study 74[J]. Diabetes, 2006, 55(6): 1832-1839. DOI:10.2337/db05-1620 |
| [26] |
TSAI C W, HUANG H C, CHIANG H Y, et al. Longitudinal lipid trends and adverse outcomes in patients with CKD: a 13-year observational cohort study[J]. J Lipid Res, 2019, 60(3): 648-660. DOI:10.1194/jlr.P084590 |
| [27] |
JI B L, ZHANG S H, GONG L L, et al. The risk factors of mild decline in estimated glomerular filtration rate in a community-based population[J]. Clin Biochem, 2013, 46(9): 750-754. DOI:10.1016/j.clinbiochem.2013.01.011 |
| [28] |
KEECH A, SIMES R J, BARTER P, et al. Effects of long-term fenofibrate therapy on cardiovascular events in 9795 people with type 2 diabetes mellitus (the FIELD study): randomised controlled trial[J]. Lancet, 2005, 366(9500): 1849-1861. DOI:10.1016/S0140-6736(05)67667-2 |
| [29] |
ISAKA Y, TAKABATAKE Y, TAKAHASHI A, et al. Hyperuricemia-induced inflammasome and kidney diseases[J]. Nephrol Dial Transplant, 2016, 31(6): 890-896. DOI:10.1093/ndt/gfv024 |
| [30] |
ZHANG L, WANG F, WANG X, et al. The association between plasma uric acid and renal function decline in a Chinese population-based cohort[J]. Nephrol Dial Transplant, 2012, 27(5): 1836-1839. DOI:10.1093/ndt/gfr597 |




