2. 400021 重庆,重庆市妇幼保健院;
3. 401147 重庆,重庆市环境科学研究院
2. Chongqing Health Center for Women and Children, Chongqing, 400021;
3. Chongqing Academy of Environmental Sciences, Chongqing, 401147, China
大气污染是全世界严重的环境问题之一。随着生活、经济水平不断提高,交通和工农业迅速发展,我国的大气污染状况也日益加重,大气污染对人体健康的危害已经受到了国内外的广泛关注。研究表明大气污染物不仅可影响呼吸系统和心血管系统,更能造成免疫系统和内分泌系统等广泛的损伤[1-3]。根据我国国家环境保护标准(GB3095-2012),大气中的主要污染物包括大气细颗粒物(PM2.5)、可吸入颗粒物(PM10)、二氧化硫(SO2)、二氧化氮(NO2)、一氧化碳(CO)和臭氧(O3)等。其中,NO2、SO2、O3和CO属于气态污染物。
在过去的20年中,越来越多的研究发现大气污染对生殖功能和妊娠结局可能产生严重而深远的影响[4-5]。大气细颗粒物暴露不仅会引起男性精液质量的下降与性激素水平的改变[6],还会造成精子DNA损伤[7],甚至引起人类生育力的下降[8]。其他研究也表明大气气态污染物在精子发育过程中会对精液质量造成不良影响,如ZHANG等[9]的研究发现:O3暴露浓度在精子发生的关键时期0~9 d、10~14 d与精子浓度呈负相关。另一研究对2013-2015年在武汉大学人民医院生殖医学中心就诊的1 852例患者的精液质量数据进行分析后,也发现SO2和NO2在采样前0~90 d的暴露浓度与精子浓度、精子总数和精子活力呈负相关[10]。然而,以往的流行病学研究仍大多聚焦于大气颗粒物暴露与男性精液质量的关联,对于SO2、NO2、CO以及O3等气态污染物对男性生殖内分泌系统影响的研究报道较少。因此,本研究在前期建立的重庆市大学生男性生殖健康队列(male reproductive health in chongqing college students, MARHCS)基础上,探讨环境空气中大气污染物暴露对男性精液质量及性激素水平的影响,阐明不同的气态污染物对男性生殖健康的可能危害。
1 资料与方法 1.1 研究对象本研究人群来自课题组前期建立的MARHCS队列,根据大学生随学业任务的变化而发生校区自然迁徙的特点,调查空气污染变化对男性生殖健康可能造成的影响。该研究于2013年6月8-21日在空气质量较好的重庆大学新校区(虎溪大学城)建立了基线调查,共招募796名合格志愿者,均为大二男生。第2年其中部分研究对象已经搬迁回空气污染较重的老校区(位于重庆市中心的沙坪坝区)继续学习。我们于2014年6月5-16日对研究对象进行了第1次随访,于2015年5月22日至6月7日进行了第2次随访。此研究获得第三军医大学伦理委员会的批准(1.0/2013.4-12)。参与对象均被告知研究目的后自愿参与,并且签署知情同意书,完成后续问卷调查及样本留存。更多详细内容参考课题组已发表的研究[11]。
1.2 方法 1.2.1 空气污染数据与暴露评估研究期间的地面气象资料来自重庆市气象局,空气污染数据(SO2、NO2、O3和CO)由重庆市生态环境检测中心(重庆市环境科学研究院)提供,其采样点分别为虎溪监测点(重庆大学虎溪校区内)和高家花园监测点(距离重庆大学老校区 < 500 m),空气采样时间为2013年1月1日至2015年12月31日。精子发生到最后发育成熟大概需要90 d,因此我们选择精液标本采集前90 d的污染物浓度作为暴露的指标。
1.2.2 精液常规参数、精子染色质结构和血清性激素水平的检测在基线和两次随访调查中,研究对象每次均提供精液、尿液和血液样本。2013-2015年共采集了2 030份精液和血液样本。志愿者在禁欲2~7 d后通过手淫法采集精液样本于1只无菌干燥的广口容器中,详细记录精液采集时间、禁欲天数、精液撒漏情况。根据WHO第5版《人类精液检查及处理实验室手册》推荐的方法分析、测量精液常规参数,如采用称量法测量精液体积;通过计算机辅助精液分析系统(CASA)分析精子总数、精液密度及精子运动参数;采用Diff-Quik染色法染色精液涂片来分析及评估精子形态。采用流式细胞仪(Cytomics FC 500, Beckman)精子染色质结构分析(SCSA)评价精子DNA损伤和完整性,其检测指标包括精子DNA断裂指数(DNA fragment index, DFI)和精子高DNA着色性(high DNA stainablity, HDS)。于志愿者的血液样本采集后分离血清,在本校第一附属医院的临床实验室采用免疫分析系统(Unicel Dxi 800,Beckman Coulter Inc, USA)检测血清6项性激素水平:雌二醇(E2)、卵泡刺激素(FSH)、黄体生成素(LH)、泌乳素(PRL)、孕酮(P)和睾酮(T)。所有检测的具体操作方法详见前期已发表的研究[12-13]。
1.3 统计学分析研究对象的人口流行病学资料和大气污染数据呈偏态分布,以中位数(四分位数)[M(P25,P75)]或[例(%)]表示,各生殖健康参数(如精液参数、血清性激素等)以箱线图表示。由于精液参数和性激素水平呈非正态分布,故对其进行lg变换使其呈正态分布或近似正态分态。然后在数据分析之后对所有结果进行反转换,以得到变化百分比和95%置信区间(CI)。Manne-Whitney U检验和χ2检验用于比较组间的人口学资料、空气污染水平和男性生殖健康参数指标。控制年龄、体质量指数(BMI)、吸烟、饮酒等混杂因素后,利用混合效应模型分析空气污染物浓度与研究对象生殖健康参数的关联,并进行Bonferroni多重检验的校正(P值×60)。所有数据采用SPSS 18.0和SAS 9.1统计软件进行分析。P < 0.05为差异具有统计学意义。
2 结果 2.1 研究对象的一般特征及采样前90 d的大气污染特征描述研究对象的一般描述性资料及采样前90 d的大气污染物暴露水平见表 1。2013年共有796名志愿者完成了基线调查。2014年共666名(84.7%)志愿者完成第1次随访。2015年共568名(71.4%)志愿者完成第2次随访。2013、2014、2015年志愿者的平均年龄分别为20、21、22岁,基本特征如年龄、BMI、吸烟、饮酒等差异无统计学意义。
| 变量 | 基线调查(2013年,虎溪) | 第1次随访(2014年) | 第2次随访(2015年) | |||
| 沙坪坝 | 虎溪 | 沙坪坝 | 虎溪 | |||
| 总例数 | 796 | 478 | 188 | 515 | 53 | |
| 年龄/岁 | 20(20.0, 21.0) | 21.0(21.0, 22.0) | 21.0(20.0, 22.0) | 22.0(22.0, 23.0) | 22.0(21.0, 23.0) | |
| 禁欲天数/d | 4.0(3.0, 6.0) | 4.0(3.0, 5.0) | 4.0(3.0, 6.0)a | 4.0(3.0, 5.0) | 4.0(3.0, 5.0) | |
| BMI/kg·m-2 | 20.94(19.59, 22.72) | 21.15(19.81, 22.86) | 20.76(19.49, 22.48) | 21.79(20.21, 23.75) | 21.42(19.48, 22.93) | |
| 吸烟情况 | ||||||
| 从不吸烟 | 593(74.5) | 345(72.2) | 138(73.8) | 380(73.8) | 34(64.2) | |
| 已戒烟 | 171(21.5) | 108(22.6) | 39(20.9) | 113(21.9) | 15(28.3) | |
| 吸烟 | 30(3.8) | 25(5.2) | 10(5.3) | 22(4.3) | 4(7.5) | |
| 饮酒情况 | ||||||
| 从不饮酒 | 409(51.4) | 92(19.2) | 38(20.2) | 110(21.4) | 12(22.6) | |
| 已戒酒 | 374(47.0) | 356(74.5) | 139(73.9) | 383(74.4) | 40(75.5) | |
| 饮酒 | 10(1.3) | 30(6.3) | 11(5.9) | 21(4.1) | 1(1.9) | |
| 大气污染情况/μg·m-3 | ||||||
| SO2 | 21.0(2.0, 60.0) | 23.0(9.0, 49.0) | 16.0(6.0, 34.0)a | 13.0(4.6, 23.0) | 15.0(7.4, 29.0)a | |
| NO2 | 20.0(9.0, 50.7) | 40.0(24.0, 60.8) | 29.0(14.0, 49.0)a | 58.0(28.0, 87.0) | 37.0(13.5, 60.0)a | |
| O3 | 75.0(21.8, 184.6) | 55.5(10.7, 161.7) | 70.5(10.0, 207.2) | 80.0(20.5, 180.0) | 102.5(34.9, 219.1)a | |
| CO | 600(260, 900) | 1 300(900, 1 800) | 900(600, 1 200)a | 1 200(760, 1 600) | 800(560, 1 300)a | |
| 温度/℃ | 36.0(23.0, 39.0) | 28.0(22.0, 33.0) | 27.0(23.0, 31.0) | 25.0(23.0, 31.0) | 25.0(23.0, 27.0) | |
| 湿度(%) | 51.0(46.0, 93.0) | 83.0(74.0, 93.0) | 83.0(83.0, 91.0) | 82.0(62.0, 89.0) | 83.0(68.0, 89.0) | |
| 风速/km·h-1 | 10.0(5.0, 14.0) | 6.0(3.0, 8.0) | 6.0(3.0, 8.0) | 8.0(3.0, 13.0) | 6.0(3.0, 10.0) | |
| a:经统计检验后两地差异具有统计学意义(P < 0.05) | ||||||
空气污染数据显示:2013年采样前90 d的环境气态污染物(SO2、NO2、O3和CO)浓度(中位数)分别为21.0、20.0、75.0、600 μg/m3。2014年在沙坪坝和虎溪两地SO2、NO2、O3、CO的浓度(中位数)分别为23.0、16.0 μg/m3,40.0、29.0 μg/m3, 55.5、70.5 μg/m3,1 300、900 μg/m3。2015年两地SO2、NO2、CO的浓度(中位数)分别为13.0、15.0 μg/m3,58.0、37.0 μg/m3,1 200、800 μg/m3。除2014年的O3浓度外,其余在两个监测点的大气污染物浓度比较差异均有统计学意义(P < 0.05),但温度、湿度等气象数据比较均无明显差异。
2.2 精液质量和血清性激素水平分析研究对象2013、2014、2015年的精液常规参数如精子活力和血清孕酮水平比较差异无统计学意义。然而2013、2014、2015年研究对象的精液量、精子密度、精子总数和精子正常形态率差异具有统计学意义(P < 0.05),且精子DNA完整性指标HDS差异也具有统计学意义(3.85% vs 3.15% vs 8.75%, P < 0.05),血清生殖激素水平如雌二醇、黄体生成素、泌乳素和睾酮等差异有统计学意义(19.0 vs 25.5 vs 30.0 pg/mL, 4.05 vs 4.41 vs 4.11 mIU/mL, 10.13 vs 10.87 vs 9.47 ng/mL, 4.35 vs 3.96 vs 3.64 ng/mL,P < 0.05,图 1)。

|
| 纵坐标由对数分布形式表示;箱中的黑线代表该组数据的中位数 图 1 2013-2015年重庆大学生精液质量和血清性激素水平变化趋势 |
2.3 采样前90 d大气污染物暴露对精液质量、血清性激素水平的影响
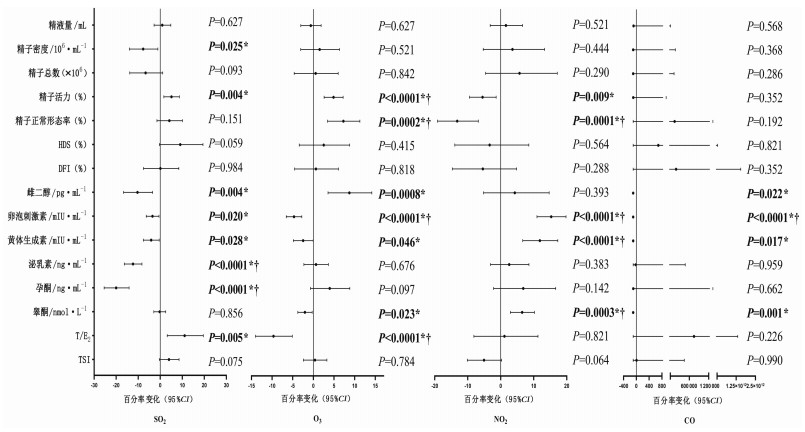
在混合效应模型中,采样前90 d的SO2暴露浓度与精子密度呈显著负相关(β=-7.76,95%CI: -14.01~ -1.04,P=0.025),与雌二醇、卵泡刺激素、黄体生成素、泌乳素和孕酮也呈负相关(P < 0.05)。O3与精子活力(β=4.88,95%CI: 2.60~7.22,P < 0.000 1)、精子正常形态(β=7.28,95%CI:3.44~11.27,P=0.002)呈正相关,其与卵泡刺激素、黄体生成素、睾酮和T/E2比值呈负相关。NO2暴露与精子活力(β=-5.51,95%CI: -9.46~-1.39, P=0.009)、精子正常形态(β=-13.18,95%CI: -19.14~-6.78, P=0.000 1)呈负相关,但与卵泡刺激素、黄体生成素和睾酮呈正相关(P < 0.05)。对于CO暴露,仅发现CO浓度与血清性激素水平如雌二醇、卵泡刺激素、黄体生成素和睾酮呈负相关(P < 0.05,图 2)。
|
| *:表示分析后采样前90 d大气气态污染物暴露与男性生殖健康各参数指标的关联性具有统计学意义(P < 0.05);†:表示经过Bonferroni多重校正后仍具有统计学意义 图 2 采样前90 d大气气态污染物暴露与男性生殖健康参数指标的混合效应模型 |
在进行了Bonferroni多重校正后,只有SO2与泌乳素、孕酮(校正P < 0.05),O3与卵泡刺激素、T/E2比值(校正P < 0.05),NO2与精子正常形态率(校正P < 0.05),CO与卵泡刺激素(校正P < 0.05)之间的相关性仍有统计学意义,且呈负相关关系。另一方面,也发现O3与精子活力、精子正常形态率,NO2与卵泡刺激素、黄体生成素和睾酮的正相关关系仍然存在(校正P < 0.05)。
3 讨论本研究通过监测环境气态污染物暴露水平,分析其与男性精液质量与血清性激素各参数指标的关联,研究环境气态污染物暴露对男性生殖健康的影响。结果表明:NO2暴露浓度与精子正常形态率呈负相关,O3与精子活力、精子正常形态率呈正相关;SO2暴露与泌乳素、孕酮呈显著负相关,O3暴露与卵泡刺激素、T/E2呈负相关,NO2与卵泡刺激素、黄体生成素、睾酮呈正相关,CO与卵泡刺激素呈负相关。该结果提示环境气态污染物SO2、NO2、O3和CO暴露均会不同程度影响血清性激素水平,此外,NO2暴露可能降低正常精子形态率,导致精液质量下降。
课题组前期在MARHCS队列的研究中,发现不同大气污染颗粒物(PM10、PM10-2.5和PM2.5)对男性生殖系统的影响作用不同。PM10暴露可能导致精子正常形态率降低,PM10-2.5可能导致精子密度降低,而PM2.5与精子参数和血清激素无关[12]。在本研究中,研究结果也显示不同的环境气态污染物也可能对男性生殖健康造成不同的影响,且与前期对重庆地区1 346名健康成年男性的调查研究结果一致,大气中PM10、SO2、NO2浓度与男性精子浓度、精子正常形态率以及精子活力均呈负相关[14]。虽然空气污染可能影响男性生育能力的生物学机制尚不清楚,但已有学者提出了几种理论。大气气态污染物,如NO2和SO2可独立诱发睾丸组织氧化损伤,导致精子发生和精子DNA完整性受损[15-16]。研究表明O3也可诱导氧化应激反应,破坏男性生殖系统功能[17]。且O3暴露引起的DNA损伤在精子生成后期将不能修复,会导致DNA碎片增加[9]。但本研究的结果显示O3暴露与精子活力、精子正常形态率呈正相关。出现这一结果的原因可能是本研究的研究人群为健康的成年大学生,其普遍精液质量较好,暴露于O3后只是对生殖参数在生理范围内扰动。此外,与ZHANG等[9]的研究地区(北京)相比,重庆市区的光、化学、烟雾污染程度相对较轻,且在研究期间重庆O3的暴露浓度也较北京低(79.2 vs 102.9 μg/m3)。因此在本研究人群的研究时段中,尚不能观察到O3的环境浓度变化对生殖系统的损害效应。
最近,已有新的证据表明中枢神经系统通路的激活可能是空气污染健康效应的一种新机制[18]。空气污染物可激活下丘脑-垂体-肾上腺轴(hypothalamic-pituitary-adrenal axis,HPA)和下丘脑-垂体-性腺轴(hypothalamic-pituitary-gonadal axis,HPG),扰乱正常男性生殖激素的产生与分泌。下丘脑分泌促性腺激素释放激素(GnRH)和促性腺激素抑制激素(GnIH),垂体分泌卵泡刺激素(FSH)和黄体生成激素(LH),LH的主要作用就是促进睾丸间质细胞合成和分泌睾酮(T)[19-20]。睾酮对精子发生具有非常重要的作用,研究表明睾酮的浓度与精子密度呈正相关,而与精子形态等指标无关[21]。在本研究中,经Bonferroni多重校正后仍发现NO2与卵泡刺激素、黄体生成素、睾酮呈正相关,与精子正常形态率呈负相关。与其他研究一致,本研究混合效应模型结果显示:NO2浓度与FSH、LH和T呈正相关,与精子密度、精子总数也呈正相关,只是统计学关联尚不显著。
近年来,有部分研究也发现空气污染物会对男性性激素水平产生影响[22]。如RADWAN等[23]发现暴露于空气污染物(PM10、PM2.5、NOx和CO)与睾酮水平呈负相关。TOMEI等[24]对意大利交通警察的研究发现:暴露于空气污染物后,其雌二醇平均水平显著低于对照组,而交通警察的FSH平均值明显高于对照组。此外,本研究结果发现SO2暴露与泌乳素、孕酮呈显著负相关,O3暴露与卵泡刺激素、T/E2呈负相关,CO与卵泡刺激素呈负相关。本研究与这些研究的结果存在差异,其原因可能为:①研究地区的不同,导致空气污染物组分差异、来源的多样性,以及暴露程度不同,导致结果缺乏统一性;②短期或长期暴露在空气污染物可能会导致完全不同的健康影响;③研究人群的选择偏倚和污染物的测量方法,以及研究设计的差异。
大气污染物的污染程度变化与不良的气象因素和污染物的来源、排放情况有关[25]。“十二五”期间,重庆市实施国务院《大气污染防治行动计划》,执行空气质量新标准,深入实施了一系列减排措施。其中燃煤污染的治理成效显著,使得SO2的污染浓度逐年降低,重庆雾霾发生天数较以前减少,空气质量明显改善,另一方面也减少了环境O3浓度。此外,重庆市机动车保有量每年都呈增长态势,城市汽车尾气污染逐渐加重,导致NO2的浓度不降反升。重庆大学的老校区位于重庆市中心的沙坪坝区,空气污染严重;而新校区位于虎溪大学城,远离城市污染,有着优良的生态环境。本研究结果中,通过对虎溪(市郊)、沙坪坝(市中心)两个采样点的空气质量进行对比,可以发现虽然空气质量逐年好转,但市区CO、NO2等污染物浓度仍显著高于大学城地区。
本研究与以往多以医院男科门诊或不孕门诊就诊者为研究对象的人群流行病学研究相比,研究对象为大学生,更能代表一般人群,且能够在很大程度上控制年龄对精液质量和血清生殖激素的影响。此外,本研究为了排除季节、气温等因素对精液质量以及空气质量的影响,3次调查均在每年的相同月份进行。但本研究也存在不足之处:①研究样本为重庆部分大学生,可能不能代表所有青年男性,因此建议将来的研究做多地、多中心的队列。②尽管我们在分析中调整了一些混杂因素,但仍可能有部分未校正的或未测量的混杂因素在一定程度上影响男性生殖健康,比如饮食习惯、作息规律和心理压力等。③本研究属于观察性研究,无法探究大气气态污染物与精液参数和性激素水平的确切因果关系,需要进一步验证目前发现的大气气态污染物对精液和性激素的效应。④对个人暴露环境气态污染物的剂量估计并不准确,目前的研究只考虑了暴露的时间变化,仅通过计算采样前90 d大气中气态污染物的暴露水平,这不能有效地评估个体的内暴露水平,可能会对生殖健康效应的评估造成偏倚。
综上所述,本研究发现环境气态污染物暴露可能会对男性生殖健康参数造成不同程度的影响。鉴于我国广泛存在的大气污染,以及日益严峻的生殖健康挑战,本研究警示了气态污染物暴露与精液质量下滑可能的相关性,进一步突出了污染防治的迫切需要,为男性生殖健康的基础研究提供了新思路。男性生殖健康与精液质量是一系列内、外因素交互作用的结果,如何充分考虑复杂因素下的联合暴露,准确评估大气污染物人群和个体暴露水平及影响因素,将是后期研究的关键环节。
| [1] |
KARIMI B, SHOKRINEZHAD B, SAMADI S. Mortality and hospitalizations due to cardiovascular and respiratory diseases associated with air pollution in Iran: a systematic review and meta-analysis[J]. Atmos Environ, 2019, 198: 438-447. DOI:10.1016/j.atmosenv.2018.10.063 |
| [2] |
ALMETWALLY A A, BIN-JUMAH M, ALLAM A A. Ambient air pollution and its influence on human health and welfare: an overview[J]. Environ Sci Pollut Res, 2020, 27(20): 24815-24830. DOI:10.1007/s11356-020-09042-2 |
| [3] |
DENG Z B, CHEN F, ZHANG M X, et al. Association between air pollution and sperm quality: a systematic review and meta-analysis[J]. Environ Pollut, 2016, 208: 663-669. DOI:10.1016/j.envpol.2015.10.044 |
| [4] |
JUREWICZ J, DZIEWIRSKA E, RADWAN M, et al. Air pollution from natural and anthropic sources and male fertility[J]. Reprod Biol Endocrinol, 2018, 16(1): 109. DOI:10.1186/s12958-018-0430-2 |
| [5] |
CONFORTI A, MASCIA M, CIOFFI G, et al. Air pollution and female fertility: a systematic review of literature[J]. Reprod Biol Endocrinol, 2018, 16(1): 117. DOI:10.1186/s12958-018-0433-z |
| [6] |
王笑臣, 田晓佳, 叶波, 等. 武汉市大气PM10暴露对精液质量的影响[J]. 中华预防医学杂志, 2018, 52(1): 73-78. WANG X C, TIAN X J, YE B, et al. Effects of atmospheric PM10 exposure on semen quality in Wuhan[J]. Chin J Preven Med, 2018, 52(1): 73-78. |
| [7] |
LAI C H, HUANG H B, CHANG Y C, et al. Exposure to fine particulate matter causes oxidative and methylated DNA damage in young adults: a longitudinal study[J]. Sci Total Environ, 2017, 598: 289-296. DOI:10.1016/j.scitotenv.2017.04.079 |
| [8] |
FRUTOS V, GONZALEZ M, SOLA I, et al. Impact of air pollution on fertility: a systematic review[J]. Gynecol Endocrinon, 2015, 31(1): 7-13. DOI:10.3109/09513590.2014.958992 |
| [9] |
ZHANG H T, ZHANG Z, CAO J, et al. Ambient ozone pollution is associated with decreased semen quality: longitudinal analysis of 8945 semen samples from 2015 to 2018 and during pollution-control period in Beijing, China[J]. Asian J Androl, 2019, 21(5): 501-507. DOI:10.4103/aja.aja_116_18 |
| [10] |
WANG X, TIAN X, YE B, et al. Gaseous pollutant exposure affects semen quality in central China: a cross-sectional study[J]. Andrology, 2020, 8(1): 117-124. DOI:10.1111/andr.12655 |
| [11] |
CHEN Q, YANG H, ZHOU N, et al. Inverse U-shaped association between sleep duration and semen quality: longitudinal observational study (MARHCS) in Chongqing, China[J]. Sleep, 2016, 39(1): 79-86. DOI:10.5665/sleep.5322 |
| [12] |
ZHOU N Y, JIANG C T, CHEN Q, et al. Exposures to atmospheric PM10 and PM10-2.5 affect male semen quality: results of MARHCS study[J]. Environ Sci Technol, 2018, 52(3): 1571-1581. DOI:10.1021/acs.est.7b05206 |
| [13] |
刘太秀, 崔志鸿, 曹佳. 重庆市大学生精液常规参数与精子DNA损伤的关联性分析[J]. 第三军医大学学报, 2016, 38(11): 1325-1330. LIU T X, CUI Z H, CAO J. Association analysis between routine semen parameters and sperm DNA damage in Chongqing college students[J]. J Third Mil Med Univ, 2016, 38(11): 1325-1330. DOI:10.16016/j.1000-5404.201603024 |
| [14] |
ZHOU N, CUI Z, YANG S, et al. Air pollution and decreased semen quality: a comparative study of Chongqing urban and rural areas[J]. Environ Pollut, 2014, 187: 145-152. DOI:10.1016/j.envpol.2013.12.030 |
| [15] |
MENG Z Q, BAI W. Oxidation damage of sulfur dioxide on testicles of mice[J]. Environ Res, 2004, 96(3): 298-304. DOI:10.1016/j.envres.2004.04.008 |
| [16] |
RENGARAJ D, KWON W S, PANG M G. Effects of motor vehicle exhaust on male reproductive function and associated proteins[J]. J Proteome Res, 2015, 14(1): 22-37. DOI:10.1021/pr500939c |
| [17] |
田晓佳, 王笑臣, 叶波, 等. 武汉市臭氧暴露对男性精液质量的影响[J]. 中华预防医学杂志, 2017, 51(3): 197-202. TIAN X J, WANG X C, YE B, et al. Effect of ozone exposure on semen quality of men in Wuhan[J]. Chin J Preven Med, 2017, 51(3): 197-202. DOI:10.3760/cma.j.issn.0253-9624.2017.03.002 |
| [18] |
SNOW S J, HENRIQUEZ A R, COSTA D L, et al. Neuroendocrine regulation of air pollution health effects: emerging insights[J]. Toxicol Sci, 2018, 164(1): 9-20. DOI:10.1093/toxsci/kfy129 |
| [19] |
HUHTANIEMI I. MECHANISMS IN ENDOCRINOLOGY: Hormonal regulation of spermatogenesis: mutant mice challenging old paradigms[J]. Eur J Endocrinol, 2018, 179(3): R143-R150. DOI:10.1530/eje-18-0396 |
| [20] |
DAS N, KUMAR T R. Molecular regulation of follicle-stimulating hormone synthesis, secretion and action[J]. J Mol Endocrinol, 2018, 60(3): R131-R155. DOI:10.1530/jme-17-0308 |
| [21] |
KOCH T, HANSEN A H, PRISKORN L, et al. a history of cryptorchidism is associated with impaired testicular function in early adulthood: a cross-sectional study of 6376 men from the general population[J]. Hum Reprod, 2020, 35(8): 1765-1780. DOI:10.1093/humrep/deaa127 |
| [22] |
CHECA VIZCAÍNO M A, GONZÁLEZ-COMADRAN M, JACQUEMIN B. Outdoor air pollution and human infertility: a systematic review[J]. Fertil Steril, 2016, 106(4): 897-904. DOI:10.1016/j.fertnstert.2016.07.1110 |
| [23] |
RADWAN M, JUREWICZ J, POLA ŃSKA K, et al. Exposure to ambient air pollution: does it affect semen quality and the level of reproductive hormones?[J]. Ann Hum Biol, 2016, 43(1): 50-56. DOI:10.3109/03014460.2015.1013986 |
| [24] |
TOMEI G, TOMAO E, CIARROCCA M, et al. Follicle-stimulating hormone levels in male workers exposed to urban chemical, physical, and psychosocial stressors[J]. Toxicol Ind Health, 2009, 25(6): 395-402. DOI:10.1177/0748233709106466 |
| [25] |
杨显双, 伍丽梅. 重庆市大气污染特征及影响因素分析[J]. 环境与可持续发展, 2015, 40(4): 173-175. YANG X S, WU L M. Analysis on characteristics and influencing factors of air pollution in Chongqing[J]. Environ Sus Develop, 2015, 40(4): 173-175. DOI:10.19758/j.cnki.issn1673-288x.2015.04.054 |




