脑室相关的深部肿瘤位于脑室系统内或旁,常引起脑脊液循环阻塞,因其手术部位深在,显露操作相对困难,为神经外科难题之一[1]。近年来, 神经内镜技术主要应用于脑室内、颅底及脊柱等手术中,而对于脑室相关的深部肿瘤,神经内镜常用于活检手术或作为显微镜的辅助工具,鲜有在单纯内镜下全切较大实体肿瘤的案例[2]。随着神经内镜技术运用日趋成熟[3],结合术中辅助工具,如一次性牵开固定器、超声吸引器(cavitron ultrasonic surgical aspirator,CUSA)、神经导航等,可发挥内镜手术独到优势,有效提高手术的全切率和安全性。本研究对本院近年应用神经内镜技术经颅治疗脑室相关深部肿瘤患者的一般临床资料、术后情况进行分析总结,拟为利用神经内镜技术在脑室相关深部肿瘤的微创治疗方面提供参考。
1 资料与方法 1.1 临床资料回顾性分析2016年1月至2019年3月本院接诊的脑室相关深部肿瘤21例患者。纳入标准:①经头颅磁共振检查确诊为脑室内或脑室旁肿瘤;②多模态影像学检查示肿瘤以实质性为主,瘤内囊性变体积不超过总体积25%;③肿瘤中心距离大脑皮层的最近距离均≥4 cm,符合深部肿瘤诊断标准[1, 4-5]。排除标准:①有手术禁忌证;②有麻醉禁忌证。患者男性10例,女性11例;年龄23~63岁,平均37.8岁。术前表现:15例存在显著高颅压症状体征;2例癫痫发作;4例颅神经功能障碍(视神经功能障碍2例,动眼神经功能障碍2例);3例肌力下降(肌力Ⅲ级2例,肌力Ⅳ级1例)。17例术前合并梗阻性脑积水。病变部位:侧脑室内10例,侧脑室旁3例,丘脑突入侧脑室内2例,第三脑室内5例,松果体区1例。病变最大直径14~69 mm,平均34.8 mm。本研究通过本院伦理委员会批准(2020-659)。
1.2 手术方法 1.2.1 手术器械硬质0°、30°、45°神经内镜(Karl Storz,德国)及其配套器械和气动式内镜支架;超声吸引器(Valleylab,美国);一次性牵开固定器(全长70 mm,上端开口直径22 mm,下端开口直径16 mm;JBW/QK702216;金柏威,武汉);神经导航(Medtronic Stealth Station S7;美国)。
1.2.2 手术准备及手术入路的选择术前完善多模态影像学检查(如CTA、CTV、PWI、DWI、DTI、MRS),了解肿瘤的病变性质、位置、水肿区域、供血动脉及引流静脉、白质纤维束走向等。拟内镜手术患者术前根据磁共振T2序列和CTA等评估肿瘤质地和血供程度,综合评判手术方式选择。
根据病变部位采取相应入路:①病变位于侧脑室内或瘤体由侧脑室旁突入脑室者采用经额中回-侧脑室入路(15例);②病变位于第三脑室内采用经额中回-侧脑室-室间孔-三脑室入路(3例)或经纵裂-胼胝体-透明隔腔-穹窿间-第三脑室入路(1例);③病变位于三脑室后份或松果体区采用幕下小脑上入路(2例)。
1.2.3 手术过程患者于术前完善影像学检查(图 1A~C,图 2A~C)。在全麻后Mayfield头架固定头部(图 1D),根据神经导航优化术前拟定入路(图 1E),确定切口及路径。开颅后在神经导航指引下置入一次性牵开固定器或脑牵开器(幕下小脑上入路)至肿瘤部位建立手术通道(图 1F),根据术中视野具体需求选取0°、30°或45°的神经内镜直视下切除。12例术中采用气动臂持镜,9例采用手动持镜;≤2 cm肿瘤整块切除,>2 cm的肿瘤分块切除,根据肿瘤质地选择性使用常规吸引器或超声吸引器(图 1G、图 2D)。切除肿瘤后,神经导航确认切除程度并在内镜下观察脑脊液通路(图 1H),根据情况行透明隔造瘘术、室间孔成形术(图 2E)、第三脑室底造瘘术。术中以含地塞米松(5 mg/500 mL)的37 ℃生理盐水反复或持续术区灌洗,活动性出血予双极电凝(图 2F),非活动性出血压迫止血,水密缝合硬膜常规关颅。术后保留脑室外引流管,并在2~4 d后根据引流情况试夹管48 h,复查CT无明显脑积水后拔管,若无法安全拔管则根据脑积水情况再行腰池引流术或分流手术。
|
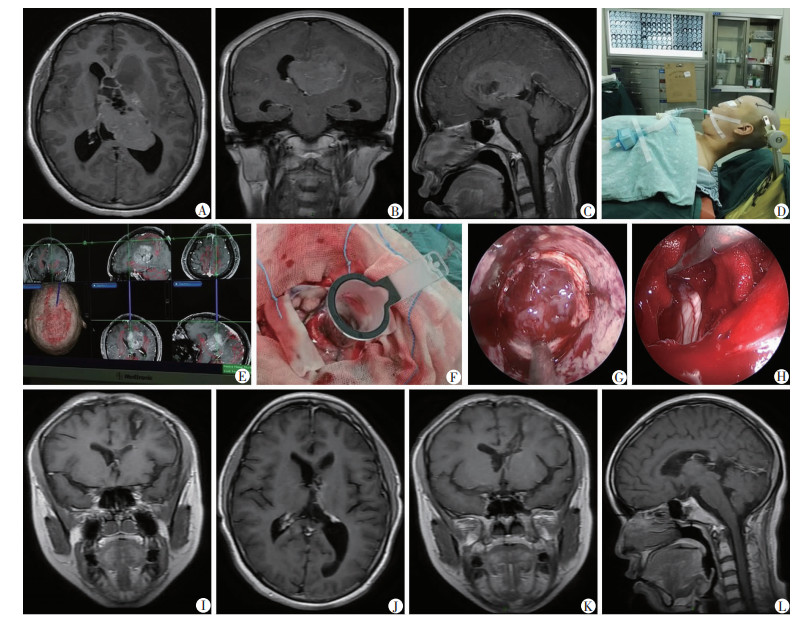
| A~C: 患者术前MRI的T1序列轴位(A)、冠状位(B)、矢状位(C)可见双侧脑室的巨大占位性病变;D: 患者取仰卧位,头部于Mayfield头架固定;E: 于神经导航下确定手术入路;F: 一次性牵开固定器放置完成;G: 肿瘤的质地与血供适合吸引器为主的切除方式;H: 切除肿瘤后光滑的脑室壁;I: 术后脑实质手术通道周围脑组织损伤小;J~L:患者术后3个月轴位(J)、冠状位(K)、矢状位(L)头颅MRI的T1增强序列显示肿瘤次全切除 图 1 神经内镜经额中回-侧脑室入路切除巨大中枢神经细胞瘤 |

|
| A~C: 患者术前MRI的T1序列矢状位(A)、冠状位(B)、轴位(C)可见左侧脑室旁突向脑室内生长的巨大占位性病变;D: 超声吸引器的使用;E: 双人两手操作下双极电凝止血;F: 切除肿瘤后附加室间孔成型,脑脊液循环通路通畅;G~I: 患者术后10个月矢状位(G)、冠状位(H)、轴位(I)头颅MRI的T1增强序列显示肿瘤完全切除 图 2 神经内镜经额中回-侧脑室入路切除室管膜瘤 |
1.3 随访
对21例患者进行术后随访,采用门诊随访与电话随访相结合的方式,主要随访患者临床症状及影像学表现。随访截止时间为2020年9月。
2 结果21例患者均在内镜下完成肿瘤切除全程操作,以术后48 h内增强MRI为主要判断依据,15例肿瘤全切除,6例肿瘤次全切除,全切率达71%。
术后病理表现:胶质母细胞瘤2例,间变少突胶质细胞瘤2例,少突胶质细胞瘤1例,毛细胞性星型细胞瘤3例,海绵状血管瘤1例,中枢神经细胞瘤4例,生殖细胞瘤2例,室管膜瘤6例。
术后并发症:5例发热,其中3例脑脊液检查证实为感染,抗生素治疗并辅助腰池引流后痊愈;2例感染证据不足,考虑为出血等刺激性发热,3~5 d后自行恢复。3例脑积水,其中1例为术后新发,考虑为三脑室内粘连形成,行脑室-腹腔分流后痊愈;余2例术前即存在脑积水,其中1例术后脑积水未明显缓解,但程度稳定且无明显临床表现,予密切随访至今无进展;1例术后脑积水稍有进展,予腰池引流1周后缓解,拔除引流后无症状和影像学进展;其余患者于术后7 d内安全拔除脑室外引流管。1例癫痫发作,抗癫痫治疗后至今未再发作。3例皮下积液,穿刺抽吸、加压包扎后痊愈。
术后无颅内血肿、严重脑水肿等并发症,除1例脑室-腹腔分流术外无非计划二次手术病例。
术后2例动眼神经功能障碍改善,1例视力好转。3例肌力下降术后均改善,其中2例肌力由术前Ⅲ级恢复至Ⅳ级,1例由Ⅳ级恢复至Ⅴ级。本组中无神经功能障碍较术前加重病例。
随访结果:患者术后影像学表现见图 1I~L,图 2G~I。随访时间18~36个月,平均23.0个月,其中完整随访19例,2位患者因失联而失访。全切组均未发现肿瘤复发,次全切组2例(均为胶质母细胞瘤)肿瘤复发并再次手术。
3 讨论 3.1 神经内镜技术治疗脑室相关深部肿瘤的优势传统显微镜优势在于有较高分辨率,视网膜直接充当感受器使色彩和景深更佳[6]。同时显微镜手术治疗脑内深部肿瘤已积累了大量手术经验,术式更加成熟。但本团队认为:神经内镜技术在治疗脑室相关深部肿瘤时在某些方面有其独到优势。首先,内镜可通过小幅度镜头移动充分利用脑室自然腔隙,减少脑组织牵拉。其次,显微镜在深度大且有弧度转角的脑室空间时会有较大光线损失或盲区,而内镜拥有广角和多角度的镜头,通过旋转或略微移动镜头即可很大程度上消除盲区,并达到“抵近观察”效果,在不增加手术通道暴露的情况下获得更多更明亮视野[7-8]。同时,在高倍率的显微镜下操作时,常常重新聚焦、调整床位,增加了手术时间。此外,近年来高分辨率和3D神经内镜的出现进一步弥补了与显微镜视觉差距[9]。
我们认为神经内镜技术治疗脑室相关的深部肿瘤的另一个优势是:术中可同时进行脑脊液通路重建,而显微镜手术受限于视野角度和深度,有时难以直视盲区的梗阻因素,可能造成脑积水不缓解。有研究指出脑室相关肿瘤显微手术后的脑积水发生率为34.7%,而本组术后脑积水仅为14.3%[10]。本组21例中多达17例术前合并梗阻性脑积水,我们在尽量全切肿瘤后,换用不同角度内镜针对性观察脑脊液循环通路的通畅性,根据具体情况分别行内镜下第三脑室底造瘘术、透明隔造瘘术或室间孔成形术;同时术中对脑室内血性脑脊液充分稀释置换、探查疏通脑室结构以及对循环瓶颈或死角部位小血凝块直视下清除,降低了术后脑积水风险。我们认为脑脊液循环重建应作为此类手术规划中的基本目标,即使肿瘤无法全切,患者的高颅压症状也可有效缓解,且神经内镜下造瘘等技术已相当成熟,可保证手术效果与安全[11]。
3.2 术中辅助工具的使用经验神经导航是内镜手术成功的一大助力。本研究显示,神经内镜良好的可视化效果,可更清晰观察肿瘤的边界及毗邻结构,同时神经导航提供实时定位,两者优势结合,可优化手术路径,有助于内镜通道的正确建立,提高肿瘤切除程度。
传统的脑牵开自持系统将压力不均匀施加于脑组织,可影响脑组织局部灌注,导致继发性脑损伤[12]。本研究在保证操作空间的基础上选择较小直径的一次性牵开固定器,其“钝性穿刺”达到肿瘤部位比脑实质造瘘的创伤更小,穿刺过程中由于其表面的圆滑,可相对安全分离白质纤维,尽可能减少纤维束的离断等永久性损伤[13]。且在穿刺过程中,通过透明的牵开器壁可直接观察到出血,此时缓慢退出牵开器可及时止血。我们认为一次性牵开固定器优点在于:①保护手术通道周围脑组织不受进出手术器械损伤,解决镜头后方视野盲区的问题;②通道至少能同时容纳2件长器械操作,确保精准操作;③圆滑表面使压力均匀分布对脑实质损伤更小[14-15];④保护镜头免受污染,保持视野清晰。但当术中意外出血且出血位置角度不佳时,一次性牵开固定器有限的操作空间可使止血变得困难,助手的熟练配合和预留的显微手术空间有助于解决此问题。
超声吸引器可乳化并安全吸除一些质地较韧肿瘤,有效提高手术效率[16-17]。本研究根据肿瘤质地逐步增加功率,以不过度破坏较大肿瘤血管为度。我们的体会是多数室管膜瘤和中枢神经细胞瘤的质地和血供程度相对更适合超声吸引器,即使体积较大也可安全有效减瘤。我们从肿瘤相对游离侧缓慢吸除肿瘤,有明显出血时及时切换双极电凝止血,止血完毕继续使用超声吸引器直至减瘤充分。通过内镜可清楚地观察充分止血后的瘤床及周围光滑的脑室壁,上述两种肿瘤病例术后均无复发或严重并发症者。在处理质地过于坚硬的肿瘤时,较大功率的超声吸引器也难以乳化其组织,须使用剪刀等锐性器械在狭窄通道内减瘤。此时对内镜下术者操作能力和器械要求相对较高,需具有一定经验基础才能操作。
关于内镜支架,我们的体会是:内镜支架不如手持内镜灵活,难以在术中及时调整内镜的位置和旋转镜头,手动下实时地移动镜头有利于弥补内镜缺乏立体视觉的缺点。故对于较大的或血供丰富的病变时,我们倾向于手动持镜;而较小的病变更适合支架持镜。即使在手动持镜时,下口直径16 mm的一次性牵开固定器内绝大部分时间内可充分保证双人两手甚至三手操作。但手动持镜对助手能力、经验要求较高,须与主刀有较好的配合默契度。
3.3 神经内镜技术治疗脑室相关深部肿瘤的局限性有观点认为,神经内镜手术适合切除直径<2 cm、完全位于脑室内的肿瘤,对于直径>4 cm实体瘤单纯内镜手术不再合适,但对于较大囊性病变仍可在内镜下完全切除[18-19]。
本组病例肿瘤均以实质性为主,平均直径34.8 mm,其中4例肿瘤的最大直径超过60 mm,我们仍在神经内镜下进行了切除,全切率达到71%。对于较大肿瘤,内镜或显微镜下均无法显露肿瘤整体。我们的手术体会是:首先应积极探查肿瘤起源部位或供血血管,尽早控制肿瘤血供,内镜的观察角度优势往往有利于提前发现传统视野盲区内血供或肿瘤起源。若实质性肿瘤体积过大无法直视处理其起源或供血时,选择从肿瘤相对游离侧分块瘤内切除,缩小肿瘤体积后再次探查,往往可顺利发现其主要血供来源。此时需注意用流动温盐水冲洗、棉片或吸收性明胶海绵保护周边阻挡出血沿脑室系统扩展、吸收性明胶海绵压迫或双极电凝止血,微小的出血常在冲洗下自行停止。需注意邻近正常室管膜应尽量减少双极使用,对室管膜结构的损伤可增加脑室内粘连的形成概率[20],本组术后新发1例脑积水可能与此有关。个别情况下,由于角度位置问题确难以有效止血操作时,也可及时转换为显微镜下操作。我们认为:肿瘤大小并非限制内镜使用的最主要因素,术前应充分利用多模态影像学技术对肿瘤质地和血供,包括血供来源位置等因素充分评估,术中利用内镜观察角度优势对上述关键位置及早控制,有助于提高内镜下切除较大肿瘤的安全性。此外,肿瘤的血供丰富,血液进入脑脊液会严重影响视野,我们采用气象条件下经内镜工作通道切除肿瘤以避免视野污染,待无明显出血后,可在液相环境下观察是否止血充分和探查脑脊液循环通路的通畅性。
传统的显微手术中视觉焦点通常保持在手术区域中心,而内镜通常保持在术野一侧以防止器械阻挡镜头,并会占用小部分手术通道。当手术器械长轴过于靠近镜头轴线时,可影响观察器械前端操作。我们的解决方法是旋转手术器械或略微移动镜头避免直线排列。当病变背后的结构被遮挡,不可直接盲目牵拉,尤其避免损伤相对脆弱的脑室内静脉结构,应将镜头移向侧方看清结构或换用更大角度镜头。目前的内镜手术专用器械已发展相当成熟,产品设计时已考虑视野和狭窄空间操作问题,如可变视野的内镜、弯头可调整剪刀,头端可旋转取瘤钳等[7, 21]。总之,整个手术过程需尽量轻柔谨慎,灵活地运用器械与角度镜头,充分发挥内镜的视野优势。同时应准备好显微镜及相关器械,当单纯的神经内镜手术无法满足要求时可流畅转换为显微镜手术或内镜辅助下的显微镜手术,以此降低手术风险。
内镜手术操作系从显微手术转化而来,其主要原则和技巧并无过大区别,良好的显微手术基础有利于提高内镜手术效率。但从显微镜手术到内镜手术的转化存在一定困难,包括:3D转变为2D的视觉效果、有限空间内器械“打架”、术中出血控制等[22]。经验积累可在很大程度上减少所需手术通道和操作相关脑损伤,年轻医师可通过在模型或尸头操作、参加手术培训班或利用实验室和模拟设备进行训练,以此缩短神经内镜的学习曲线[22-23]。本团队近3年来采用手术录像回顾、尸头解剖、线上交流、线下内镜模拟器练习、VR技术训练等方式培养年轻医师,在已完成基本显微操作培训基础上,以能在内镜下进行熟练一助操作或主刀完成小于2.5 cm直径肿瘤为培训目标,所需的学习曲线约9个月。
综上所述,本研究将神经内镜结合术中辅助工具应用于脑室相关的深部肿瘤手术,取得了良好临床疗效,能保证肿瘤的切除率和手术安全性,值得进一步研究探索。但本研究病例数量有限,且为单中心的回顾性研究,尚不能提供高级别的循证医学证据。仍需要多中心的随机临床对照试验来证实神经内镜技术应用于脑室相关的深部肿瘤手术的真正价值。
| [1] |
TOMLINSON S B, HENDRICKS B K, TORREGROSSA F, et al. Innovations in the art of microneurosurgery for reaching deep-seated cerebral lesions[J]. World Neurosurg, 2019, 131: 321-327. DOI:10.1016/j.wneu.2019.06.210 |
| [2] |
KIM M H. Transcortical endoscopic surgery for intraventricular lesions[J]. J Korean Neurosurg Soc, 2017, 60(3): 327-334. DOI:10.3340/jkns.2017.0101.008 |
| [3] |
神经内镜技术临床应用专家共识编写组. 神经内镜手术技术治疗脑室脑池系统疾病中国专家共识[J]. 中华神经外科杂志, 2016, 32(8): 757-766. Consensus Working Group for Clinical Application of Neuroendoscopy. Consensus of Chinese expert panel on neuroendoscopic surgery techniques for treatment of ventricular and cistern system diseases[J]. Chin J Neurosurg, 2016, 32(8): 757-766. DOI:10.3760/cma.j.issn.1001-2346.2016.08.001 |
| [4] |
王强, 徐维林, 张宏伟, 等. 术中超声联合术中磁共振对脑深部肿瘤切除的初步探讨[J]. 解放军医学院学报, 2016, 37(6): 576-578. WANG Q, XU W L, ZHANG H W, et al. Intraoperative ultrasound combined magnetic resonance imaging in resection of deep-seated brain leisions[J]. Acad J Pla Postgrad Med Sch, 2016, 37(6): 576-578. DOI:10.3969/j.issn.2095-5227.2016.06.014 |
| [5] |
AKIYAMA Y, WANIBUCHI M, MIKAMI T, et al. Rigid endoscopic resection of deep-seated or intraventricular brain tumors[J]. Neurol Res, 2015, 37(3): 278-282. DOI:10.1179/1743132814y.0000000439 |
| [6] |
SCHROEDER H W. General principles and intraventricular neuroendoscopy: endoscopic techniques[J]. World Neurosurg, 2013, 79(2 suppl): S14. e23-S14. e28. DOI:10.1016/j.wneu.2012.02.031 |
| [7] |
GAAB M R. Instrumentation: endoscopes and equipment[J]. World Neurosurg, 2013, 79(2 suppl): S14. e11-S14. e21. DOI:10.1016/j.wneu.2012.02.032 |
| [8] |
AKIYAMA O, MATSUSHIMA K, GUNGOR A, et al. Microsurgical and endoscopic approaches to the pulvinar[J]. J Neurosurg, 2017, 127(3): 630-645. DOI:10.3171/2016.8.jns16676 |
| [9] |
SHOAKAZEMI A, EVINS A I, BURRELL J C, et al. A 3D endoscopic transtubular transcallosal approach to the third ventricle[J]. J Neurosurg, 2015, 122(3): 564-573. DOI:10.3171/2014.11.jns14341 |
| [10] |
付强, 李绍山, 刘力豪, 等. 幕上脑室及脑室旁肿瘤术后继发梗阻性脑积水的预防及治疗[J]. 新疆医学, 2019, 49(6): 545-550. FU Q, LI S S, LIU L H, et al. Prevention and treatment of postoperative obstructive hydrocephalus to supratentorial intraventricular and paraventricular tumors[J]. Xinjiang Med, 2019, 49(6): 545-550. |
| [11] |
DEMERDASH A, ROCQUE B G, JOHNSTON J, et al. Endoscopic third ventriculostomy: a historical review[J]. Br J Neurosurg, 2017, 31(1): 28-32. DOI:10.1080/02688697.2016.1245848 |
| [12] |
ZHONG J, DUJOVNY M, PERLIN A R, et al. Brain retraction injury[J]. Neurol Res, 2003, 25(8): 831-838. DOI:10.1179/016164103771953925 |
| [13] |
EICHBERG D G, BUTTRICK S, BRUSKO G D, et al. Use of tubular retractor for resection of deep-seated cerebral tumors and colloid cysts: single surgeon experience and review of the literature[J]. World Neurosurg, 2018, 112: e50-e60. DOI:10.1016/j.wneu.2017.12.023 |
| [14] |
SHARIF S, SHAIKH M Y, ALI S M. Novel tool for minimally invasive brain surgery: syringe port system[J]. World Neurosurg, 2019, 131: 339-345. DOI:10.1016/j.wneu.2019.06.202 |
| [15] |
JO K W, SHIN H J, NAM D H, et al. Efficacy of endoport-guided endoscopic resection for deep-seated brain lesions[J]. Neurosurg Rev, 2011, 34(4): 457-463. DOI:10.1007/s10143-011-0319-4 |
| [16] |
黄海常, 农胜德, 陆明雄, 等. 超声吸引器在颅内肿瘤显微外科手术中的应用进展[J]. 中外医学研究, 2019, 17(2): 172-174. HUANG H C, NONG S D, LU M X, et al. Application progress of cavitron ultrasonic surgical aspirator in microsurgery of intracranial tumor[J]. Chin Foreign Med Res, 2019, 17(2): 172-174. |
| [17] |
IBÁÑEZ-BOTELLA G, SEGURA M, DE MIGUEL L, et al. Purely neuroendoscopic resection of intraventricular tumors with an endoscopic ultrasonic aspirator[J]. Neurosurg Rev, 2019, 42(4): 973-982. DOI:10.1007/s10143-018-1011-8 |
| [18] |
QIAO L, SOUWEIDANE M M. Purely endoscopic removal of intraventricular brain tumors: a consensus opinion and update[J]. Minim Invasive Neurosurg, 2011, 54(4): 149-154. DOI:10.1055/s-0031-1284386 |
| [19] |
SCHROEDER H W S. Intraventricular tumors[J]. World Neurosurg, 2013, 79(2): S17. e15-S17. e19. DOI:10.1016/j.wneu.2012.02.023 |
| [20] |
詹潮鸿, 张向阳, 肖格磊. 脑积水发病机制的研究进展[J]. 中南大学学报(医学版), 2019, 44(10): 1188-1195. ZHAN C H, ZHANG X Y, XIAO G L. Advances in research on the pathogenesis of hydrocephalus[J]. J Central South Univ Med Sci, 2019, 44(10): 1188-1195. |
| [21] |
EBNER F H, ROSER F, RODER C, et al. Rigid, variable-view endoscope in neurosurgery: first intraoperative experience[J]. Surg Innov, 2015, 22(4): 390-393. DOI:10.1177/1553350614543382 |
| [22] |
YADAV Y R, BAJAJ J, PARIHAR V, et al. Practical aspects of neuroendoscopic techniques and complication avoidance: a systematic review[J]. Turk Neurosurg, 2018, 28(3): 329-340. DOI:10.5137/1019-5149.JTN.18923-16.1 |
| [23] |
YADAV Y R, PARIHAR V S, RATRE S, et al. Avoiding complications in endoscopic third ventriculostomy[J]. J Neurol Surg A Cent Eur Neurosurg, 2015, 76(6): 483-494. DOI:10.1055/s-0035-1551828 |




