先天性心脏病(congenital heart disease, CHD)是全世界最常见的先天性缺陷[1],大量CHD患者需要接受体外循环下心脏畸形的手术治疗。随着麻醉、手术技术、体外循环、心肌保护及围术期监护治疗技术的进步,先心病术后患儿的生存率有了显著提高。肺炎是CHD儿童患者术后较常见的并发症,重症肺炎则是延长重症监护病房停留时间、机械通气时间、增加医疗费用和术后死亡的重要原因[2-3]。研究儿童先心病手术后发生重症肺炎的危险因素,并由此创建临床预测模型,可能有助于临床预判儿童先心病术后发生重症肺炎的风险程度,并提前实施针对性的干预措施,最终改善儿童先心病的手术效果。国内外关于先心病手术后发生重症肺炎的预测模型的相关研究报道鲜见[2, 4-5]。本研究基于本科近年来先心病手术治疗病例的相关资料,创建儿童先心病手术后发生重症肺炎的临床预测模型,并构建列线图,初步探讨该模型的临床价值。
1 资料与方法 1.1 研究对象回顾性分析2014年1月至2018年10月重庆医科大学附属儿童医院胸心外科行手术治疗的先天性心脏病患者的临床资料。所有入组对象在入院时签署知情同意书,本研究取得本院伦理委员会批准[(2019)年伦审(研)第(258)号]。纳入标准:接受体外循环下手术治疗的先天性心脏病儿童患者。排除标准:①术前1周内存在肺炎;②临床资料不全的病例。根据临床症状、实验室检查和影像学检查诊断肺炎并评估严重程度。肺炎的临床诊断标准:胸片显示新发或加重的肺部浸润影(无法用其他原因解释),咳脓痰或气管内有脓性分泌物,并具有以下任意一项者:①支气管肺泡灌洗液(BALF)或防污染毛刷采样定量培养阳性;②下呼吸道培养和血培养均阳性且为同一病原体;③下呼吸道培养和胸水培养均阳性且为同一病原体[6]。重症肺炎的诊断标准为临床表现和/或辅助检查存在以下任一项者:①呼吸空气条件下,SaO2≤0.92;②呼吸空气条件下,RR >70次/min(婴儿),RR>50次/min(年长儿),除外发热、哭吵等因素的影响;③呼吸困难:胸壁吸气性凹陷、鼻翼扇动;④胸片等影像学资料证实双侧或多肺叶受累或肺叶实变并肺不张、胸腔积液或短期内病变进展者[7]。
将2014年1月至2017年12月的病例纳入建模组,2018年1-10月的病例纳入验证组。
1.2 数据采集从病历资料中获取以下信息:①一般信息(性别、年龄、体质量);②术前资料(先心病手术风险评分RACHS-1、是否合并肺动脉高压、术前住院时间、术前总蛋白、术前白蛋白);③术中资料(麻醉时间、体外循环时间、主动脉阻断时间、手术时间、术中输血)。将性别,肺动脉高压和输血设置为二分类变量。年龄、体质量、术前住院时间、麻醉时间、体外循环时间、主动脉阻断时间、手术时间、术前总蛋白和术前白蛋白按最优尺度回归分组(表 1)。按照相关文献的研究方法,根据RACHS-1评分将患者分为两组[8-11]。
| 基线资料 | 建模组(n=1 415)a | 验证组(n=395)a | |||||
| 有(n=144) | 无(n=1 271) | P | 有(n=38) | 无(n=357) | P | ||
| 性别 | 0.799 | 0.081 | |||||
| 男 | 76(52.8) | 685(53.9) | 15(39.5) | 194(54.3) | |||
| 女 | 68(47.2) | 586(46.1) | 23(60.5) | 163(45.7) | |||
| 年龄/月 | < 0.001 | < 0.001 | |||||
| < 6 | 34(23.6) | 99(7.8) | 14(36.8) | 20(5.6) | |||
| 6~ < 12 | 55(38.2) | 229(18.0) | 8(21.1) | 72(20.2) | |||
| 12~24 | 38(26.4) | 318(25.0) | 12(31.6) | 117(32.8) | |||
| > 24 | 17(11.8) | 625(49.2) | 4(10.5) | 148(41.4) | |||
| 体质量/kg | < 0.001 | < 0.001 | |||||
| < 6 | 39(27.1) | 112(8.8) | 13(34.2) | 38(10.6) | |||
| 6~12 | 96(66.7) | 663(52.2) | 23(60.5) | 215(60.2) | |||
| > 12 | 9(6.2) | 496(39.0) | 2(5.3) | 104(29.1) | |||
| 肺动脉高压 | 0.027 | 0.531 | |||||
| 有 | 95(66.0) | 716(56.3) | 17(44.7) | 141(39.5) | |||
| 无 | 49(34.0) | 555(43.7) | 21(55.3) | 216 (60.5) | |||
| RACHS-1评分 | < 0.001 | < 0.001 | |||||
| ≤2 | 38(26.4) | 1103(86.8) | 10(26.3) | 311(87.1) | |||
| ≥3 | 104(73.6) | 168(13.2) | 28(73.7) | 46(12.9) | |||
| 术前住院时间/h | < 0.001 | 0.004 | |||||
| < 96 | 9(6.3) | 299(23.5) | 1(2.6) | 78(21.8) | |||
| 96~168 | 59(41.0) | 611(48.1) | 17(44.7) | 166(46.5) | |||
| > 168 | 76(52.7) | 361(28.4) | 20(52.6) | 113(31.7) | |||
| 麻醉时间/min | < 0.001 | < 0.001 | |||||
| < 250 | 48(33.3) | 1 040(81.8) | 9(23.7) | 305(85.4) | |||
| 250~290 | 44(30.6) | 171(13.5) | 16(42.1) | 41(11.5) | |||
| > 290 | 52(36.1) | 60(4.7) | 13(34.2) | 11(3.1) | |||
| 体外循环时间/min | < 0.001 | < 0.001 | |||||
| < 75 | 7(4.9) | 726(57.1) | 5(13.2) | 223(62.5) | |||
| 75~ < 105 | 32(22.2) | 377(29.7) | 8(21.0) | 87(24.4) | |||
| 105~125 | 36(25.0) | 105(8.3) | 7(18.4) | 31(8.7) | |||
| > 125 | 69(47.9) | 63(4.9) | 18(47.4) | 16(4.4) | |||
| 主动脉阻断时间/min | < 0.001 | < 0.001 | |||||
| < 55 | 32(22.2) | 1 039(81.7) | 12(31.6) | 291(81.5) | |||
| 55~75 | 43(29.9) | 142(11.2) | 7(18.4) | 39(10.9) | |||
| > 75 | 69(47.9) | 90(7.1) | 19(50.0) | 27(7.6) | |||
| 手术时间/min | < 0.001 | < 0.001 | |||||
| < 120 | 1(0.7) | 135(10.6) | 0(0.0) | 58(16.3) | |||
| 120~180 | 46(31.9) | 894(70.3) | 9(23.7) | 250(70.0) | |||
| > 180 | 97(67.4) | 242(19.0) | 29(76.3) | 49(13.7) | |||
| 术中输血 | < 0.001 | < 0.001 | |||||
| 有 | 98(68.1) | 291(22.9) | 27(71.1) | 94(26.3) | |||
| 无 | 46(31.9) | 980(77.1) | 11(28.9) | 263(73.7) | |||
| 术前总蛋白/g·L-1 | 0.002 | 0.437 | |||||
| < 59 | 30(20.8) | 148(11.6) | 5(13.2) | 33(9.2) | |||
| ≥59 | 114(79.2) | 1 123(88.4) | 33(86.8) | 324(90.8) | |||
| 术前白蛋白/g·L-1 | 0.009 | 0.401 | |||||
| < 39 | 8(5.6) | 26(2.0) | 2(5.3) | 10(2.8) | |||
| ≥39 | 136(94.4) | 1 245(98.0) | 36(94.7) | 347(97.2) | |||
| a:两组分别按术后是否发生重症肺炎分为“有”“无”两个亚组 | |||||||
1.3 统计学分析
采用SPSS 24软件、RStudio软件进行统计分析。本研究中所有数据均为分类变量,采用n(%)表示,组间比较采取χ2检验。使用多重共线性检测用以排除可能的混杂因素。相关的危险因素采取单因素Logistic回归分析,为避免有意义的因素被筛选出去,将P < 0.1设定为有统计学意义,将单因素分析有统计学意义的因素纳入多因素Logistic回归分析,最终还有统计学意义的即为独立危险因素。如果方差膨胀因子(VIF)大于10,也不会被纳入到多因素Logistic回归中。将最终具有统计学意义的独立危险因素使用列线图工具进行可视化,列线图最上方的“分数”是对应的评分分数,下方分别列举的是每个独立危险因素所对应的评分,根据每个因素所对应的具体得分,并将所有因素的得分相加即可得到“总分”,通过该分值即可获得术后发生重症肺炎的预测概率。最后,将使用另一组不同时间的数据集进行外部验证。
使用受试者工作特征曲线(ROC)下的面积(AUC)及校准曲线进行预测模型的区分能力和校准度性能评估。区分能力是指其区分术后发生重症肺炎的患者和没有发生重症肺炎患者的能力,校准性能是判断预测结果和实际结果的一致性程度。AUC值在0.5~1.0,AUC值越接近1,则预测模型的区分度越好。一般而言,AUC值在0.5~0.75被认为是可以接受的,而AUC值>0.75则表示该模型具有良好的区分能力[12]。
2 结果 2.1 一般资料共纳入1 810名患者,其中建模组1 415例,验证组395例。在建模组中,有144例患者术后发生了重症肺炎。在验证组中,有38例患者发生了重症肺炎。与没有发生重症肺炎组相比,发生重症肺炎组的年龄和体质量显著降低(P < 0.001),RACHS-1评分更高,术前的住院时间明显更长,术中输血的发生率更高(P < 0.001)。在非重症肺炎组中,麻醉时间、体外循环时间、主动脉阻断时间和手术时间均明显短于重症肺炎组(P < 0.001,表 1)。
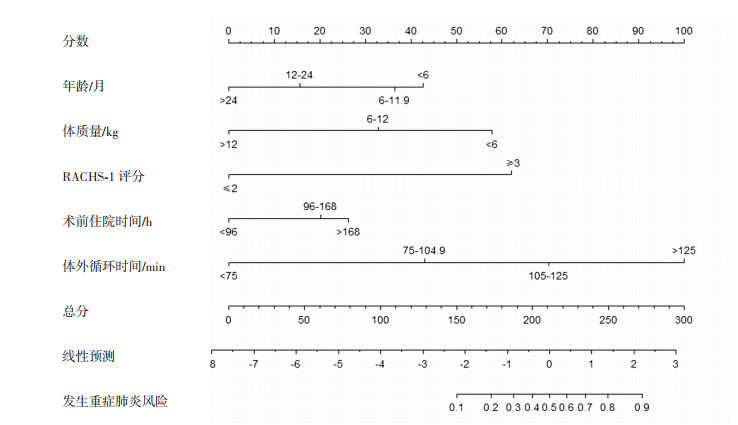
2.2 风险预测模型的构建单因素Logistic回归分析显示,建模组年龄、体质量、肺动脉高压、RACHS-1评分、术前住院时间、麻醉时间、体外循环时间、主动脉阻断时间、术中输血、术前总蛋白及术前白蛋白(P < 0.1)是相关的危险因素,将它们纳入多因素分析中,最终结果显示年龄、体质量、RACHS-1评分、术前住院时间、体外循环时间这5个因素是CHD术后发生重症肺炎的独立危险因素(表 2)。上述独立风险因素的多重共线性检测的方差膨胀因子VIF分别为2.485、2.478、1.297、1.073和1.355,表明5个独立风险因素之间没有多重共线性。基于年龄、体质量、RACHS-1评分、术前住院时间、体外循环时间等5个独立的危险,将Logistic回归方程图形化为个体化列线图预测模型(图 1)。
| 基线资料 | 单因素分析 | 多因素分析 | ||||
| OR(95%CI) | P | OR(95%CI) | P | |||
| 性别 | 1.046(0.741-1.477) | 0.799 | NA | |||
| 年龄/岁 | < 6 | |||||
| 6~ < 12 | 0.699(0.429-1.140) | 0.151 | 0.894(0.384-2.079) | 0.795 | ||
| 12~24 | 0.348(0.208-0.582 | < 0.001 | 0.410(0.157-1.073) | 0.069 | ||
| > 24 | 0.079(0.043-0.147) | < 0.001 | 0.230(0.070-0.762) | 0.016 | ||
| 体质量/kg | < 6 | |||||
| 6~12 | 0.416(0.273-0.635) | < 0.001 | 0.340(0.151-0.765) | 0.009 | ||
| > 12 | 0.052(0.025-0.111) | < 0.001 | 0.114(0.030-0.441) | 0.002 | ||
| 肺动脉高压 | 0.665(0.463-0.956) | 0.027 | NA | |||
| RACHS-1评分 | 18.314(12.220-27.447) | < 0.001 | 8.848(5.129-15.262) | < 0.001 | ||
| 术前住院时间/h | < 96 | |||||
| 96~168 | 3.208(1.570-6.557) | 0.001 | 2.039(0.834-4.989) | 0.118 | ||
| > 168 | 6.994(3.446-14.194) | < 0.001 | 2.507(1.025-6.131) | 0.044 | ||
| 麻醉时间/min | < 250 | NA | ||||
| 250~290 | 5.575(3.591-8.655) | < 0.001 | NA | |||
| > 290 | 18.778(11.727-30.067) | < 0.001 | NA | |||
| 体循时间/min | < 75 | |||||
| 75~ < 105 | 8.803(3.849-20.133) | < 0.001 | 3.786(1.440-9.952) | 0.007 | ||
| 105~125 | 35.559(15.427-81.964) | < 0.001 | 8.820(2.459-31.641) | 0.001 | ||
| > 125 | 113.592(50.081-257.646) | < 0.001 | 25.873(5.738-116.665) | < 0.001 | ||
| 主动脉阻断时间/min | < 55 | NA | ||||
| 55~75 | 9.832(6.023-16.050) | < 0.001 | NA | |||
| > 75 | 24.893(15.538-39.879) | < 0.001 | NA | |||
| 手术时间/min | < 120 | NA | ||||
| 120~180 | 6.946(0.950-50.786) | 0.056 | NA | |||
| > 180 | 54.112(7.462-392.410) | < 0.001 | NA | |||
| 术中输血 | 7.175(4.936-10.428) | < 0.001 | NA | |||
| 术前总蛋白 | 0.501(0.323-0.775) | 0.002 | NA | |||
| 术前白蛋白 | 0.355(0.158-0.800) | 0.012 | NA | |||
|
| 按照每个因素所对应的值,画一条直线确定对应的分数,然后根据5个因素的总分,在发生重症肺炎风险上画一条直线,最终确定发生重症肺炎的可能性 图 1 发生重症肺炎风险预测列线图 |
2.3 风险预测模型的验证和评估
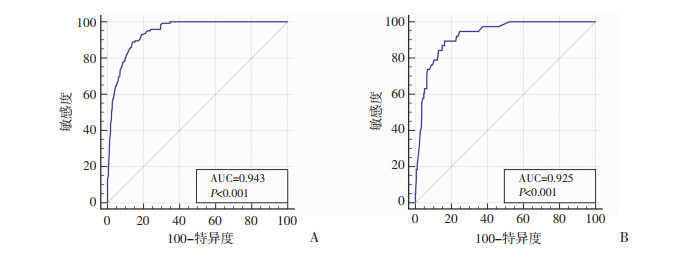
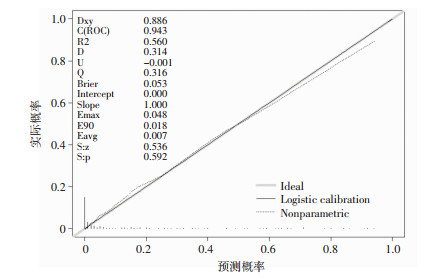
通过区分能力和校准度评价来验证模型的可靠性。通过分别绘制建模组及验证组的ROC曲线(图 2),并计算两组各自对应的AUC值。同时,使用ROC曲线比较了列线图和多因素Logistic回归分析出的5个独立危险因素的AUC值(表 3),差异均具有统计学意义(P < 0.05)。建模组和验证组的AUC值分别为0.942和0.925。两组校准图的P值分别为0.592和0.256(图 3、4),因此,模型的预测概率与实际概率相一致。
|
| 图 2 建模组(A)和验证组(B)的ROC曲线 |
| 变量 | 建模组 | 验证组 | |||||
| AUC | 95%CI | P值 | AUC | 95%CI | P值 | ||
| 列线图 | 0.943 | 0.929-0.954 | < 0.001 | 0.925 | 0.894-0.949 | < 0.001 | |
| 年龄 | 0.737 | 0.713-0.759 | < 0.001 | NA | NA | NA | |
| 体质量 | 0.705 | 0.681-0.729 | < 0.001 | NA | NA | NA | |
| RACHS-1评分 | 0.802 | 0.780-0.822 | < 0.001 | NA | NA | NA | |
| 术前住院时间 | 0.655 | 0.630-0.680 | < 0.001 | NA | NA | NA | |
| 体外循环时间 | 0.868 | 0.850-0.886 | < 0.001 | NA | NA | NA | |
|
| Logistic calibration为校准后曲线,ideal为标准曲线 图 3 建模组的校准图 |

|
| Logistic calibration为校准后曲线,ideal为标准曲线 图 4 验证组的校准图 |
3 讨论
重症肺炎是儿童心脏外科手术后死亡的主要原因之一[2]。临床上,先心病儿童体外循环心脏直视手术后一旦发生重症肺炎,将延长机械通气时间和/或重症监护病房的停留时间,增加病死率和医疗费用。研究先心病术后发生重症肺炎的相关危险因素并更早期地识别高危患者,对改善儿童先心病手术的临床转归、降低医疗费用有极重要的意义。尽管既往的研究揭示了先天性心脏病或者后天性心脏病体外循环手术后发生肺炎的相关危险因素,但少见儿童先天性心脏病体外循环术后重症肺炎的风险预测模型的相关研究[2, 4-5, 13]。而风险预测模型较单纯的风险因素具有更精准的预判价值,为更早期科学制定临床诊疗和防治决策提供更加有力的支持。另外,早期预测并告知可能的风险,有助于家属做好相应的心理和费用方面的准备,有利于构建更加和谐的医患关系[14]。
本研究纳入了接受体外循环下心脏手术的1 810例患者,其中建模组1 415例,共13个预测变量被纳入分析。分析显示本组患儿发生先心病术后重症肺炎的危险因素是年龄、体质量、RACHS-1评分、术前住院时间、体外循环时间,以该5项指标联合建立预测模型。由于没有现成的相似的风险预测模型可以比较,本研究构建了包含395例患儿的外部验证数据集来验证该模型。验证结果显示建模组和验证组的AUC值分别为0.942和0.925,均大于0.75,因此,该模型对患者术后是否发生重症肺炎有良好的预测能力。两组校准图的P值分别为0.592和0.256,显示预测结果和实际结果具有较好的一致性。所以我们认为该模型有助于重症监护病房的医护人员早期预测患者术后发生重症肺炎的风险。根据Logistic回归方程制作的列线图,将多个统计预测模型简化为发生概率的数字估计[15]。根据该列线图,临床医护人员可以将各危险因素对应的分值求和得到总分,通过总分预判先心病患儿手术后发生重症肺炎的概率,从而早期决策下一步诊疗措施,包括严密监测临床表现、影像学及实验室结果,同时术后加强气道管理,当然,必要时直接采取治疗性抗生素进行干预。列线图操作简便,更具有临床使用价值。
既往的研究显示,体外循环心脏手术后发生肺炎的危险因素包括年龄、体质量、RACHS-1评分、体外循环时间、输血等[2, 11, 16-17]。本研究中多因素Logistic回归分析提示先心病患儿体外循环手术后发生重症肺炎的独立危险因素为:年龄、体质量、RACHS-1评分、术前住院时间、体外循环时间。部分指标同已有的研究结果相似。体外循环可以导致全身炎症反应,机械通气、缺血再灌注也可导致肺部的损伤、渗出,发生非感染性肺炎。同时,先心病患儿总体的术前营养状态、免疫功能可能不及健康孩子,相当多的患儿可能处于无症状感染或者反复呼吸道感染等亚健康状态,手术创伤应激状态下,免疫力进一步受损,术后也相对容易发生感染性肺炎。文献显示,低体重、小年龄的患者因其自身呼吸道发育不完善,自身免疫功能尚未完全建立,先天性心脏病术后更容易发生重症肺炎[2, 4, 11]。本研究显示,RACHS-1评分≥3分的患者是术后发生重症肺炎最重要的一项因素,这与之前相关的分组研究结果基本一致[11]。目前已知BARKER等[13]基于患者术前数据制作的用于评估先心病术后主要感染的评分表,但是,还未有研究基于患者术前及术中的相关危险因素开发出一款能用于临床上预测先心病术后发生重症肺炎的简易的可视化模型。
本研究中纳入的患者在术前均使用第一代头孢类抗生素预防感染,在手术结束后,第一时间被转入重症监护病房,由重症监护病房的医护人员单独护理,在很大程度上减少了与患者家属及外界环境有关的感染影响,但仍不能排除存在交叉感染的可能性。尽管使用了RACHS-1评分来细化先心病复杂程度,同时RACHS-1评分为术后发生重症肺炎的有意义指标,但本研究中包含的先心病种类仍较多,不同种类的先心病对于术后发生重症肺炎的具体影响有待进一步研究。
本研究是一项单中心回顾性研究,收集的样本量尽管较多,但无法避免可能存在的选择偏倚。本研究纳入的观察指标仅考虑到临床住院的患儿,存在相关的危险因素考虑不全的可能。本研究尽管使用本中心不同时期的另一组患者来验证该模型,但未能在多中心、更大的样本数上得到验证。因此,未来可尝试进行多中心研究以进一步评估和验证该模型。本研究是有关儿童先天性心脏病体外循环术后重症肺炎的首个风险预测模型,尚无其他相似的风险预测模型进行对照评价。
综上所述,本研究通过多因素Logistic回归分析得出的危险因素,建立了先天性心脏病体外循环术后重症肺炎的风险预测模型,并制作相应的列线图。该模型预测能力较高,便于临床上早期识别儿童先天性心脏病体外循环术后重症肺炎的高风险患者,最终改善先心病患儿手术治疗的结局。同时,该风险预测模型有待于进一步多中心大样本的临床验证。
| [1] |
VAN DER LINDE D, KONINGS E E, SLAGER M A, et al. Birth prevalence of congenital heart disease worldwide: a systematic review and meta-analysis[J]. J Am Coll Cardiol, 2011, 58(21): 2241-2247. DOI:10.1016/j.jacc.2011.08.025 |
| [2] |
LEVY I, OVADIA B, EREZ E, et al. Nosocomial infections after cardiac surgery in infants and children: incidence and risk factors[J]. J Hosp Infect, 2003, 53(2): 111-116. DOI:10.1053/jhin.2002.1359 |
| [3] |
URREA M, PONS M, SERRA M, et al. Prospective incidence study of nosocomial infections in a pediatric intensive careunit[J]. Pediatr Infect Dis J, 2003, 22(6): 490-494. DOI:10.1097/01.inf.0000069758.00079.d3 |
| [4] |
GUARDIA CAMÍ M T, JORDAN GARCÍA I, URREA AYALA M. Nosocomial infections in pediatric patients following cardiac surgery[J]. An Pediatr (Barc), 2008, 69(1): 34-38. DOI:10.1157/13124216 |
| [5] |
VALERA M, SCOLFARO C, CAPPELLO N, et al. Nosocomial infections in pediatric cardiac surgery, Italy[J]. Infect Control Hosp Epidemiol, 2001, 22(12): 771-775. DOI:10.1086/501861 |
| [6] |
《中华儿科杂志》编辑委员会, 中华医学会儿科学分会呼吸学组, 中华医学会儿科学分会急救学组, 等. 儿童医院获得性肺炎管理方案(2010版)[J]. 中华儿科杂志, 2011, 49(2): 106-115. Editorial Board of Chinese Journal of Pediatrics, Subspecialty Group of Respiratory Diseases of CMA, The Subspecialty Group of Emergency of CMA, et al. The management of hospital acquired pneumonia in children (2010)[J]. Chin J Pediatr, 2011, 49(2): 106-115. DOI:10.3760/cma.j.issn.0578-1310.2011.02.008 |
| [7] |
中华医学会儿科学分会呼吸学组, 《中华儿科杂志》编辑委员会. 儿童社区获得性肺炎管理指南(2013修订)(下)[J]. 中华儿科杂志, 2013, 51(11): 856-862. Department of Respiratory Medicine of Pediatrics Branch of CMA, Editorial Board of Chinese Journal of Pediatrics. Guidelines for management of childhood community acquired pneumonia (for trial implementation) (Ⅱ)[J]. Chin J Pediatrics, 2013, 51(11): 856-862. DOI:10.3760/cma.j.issn.0578-1310.2013.11.012 |
| [8] |
JENKINS K J. Risk adjustment for congenital heart surgery: the RACHS-1 method[J]. Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu, 2004, 7: 180-184. DOI:10.1053/j.pcsu.2004.02.009 |
| [9] |
LACOUR-GAYET F, CLARKE D, JACOBS J, et al. The Aristotle score: a complexity-adjusted method to evaluate surgical results[J]. Eur J Cardiothorac Surg, 2004, 25(6): 911-924. DOI:10.1016/j.ejcts.2004.03.027 |
| [10] |
JENKINS K J, GAUVREAU K, NEWBURGER J W, et al. Consensus-based method for risk adjustment for surgery for congenital heart disease[J]. J Thorac Cardiovasc Surg, 2002, 123(1): 110-118. DOI:10.1067/mtc.2002.119064 |
| [11] |
GARCÍA H, CERVANTES-LUNA B, GONZÁLEZ-CABELLO H, et al. Risk factors for nosocomial infections after cardiac surgery in newborns with congenital heart disease[J]. Pediatr Neonatol, 2018, 59(4): 404-409. DOI:10.1016/j.pedneo.2017.11.014 |
| [12] |
STYNES S, KONSTANTINOU K, OGOLLAH R, et al. Clinical diagnostic model for sciatica developed in primary care patients with low back-related leg pain[J]. PLoS ONE, 2018, 13(4): e0191852. DOI:10.1371/journal.pone.0191852 |
| [13] |
BARKER G M, O'BRIEN S M, WELKE K F, et al. Major infection after pediatric cardiac surgery: a risk estimationmodel[J]. Ann Thorac Surg, 2010, 89(3): 843-850. DOI:10.1016/j.athoracsur.2009.11.048 |
| [14] |
杨立, 常云峰, 蔡继峰, 等. 医疗损害责任纠纷原因分析:以医院、患者及社会为视角[J]. 中国司法鉴定, 2018(4): 32-36. YANG L, CHANG Y F, CAI J F, et al. Analysis of the causes of medical disputes: from the aspects of hospitals, patients and the society[J]. Chin J Forensic Sci, 2018(4): 32-36. DOI:10.3969/j.issn.1671-2072.2018.04.006 |
| [15] |
IASONOS A, SCHRAG D, RAJ G V, et al. How to build and interpret anomogram for cancer prognosis[J]. J Clin Oncol, 2008, 26(8): 1364-1370. DOI:10.1200/JCO.2007.12.9791 |
| [16] |
TANG C W, LIU P Y, HUANG Y F, et al. Ventilator-associated pneumonia after pediatric cardiac surgery in southernTaiwan[J]. J Microbiol Immunol Infect, 2009, 42(5): 413-419. |
| [17] |
YU X D, CHEN M L, LIU X, et al. Risk factors of nosocomial infection after cardiac surgery in children with congenital heart disease[J]. BMC Infect Dis, 2020, 20(1): 64. DOI:10.1186/s12879-020-4769-6 |




