系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种累及肾脏等多系统的自身免疫性疾病,其中38.3%的患者可发展为狼疮性肾炎(lupus nephritis,LN),不同病理分型LN的疾病活动性及其预后不同[1]。目前大多数研究认为,相对于LN-Ⅱ/Ⅴ,以毛细血管内细胞增多为主要病变的LN-Ⅲ/Ⅳ属重型,是临床治疗的难点[2-3]。而伴和不伴膜性病变(LN-Ⅴ)的LN-Ⅲ/Ⅳ相比,两者对治疗的反应及预后尚有争议[4-6]。此外,在我国超过30%的LN患者可在20年内进展为终末期肾脏病(end-stage renal disease,ESRD)[3],早期识别高危患者非常重要。基于此,本研究分析LN-Ⅱ/Ⅴ和LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ),LN-Ⅲ/Ⅳ和LN-Ⅲ/Ⅳ+Ⅴ之间疾病活动性和预后的差异,探索ESRD的危险因素,为临床诊治提供一定的参考。
1 资料与方法 1.1 病例资料共纳入2013-2018年本院住院并确诊为LN的305例患者,其中男性62例,女性243例,男:女为1 :3.9,发病年龄(31.1±12.5)岁,病程(40.4±15.7)个月。纳入标准: ①初次诊断为LN,符合美国风湿病协会1997年修订的SLE诊断标准[7],伴肾损害表现(如蛋白尿、血尿或伴肾功能不全);②行超声引导下经皮肾穿刺,病理结果按2018年国际肾脏病/肾脏病理协会(ISN/RPS)分型方案分型[8];③有完整的临床表现记录和实验室检查。排除标准: ①病历资料不完整;②少见的病理分型: Ⅰ型(仅1例)和Ⅵ型(仅1例)。本研究获得陆军军医大学第一附属医院医学伦理委员会批准(KY2019119),并免除知情同意。
1.2 分组以ISN/RPS2018分型方案为标准,将患者按肾脏病理分型是否有“毛细血管内细胞增多”病变分为: ①非毛细血管内细胞增多性LN: LN-Ⅱ/Ⅴ组;②毛细血管内细胞增多性LN: LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)组。
1.3 观察指标 1.3.1 临床指标选择疾病活动性相关的临床指标,包括浆膜炎、皮疹、关节痛、脱发、发热、口腔溃疡、光敏感。
1.3.2 实验室指标血常规、尿常规、自身抗体(抗SSA、Sm、ds-DNA、AnuA抗体)等。判断为异常的标准: ①白细胞减少:白细胞 < 4×109/L;②贫血:血红蛋白 < 110 g/L(女)或120 g/L(男);③血小板减少:血小板 < 100×109/L;④补体C3减少: C3 < 0.8 g/L;⑤低蛋白血症:白蛋白 < 30 g/L;⑥高尿酸血症:男性尿酸(UA)>420 μmol/L,女性UA>360 μmol/L;⑦血尿:高倍镜镜下红细胞>5/HP;⑧大量尿蛋白:尿蛋白>3.5 g/24 h;⑨血肌酐增高:血肌酐≥133 μmol/L;⑩ESRD:肾小球滤过率 < 15 mL/(min·1.73 m2)。
1.3.3 LN病理指数参照美国国立卫生研究院关于LN活动性指数(activity index, AI)和慢性化指数(chronic index, CI)评分系统。
1.3.4 系统性红斑狼疮疾病活动性指数(systemic lupus erythematosus disease activity index, SLEDAI)参照SLEDAI-2K计分法进行评估。
1.3.5 随访及终点事件通过患者在本院就诊记录以及电话咨询等方式随访患者疾病进展情况和生存状态,末次随访时间为2019年12月,中位随访时间为59.5个月。终点事件:死亡。
1.4 统计学分析采用SPSS 20.0统计学软件进行分析,计量资料以x±s表示,非正态分布数据用Mann-Whitney U检验,正态分布数据用t检验;计数资料行χ2检验。运用单因素Logistic回归分析评估终末肾病的危险因素,单因素分析有统计学意义(P < 0.1)或有临床意义的变量纳入多因素Logistic回归分析,并运用向前法进行变量筛选,利用容忍度和方差膨胀因子检验自变量的共线性。使用Kaplan Meier方法和Log-Rank检验进行生存分析。检验水准α=0.05。
2 结果 2.1 两组患者纳入例数305例患者中,LN-Ⅱ/Ⅴ组53例(17.4%);LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)组252例(82.6%),其中LN-Ⅲ/Ⅳ146例,LN-Ⅲ/Ⅳ+Ⅴ106例。
2.2 两组患者的疾病活动性指标LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)组患者SLEDAI评分≥10分的比例(66.3%)高于LN-Ⅱ/Ⅴ组(45.3%,P < 0.05),出现浆膜炎、脱发、贫血、血肌酐增高、血尿以及抗ds-DNA、AnuA抗体阳性的比例均较LN-Ⅱ/Ⅴ组高,而LN-Ⅱ/Ⅴ组出现关节炎、抗SSA抗体阳性的比例较高,差异均有统计学意义(P < 0.05,表 1)。LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)组中,LN-Ⅲ/Ⅳ+Ⅴ型患者的皮疹发生率较LN-Ⅲ/Ⅳ型高(59.4% vs 42.5%,P=0.008),而血尿发生率较低(78.3% vs 90.4%,P=0.007),差异均有统计学意义。
| 临床特征 | LN-Ⅱ/Ⅴ(n=53) | LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)(n=252) | t/χ2值 | P值 |
| 首次发病年龄/岁 | 32.4±11.9 | 30.7±12.7 | 0.890 | 0.374 |
| 病程/月 | 44.2±14.9 | 39.6±15.8 | 1.956 | 0.051 |
| 女性 | 43(81.1) | 200(79.4) | 0.084 | 0.771 |
| SLEDAI评分≥10分 | 24(45.3) | 167(66.3) | 8.240 | 0.004 |
| 浆膜炎 | 24(45.3) | 160(63.5) | 6.067 | 0.014 |
| 皮疹 | 23(43.4) | 125(49.6) | 0.675 | 0.411 |
| 关节痛 | 31(58.5) | 104(41.3) | 5.264 | 0.022 |
| 脱发 | 5(9.4) | 60(23.8) | 5.396 | 0.020 |
| 发热 | 15(28.3) | 57(22.6) | 0.784 | 0.376 |
| 口腔溃疡 | 8(15.1) | 45(17.9) | 0.233 | 0.629 |
| 光敏感 | 4(7.6) | 39(15.5) | 2.273 | 0.132 |
| 白细胞减少 | 39(73.6) | 170(67.5) | 0.762 | 0.383 |
| 贫血 | 39(73.6) | 226(89.7) | 9.959 | 0.002 |
| 血小板减少 | 20(37.7) | 100(39.7) | 0.070 | 0.792 |
| 高尿酸血症 | 47(88.7) | 231(91.7) | 0.484 | 0.486 |
| 血肌酐增高 | 22(41.5) | 168(66.7) | 11.799 | 0.001 |
| 血尿 | 33(62.3) | 215(85.3) | 15.318 | 0.000 |
| 大量尿蛋白 | 25(47.2) | 156(61.9) | 3.004 | 0.083 |
| 补体C3降低 | 49(92.5) | 245(97.2) | 2.865 | 0.091 |
| 抗SSA抗体 | 43(81.1) | 165(65.5) | 4.949 | 0.026 |
| 抗Sm抗体 | 28(52.8) | 124(49.2) | 0.230 | 0.632 |
| 抗ds-DNA抗体 | 21(39.6) | 179(71.0) | 19.137 | 0.000 |
| 抗AnuA抗体 | 26(49.1) | 177(70.2) | 8.827 | 0.003 |
| AI | 2.5±0.6 | 6.7±1.4 | 11.678 | 0.000a |
| CI | 1.4±0.8 | 2.4±1.3 | 4.944 | 0.000 |
| 死亡 | 0(0.0) | 9(3.6) | / | 0.368b |
| 终末肾病 | 2(3.8) | 42(16.7) | 5.897 | 0.016c |
| a:采用Mann-Whitney U检验;b:采用Fisher确切概率法;c:采用连续校正的卡方检验 | ||||
2.3 两组患者的ESRD累积发病率
随访期间,累积44例(14.4%)患者出现ESRD。两组ESRD累积发病率差异有统计学意义(3.8% vs 16.7%,P=0.016,表 1)。LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)组中,LN-Ⅲ/Ⅳ和LN-Ⅲ/Ⅳ+Ⅴ的ESRD累积发病率差异无统计学意义(19.2% vs 13.2%,P=0.209)。
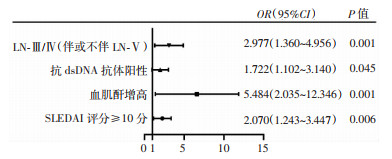
2.4 ESRD的危险因素分析单因素Logisitc回归分析(表 2)显示,LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)是ESRD的危险因素(OR=2.818,95%CI:1.538~5.166,P=0.001)。多因素Logisitc回归分析(图 1)显示,LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)是ESRD的独立危险因素(OR=2.977,95%CI:1.360~4.956,P=0.001)。此外,抗dsDNA抗体阳性(OR=1.722,95%CI:1.102~3.140,P=0.045)、血肌酐增高(OR=5.484,95%CI:2.035~12.346,P=0.001)、SLEDAI评分≥10分(OR=2.070,95%CI:1.243~3.447,P=0.006)均为ESRD的独立危险因素。所有变量的容忍度>0.1,且方差膨胀因子均<10,不存在多重共线性。
| 变量 | P值 | OR | 95% CI |
| 贫血 | 0.285 | 1.155 | 0.887~1.503 |
| 脱发 | 0.887 | 0.960 | 0.546~1.687 |
| 关节痛 | 0.330 | 0.793 | 0.498~1.264 |
| 浆膜炎 | 0.110 | 0.676 | 0.418~1.093 |
| 皮疹 | 0.090 | 0.668 | 0.420~2.550 |
| 血肌酐增高 | 0.001 | 4.503 | 1.901~10.664 |
| 血尿 | 0.287 | 1.349 | 0.778~2.340 |
| 抗核小体抗体阳性 | 0.464 | 1.200 | 0.736~1.958 |
| 抗SSA抗体阳性 | 0.884 | 0.964 | 0.586~1.586 |
| 抗dsDNA抗体阳性 | 0.066 | 1.573 | 0.970~2.550 |
| LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ) | 0.001 | 2.818 | 1.538~5.166 |
| AI | 0.600 | 1.051 | 0.874~1.263 |
| CI | 0.010 | 1.163 | 1.037~1.305 |
| SLEDAI评分≥10分 | 0.001 | 2.293 | 1.420~3.704 |
|
| 图 1 LN患者出现ESRD的多因素分析 |
2.5 两组患者的生存分析
到随访截止时间,共9例患者死亡,主要死亡原因为:严重感染4例(44.4%),肾脏衰竭、心脏衰竭、呼吸衰竭、狼疮脑病、小肠多发性肠炎坏死伴穿孔各1例(11.1%)。整个随访期间(82个月),LN-Ⅱ/Ⅴ和LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)组患者的生存时间分别为39.4~49.6(44.5±2.6)个月、36.7~41.3(39.0±1.2)个月,两组患者的生存时间差异无统计学意义(P=0.119)。LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)组中,LN-Ⅲ/Ⅳ和LN-Ⅲ/Ⅳ+Ⅴ型患者的生存时间分别为37.1~42.9(40.0±1.5)个月、33.8~40.2(37.0±1.6)个月,两种类型患者的生存时间差异无统计学意义(P=0.856,图 2)。

|
| A: LN-Ⅱ/Ⅴ和LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)的生存率;B: LN-Ⅲ/Ⅳ和LN-Ⅲ/Ⅳ+Ⅴ的生存率 图 2 患者不同病理分型对生存期的影响 |
3 讨论
肾脏是系统性红斑狼疮的重要靶器官,进展为ESRD的患者多依赖于血液透析或腹膜透析,生活质量差,经济负担重,早期、准确地诊断成为迫切需求。肾脏活检作为早期诊断、制定治疗方案和判断预后的关键,已被越来越多的患者所接受。本研究中LN病理分型以LN-Ⅲ/Ⅳ为主(47.9%),LN-Ⅲ/Ⅳ+Ⅴ次之(34.8%),LN-Ⅱ/Ⅴ最少(17.4%),同文献[3, 9]报道一致。
本研究显示,与LN-Ⅲ/Ⅳ组相比,LN-Ⅲ/Ⅳ+Ⅴ组的皮疹发生率更高(59.4% vs 42.5%,P=0.008),血尿发生率更低(78.3% vs 90.4%,P=0.007),但两组的疾病活动性、免疫学特征、ESRD累积发病率和平均生存时间的差异均无统计学意义,与ILORI等[5]报道一致,提示膜性病变可能未引起LN临床特征的显著改变。此外,与LN-Ⅱ/Ⅴ组相比,LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)组患者出现SLEDAI评分≥10分的比例更高(66.3% vs 45.3%,P < 0.05),SLEDAI评分指标中的临床表现如浆膜炎和脱发,异常的实验室指标如血尿和抗ds-DNA阳性的比例也更高,与既往研究[9-10]一致。提示临床上LN-Ⅲ/Ⅳ型(伴或不伴LN-Ⅴ)患者疾病活动性更高,表现为更严重的肾脏及肾外组织器官损伤,以及更多的自身抗体产生。
作为SLEDAI评分指标,抗ds-DNA抗体为SLE特异性抗体,而研究认为抗AnuA抗体比抗ds-DNA抗体有更好的敏感性,可减少因后者假阴性而导致的漏诊[11]。本研究显示,抗AnuA抗体和抗ds-DNA抗体的阳性率在LN-Ⅲ/Ⅳ组(伴或不伴LN-Ⅴ)中均远高于LN-Ⅱ/Ⅴ组(70.2% vs 49.1%和71.0% vs 39.6%),提示这两种抗体均与肾脏损害相关,可能在预测肾脏病理分型和疾病活动性方面发挥作用[9, 11-12]。贫血是常见的肾外表现,既往报道认为贫血虽然不是SLEDAI评分指标,但其不仅与疾病活动性相关,还是肾脏病变预后不良的危险因素[9, 13]。本研究中305例患者的贫血发生率高达86.9%,其中LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)组高于LN-Ⅱ/Ⅴ组(89.7% vs 73.6%,P < 0.05),可能由于毛细血管内细胞增多性病变可导致更重的血尿(85.3% vs 62.3%,P < 0.001)和肾性贫血,也可能与疾病活跃性更高而产生大量抗红细胞抗体导致自身免疫性溶血性贫血有关[14-15]。
不同国家10年ESRD累积发生率差异较大(7%~ 48%),本组患者病程为(40.4±15.7)个月,ESRD累积发病率为14.4%,略高于国内南方地区的10年ESRD累积发生率(12.1%)[3, 16],可能与地域、经济等有关。本研究显示,LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)的ESRD累积发病率高于LN-Ⅱ/Ⅴ(16.7% vs 3.8%,P=0.016),多因素Logistic回归分析也显示LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)是ESRD的独立危险因素。这与文献[3, 6, 9]报道一致,提示临床上应积极治疗LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)型患者,延长其进展为ESRD的时间,改善生活质量。此外,本研究还显示,血肌酐增高、抗ds-DNA抗体阳性、SLEDAI评分≥10分均为ESRD的独立危险因素,既往文献[17-19]中也有相同报道,提示ESRD与疾病活动性相关,是多因素作用结果,随访时需要全面评估。
随着治疗的规范化,SLE患者5年生存率从20世纪60年代的70%和80年代的90%上升到95%以上[20]。TANG等[19]在一项纳入681例LN患者的研究中发现,我国LN患者死亡率为5.3%,严重感染为首要死因,发生率为41.7%。本研究随访时间较短,死亡率(2.9%)略低于该研究,但首位死因也是严重感染(44.4%)。研究认为积极的免疫抑制疗法改善了预后,但也增加严重感染风险[19, 21]。因此,临床上需加强定期随访,在感染早期合理运用抗感染药物,提高感染防治的有效率。此外,本研究中不同病理分型组患者的平均生存时间的差异无统计学意义,可能与随访期较短、死亡人数较少有关。
综上,与LN-Ⅱ/Ⅴ相比,LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)患者的疾病活动性更高,肾脏、肾外损害更重,更易进展为ESRD。LN-Ⅲ/Ⅳ(伴或不伴LN-Ⅴ)、抗dsDNA抗体阳性、血肌酐增高和SLEDAI评分≥10分是ESRD的独立危险因素,临床上应对伴有上述表现的患者加强关注,及早、规律的治疗和随访,以降低其进展为ESRD的风险。本研究样本量偏小,尤其LN-Ⅱ/Ⅴ患者比例较小,研究结果存在一定局限性,未来还需要大样本研究进一步证实。
| [1] |
HANLY J G, O'KEEFFE A G, SU L, et al. The frequency and outcome of lupus nephritis: results from an international inception cohort study[J]. Rheumatology (Oxford), 2016, 55(2): 252-262. DOI:10.1093/rheumatology/kev311 |
| [2] |
FARINHA F, PEPPER R J, OLIVEIRA D G, et al. Outcomes of membranous and proliferative lupus nephritis: analysis of a single-centre cohort with more than 30 years of follow-up[J]. Rheumatology (Oxford), 2020.[Epub ahead of print]. DOI: 10.1093/rheumatology/keaa103.
|
| [3] |
YANG J, LIANG D, ZHANG H, et al. Long-term renal outcomes in a cohort of 1814 Chinese patients with biopsy-proven lupus nephritis[J]. Lupus, 2015, 24(14): 1468-1478. DOI:10.1177/0961203315593166 |
| [4] |
YAP D Y H, TANG C S O, MA M K M, et al. Survival analysis and causes of mortality in patients with lupus nephritis[J]. Nephrol Dial Transplant, 2012, 27(8): 3248-3254. DOI:10.1093/ndt/gfs073 |
| [5] |
ILORI T O, ENOFE N, OOMMEN A, et al. Comparison of outcomes between individuals with pure and mixed lupus nephritis: a retrospective study[J]. PLoS ONE, 2016, 11(6): e0157485. DOI:10.1371/journal.pone.0157485 |
| [6] |
AYODELE O E, OKPECHI I G, SWANEPOEL C R. Long-term renal outcome and complications in South Africans with proliferative lupus nephritis[J]. Int Urol Nephrol, 2013, 45(5): 1289-1300. DOI:10.1007/s11255-012-0376-9 |
| [7] |
HOCHBERG M C. Updating the American College of Rheumatology revised criteria for the classification of systemic lupus erythematosus[J]. Arthritis Rheum, 1997, 40(9): 1725. DOI:10.1002/art.1780400928 |
| [8] |
BAJEMA I M, WILHELMUS S, ALPERS C E, et al. Revision of the International Society of Nephrology/Renal Pathology Society classification for lupus nephritis: clarification of definitions, and modified National Institutes of Health activity and chronicity indices[J]. Kidney Int, 2018, 93(4): 789-796. DOI:10.1016/j.kint.2017.11.023 |
| [9] |
YUAN F, WEI F, HUANG H, et al. The predictive value of autoantibody spectrum on organ damage in patients with systemic lupus erythematosus[J]. Arch Rheumatol, 2019, 34(2): 157-165. DOI:10.5606/archrheumatol.2019.6981 |
| [10] |
AUSTIN H A, ILLEI G G, BRAUN M J, et al. Randomized, controlled trial of prednisone, cyclophosphamide, and cyclosporine in lupus membranous nephropathy[J]. J Am Soc Nephrol, 2009, 20(4): 901-911. DOI:10.1681/asn.2008060665 |
| [11] |
YANG J F, XU Z Z, SUI M S, et al. Co-positivity for anti-dsDNA, -nucleosome and -histone antibodies in lupus nephritis is indicative of high serum levels and severe nephropathy[J]. PLoS ONE, 2015, 10(10): e0140441. DOI:10.1371/journal.pone.0140441 |
| [12] |
胡伟新, 刘春蓓, 孙海鸥, 等. 1352例狼疮性肾炎的临床与免疫学特征[J]. 肾脏病与透析肾移植杂志, 2006, 15(5): 401-408, 442. HU W X, LIU C B, SUN H O, et al. Clinical and immunological features of 1352 Chinese patients with lupus nephritis[J]. Chin J Nephrol Dial Transplant, 2006, 15(5): 401-408, 442. DOI:10.3969/j.issn.1006-298X.2006.05.002 |
| [13] |
LI W G, YE Z Z, YIN Z H, et al. Clinical and immunological characteristics in 552 systemic lupus erythematosus patients in a southern province of China[J]. Int J Rheum Dis, 2017, 20(1): 68-75. DOI:10.1111/1756-185x.12480 |
| [14] |
RAHBAR M, CHITSAZIAN Z, ABDOLI F, et al. Pure red cell aplasia due to antibody against erythropoietin in hemodialysis patients[J]. J Nephropathol, 2017, 6(1): 25-29. DOI:10.15171/jnp.2017.05 |
| [15] |
LEVINE A B, ERKAN D. Clinical assessment and management of cytopenias in lupus patients[J]. Curr Rheumatol Rep, 2011, 13(4): 291-299. DOI:10.1007/s11926-011-0179-5 |
| [16] |
ALMAANI S, MEARA A, ROVIN B H. Update on lupus nephritis[J]. Clin J Am Soc Nephrol, 2017, 12(5): 825-835. DOI:10.2215/CJN.05780616 |
| [17] |
AHN S S, YOO J, JUNG S M, et al. Comparison of clinical features and outcomes between patients with early and delayed lupus nephritis[J]. BMC Nephrol, 2020, 21(1): 258. DOI:10.1186/s12882-020-01915-5 |
| [18] |
TSELIOS K, GLADMAN D D, SU J, et al. Advanced chronic kidney disease in lupus nephritis: is dialysis inevitable?[J]. J Rheumatol, 2020, 47(9): 1366-1373. DOI:10.3899/jrheum.191064 |
| [19] |
TANG Y, ZHANG X, JI L, et al. Clinicopathological and outcome analysis of adult lupus nephritis patients in China[J]. Int Urol Nephrol, 2015, 47(3): 513-520. DOI:10.1007/s11255-014-0903-y |
| [20] |
LERANG K, GILBOE I M, STEINAR THELLE D, et al. Mortality and years of potential life loss in systemic lupus erythematosus: a population-based cohort study[J]. Lupus, 2014, 23(14): 1546-1552. DOI:10.1177/0961203314551083 |
| [21] |
WU X Y, YANG M, XIE Y S, et al. Causes of death in hospitalized patients with systemic lupus erythematosus: a 10-year multicenter nationwide Chinese cohort[J]. Clin Rheumatol, 2019, 38(1): 107-115. DOI:10.1007/s10067-018-4259-z |



