2. 401120 重庆,重庆医科大学附属第三医院(捷尔医院)神经疾病中心
2. Department of Neurology and Neurosurgery, the Third Affiliated Hospital of Chongqing Medical University, Chongqing, 401120, China
创伤性脑损伤(traumatic brain injury,TBI)是儿童创伤死亡和致残的首位原因[1]。重型创伤性脑创伤(severe TBI, STBI)是指格拉斯哥昏迷指数(glasgow coma scale, GCS)评分≤8分的颅脑外伤,常会导致患儿预后不良。高颅内压(intracranial hypertension,ICH)常由严重的TBI引起[2],大量临床研究表明其与预后显著相关,因此颅内压(intracranial pressure,ICP)监测被认为是诊治ICH的基石。目前对于脑创伤患儿的ICP及脑灌注压(cerebral perfusion pressure,CPP)治疗阈值尚无统一标准。本研究团队的前期研究发现,不同年龄组的颅脑创伤患儿的颅内压及脑灌注压的水平不同,年龄越大,颅内压及脑灌注压水平越高,因此不同的年龄组儿童的颅内压及脑灌注压治疗阈值可能不同[3]。本文对2014年6月至2018年6月重庆医科大学附属儿童医院神经外科收治的115例STBI患儿进行前瞻性分析研究,拟制定患儿颅内压及脑灌注压的治疗阈值,指导临床治疗工作。
1 资料与方法 1.1 一般资料本研究方案获重庆医科大学附属儿童医院伦理评审委员会批准(2014年伦审第045号,批准日期:2014年4月21日)。患者全部信息资料由神经外科高年资医生按照统一标准通过询问病史、体格检查等方法进行观察记录。本研究共纳入2014年6月至2018年6月重庆医科大学附属儿童医院神经外科收治的STBI患儿115例,其中男性78例,女性37例;年龄5个月27天至14岁[(5.80±3.40)岁];GCS评分:3~ 8分[(6.64±1.35)分];病程1~23 h[(5.43± 4.72)h];手术距受伤时间:4~24 h[(11.79±6.99)h];术后ICP监测时间:79~327 h[(168.20±55.11)]h。致伤机制:车祸伤49例、高坠48例、床上/台阶/平地跌伤16例、自行车摔伤2例。按年龄分为3组:< 2岁组25例,2~7岁组52例,>7岁组38例。脑外伤类型:颅骨骨折76例,蛛网膜下腔出血60例,脑疝54例,硬膜外出血/血肿48例,硬膜下出血/血肿42例,脑叶挫伤32例,脑内血肿20例,颅底骨折20例,脑室出血/脑积水18例,弥漫性轴索损伤12例,脑肿胀10例,颌面骨骨折10例,脑干挫伤8例,静脉窦破裂8例,丘脑挫伤4例。
1.2 纳入与排除标准纳入标准:①有明确颅脑外伤史;②年龄 < 16岁;③入院时GCS评分≤8分;④家属同意行有创颅内压监测;⑤伤后24 h内行有创颅内压监测探头置入术。排除标准:合并其他脏器的严重损伤者。
1.3 仪器设备使用美国强生公司生产的Codman ICP EXPRESS颅内压监测仪行颅内压监测,探头为82-6631型(脑实质型)或82-6653型(脑室型),具体类型依据患儿头颅CT结果及临床病情而定。
1.4 治疗方法本组患儿以2012年美国脑创伤基金协会(brain trauma foundation,BTF)第2版《关于婴儿、儿童、青少年重型脑创伤诊疗指南》[4]及2015年中国医师协会神经外科医师分会、中华神经创伤专家委员会的《中国颅脑创伤外科手术指南》[5]为参考进行治疗。对幕上血肿量>25 mL或后颅窝血肿量>10 mL、CT扫描有占位效应的患儿,立即开颅清除血肿,术中按照血肿部位采取相应区域骨瓣开颅,清除血肿和彻底止血,骨窗缘悬吊硬脑膜,骨瓣原位复位固定。但对于巨大硬膜外/硬膜下/脑内血肿、中线移位明显、出现脑疝、瞳孔散大的患者,采用去骨瓣减压和硬脑膜减张缝合技术。对于无脑内血肿、额颞顶广泛脑挫裂伤脑肿胀合并难以控制高颅压、出现小脑幕切迹疝征象的患者,常规行标准外伤大骨瓣开颅,硬膜减张缝合,去骨瓣减压。对于凹陷性骨折深度超过5 mm、位于脑功能区、压迫导致神经功能障碍、开放性凹陷性骨折、骨折压迫静脉窦导致血液回流的患儿,应同时行凹陷骨折复位。对于开放性TBI的患者,予以彻底清创,修复硬脑膜,必要时去除污染颅骨[5]。术毕再行颅内压监测探头置入术。脑实质型颅内压监测探头置入深度约2.5~3.0 cm,脑室型颅内压监测探头一般选择右侧脑室额角穿刺,探头植入侧脑室。有创颅内压监测探头置入前在生理盐水中调零并准确记录调零校准参数。术后处理包括止血、补液、营养支持、抑酸护胃、镇静镇痛、预防癫痫、必要时预防感染(开放性颅脑损伤或合并肝肺挫伤等情况)、高渗疗法:包括高渗性盐水[30 g/L高渗盐水,6.5~10.0 mL/kg急性期使用或0.1~1.0 mL/(kg·h)持续输入]及甘露醇(0.25~1.00 g/kg)[4]。
第2版《关于婴儿、儿童、青少年重型脑创伤诊疗指南》[4]建议:所有年龄段儿童颅内压治疗阈值为20 mmHg;CPP阈值为40~50 mmHg,最低值不低于40 mmHg。本组患儿暂以颅内压高于20.0 mmHg(1 mmHg=0.133 kPa)、脑灌注压低于50.0 mmHg(持续时间超过5 min)作为干预阈值,干预上主要采用高渗液体。颅内压降至治疗阈值以下并持续24 h以上可拔除颅内压监测探头。术后每小时记录1次颅内压及相应的动脉血压,并根据公式计算相应的脑灌注压(脑灌注压=平均动脉压-颅内压;平均动脉压=舒张压+1/3脉压差),记录时保持患儿处于安静放松状态;患者出院后6个月,电话或门诊随访GOS评分(1~3分,预后不良;4~5分,预后良好)。
1.5 检验指标很多研究方法仅简单总结了监测的数据,没有同时考虑损伤的程度和作用持续时间,可能难以准确反映颅内压升高和低脑灌注压总的潜在损害[6]。CHAMBER等[7]研究发现脑灌注压压力时间指数(pressure-time index,PTI)对于儿童颅脑创伤的预后有非常高的预测价值。因此,本研究利用了该指标来探索STBI患儿的颅内压和脑灌注压治疗阈值。分别计算颅内压压力时间指数(pressure-time index for intracranial pressure,PTIi, mmHg/h)和脑灌注压压力时间指数(pressure-time index for cerebral perfusion pressure,PTIc,mmHg/h)。具体计算方法如下:
CPP(cerebral perfusion pressure):脑灌注压;ICP(intracranial pressure):颅内压;tsample interval(单位:min):时间间隔,本组数据记录间隔时间为60 min。PTIi即反应所有超过阈值的持续时间颅内压总和,可以有效反应高于颅内压阈值的损伤的程度及作用时间(尽管不同患儿监测时间长短不一致,但本研究达到治疗阈值以下24 h即拔出颅内压监测探头,可认为拔出探头后超过阈值压力和为0);同理可理解PTIc。
根据相关研究及指南[3, 4, 7],分别假设各个年龄组儿童的颅内压和脑灌注压治疗阈值,并在此阈值的基础上分别增加或减去10%和20%,获得理论颅内压和脑灌注压治疗阈值(表 1)。计算不同颅内压及脑灌注压阈值水平时的每个患儿的PTIi和PTIc,并应用Medcalc 19.1软件计算各个年龄组各相应阈值的ROC曲线及曲线下面积(area under curve,AUC),AUC最大的PTIi和PTIc相对应的颅内压和脑灌注压治疗阈值即为该年龄组患儿的最佳颅内压和脑灌注压治疗阈值。
| 组别 | 颅内压 | 脑灌注压 | |||||||||
| -20% | -10% | 阈值 | +10% | +20% | -20% | -10% | 阈值 | +10% | +20% | ||
| < 2岁组 | 12.8 | 14.4 | 16.0 | 17.6 | 19.2 | 36.0 | 40.5 | 45.0 | 49.5 | 54.0 | |
| 2~7岁组 | 16.0 | 18.0 | 20.0 | 22.0 | 24.0 | 40.0 | 45.0 | 50.0 | 55.0 | 60.0 | |
| >7岁组 | 19.2 | 21.6 | 24.0 | 26.4 | 28.8 | 44.0 | 49.5 | 55.0 | 60.5 | 66.0 | |
1.6 统计学分析
应用SPSS 26.0统计软件和Medcalc 19.1软件进行分析。符合正态分布的计量资料以x±s表示,采用方差分析或t检验,偏态分布的计量资料以M(P25,P75)表示,采用Wilcoxon秩和检验;计数资料采用χ2检验或Fisher精确概率法。
2 结果 2.1 各年龄组患儿的一般情况3个年龄组患儿除年龄的差异存在统计学意义外(P < 0.05),在性别分布、病程、手术距离受伤的时间、GCS评分、颅内压监测方式、颅内压监测时间及预后方面各年龄组之间差异没有统计学意义(P>0.05,表 2)。
| 组别 | n | 男/女(例) | 病程/h | 手术距受伤时间/h | 年龄/d | GCS评分/分 | 脑室型/脑实质(例) | 监测时间/h | GOS1评分3分/4~5分 |
| < 2岁组 | 25 | 16/9 | 6.50±5.61 | 10.38±5.42 | 403.75±221.59 | 6.63±1.11 | 6/19 | 181.50±42.11 | 6/19 |
| 2~7岁组 | 52 | 36/16 | 5.35±4.39 | 12.46±8.10 | 1 639.04±508.55 | 6.42±1.47 | 14/38 | 174.54±52.75 | 10/42 |
| >7岁组 | 38 | 26/12 | 5.11±4.68 | 11.16±6.12 | 3 566.05±711.68 | 7.00±1.21 | 4/34 | 149.53±62.12 | 6/32 |
| 统计值 | 0.22 | 0.24 | 0.33 | 103.46 | 0.97 | 3.76 | 1.40 | 0.66 | |
| P | 0.90 | 0.79 | 0.72 | < 0.001 | 0.39 | 0.15 | 0.26 | 0.72 |
2.2 各年龄组患儿颅内压及脑灌注压临床特点
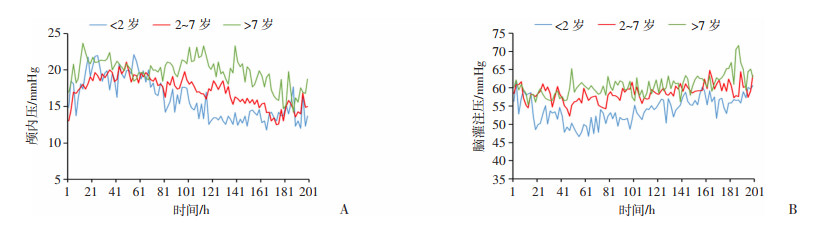
术后各组颅内压经历短暂较低水平后迅速升高,并在术后1~2 d达到高峰,3~5 d后逐渐下降至基本正常范围,并趋于稳定,且年龄越大,颅内压越高,均值具有显著差异(P < 0.001, 图 1);术后各组脑灌注压均较高,术后2 d左右到达低谷,之后又逐渐回升,趋于稳定,且年龄越大,脑灌注压水平越高,均值具有显著差异(P < 0.001, 图 1)。
|
| 图 1 各年龄组患儿颅内压-时间曲线(A)与脑灌注压-时间曲线(B) |
2.3 各年龄组组患儿PTIi和PTIc临床特点
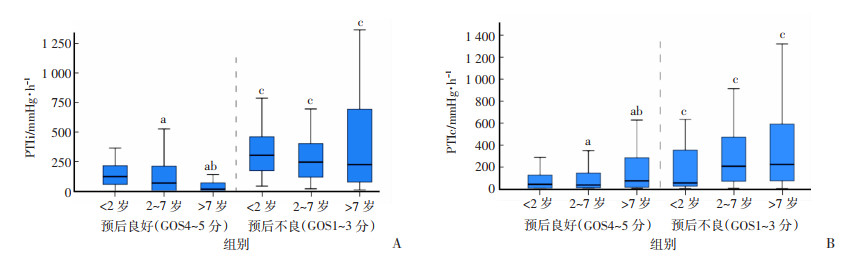
预后良好组不同年龄段PTIi值差异有统计学意义(P=0.003),预后不良组不同年龄段PTIi值差异无统计学意义(P=0.414),预后不良组和预后良好组间PTIi差异有统计学意义(P < 0.001,图 2);预后良好组不同年龄段PTIc值差异有统计学意义(P=0.004,表 3),预后不良组不同年龄段PTIc值差异无统计学意义(P= 0.201),预后不良组和预后良好组间PTIc差异有统计学意义(P < 0.001,图 2)。
|
| a: P < 0.01, 与 < 2岁组比较;b: P < 0.01, 与2~7岁组比较;c: P < 0.01, 与预后良好组比较 图 2 不同年龄组患儿PTIi(A)、PTIc(B)及预后箱图 |
| 预后(GOS评分) | 平均PTLi | 平均PTLc | |||||
| < 2岁 | 2~7岁 | >7岁 | < 2岁 | 2~7岁 | >7岁 | ||
| 良好(4~5分) | 141.00 | 129.44 | 82.70 | 99.31 | 114.90 | 187.37 | |
| 不良(1~3分) | 333.87 | 314.58 | 404.95 | 197.03 | 309.97 | 367.26 | |
| F | 44.42 | 39.76 | 50.96 | 8.69 | 37.72 | 10.49 | |
| P | < 0.001 | < 0.001 | < 0.001 | 0.004 | < 0.001 | 0.001 | |
2.4 年龄相关性的颅内压治疗阈值
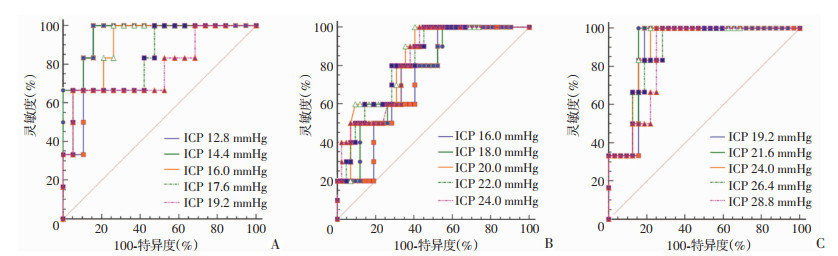
各个年龄组的不同颅内压阈值水平相应的PTIi的AUC见表 4~6,各个年龄组的AUC最大的PTIi相应的颅内压治疗阈值水平:<2岁组为14.4 mmHg,2~7岁组为20.0 mmHg,>7岁组为21.6 mmHg。相应的ROC曲线见图 3。
| ICP阈值 | AUC | SEa | CIb |
| 12.8 mmHg | 0.921 | 0.055 | 0.741~0.990 |
| 14.4 mmHg | 0.956 | 0.038 | 0.791~0.999 |
| 16.0 mmHg | 0.904 | 0.063 | 0.718~0.984 |
| 17.6 mmHg | 0.833 | 0.101 | 0.631~0.951 |
| 19.2 mmHg | 0.781 | 0.131 | 0.571~0.920 |
| a:DeLong et al., 1988; b:Binomial exactzhu | |||
| ICP阈值 | AUC | SEa | CIb |
| 16.0 mmHg | 0.729 | 0.076 | 0.587~0.843 |
| 18.0 mmHg | 0.764 | 0.076 | 0.626~0.871 |
| 20.0 mmHg | 0.832 | 0.063 | 0.703~0.921 |
| 22.0 mmHg | 0.821 | 0.065 | 0.690~0.914 |
| 24.0 mmHg | 0.815 | 0.067 | 0.684~0.909 |
| a:DeLong et al., 1988; b:Binomial exactzhu | |||
| ICP阈值 | AUC | SEa | CIb |
| 19.2 mmHg | 0.891 | 0.058 | 0.747~0.968 |
| 21.6 mmHg | 0.901 | 0.052 | 0.760~0.974 |
| 24.0 mmHg | 0.896 | 0.054 | 0.753~0.971 |
| 26.4 mmHg | 0.88 | 0.06 | 0.734~0.963 |
| 28.8 mmHg | 0.859 | 0.066 | 0.708~0.950 |
| a:DeLong et al., 1988; b:Binomial exactzhu | |||
|
| A: < 2岁组; B: 2~7岁组; C: >7岁组 图 3 各年龄组患儿不同颅内压阈值水平相应的PTIi值ROC曲线 |
2.5 年龄相关性的脑灌注压治疗阈值
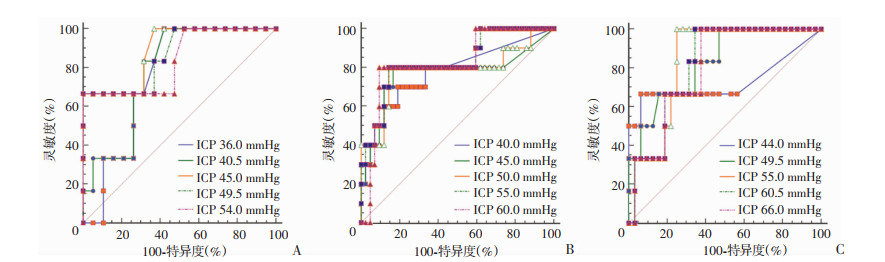
各个年龄组的不同脑灌注压阈值水平相应PTIc的AUC详见表 7~9,可找到各个年龄组的ROC曲线下面积最大的平均PTIc相应的脑灌注压治疗阈值水平如下:<2岁组为45.0 mmHg、2~7岁组为55 mmHg、>7岁组为55.0 mmHg。2~7岁组与>7岁组的脑灌注压阈值水平相同。相应的ROC曲线见图 4。
| CCP阈值 | AUC | SEa | CIb |
| 36.0 mmHg | 0.754 | 0.097 | 0.543~0.903 |
| 40.5 mmHg | 0.785 | 0.095 | 0.576~0.923 |
| 45.0 mmHg | 0.890 | 0.078 | 0.701~0.979 |
| 49.5 mmHg | 0.864 | 0.094 | 0.668~0.967 |
| 54.0 mmHg | 0.838 | 0.110 | 0.636~0.953 |
| a:DeLong et al., 1988; b:Binomial exactzhu | |||
| CCP阈值 | AUC | SEa | CIb |
| 40.0 mmHg | 0.779 | 0.093 | 0.642~0.882 |
| 45.0 mmHg | 0.769 | 0.111 | 0.631~0.875 |
| 50.0 mmHg | 0.786 | 0.105 | 0.650~0.887 |
| 55.0 mmHg | 0.831 | 0.080 | 0.701~0.921 |
| 60.0 mmHg | 0.824 | 0.079 | 0.693~0.915 |
| a:DeLong et al., 1988; b:Binomial exactzhu | |||
| CCP阈值 | AUC | SEa | CIb |
| 44.0 mmHg | 0.729 | 0.163 | 0.561~0.860 |
| 49.5 mmHg | 0.831 | 0.088 | 0.674~0.932 |
| 55.0 mmHg | 0.839 | 0.068 | 0.683~0.938 |
| 60.5 mmHg | 0.818 | 0.075 | 0.659~0.924 |
| 66.0 mmHg | 0.802 | 0.081 | 0.641~0.913 |
| a:DeLong et al., 1988; b:Binomial exactzhu | |||
|
| A: < 2岁组; B: 2~7岁组; C: >7岁组 图 4 各年龄组患儿不同颅内压阈值水平相应的PTIc值ROC曲线 |
3 讨论
TBI是儿童较常见的危急重症,高颅压在STBI患儿的发生率高,且颅内高压与神经系统不良预后及死亡相关,大约有40%~60%患儿会出现长期神经功能缺陷[8-9],因此在ICP监测基础上成功治疗颅内高压及低脑灌注压,可以提高生存率并改善神经系统愈后。有关ICP及CCP治疗阈值的研究不多,既往由于研究设计的局限性,获得的相应阈值标准并未获得普遍认可,且报道中多以成人为主,由于生长发育过程中儿童本身的正常血压范围和脑顺应性的差异,脑血流随着年龄改变而改变,简单地从成人指南外推到儿童是存在问题的。在2019更新的第3版婴儿、儿童和青少年重型脑创伤诊疗指南建议:所有年龄段儿童颅内压为20 mmHg(Ⅲ级推荐);CPP阈值为40~50 mmHg,最低值不低于40 mmHg(Ⅲ级推荐),根据年龄适当调整确定最佳值[10]。早期有研究发现儿童脑创伤后6个月不同预后患儿的峰值颅内压水平差异没有统计学意义[11]。MILLER等[6]研究发现儿童重型颅脑创伤后ICP>20.0 mmHg和CCP<45.0 mmHg的持续时间对于预后不良有最佳的分辨能力,且颅内压>20.0 mmHg的持续时间每增加1 h,预后不良的概率增加4.6%。故研究STBI患儿的ICP和CCP治疗阈值时需同时考虑高颅内压和低脑灌注压水平和持续时间的影响。本研究依据CHAMBERS等[7]提出的将PTI作为参考指标,可同时反映高颅内压和低脑灌注压水平作用强度及持续时间的综合影响,根据PTIi和PTIc与预后的关系寻找不同年龄组患儿的ICP及CCP治疗阈值。本组研究平均各年龄组平均PTIi和平均PTIc与预后均相关(P < 0.05),证实了PTIi和PTIc对儿童TBI预后具有较高的预测价值。
正常成人的颅内压为7~15 mmHg,儿童为3~7 mmHg,婴儿为1.5~6.0 mmHg。这一颅内压的范围,并不是恒定的,颅内压会因个体、年龄等因素的不同而呈现个体化[12]。本组患儿有86.09%出现高颅压(99/115,ICP>20 mmHg),在术后1~2 d颅内压达高峰、脑灌注压达低谷,前者在3~5 d后逐渐下降并稳定,后者在3~4 d后轻微回升并稳定,与本团队之前研究结果接近[3]。但本次研究STBI高颅内压及低灌注压出现时间更早,持续时间更长。
STBI后往往易出现难治性高颅压而预后不良,临床医生应当颅内压达到一定值后予以相关治疗。成人TBI后颅内压治疗阈值为20 mmHg或22 mmHg[12-15],儿童领域大多数研究者设定为20 mmHg。因基于正常的血压及颅内压具有年龄相关性,故推测儿童STBI后颅内压治疗阈值也理当与年龄有关[16]。DAVID等[17]研究发现平均ICP低[(11.9±4.7) mmHg]的患儿预后好,而平均ICP高[(24.9±26.3)mmHg]的患儿预后差(P < 0.05),但作者并没有评估高颅压阈值对不同年龄阶段患儿愈后的影响。MEHTA等[18]回顾了2岁以下的重型脑创伤患儿,分别以颅内压高于15.0 mmHg和20.0 mmHg作为阈值分析,发现两种颅内压阈值水平预后没有显著差异。既往研究多单纯考虑高颅内压水平与预后指标之间的关系,未将高颅内压持续时间纳入考虑,故对儿童STBI后高颅内压损伤的强度评估不够准确。本研究通过PTIi这一新的指标来反映高颅内压损伤的强度,并通过ROC曲线分析其与预后的关系,研究发现<2岁组、2~7岁组、>7岁组STBI患儿的颅内压治疗阈值分别为14.4、20.0、21.6 mmHg。
CPP是驱使脑血流动力的压力,在正常状态下具有自我调节能力,与脑组织氧代谢率相匹配。重型TBI后CPP的自我调节能力将被损害。在CPP的控制目标上,美国第四版成人《重型颅脑创伤指南》建议控制CPP为60~70 mmHg。最佳的处理阈值低限尚不明确,可能还取决于患者的自身调节系统[12]。并有研究指出,CPP超过70 mmHg可以改善预后[19-21]。儿童STBI中CPP>40 mmHg的患儿愈后较CPP<40 mmHg的患儿好[22-23]。2006年CHAMBER[7]等曾对2~16岁的81例脑外伤患儿进行前瞻性研究,根据PTIc分析指出不同年龄儿童颅内压和脑灌注压的阈值:2~6岁、7~10岁、11~15岁分别为48.0、54.0、58.0 mmHg,但该项研究没有纳入2岁以下的儿童,使其应用受到了一定限制。2010年MEHTA等[18]进一步对22例2岁以下的脑创伤儿童回顾性分析后指出2岁的颅脑创伤患儿脑灌注压低于45.0 mmHg与预后不良相关,但其样本量少,故参考价值有限。2020年新指南推荐[10]:①在儿童重型TBI中维持最小CPP 40 mmHg;②CPP阈值40~50 mmHg,可能存在年龄特异性阈值,婴幼儿阈值为此范围低限,而青少年阈值为此范围高限。2014年ALLEN等[24]进行了1项多达2 074例的多中心的前瞻性观察性研究,其通过分析比较不同年龄段的颅内压和脑灌注压水平与出院后2周的生存率的关系指出不同年龄段的脑灌注压阈值分别为:成人>50.0/60.0 mmHg,6~17岁>50.0 mmHg,0~5岁>40.0 mmHg,但该项研究中多达84.7%的患者为年龄>18岁的成人,且结局指标没有考虑患者的远期神经功能预后,对儿童的CPP阈值预测有一定局限性。本研究通过PTIc与预后关系研究发现<2岁组、2~7岁组、>7岁组STBI儿童的脑灌注压治疗阈值分别为45.0、55.0、55.0 mmHg。
本组研究发现 < 2岁与≥2岁患儿在颅内压、脑灌注压治疗阈值明显不同,考虑这可能与大部分儿童的前囟在2周岁左右闭合有关,但需要进一步研究明确。
综上所述,不同年龄阶段的STBI患儿的颅内压和脑灌注压治疗阈值不同,< 2岁组、2~7岁组、>7岁组的颅内压治疗阈值分别为14.4、20.0、21.6 mmHg,脑灌注压治疗阈值分别为45.0、55.0、55.0 mmHg。本研究病例数相对较少,进一步开展多中心前瞻性研究具有重要意义。
| [1] |
LOVETT M E, O'BRIEN N F, LEONARD J R. Children with severe traumatic brain injury, intracranial pressure, cerebral perfusion pressure, what does it mean? A review of the literature[J]. Pediatr Neurol, 2019, 94: 3-20. DOI:10.1016/j.pediatrneurol.2018.12.003 |
| [2] |
BENNETT T D, MARSH R, MAERTENS J A, et al. Decision- making about intracranial pressure monitor placement in children with traumatic brain injury[J]. Pediatr Crit Care Med, 2019, 20(7): 645-651. DOI:10.1097/pcc.0000000000001934 |
| [3] |
张雷, 梁平, 翟瑄, 等. 儿童颅脑创伤后颅内压及脑灌注压的临床特点[J]. 中华创伤杂志, 2014, 30(10): 995-999. ZHANG L, LIANG P, ZHAI X, et al. Clinical features of intracranial pressure and cerebral perfusion pressure after craniocerebral trauma in children[J]. Chin J Trauma, 2014, 30(10): 995-999. DOI:10.3760/cma.j.issn.1001-8050.2014.10.007 |
| [4] |
CARNEY N A, CHESNUT R, KOCHANEK P M. Guidelines for the acute medical management of severe traumatic brain injury in infants, children, and adolescents[J]. Pediatr Crit Care Med, 2003, 4(supplement): S1. DOI:10.1097/01.ccm.0000067635.95882.24 |
| [5] |
中国医师协会神经外科医师分会, 中国神经创伤专家委员会. 中国颅脑创伤外科手术指南[J]. 中华神经外科杂志, 2015, 25(1): 100-101. Neurosurgeons Branch of Chinese Medical Doctors Association, China Neurotrauma Expert Committee. Guidelines for the surgical management of traumatic brain injury in China[J]. Chin J Neurosurg(Electron Ed), 2015, 25(1): 100-101. DOI:10.3877/cma.j.issn.2095-9141.2015.01.018 |
| [6] |
MILLER FERGUSON N, SHEIN S L, KOCHANEK P M, et al. Intracranial hypertension and cerebral hypoperfusion in children with severe traumatic brain injury: thresholds and burden in accidental and abusive insults[J]. Pediatr Crit Care Med, 2016, 17(5): 444-450. DOI:10.1097/PCC.0000000000000709 |
| [7] |
CHAMBERS I R, JONES P A, LO T Y M, et al. Critical thresholds of intracranial pressure and cerebral perfusion pressure related to age in paediatric head injury[J]. J Neurol Neurosurg Psychiatry, 2006, 77(2): 234-240. DOI:10.1136/jnnp.2005.072215 |
| [8] |
JAGANNATHAN J, OKONKWO D O, YEOH H K, et al. Long-term outcomes and prognostic factors in pediatric patients with severe traumatic brain injury and elevated intra-cranial pressure[J]. J Neurosurg Pediatr, 2008, 2(4): 240-249. DOI:10.3171/ped.2008.2.10.240 |
| [9] |
MILES D K, PONISIO M R, COLVIN R, et al. Predictors of intracranial hypertension in children undergoing ICP monitoring after severe traumatic brain injury[J]. Childs Nerv Syst, 2020, 36(7): 1453-1460. DOI:10.1007/s00381-020-04516-7 |
| [10] |
KOCHANEK P M, TASKER R C, CARNEY N, et al. Guidelines for the management of pediatric severe traumatic brain injury, third edition[J]. Pediatr Crit Care Med, 2019, 20(3): 280-289. DOI:10.1097/pcc.0000000000001736 |
| [11] |
GRINKEVICIŪTE D E, KEVALAS R, MATUKEVICIUS A, et al. Significance of intracranial pressure and cerebral perfusion pressure in severe pediatric traumatic brain injury[J]. Medicina (Kaunas), 2008, 44(2): 119-125. DOI:10.3390/medicina44020015 |
| [12] |
CARNEY N, TOTTEN A M, O'REILLY C, et al. Guidelines for the management of severe traumatic brain injury, fourth edition[J]. Neurosurgery, 2017, 80(1): 6-15. DOI:10.1227/neu.0000000000001432 |
| [13] |
ZEILER F A, ERCOLE A, CABELEIRA M, et al. Patient-specific ICP epidemiologic thresholds in adult traumatic brain injury[J]. J Neurosurg Anesthesiol, 2019. DOI:10.1097/ANA.0000000000000616.Onlineaheadofprint |
| [14] |
吴翔, 高国一, 冯军峰, 等. 颅脑创伤患者颅内压相关参数与预后关系的研究[J]. 中华神经外科杂志, 2018, 34(2): 119-123. WU X, GAO G Y, FENG J F, et al. Analysis of correlation between intracranial pressure and outcome in traumatic brain injury patients[J]. Chin J Neurosurg, 2018, 34(2): 119-123. DOI:10.3760/cma.j.issn.1001-2346.2018.02.003 |
| [15] |
MYBURGH J A. Intracranial pressure thresholds in severe traumatic brain injury: Pro[J]. Intens Care Med, 2018, 44(8): 1315-1317. DOI:10.1007/s00134-018-5264-z |
| [16] |
符跃强, 许峰. 儿童创伤性颅内高压治疗进展[J]. 中华实用儿科临床杂志, 2013, 28(24): 1912-1914. FU Y Q, XU F. Progress in treatment of traumatic intra-cranial hypertension in children[J]. Chin J Appl Clin Pediatr, 2013, 28(24): 1912-1914. |
| [17] |
ADELSON P D, RAGHEB J, KANEV P, et al. Phase Ⅱ clinical trial of moderate hypothermia after severe traumatic brain injury in children[J]. Neurosurgery, 2005, 56(4): 740-754. DOI:10.1227/01.neu.0000156471.50726.26 |
| [18] |
MEHTA A, KOCHANEK P M, TYLERKABARA E C, et al. Relationship of intracranial pressure and cerebral perfusion pressure with outcome in young children after severe traumatic brain injury[J]. Dev Neurosci, 2010, 32: 413-419. DOI:10.1159/000316804 |
| [19] |
SORRENTINO E, DIEDLER J, KASPROWICZ M, et al. Critical thresholds for cerebrovascular reactivity after traumatic brain injury[J]. Neurocrit Care, 2012, 16(2): 258-266. DOI:10.1007/s12028-011-9630-8 |
| [20] |
GVIZA F, MEYFROIDT G, PIPER I, et al. Cerebral perfusion pressure insults and associations with outcome in adult traumatic brain injury[J]. J Neurotrauma, 2017, 34(16): 2425-2431. DOI:10.1089/neu.2016.4807 |
| [21] |
LIN J W, TSAI J T, LIN C M, et al. Evaluation of optimal cerebral perfusion pressure in severe traumatic brain injury[J]. Acta Neurochir Suppl, 2008, 101: 131-136. DOI:10.1007/978-3-211-78205-7_22 |
| [22] |
FIGAJI A A, ZWANE E, THOMPSON C, et al. Brain tissue oxygen tension monitoring in pediatric severe traumatic brain injury. Part 2: Relationship with clinical, physiological, and treatment factors[J]. Childs Nerv Syst, 2009, 25(10): 1335-1343. DOI:10.1007/s00381-009-0821-y |
| [23] |
CHAIWAT O, SHARMA D, UDOMPHORN Y, et al. Cerebral hemodynamic predictors of poor 6-month Glasgow Outcome Score in severe pediatric traumatic brain injury[J]. J Neurotrauma, 2009, 26(5): 657-663. DOI:10.1089/neu.2008.0770 |
| [24] |
ALLEN B B, CHIU Y, GERBER L M, et al. Age-specific cerebral perfusion pressure thresholds and survival in children and adolescents with severe traumatic brain injury[J]. Pediatr Crit Care Med, 2014, 15(1): 62-70. DOI:10.1097/PCC.0b013e3182a556ea |




