2. 430000 武汉,华中科技大学同济医学院附属武汉市中心医院耳鼻咽喉头颈外科
2. Department of Otolaryngology, the Central Hospital of Wuhan, Tongji Medical College, Huazhong University of Science and Technology, Wuhan, Hubei Province, 430000, China
鼻咽纤维血管瘤(juvenile nasopharyngeal angiofibroma,JNA)多发于10~20岁的青春期男性,男性患病率可能与雄激素受体(AR)高表达有关,提示JNA具有雄激素依赖性[1],又名为“青春期鼻咽纤维血管瘤”,是高度血管化、少见的、良性的、进行性侵袭的肿瘤,这些病变的解剖来源最常见的是鼻后外侧壁的血管结构和蝶骨翼突的根部,其发病率占整个头颈部肿瘤的0.05%[2]。JNA可能表现出一种从蝶窦和蝶腭孔开始的侵袭性和破坏性的膨胀性生长模式[3]。其随后的扩散可通过眼眶、颅底等通路到达颅内和眶内。该病主要根据症状及检查结果,结合年龄和性别进行诊断,活检虽可确诊,但易引起严重出血,绝大多数JNA在诊断及术前不需要活检,影像学技术的发展更大大降低了活检率,避免了活检可能导致的大出血。手术切除是治疗鼻咽纤维血管瘤的首选治疗方式[4-6],但因其血管密度大、血供丰富、生长的部位深在,可能局部侵犯骨质,侵及翼腭窝、海绵窦、颅底,甚至颅内,故JNA手术难度大、术中出血多、术后复发率高。多种手术径路被运用于JNA的切除,传统手术包括鼻侧切开、面中部掀翻等[7]。近十多年来,随着手术入路的革新、鼻内镜手术的发展及广泛应用,经鼻内窥镜切除更多地运用于鼻咽纤维血管瘤[8-9]。该方法的主要优点是较小的软组织分离、避免面部切口、提供更好的照明和放大的视野。这样可以对肿瘤边缘进行更全面的检查,完整切除JNA,复发率更低[10]。另外,多学科协作所采取的术前控制性降压、术前栓塞、术后放化疗等,使鼻咽纤维血管瘤手术的出血量及术后复发率都明显降低[11]。本研究通过回顾分析20例鼻咽纤维血管瘤患者,经鼻内镜技术作为JNA Ⅰ期和Ⅱ期肿瘤Radkowski分期的主要治疗方式的经验,比较和讨论不同手术方式在中小型JNA中的疗效,为该病的诊治提供参考。
1 资料与方法 1.1 研究对象回顾性分析2002年1月至2018年12月就诊于陆军军医大学第一附属医院的JNA患者的临床资料,将首次手术治疗、病理学确诊为JNA的病例纳入本研究。根据Radkowski分期(表 1)系统进行肿瘤分期[12]。所有病例术前均行增强CT(图 1A)或MRI、纤维鼻咽喉镜(图 1B)检查,评估肿瘤的大体形态、生长部位,了解肿瘤与临界结构的毗邻关系,尤其是肿瘤与眶下裂、海绵窦、翼管、颈动脉的关系。常规评估患者全身一般情况,并对所有患者进行疗效分析和术后随访(随访时间12个月至6年),主要包括手术方式的选择、术中出血量、术后住院时间、术后拔出鼻腔纱条时间、并发症的发生、复发和目前的身体状况。所有病例术前通过Seldinger技术,使用适量明胶海绵颗粒进行肿瘤供血动脉栓塞,复查造影病灶均见动脉栓塞良好。手术方式根据肿瘤的侵犯范围,结合内镜技术水平的不断提升,分为鼻内镜下手术(11例)和传统手术(9例)。本研究经陆军军医大学第一附属医院伦理委员会批准[2017年科研第(14)号],并在中国临床试验中心注册(ChiCTR1800019377)。
| 分期 | Radkowski分期标准 |
| Ⅰa | 局限于鼻后或鼻咽穹窿的肿瘤 |
| Ⅰb | 累及至少1个副鼻窦,累及后鼻孔和/或鼻咽穹窿 |
| Ⅱa | 局部延伸至翼腭窝外侧 |
| Ⅱb | 充分侵犯翼腭窝,有或没有向上侵犯眶 |
| Ⅱc | 延伸到颞下窝或翼状板的后面 |
| Ⅲa | 颅底侵蚀-少量颅内延伸 |
| Ⅲb | 广泛的颅内延伸,有或没有延伸到海绵窦 |
|
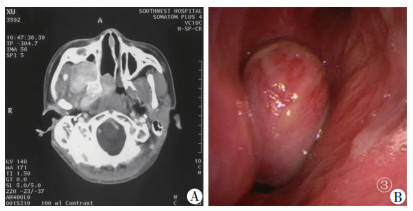
| A:鼻咽部增强CT表现右侧鼻咽部、翼腭窝和颞下窝附近见不规则软组织肿块影,增强扫描呈不均匀性强化;B:电子喉镜检查见鼻腔黏膜稍充血,右鼻腔中后部见新生物隆起 图 1 鼻咽纤维血管瘤患者术前影像学表现及电子鼻咽镜检查结果 |
1.2 鼻内镜外科手术
全组患者术前24~48 h行介入栓塞。患者平卧位,术前控制性降压麻醉,常规消毒铺巾。以生理盐水肾上腺素棉片行患侧中鼻道、总鼻道收缩3次。切除患侧中鼻甲,咬除钩突,依次开放前组筛窦、后组筛窦、上颌窦。扩大窦腔开口,松解血管瘤周围粘连。观察瘤体与周围组织结构的毗邻关系,用电刀沿血管瘤基底部外缘5 mm切开粘骨膜,剥离器剥开黏膜,将血管瘤根部分离,完整取出血管瘤(图 2A)。扩大蝶窦及额窦自然开口,探查有无新生物生长,创面双极电凝止血。当肿瘤浸润蝶窦或翼腭窝时,在肿物上方切开蝶窦。对于翼腭窝或颞窝占位的患者,行扩大内侧上颌窦造口术,切除上颌窦后壁,移开肿瘤外侧部,然后全块切除。在某些情况下,经鼻整体切除空间狭小,需要肿块移位到口咽,然后经口切除。以碘仿纱条填塞患侧鼻腔。
|
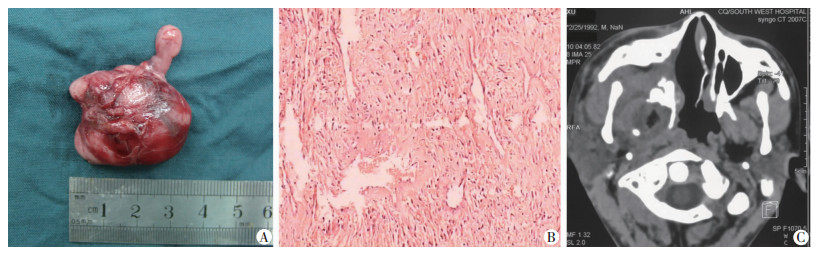
| A:完整切除的肿瘤组织,蒂在蝶腭孔处,大小约5 cm×3 cm×2 cm,呈分叶状;B:HE染色示鼻咽部纤维血管瘤(×200);C:术后2周增强CT提示鼻咽部未见明显异常强化影 图 2 鼻咽纤维血管瘤的形态、病理学切片及术后影像学随访 |
1.3 术后处理及随访
患者病理学均确诊为JNA(图 2B),术后2周和8周行鼻咽内镜和CT或MRI检查(图 2C),记录患者术后恢复状况。术后6个月和1年,行CT或MRI评估肿瘤有无复发和骨性结构的恢复情况。术后3年内,每6个月进行1次鼻咽内镜检查,对于怀疑复发的病例同时行影像学检查。术后3年后,每年进行1次鼻咽内镜检查。
2 结果20例患者均为青少年男性,年龄13~18岁,平均14.6岁。大部分患者有渐进性的鼻塞(n=16,80%)症状,其次是出现反复鼻出血(n=14,65%),见表 2。在评估肿瘤大小和位置的基础上,根据Radkowski分期将肿瘤分为Ⅰa期4例,Ⅰb期4例,Ⅱa期5例,Ⅱb期4例,Ⅱc期3例。9例患者于2008年以前接受经面中部掀翻、硬腭入路治疗。2008-2018年,11例患者(肿瘤分期为Ⅰa~Ⅱc)行鼻内镜切除术。鼻内镜手术组术中出血量、住院时间、复发例数明显少于传统手术组(表 3)。采用内窥镜治疗的患者平均失血量为509 mL,采用传统手术组平均出血量为1 072 mL,其中面中部入路治疗的患者失血量为930 mL,采用经硬腭入路治疗的患者失血量为1 250 mL。内镜入路平均手术时间135 min,传统手术组平均手术时间283 min,其中面中部掀翻手术时间258 min,经硬腭入路手术时间315 min。术后平均住院时间:内镜入路5.5 d,面中部入路10 d,经硬腭入路11.8 d。11例内镜患者均在3 d内取出鼻腔填塞物,传统手术组至少在6 d后取出。
| 症状和体征 | %(例) |
| 鼻塞 | 80(16/20) |
| 鼻出血 | 65(14/20) |
| 头痛 | 33(6/20) |
| 面部畸形 | 25(5/20) |
| 听力减退 | 15(3/20) |
| 视力下降 | 10(2/20) |
| 病例编号 | 年龄/岁 | 入院时间 | 手术方式 | Radowski分期 | 手术时间/min | 术中出血量/mL | 术后住院时间/d | 取出鼻腔填塞物时间/d | 复发 |
| 1 | 16 | 2018年 | 鼻内镜 | Ⅰa | 120 | 350 | 4 | 3 | 无 |
| 2 | 14 | 2016年 | 鼻内镜 | Ⅱa | 130 | 500 | 6 | 3 | 无 |
| 3 | 13 | 2015年 | 鼻内镜 | Ⅱc | 150 | 800 | 6 | 3 | 无 |
| 4 | 16 | 2014年 | 鼻内镜 | Ⅰa | 110 | 400 | 5 | 3 | 无 |
| 5 | 15 | 2013年 | 鼻内镜 | Ⅰb | 130 | 500 | 5 | 3 | 无 |
| 6 | 14 | 2012年 | 鼻内镜 | Ⅱa | 150 | 550 | 6 | 3 | 无 |
| 7 | 15 | 2012年 | 鼻内镜 | Ⅱb | 150 | 800 | 6 | 3 | 无 |
| 8 | 17 | 2011年 | 鼻内镜 | Ⅱb | 130 | 450 | 6 | 3 | 无 |
| 9 | 13 | 2010年 | 鼻内镜 | Ⅱa | 150 | 450 | 6 | 3 | 无 |
| 10 | 14 | 2009年 | 鼻内镜 | Ⅰb | 150 | 400 | 5 | 3 | 无 |
| 11 | 15 | 2008年 | 鼻内镜 | Ⅰa | 120 | 400 | 5 | 3 | 无 |
| 12 | 16 | 2007年 | 面中部掀翻 | Ⅱa | 240 | 850 | 9 | 6 | 无 |
| 13 | 13 | 2007年 | 面中部掀翻 | Ⅱc | 270 | 1 200 | 10 | 7 | 术后3个月 |
| 14 | 18 | 2006年 | 面中部掀翻 | Ⅰb | 240 | 900 | 10 | 6 | 无 |
| 15 | 17 | 2005年 | 面中部掀翻 | Ⅱc | 270 | 1 000 | 11 | 7 | 无 |
| 16 | 17 | 2005年 | 面中部掀翻 | Ⅱb | 270 | 700 | 10 | 7 | 术后6个月 |
| 17 | 15 | 2004年 | 经硬腭 | Ⅰb | 300 | 1 000 | 12 | 7 | 无 |
| 18 | 14 | 2003年 | 经硬腭 | Ⅱb | 330 | 1 300 | 12 | 7 | 无 |
| 19 | 15 | 2002年 | 经硬腭 | Ⅱa | 300 | 1 500 | 12 | 6 | 无 |
| 20 | 16 | 2002年 | 经硬腭 | Ⅰa | 330 | 1 200 | 11 | 7 | 无 |
随访期间,患者术后均无脑脊液鼻漏、大出血、颅内感染、视野缺损等并发症,有2例患者肿瘤复发,手术方式均为面中部掀翻进路,复发时间均小于术后6个月,鼻内镜下手术组未见复发病例。余下随访1~6年,定期鼻内镜及影像学检查未见明显复发灶,无死亡病例。
3 讨论鼻咽纤维血管瘤组织学上富含血管纤维组织,管壁缺乏成熟的平滑肌肌层,瘤体血供丰富,含大量毛细血管网,故伴有大出血的危险。有研究表明,血管内皮生长因子(VEGF)在JNA发病机制中起重要作用,它与细胞增殖和血管密度增加有关,其表达和肿瘤的血管密度、肿瘤分期、肿瘤的生长有着重要的联系[13-14]。肿瘤的起源部位与肿瘤的扩散方式有关,也提示手术的径路。多种肿瘤分类被不同学者提出[11],我们认为,Radkowski的分类能准确反映翼腭窝和颅底侵犯的程度,对于术中出血量、肿瘤残留和复发风险方面的评估优于其他分期系统。治疗JNA的潜在预后因素包括肿瘤的大小、位置和范围。如果肿瘤扩展到内侧颞下窝或内侧海绵窦,则需要切除内侧上颌骨。当肿瘤扩展至蝶窦时,由于侧位暴露有限,宜采用经硬腭入路。Le Fort Ⅰ技术能更好地暴露副鼻窦、翼腭窝和颞下窝。手术最大的挑战不仅要考虑肿瘤的大小和范围,而且包含不能通过栓塞或结扎血管分支来控制的出血。手术治疗是JNA的首选治疗已被广泛认同,但手术方法仍在讨论中。以往进行JNA的切除多采取开放性手术方式,其缺点包括创伤大,甚至造成面部畸形、上颌骨坏死或咬合关系异常等。鼻内窥镜手术具有较多优势,包括术后低复发率和能避免影响面部发育的截骨术,并可显著缩短手术时间,肿瘤一旦复发,内镜切除仍可以很好地保存鼻腔的解剖和生理结构[15]。预防和控制术中失血对于儿童及青少年患者至关重要。本组病例中,传统手术采用了硬腭路径及面中部掀翻手术,随着鼻内镜手术的广泛应用和手术技术的提升,此后对JNA采用经鼻内镜切除。与传统手术比较,经鼻内镜手术具有术中出血量少、手术时间短、术后住院时间短的优势。由于绝大部分JNA发生在青少年男性,此时正处于额面部生长发育的关键时间,内镜手术避免了面部的切口,减少了软组织的损伤和骨质的破坏,可明显改善患者远期生活质量,尤其是内镜下手术更好地保留了鼻腔的解剖结构和生理功能。同时内镜下手术放大了肿瘤结构及与周围组织的关系,能多角度观察肿瘤结构,对减少肿瘤残留、减低复发率具有重要意义。内镜下剥离肿瘤应注意术野的清晰、肿瘤的侵犯范围、出血的控制和肿瘤附着处骨组织的处理。对于较大的肿瘤,应将肿瘤分成与血管区域相对应的节段,每个血管段依次切除,以限制失血量,并在必要时允许手术分期。在我们的经验中,Ⅱc期肿瘤未侵犯颅内,内镜下切除肿瘤也是行之有效的方法,手术过程中,应在肿瘤边缘进行肿瘤剥离,确定肿瘤的界限,识别关键的解剖标志,尽量减少对肿瘤的操作,待充分游离根底部,再实施肿块切除。鼻内镜颅底手术已被越来越多地应用于儿童颅底外科中[16],尤其应重视颅底重要解剖结构的保护,并要求术者对鼻颅底解剖基础及内镜技术充分熟悉,达到切除肿瘤且不损伤周围重要组织的目的。
鼻内镜手术亦有某些局限性。对于Ⅲ期患者采用鼻内镜暴露瘤体较困难,不易判断肿瘤的基底部及侵及方向,鼻内镜手术操作不慎,可能造成比传统径路更大的伤害和出血量。此种情况下,可考虑鼻内镜联合鼻外径路入路或联合耳前颞下窝入路,联合手术方式的采用不仅使瘤体暴露更加充分,在术中止血方面也更有优势[17]。我们认为,鼻颅底区域复杂,最佳术式仍无定论,手术具有挑战性,手术的选择要兼顾根除疾病、美容和功能恢复等,各方面需取得平衡。经鼻内镜术式是目前理想的选择,可解决大多数问题,而鼻内外联合径路仍然有一席之地。HACKMAN等[18]认为,血管纤维瘤手术治疗的最大挑战是如何处理这些肿瘤的血管增生。即使是有颅内延伸和残留血管的大型血管纤维瘤,也可以由颅底团队使用内窥镜技术成功处理。
鼻咽纤维血管瘤手术过程中,如何减少术中出血、保证术野清楚,是保证手术顺利的关键。术前血管内栓塞治疗是减少鼻咽纤维血管瘤出血行之有效的方法,可明显减少术中出血量[19-20]。JNA相关的供血血管来自于颈外动脉系统(上颌内动脉和咽升动脉),但颈内动脉也可以为大型肿瘤提供血液供应。术前24~48 h是介入栓塞的理想时期,栓塞时间过长,可导致血管再通或侧支循环建立,使术中出血量增多;栓塞时间过短、瘤体缩小及减少术中出血效果不明显。本组病例中,肿瘤术前24 h均行血管栓塞,患者术后均未见明显并发症,部分病例出血量仍较大,大的出血量可能与肿瘤侵及范围广泛、与周围骨质粘连紧密、分离瘤体相对困难等因素相关。虽然栓塞可能引起头痛、眩晕等并发症或者某些额外的风险,但是栓塞对减少肿瘤同侧和对侧供血血管供血,提高手术安全性具有重要意义。JNA患者的年龄是强烈推荐术前栓塞的另一个原因,青少年患者对术中失血耐受性较差,栓塞大大减少了输血的风险。
JNA复发的原因在于手术后肿瘤残留。较高分期的肿瘤因颅底区血管神经结构复杂,手术难度大,肿瘤往往难以彻底切除。术中精细地处理翼状肌基底部、翼管、蝶骨基底部将减少血管瘤的复发[21]。影响JNA复发的因素较多,常见的影响因素包括:肿瘤大小、侵犯部位、术前栓塞、手术方式、术中出血等。在本组病例中,2例患者术前评估提示肿瘤侵及颞下窝、翼腭窝或眶内,均因再次出现鼻塞、鼻出血症状而就诊,症状复发时间均小于术后半年,此时增强CT及MRI检查肿瘤已经明显增大,并且出现周围结构受累甚至颅内侵犯,故对术后患者进行规范的影像学和鼻咽内镜随访具有重要意义,能早期发现肿瘤的复发,使患者及时接受手术治疗,提高治疗效果。根据我们的诊疗经验,认为术后2~6个月为肿瘤复发的“高峰期”,我们结合患者术后影像学检查、临床症状与体征提出以下随访方案,术后2个月复查:①影像学残余病灶(-),再发临床症状(-),鼻内镜(-),继续临床观察;②影像学残余病灶(+),再发临床症状(-),鼻内镜(-),则2~6个月复查(2个月后复查病灶体积变小、强化程度减低或无变化,则6个月后再行影像学检查;若病变未进展,则只需对患者进行临床观察;若6个月后病灶体积增大,则需再次手术治疗);③影像学残余病灶(+),再发临床症状(+),鼻内镜(-),再手术。
无论传统手术或鼻内镜手术,操作的核心仍是如何在完整切除肿瘤的同时保护周围的重要结构。栓塞后的内镜手术是一种安全有效的技术,是治疗中小型JNA的理想方法。我们认为,肿瘤切除综合获益的重要因素包含:肿瘤的充分暴露、控制出血的能力、避免术后面部疤痕或畸形、不干扰面部骨骼的生长。由于鼻咽纤维血管瘤疾病少见,本研究的病例样本量有限,有待进一步收集数据进行分析。通过回顾性研究,我们认识到,随着鼻内镜技术的成熟,以及新型多学科的协作,绝大部分JNA可选择经鼻内镜入路,与传统手术比较,具有创伤较小、出血量少、复发率低、住院天数少等优势。手术应当充分考虑青少年患者发育解剖的特殊性,减少出血及控制可能的并发症。对于较高分期JNA患者,可考虑鼻内镜联合鼻外径路入路,达到完整切除肿瘤且不损伤颅底正常组织的目的。
| [1] |
SCHICK B, RIPPEL C, BRUNNER C, et al. Numerical sex chromosome aberrations in juvenile angiofibromas: genetic evidence for an androgen-dependent tumor?[J]. Oncol Rep, 2003, 10(5): 1251-1255. |
| [2] |
LI W P, NI Y, LU H Y, et al. Current perspectives on the origin theory of juvenile nasopharyngeal angiofibroma[J]. Discov Med, 2019, 27(150): 245-254. |
| [3] |
ALIMLI A G, UCAR M, OZTUNALI C, et al. Juvenile nasopharyngeal angiofibroma: magnetic resonance imaging findings[J]. J Belg Soc Radiol, 2016, 100(1): 63. DOI:10.5334/jbr-btr.1090 |
| [4] |
SHENOUDA K, YUHAN B T, MIR A, et al. Endoscopic resection of pediatric skull base tumors: an evidence-based review[J]. J Neurol Surg B Skull Base, 2019, 80(5): 527-539. DOI:10.1055/s-0038-1676305 |
| [5] |
KOPEĆ T, BORUCKI Ł, SZYFTER W. Fully endoscopic resection of juvenile nasopharyngeal angiofibroma-own experience and clinical outcomes[J]. Int J Pediatr Otorhinolaryngol, 2014, 78(7): 1015-1018. DOI:10.1016/j.ijporl.2014.03.027 |
| [6] |
ÁLVAREZ F L, SUÁREZ V, SUÁREZ C, et al. Multimodality approach for advanced-stage juvenile nasopharyngeal angiofibromas[J]. Head Neck, 2013, 35(2): 209-213. DOI:10.1002/hed.22947 |
| [7] |
MISHRA A, MISHRA S C, VERMA V, et al. In defence of transpalatal, transpalatal-circumaxillary (transpterygopalatine) and transpalatal-circumaxillary-sublabial approaches to lateral extensions of juvenile nasopharyngeal angiofibroma[J]. J Laryngol Otol, 2016, 130(5): 462-473. DOI:10.1017/S0022215116000773 |
| [8] |
MIDILLI R, KARCI B, AKYILDIZ S. Juvenile nasopharyngeal angiofibroma: analysis of 42 cases and important aspects of endoscopic approach[J]. Int J Pediatr Otorhinolaryngol, 2009, 73(3): 401-408. DOI:10.1016/j.ijporl.2008.11.005 |
| [9] |
ROGERS D J, BEVANS S E, HARSHA W J. Endoscopic resection of juvenile nasopharyngeal angiofibroma[J]. Adv Otorhinolaryngol, 2012, 73: 132-136. DOI:10.1159/000334470 |
| [10] |
REYES C, BENTLEY H, GELVES J A, et al. Recurrence rate after endoscopic vs. open approaches for juvenile nasopharyngeal angiofibroma: a meta-analysis[J]. J Neurol Surg B Skull Base, 2019, 80(6): 577-585. DOI:10.1055/s-0038-1676562 |
| [11] |
SAFADI A, SCHREIBER A, FLISS D M, et al. Juvenile angiofibroma: current management strategies[J]. J Neurol Surg B Skull Base, 2018, 79(1): 21-30. DOI:10.1055/s-0037-1615810 |
| [12] |
RADKOWSKI D, MCGILL T J, HEALY G B, et al. Angiofibroma: changes in staging and treatment[J]. Arch Otolaryngol-Head Neck Surg, 1996, 122(2): 122-129. DOI:10.1001/archotol.1996.01890140012004 |
| [13] |
JONES J W, USMAN S, NEW J, et al. Differential gene expression and pathway analysis in juvenile nasopharyngeal angiofibroma using RNA sequencing[J]. Otolaryngol Head Neck Surg, 2018, 159(3): 572-575. DOI:10.1177/0194599818769879 |
| [14] |
MISHRA A, JAISWAL R, AMITA P, et al. Molecular interactions in juvenile nasopharyngeal angiofibroma: preliminary signature and relevant review[J]. Eur Arch Otorhinolaryngol, 2019, 276(1): 93-100. DOI:10.1007/s00405-018-5178-y |
| [15] |
EL SHARKAWY A A, ELMORSY S M. Transnasal endoscopic management of recurrent juvenile nasopharyngeal angiofibroma[J]. Int J Pediatr Otorhinolaryngol, 2011, 75(5): 620-623. DOI:10.1016/j.ijporl.2011.01.033 |
| [16] |
付依雯, 蒋卫红, 张俊毅, 等. 儿童颅底肿瘤经鼻内镜外科手术治疗分析[J]. 中国耳鼻咽喉颅底外科杂志, 2020, 26(2): 121-125. FU Y W, JIANG W H, ZHANG J Y, et al. Clinical analysis on endonasal endoscopic surgery of pediatric skull base tumors[J]. China J Otorhinolaryngol-Skull Base Surg, 2020, 26(2): 121-125. DOI:10.11798/j.issn.1007-1520.202002003 |
| [17] |
GUPTA R, AGARWAL S P. Juvenile nasopharyngeal angiofibroma: combined approach for excision, transpalatal and endoscopic; A new perspective[J]. Indian J Otolaryngol Head Neck Surg, 2018, 70(1): 125-129. DOI:10.1007/s12070-016-1027-8 |
| [18] |
HACKMAN T, SNYDERMAN C H, CARRAU R, et al. Juvenile nasopharyngeal angiofibroma: The expanded endonasal approach[J]. Am J Rhinol Allergy, 2009, 23(1): 95-99. DOI:10.2500/ajra.2009.23.3271 |
| [19] |
SANTAOLALLA F, ARALUCE I, ZABALA A, et al. Efficacy of selective percutaneous embolization for the treatment of intractable posterior epistaxis and juvenile nasopharyngeal angiofibroma (JNA)[J]. Acta Otolaryngol, 2009, 129(12): 1456-1462. DOI:10.3109/00016480902725221 |
| [20] |
赵青, 周涵, 殷敏, 等. 鼻咽纤维血管瘤术前超选择性血管栓塞的应用价值[J]. 山东大学耳鼻喉眼学报, 2019, 33(3): 100-105. ZHAO Q, ZHOU H, YIN M, et al. Value of preoperative hyperselective vascular embolization in juvenile nasopharyngeal angiofibroma treatment[J]. J Otolaryngol Ophthalmol Shandong Univ, 2019, 33(3): 100-105. DOI:10.6040/j.issn.1673-3770.1.2019.013 |
| [21] |
LIU Z F, HUA W, ZHANG H K, et al. The risk factors for residual juvenile nasopharyngeal angiofibroma and the usual residual sites[J]. Am J Otolaryngol, 2019, 40(3): 343-346. DOI:10.1016/j.amjoto.2018.11.010 |



