小儿急性阑尾炎是导致急腹症的最常见原因,也是临床手术中最常见的问题。据统计,该病发病风险在男性中约为8.6%,女性约为6.7%,有逐年上升的趋势[1-3]。一系列研究显示急性阑尾炎的病理生理学特征是炎症反应,但许多疾病与急性阑尾炎有相似的表现,并与炎症反应有关[4, 5]。为了减少对小儿急性阑尾炎诊断的干扰,除了常规的炎症指标C反应蛋白(C-reactive protein, CRP)和改良Alvarado评分外,还需要不断寻找新的生物标志物[6-8]。近年来多篇文章提示尿激酶型纤溶酶原激活物受体(urokinase-type plasminogen activator receptor, uPAR)与阑尾炎症紧密相关,可能是诊断儿童急性阑尾炎的可靠生物学指标[9-11]。目前,单一指标诊断的灵敏度并不理想,uPAR与相关生化指标联合有利于提高临床诊断效能。然而,uPAR与急性阑尾炎的相关研究并不多见,相比于传统指标,其诊断能力及评估疾病炎症程度的价值还需探索。本研究的目的在于分析急性阑尾炎患儿血液中uPAR水平,并将该指标与传统指标CRP、改良Alvarado评分相结合,探索此模型对儿童阑尾炎诊断的准确性。
1 对象和方法 1.1 研究对象本研究选取2017年6月至2019年6月我科收治的急性阑尾炎患儿57例作为观察组(阑尾炎组),纳入标准:①年龄2~16岁;②患儿均行阑尾切除术。该组患儿阑尾切除标本均在病理实验室进行评估。患儿年龄在3~16岁,男性36例,女性21例。对照组为同期入院的非阑尾炎腹痛患儿44例,男性28例,女性16例。阑尾炎组及对照组排除标准:①在进入研究前2周内有慢性病、使用药物或出现感染症状;②入院7 d内有腹部外伤史。所有患儿在调查前都提供了签署的知情同意书,本研究获河北北方学院附属第一医院伦理委员会批准[2017年伦审(K112号)]。
1.2 方法所有患儿在入院清晨采集外周静脉血,分离血清,采用酶联免疫吸附试验(ELISA)检测样本血清中的uPAR含量,高灵敏度免疫散射比浊法测定血清CRP水平,试剂盒均购于上海钰博生物科技有限公司。同时用全自动血液分析仪对全血标本进行WBC及其成分分析,中性粒细胞/淋巴细胞比值(neutrophil to lymphocyte ratio, NLR)由中性粒细胞数除以淋巴细胞数得出。
1.3 诊断标准阑尾切除标本用10%福尔马林缓冲液固定,石蜡包埋,5 μm切片,HE染色。镜下可见溃疡、穿孔、坏疽、粪石、管腔闭塞和扩张。所有急性阑尾炎患儿均根据临床症状、体格检查、白细胞(white blood cell, WBC)、NLR、CRP、腹部超声(用于测量阑尾直径和壁厚)及其他阑尾炎表现进行诊断,金标准为术后病理检查结果。
1.4 统计学分析统计分析过程使用软件SPSS 22.0、MedCalc 10.2.0.0及R 3.6.2完成。近似正态分布的定量数据以x±s表示,两组间比较使用t检验,偏态分布数据以M(P25,P75)表示,两组间比较使用Mann-Whitney U检验,计数资料比较采用χ2或Fisher检验。采用Pearson或Spearman相关检验分析uPAR与传统指标之间的关系。受试者工作特征(ROC)曲线、净重新分类指数(net reclassification improvement, NRI)和整体鉴别指数(integrated discrimination index,IDI)评价评估各指标对小儿急性阑尾炎的诊断能力。
2 结果 2.1 两组基本资料比较两组患儿基线资料及实验室检测指标如表 1所示,与对照组相比,急性阑尾炎患儿右下腹压痛人数、WBC、中性粒细胞百分数及NLR明显增高,差异有统计学意义(P < 0.05)。而两组患者年龄、性别及最高体温的差别无统计学意义(P>0.05)。
| 变量 | 总体(n=101) | 急性阑尾炎(n=57) | 对照(n=44) | Z/χ2 | P |
| 年龄 | 8.8(6.9, 12.4) | 8.5(7.1, 12.4) | 9.3(6.9, 13.3) | 0.182 | 0.856 |
| 男性 | 61.0(60.4) | 36.0(63.2) | 25.0(56.8) | 0.853 | 0.356 |
| 右下腹压痛 | 54.0(53.7) | 42.0(73.7) | 12.0(27.3) | 43.064 | < 0.001 |
| 最高体温(℃) | 37.8(37.2, 38.5) | 38.1(37.2, 38.7) | 37.8(37.1, 38.2) | 1.948 | 0.051 |
| WBC(×109/L) | 12.4(9.9, 15.2) | 15.5(13, 17.1) | 10.2(8.5, 12.8) | 6.531 | < 0.001 |
| 中性粒细胞百分数(%) | 65.7(62.1, 76.1) | 70.7(61.3, 82.6) | 64.9(62.5, 72.0) | 1.538 | 0.124 |
| NLR(%) | 6.8(4.4, 10.6) | 9.9(6.2, 12.8) | 4.6(3.3, 7.1) | 5.641 | < 0.001 |
2.2 两组患儿常规检测指标比较
对比两组患儿传统检测指标CRP、改良Alvarado结果显示:急性阑尾炎及对照组患儿的CRP中位数分别为19.7、11.8 mg/L,改良Alvarado中位数分别为6、3.5,两组相比,急性阑尾炎患儿CRP及改良Alvarado的数值明显增高(P < 0.05)。分析血清uPAR水平,急性阑尾炎患儿为4.75(2.47, 6.27),明显高于对照组2.07(0.85, 3.03), 差异具有统计学意义(P < 0.05)。两组检测指标水平如图 1所示。

|
| A:CRP;B:改良Alvarado评分;C:uPAR;a: P < 0.05,与对照组比较 图 1 两组儿童CRP、改良Alvarado评分及uPAR水平比较(x±s) |
2.3 血清uPAR与传统指标的相关性分析
Spearman相关性分析显示:uPAR水平与CRP、改良Alvarado评分间存在显著相关性(P < 0.05),与CRP(r=0.779)、改良Alvarado评分(r=0.806)均呈显著正相关。
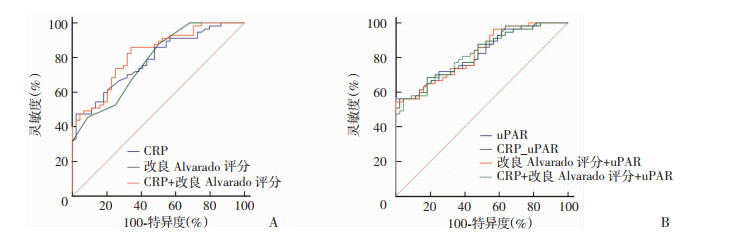
2.4 各指标诊断能力的ROC曲线分析CRP、改良Alvarado评分、CRP联合改良Alvarado评分及uPAR诊断儿童急性阑尾炎的ROC曲线下面积分别为0.785(0.693~0.861)、0.779(0.686~0.856)、0.819(0.730~0.888);相应的敏感度分别为:57.4%、54.4%、76.0%;相应的特异度则为87.7%、92.5%、78.9%。联合uPAR后,uPAR、CRP+uPAR、改良Alvarado评分+uPAR、CRP+改良Alvarado评分+uPAR的AUC分别上升为0.817(0.730~0.889)、0.818(0.729~0.888)、0.821(0.733~0.890)、0.823(0.734~0.891);对应的敏感度分别为:77.1%、66.1%、56.1%、82.7%;特异度分别为75.4%、85.3%、95.8%、70.0%。CRP+改良Alvarado评分+uPAR的Youden index为0.516。对比CRP+改良Alvarado评分+uPAR与CRP+改良Alvarado评分的诊断能力,差异无统计学意义(P=0.819,图 2)。
|
| A:CRP、改良Alvarado评分及两者联合;B:联合uPAR 图 2 各指标单独及联合uPAR的ROC曲线 |
2.5 净重新分类指数(NRI)与整体鉴别指数(IDI)
以40%为最佳阳性界值,评价传统指标及联合uPAR对急性阑尾炎和对照重分类的影响。与传统指标CRP、改良Alvarado评分、CRP+改良Alvarado评分相比,联合uPAR,可将其诊断急性阑尾炎的能力提高0.711%、0.536%、0.653%;其IDI也相应增高0.073%、0.083%、0.086%,差异均具有统计学意义(P < 0.05),详见表 2。
| 指标 | NRI(95%CI) | P | IDI(95%CI) | P |
| CRP+uPAR | 0.711(0.344~1.079) | < 0.001 | 0.073(0.020~0.125) | 0.007 |
| 改良Alvarado评分+uPAR | 0.536(0.157~0.915) | 0.006 | 0.083(0.026~0.139) | 0.004 |
| CRP+改良Alvarado评分+uPAR | 0.653(0.316~0.990) | < 0.001 | 0.086(0.036~0.136) | < 0.001 |
3 讨论
相关研究显示,仅有50%~70%的阑尾炎患儿能在初诊时确诊,且病情严重程度难以判断[12, 13]。尽管已有了CRP、改良Alvarado评分、超声等几种诊断指标应用于临床,但不同年龄儿童的误诊率仍居高不下[14],提示现有指标对阑尾炎与其他腹痛病因的鉴别能力有限,需要一个较为准确的生化标记物来辅助判断。在本研究中,我们比较了经病理确诊的急性阑尾炎患儿和同期入院的非阑尾炎腹痛患儿的血清uPAR水平,以评估该生物标记物的临床应用前景。此外,我们还进一步研究了uPAR对CRP及改良Alvarado评分等最常用生物标志物诊断能力的影响,并试图找到一个较为可靠的联合诊断方案。
WBC、NLR、中性粒细胞百分数是判断急性阑尾炎最常用的标志物。与许多研究结果一致,本文急性阑尾炎患儿的WBC、NLR、中性粒细胞百分数与非阑尾炎腹痛者相比明显升高。据报道,WBC对急性阑尾炎的敏感性和特异性分别为65%~85%和32%~82%,NLR检测的敏感性和特异性分别为58%~83%和28%~82%[15]。同时,DELGADO-MIGUEL等[16]研究显示,在患有肺炎、胃肠炎、咽炎和尿路感染等炎症性疾病的儿童中,WBC和NLR均显著升高,提示上述指标均不是儿童急性阑尾炎的特异性指标。随着对该疾病病理过程研究的深入,更多炎症因子与急性阑尾炎的关系被发掘,包括CRP和uPAR。CRP是炎症和组织损伤的敏感标志物,已在多篇研究中显示出对急性阑尾炎的诊断价值[17-19]。而uPAR系统是细胞迁移和组织重塑的关键,在胚胎发生、伤口愈合、炎症、血管生成、肿瘤侵袭甚至转移中发挥着重要作用。在感染或炎症的情况下,uPAR可加速基质蛋白水解,促进白细胞向感染区的迁移和黏附,以增强炎症反应并调用其他防御细胞[20-22]。基于uPAR增高的病理生理机制,uPAR可作为炎症和免疫系统激活的可靠指标,提示阑尾炎病情进展。我们的研究结果也发现急性阑尾炎患儿的uPAR、CRP均显著高于对照组,且uPAR与传统指标CRP、改良Alvarado评分呈显著正相关,说明血中uPAR升高与急性阑尾炎的发生及进展有密切关系。
最近的研究表明,同时使用CRP和改良Alvarado评分水平可以提高阳性预测的实用性。然而,FATIH等[23]人报道,仅靠CRP和改良Alvarado评分并不能有效地诊断儿童阑尾炎。据我们的研究结果,CRP+改良Alvarado评分对阑尾炎的诊断能力高于CRP、改良Alvarado评分的单独应用。在联合uPAR后,CRP、改良Alvarado评分、CRP+改良Alvarado评分的AUC均有了进一步的提高,这表明uPAR能提高传统指标的诊断效能。此外,uPAR可以通过相对简单和低成本的ELISA在儿童血液样本中检测到,联合其他血清学指标的临床应用前景较好。与各联合指标相比,uPAR+CRP+改良Alvarado评分的AUC最为理想,但相比CRP+改良Alvarado评分,无统计学差异。这说明uPAR的加入对AUC的影响并不显著,然而新的联合模型所导致的风险重新分类的个体数量及NRI是需要确定的。本研究发现CRP+uPAR、改良Alvarado评分+uPAR、uPAR+CRP+改良Alvarado评分的NRI及IDI值得到了显著提高,提示uPAR的加入使得CRP、改良Alvarado评分、CRP+改良Alvarado评分的诊断能力有所改善。uPAR联合CRP、改良Alvarado评分显出了较高的灵敏度和特异度,较其余指标诊断价值更高。本文结果也表明其能够有效、准确地诊断儿童急性阑尾炎,该联合模型对指导后续的临床治疗益处颇多。此外,根据阑尾炎的传统分类,急性阑尾炎的不同阶段可分为非穿孔性或穿孔性。本文57例急性阑尾炎患儿中有23例单纯性阑尾炎,18例化脓性阑尾炎,16例发生阑尾穿孔。由于研究时间和方法等原因,本文未对于阑尾炎穿孔的患儿进行分组分析,我们将在后续研究中进一步完善以验证我们的结论。
总之,uPAR可以显著提升CRP、改良Alvarado评分对儿童急性阑尾炎的诊断效能,其联合CRP、改良Alvarado评分在鉴别急性阑尾炎和非阑尾炎腹痛中起着重要的作用,有利于临床医师判断病情进展,及时治疗以免延误病情。
| [1] |
顾秀婷, 王苇, 尹笑笑, 等. 小儿急性阑尾炎多层螺旋CT分级与病理表现比较研究[J]. 临床放射学杂志, 2018, 37(1): 118-121. GU X T, WANG W, YIN X X, et al. Pediatric acute appendicitis: multi-slice spiral CT grade and pathological findings[J]. J Clin Radiol, 2018, 37(1): 118-121. |
| [2] |
SARSU S B, ERBAGCI A B, ULUSAL H, et al. The place of calprotectin, lactoferrin, and high-mobility group box 1 protein on diagnosis of acute appendicitis with children[J]. Indian J Surg, 2017, 79(2): 131-136. DOI:10.1007/s12262-015-1441-2 |
| [3] |
SWENSON D W, AYYALA R S, SAMS C, et al. Practical imaging strategies for acute appendicitis in children[J]. Am J Roentgenol, 2018, 211(4): 901-909. DOI:10.2214/ajr.18.19778 |
| [4] |
DZIB-CALAN E A, HERNÁNDEZ-ROJAS M A, MURATA C, et al. Modification of Alvarado score with pain semiology for the diagnosis of acute appendicitis[J]. Cir Cir, 2019, 87(6): 674-681. DOI:10.24875/ciru.19000866 |
| [5] |
RASTOVIC P, TRNINIC Z, GALIC G, et al. Accuracy of modified alvarado score, eskelinen score and ohmann score in diagnosing acute appendicitis[J]. Psychiatr Danub, 2017, 29(suppl2): 134-141. |
| [6] |
ORLOVA E, YEH A, SHI M, et al. Genetic association and differential expression of PITX2 with acute appendicitis[J]. Hum Genet, 2019, 138(1): 37-47. DOI:10.1007/s00439-018-1956-2 |
| [7] |
STRINGER M D. Acute appendicitis[J]. J Paediatr Child Health, 2017, 53(11): 1071-1076. DOI:10.1111/jpc.13737 |
| [8] |
REISMANN J, ROMUALDI A, KISS N, et al. Diagnosis and classification of pediatric acute appendicitis by artificial intelligence methods: an investigator-independent approach[J]. PLoS ONE, 2019, 14(9): e0222030. DOI:10.1371/journal.pone.0222030 |
| [9] |
KEASEY M P, JIA C H, PIMENTEL L F, et al. Bloodvitronectin is a major activator of LIF and IL-6 in the brain through integrin -FAK and uPAR signaling[J]. J Cell Sci, 2018, 131(3): 1-13. DOI:10.1242/jcs.202580 |
| [10] |
RUBINA K A, SYSOEVA V Y, ZAGORUJKO E I, et al. Increased expression of uPA, uPAR, and PAI-1 in psoriatic skin and in basal cell carcinomas[J]. Arch Dermatol Res, 2017, 309(6): 433-442. DOI:10.1007/s00403-017-1738-z |
| [11] |
ALI A, MUCAGIT G, ÖMER V Ö, et al. The diagnostic value of serum urokinase-type plasminogen activator receptor in acute appendicitis[J]. Ulus Travma Acil Cerrahi Derg, 2019, 25(5): 467-473. DOI:10.5505/tjtes.2019.55623 |
| [12] |
SNYDER M J, GUTHRIE M, CAGLE S. Acute appendi-citis: efficient diagnosis and management[J]. Am Fam Phy-sician, 2018, 98(1): 25-33. |
| [13] |
HORI T, MACHIMOTO T, KADOKAWA Y, et al. Laparoscopic appendectomy for acute appendicitis: How to discou-rage surgeons using inadequate therapy[J]. World J Gastroenterol, 2017, 23(32): 5849-5859. DOI:10.3748/wjg.v23.i32.5849 |
| [14] |
SALMINEN P, TUOMINEN R, PAAJANEN H, et al. Five-year follow-up of antibiotic therapy for uncomplicated acute appendicitis in the APPAC randomized clinicaltrial[J]. JAMA, 2018, 320(12): 1259-1265. DOI:10.1001/jama.2018.13201 |
| [15] |
雷斌, 戚雯琰. 降钙素原在小儿急性阑尾炎诊治中的临床应用[J]. 实用医学杂志, 2014, 30(12): 1984-1986. LEI B, QI W Y. Clinical application of procalcitonin in the diagnosis and treatment of acute appendicitis in children[J]. J Pract Med, 2014, 30(12): 1984-1986. DOI:10.3969/j.issn.1006-5725.2014.12.043 |
| [16] |
DELGADO-MIGUEL C, MUNOZ-SERRANO A J, BARRENA DELFA S, et al. Neutrophil-to-lymphocyte ratio as a predictor of peritonitis in acute appendicitis in children[J]. Cir Pediatr, 2019, 32(4): 185-189. |
| [17] |
艾龙龙, 张玉江, 张童鑫, 等. RIPASA评分和血清总胆红素及C反应蛋白在急性阑尾炎中的诊断价值研究[J]. 中国全科医学, 2018, 21(32): 58-63. AI L L, ZHANG Y J, ZHANG T X, et al. RIPASA score, serum total bilirubin and c-reactive protein for the diagnosis of acute appendicitis[J]. Chin Gen Prac, 2018, 21(32): 58-63. DOI:10.12114/j.issn.1007-9572.2018.00.021 |
| [18] |
WITHERS A S, GRIEVE A, LOVELAND J A. Correlation of white cell count and CRP in acute appendicitis in paediatric patients[J]. S Afr J Surg, 2019, 57(4): 40. |
| [19] |
MATUSZCZAK E, TYLICKA M, DEBEK W, et al. Concentration of proteasome in the blood plasma of children with acute appendicitis, before and after surgery, and its correlation with CRP[J]. World J Surg, 2018, 42(7): 2259-2264. DOI:10.1007/s00268-017-4407-7 |
| [20] |
GUO H, ZHOU L X, MA H Z, et al. Soluble urokinase-type plasminogen activator receptor and urokinase-type plasminogen activator receptor contribute to chemoresistance in leukemia[J]. Oncol Lett, 2017, 14(1): 383-389. DOI:10.3892/ol.2017.6150 |
| [21] |
NUSSHAG C, RUPP C, SCHMITT F, et al. Cell cycle biomarkers and soluble urokinase-type plasminogen activator receptor for the prediction of Sepsis-induced acute kidney injury requiring renal replacement therapy: a prospective, exploratory study[J]. Crit Care Med, 2019, 47(12): e999-e1007. DOI:10.1097/ccm.0000000000004042 |
| [22] |
ICHIHARA N, MIYAMURA M, MAEDA D, et al. Association between serum soluble urokinase-type plasminogen activator receptor and atrial fibrillation[J]. J Arrhythm, 2017, 33(5): 469-474. DOI:10.1016/j.joa.2017.05.003 |
| [23] |
DAL F. Role of alvarado score and biological indicators of c-reaktif protein, procalicitonin and neopterin in diagnosis of acute appendicitis[J]. Ulus Travma Acil Cerrahi Derg, 2018, 25(3): 229-237. DOI:10.5505/tjtes.2018.57362 |



