外科夹闭和血管内弹簧圈栓塞术是目前公认治疗颅内动脉瘤的重要方法[1]。动脉瘤血管内弹簧圈栓塞治疗虽是一种微创治疗,但也存在一定的风险,如术中动脉瘤破裂、术中血管痉挛、弹簧圈发生移位和动脉瘤再通等,影像随访是术后动脉瘤复查的重要手段。数字减影血管造影(digital subtraction angiography,DSA)被认为是弹簧圈栓塞术后观察血管解剖结构的金标准,但DSA是一种侵入性、高辐射剂量、耗时的检查,且存在一定的血栓栓塞事件的风险[2]。计算机断层扫描(computed tomograhy,CT)和CT血管成像(CT angiography,CTA)作为一种无创技术,能够用于评估手术和血管内动脉瘤弹簧圈置入治疗后血管结构和周围脑实质情况[1]。然而,由动脉瘤夹和弹簧圈产生的金属伪影严重影响CT图像质量,并可能对影像学的解释能力产生负面影响,特别是对小动脉瘤残余、复发和再生长的评估影响[3]。随着CT技术的不断发展,能谱CT单能量成像技术以及金属伪影消除技术可有效去除体内金属置入物伪影对图像质量的影像[4]。本研究主要探讨联合应用多伪影去除(multi-artifact reduction, MAR)技术,找出去除颅内动脉瘤弹簧圈栓塞术后金属伪影的最佳单能量成像范围。
1 资料与方法 1.1 一般资料收集本院2019年1-10月共32例经导管颅内动脉瘤弹簧圈栓塞术后患者,其中男性12例,女性20例,年龄32~69岁,均采用能谱CT复查,弹簧圈为美国Guglielmi弹簧圈(GDC),材料为铂-钨合金,患者一般状况良好,能配合检查并保持头颅不动、采集图像时不做吞咽动作,无碘对比剂过敏史及检查禁忌证(哮喘、心肾功能不全等)。
1.2 方法 1.2.1 扫描参数美国GE公司Revolution CT,能谱模式(gemstone spectral imaging,GSI)80 kV/140 kV快速自动切换,管电流370 mA,螺旋扫描,迭代重建(adaptive statistical iterative reconstruction,ASIR) 50%,探测器宽度80 mm,螺距(pitch) 0.992 :1,转速0.5 s/360°,扫描层厚、间距5 mm,扫描时间0.5 s,扫描范围颅底至颅顶,在Recon Setting里面打开MAR,重建0.625 mm Data薄层数据传至AW4.7工作站。
1.2.2 检查方法选择右侧肘正中静脉为注射通道,用小剂量团注测试法确定扫描延迟时间:对比剂15 mL(碘帕醇,370 mgI/mL), 生理盐水20 mL,注射流速4.5 mL,监测线在颈6水平,在该平面选择一侧颈内动脉放置1个ROI,分析时间-密度曲线,得出血管成像的最佳扫描时间。血管成像扫描:对比剂60 mL(碘帕醇,370 mgI/mL), 生理盐水20 mL,注射流速4.5 mL;用减影法,在对比剂注射前先进行颈6水平至颅顶的1次无对比剂平扫扫描,紧接着按照计算的阈值时间再完成颈6水平至颅顶的对比剂注射扫描,两次扫描要求起始位置完全一致,图像采集过程中患者头部保持静止不动。
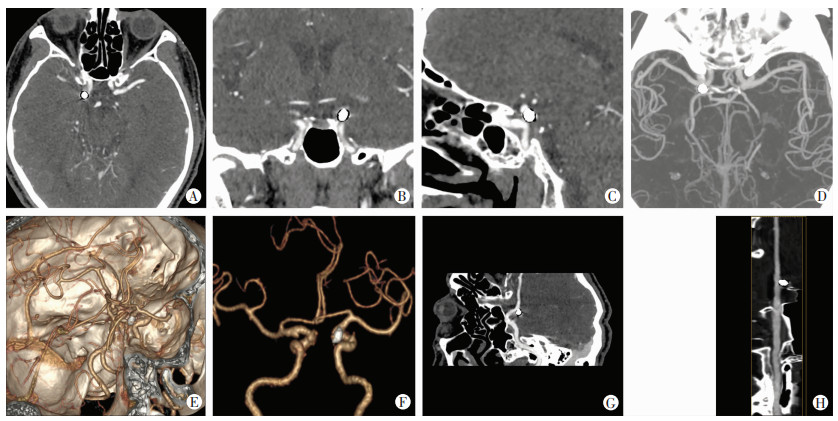
1.2.3 图像后处理方法包括容积再现(volume rendering, VR)、多平面重建(multi planar reformation, MPR)、最大密度投影(maximum intensity projection, MIP)、曲面重建(curved plannar reformation, CPR)及血管分析。将0.625 mm的能谱Data数据导入工作站,在40~140 KeV,每间隔10 KeV,共生成10个不同能级的单能量数据VR图像;由两位高年资医师依据血管显示情况对各能级图像进行初步筛选,40 KeV和≥100 KeV单能量数据因图像质量较差被排除使用,保留50~90 KeV区间;然后每间隔5 KeV为1个能级,即50、55、60、65、70、75、80、85、90 KeV,再次重建共9个能级的单能量数据。分别对32例病例的每一级单能量数据进行MPR、MIP、VR、CPR重建以及血管拉直分析(图 1);VR及MIP图像能够提供直观的三维血管图像,CPR重建及血管拉直分析图像更有利于观察弹簧圈栓塞后动脉瘤有无再通和弹簧圈是否脱出瘤体及其与血管的关系。
|
| A:原始轴位图像;B、C:分别为冠状位及矢状位MPR重建图像;D:MIP重建图像;E、F:分别为带骨VR及去骨VR重建图像;G、H:分别为CPR重建及血管拉直分析图 图 1 右侧颈内动脉C7段动脉瘤弹簧圈介入患者(男,70岁)术后复查能谱CT单能量成像表现 |
1.2.4 图像评价方法
分别采用主观和客观方法进行评价。
1.2.4.1 主观评价由两位高年资的介入医师对图像质量进行评价,根据血管显示情况及周围软组织对比度及去金属伪影效果,结合李克特量表评分法[5-6]按5分制评分,先对40~140 KeV 10个能量级的头颅血管后处理图像进行初步评价,每1个能量级(间隔10 KeV)都有1个评分点,即40、50、60、70、80、90、100、110、120、130、140 KeV。1分:血管显示差,金属伪影重,周围软组织受金属干扰强,不能诊断;2分:血管显示较差,金属伪影较重,有金属伪影干扰,诊断难度大;3分:血管显示良好,软组织等受金属伪影影响小;4分:血管显示清晰,且金属伪影小;5分:血管及周围软组织清晰显示,基本无金属伪影。评分结果显示:40 KeV和≥100 KeV重建图像得分均在2分以下,图像质量较差没有临床诊断价值,故将这部分数据不纳入客观评价之内。
1.2.4.2 客观评价通过主观评价大致筛选后,保留50~90 KeV区间,间隔5 KeV为1个能量级数据进行客观评价,即50、55、60、65、70、75、80、85、90 KeV,共9个能量级图像数据,测量并记录同一患者9个不同的KeV能量级横断面图像的相同位置相同ROI的CT值、噪声值(standard deviation, SD)、信噪比(signal to noise ratio, SNR)、伪影指数(artifact index, AI)。其中目标分析兴趣区标记为ROI1,为靠近弹簧圈处血管金属伪影较重区域的ROI,测量并记录该处ROI的CT值、噪声值(SD1),以此计算SNR(CT/SD1)。选取同层面远离弹簧圈的且无金属伪影干扰区域的血管处兴趣区,标记为ROI2,测量并记录该处的CT值、噪声值(SD2)。计算AI:AI=(SD12-SD22)1/2[7-8],且同一患者不同单能量图像上选取的ROI的位置和面积必须一致,再进行统计学评价。
1.3 统计学分析采用SPSS 21.0统计软件,计数资料均不服从正态分布,故采用中位数M(P25,P75)表示。组间SNR比较采用秩和检验,检验水准为0.05。
2 结果 2.1 主观评价结果两名医师评分均值结果显示:50~90 KeV单能量区间图像质量具有诊断学意义,其中60~70 KeV单能量区间图像质量评分较高(表 1)。
| 项目 | 40 KeV | 50 KeV | 60 KeV | 70 KeV | 80 KeV | 90 KeV | 100 KeV |
| 主观评分 | 2.00(1.50, 2.50) | 3.50(3.50, 4.00) | 4.50(4.00, 4.50) | 4.50(4.00, 4.50) | 2.50(1.50, 2.50) | 1.50(1.25, 2.00) | 0.50(0, 0.50) |
| 项目 | 50 KeV | 55 KeV | 60 KeV | 65 KeV | 70 KeV | 75 KeV | 80 KeV |
| SNR | 6.54(4.54, 8.16) | 6.31(4.57, 8.10) | 6.37(4.57, 8.04) | 6.38(4.55, 8.02) | 6.22(4.54, 8.04) | 6.35(4.50, 8.06) | 6.18(4.47, 8.09) |
| 40 KeV和≥100 KeV单能量图像质量评分很低,说明图像诊断价值较低, 这部分数据没有纳入客观评价 | |||||||
2.2 客观评价结果
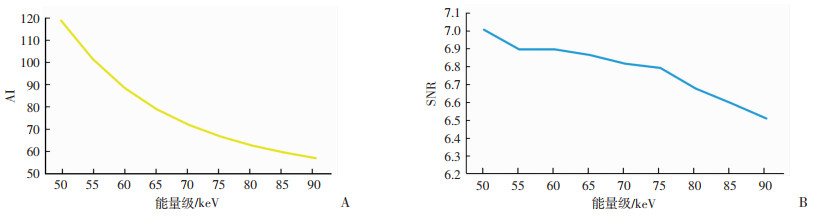
主观评价筛选后,保留50~90 KeV区间单能量图像并分析图像的AI、SNR,曲线图分析显示:图像AI值随着单能量能级的增加而降低,表明图像质量受金属伪影干扰越来越小(表 1,图 2A);而图像血管SNR随着单能量能级的增加越来越低,表明血管图像质量越来越差(图 2B)。进行组间SNR比较,其中65 KeV与70、75、80 KeV单能量能级比较,差异有统计学意义(P < 0.05,表 2),其余组间比较差异均无统计学意义。高于75 KeV处SNR陡降,且医师评分图像质量较差,而低于75 KeV显示血管较好,结合在60~65 KeV范围内AI指数较低,客观评分最高,经综合比较确认:利用能谱加MAR技术后,该范围单能量图像对弹簧圈术后血管显示较佳(图 3)。
|
| SNR曲线55 KeV及75 KeV出现陡降趋势,在55~75 KeV区间走行平缓 图 2 50~90 KeV AI(A)及SNR(B)曲线 |

|
| A、C:为轴位及冠状位65 KeV图像,可见弹簧圈产生放射状金属伪影,周边组织及血管显示受到明显干扰;B、D:为轴位及冠状位65 KeV加MAR图像,弹簧圈金属伪影显著降低,周边组织及血管显影良好 图 3 右侧大脑后动脉P2段动脉瘤弹簧圈栓塞患者(女,30岁)术后复查能谱CT单能量成像表现 |
| 统计值 | 50 vs 55 KeV | 55 vs 60 KeV | 60 vs 65 KeV | 65 vs 70 KeV | 70 vs 75 KeV | 75 vs 80 KeV |
| Z值 | -1.421 | -0.879 | -1.346 | -2.001 | -1.945 | -2.580 |
| P值 | 0.155 | 0.379 | 0.178 | 0.045 | 0.052 | 0.010 |
3 讨论
有研究报道能谱成像单能量KeV值越高去金属伪影效果越好,且120 KeV为最佳单能量成像点,70 KeV为伪影减除的分界点[4, 9],而对于单纯的无金属伪影影响的血管,单能量成像KeV值越低,血管优化显示越好,提示最佳血管显示的单能量图像KeV范围为57~63 KeV[5]。而对于颅内动脉瘤弹簧圈栓塞术后患者,如果采用CT复查,既要有效去除金属伪影(高KeV值),又要最优化显示血管(低KeV值),两者是相互矛盾的。本研究通过对SNR、AI等的测量分析及高年资医师主观评价,寻找出既能有效去除金属伪影又能最优化显示血管的最佳KeV值范围。本研究结果显示:AI指数为一平滑下降的曲线,55 KeV处及75 KeV处出现陡降趋势,而55~75 KeV区间走行平缓,结合客观统计学评价及高年资医师评价,最后得出60~65 KeV单能量区间范围为颅内动脉瘤弹簧圈栓塞术后复查的理想范围,该范围与其他研究[4, 10]单纯无金属伪影影响的血管最佳单能量范围比较接近,因此,加MAR[11-12]技术在该单能量区间几乎完全达到了去金属伪影的效果。本研究得出的结论“60~65 KeV单能量区间范围为颅内动脉瘤弹簧圈栓塞术后复查的理想范围”,与董鑫等[12]得出的结论“70~90 KeV为颅内弹簧圈最佳血管显示范围,且70 KeV为最佳单能量值”有一定的差别,分析有以下几个原因:①该院采用的CT设备为美国GE公司的宝石750CT,而我院CT设备为GE公司Revolution宽体CT,不同设备的加MAR技术效果是否相当值得探讨;②我院弹簧圈为美国进口Guglielmi弹簧圈(GDC),材料为铂-钨合金,而该院未提及弹簧圈材料及厂家,不同金属含量的材质差异可能会对去伪影效果产生影响;③两篇文献采取了不同的实验设计及统计方法,且对比剂使用浓度及用量也有差别。
CT金属伪影产生的原因有:①射线硬化效应,源于X线的固有特性,当X线穿过密度较高的金属时,低能部分被吸收,透过的X线平均能量增高,X线即被硬化;②部分容积效应,由探测器测量尺寸误差产生,如某一区域出现一半低能量一半高能量,探测器会取平均值作为输出信号;③电子饥饿效应,指X线穿过金属物体后,衰减过大而导致到达探测器的光子量过少,噪声明显增大,导致图像产生明显的黑白条纹状伪影[13]。怎样有效去除金属伪影成为目前研究的热点。本研究联合应用加MAR技术及单能量技术,加MAR技术是一种基于迭代重建的去金属伪影的后处理技术[14-15],不改变扫描条件,也不增加辐射剂量,通过改进图像重建算法,对图像中的投影数据进行反复迭代运算,剔除有金属伪影的原始数据,直至图像不再受大量金属伪影的干扰,同时也不影响非金属区域图像。
本研究结果显示:有31例SNR及AI值均为曲线,1例呈抛物线。分析原因可能跟该患者在介入手术中同时使用了弹簧圈和动脉瘤夹有关。本院动脉瘤夹采用的是德国贝朗公司的蛇牌动脉瘤夹,该动脉瘤夹分别有两种材料,钴合金动脉瘤夹和钛合金动脉瘤夹,根据不同的适应证选取材料,本例患者动脉瘤夹的材料为钛合金,而弹簧圈材料为铂-钨合金,两者为不同成分的金属材料,弹簧圈和动脉夹两种不同金属材质之间是否相互产生了影响,值得进一步探讨。因此,本方法适用于在介入手术中使用单一材料弹簧圈栓塞术后复查的患者。
| [1] |
IHN Y K, SHIN S H, BAIK S K, et al. Complications of endovascular treatment for intracranial aneurysms: Management and prevention[J]. Interv Neuroradiol, 2018, 24(3): 237-245. DOI:10.1177/1591019918758493 |
| [2] |
ZHU C, WANG X, EISENMENGER L, et al. Surveillance of unruptured intracranial saccular aneurysms using noncontrast 3D-black-blood MRI: comparison of 3D-TOF and contrast-enhanced MRA with 3D-DSA[J]. AJNR Am J Neuroradiol, 2019, 40(6): 960-966. DOI:10.3174/ajnr.A6080 |
| [3] |
DUNDAR T T, ARALASMAK A, KITIŞ S, et al. Comparison of subtracted computed tomography from computed tomography perfusion and digital subtraction angiography in residue evaluation of treated intracranial aneurysms[J]. World Neurosurg, 2019, 132: e746-e751. DOI:10.1016/j.wneu.2019.08.028 |
| [4] |
DUNET V, BERNASCONI M, HAJDU S D, et al. Impact of metal artifact reduction software on image quality of gemstone spectral imaging dual-energy cerebral CT angiography after intracranial aneurysm clipping[J]. Neuroradiology, 2017, 59(9): 845-852. DOI:10.1007/s00234-017-1871-6 |
| [5] |
邓小林, 谢惠, 屈亚林, 等. 能谱CT最佳单能量技术优化头颈部CTA图像质量的研究[J]. CT理论与应用研究, 2018, 27(6): 719-726. DENG X L, XIE H, QU Y L, et al. Spectral CT with optimal monochromatic energy to improve CTA image quality of head and neck[J]. Comput Tomogr Theory Appl, 2018, 27(6): 719-726. DOI:10.15953/j.1004-4140.2018.27.06.05 |
| [6] |
张志伟, 吕发金, 曾勇明, 等. 数字减影CT血管造影术在颅内动脉瘤中的临床应用[J]. 中国医学影像技术, 2007, 23(3): 450-452. ZHANG Z W, LYU F J, ZENG Y M, et al. Digital subtraction CT angiography for detection of intracranial aneurysms[J]. Chin J Med Imaging Technol, 2007, 23(3): 450-452. DOI:10.13929/j.1003-3289.2007.03.038 |
| [7] |
SUN X, SHAO X D, CHEN H S. The value of energy spectral CT in the differential diagnosis between benign and malignant soft tissue masses of the musculoskeletal system[J]. Eur J Radiol, 2015, 84(6): 1105-1108. DOI:10.1016/j.ejrad.2015.02.028 |
| [8] |
KAMIYA K, KUNIMATSU A, MORI H, et al. Preliminary report on virtual monochromatic spectral imaging with fast kVp switching dual energy head CT: comparable image quality to that of 120-kVp CT without increasing the radiation dose[J]. Jpn J Radiol, 2013, 31(4): 293-298. DOI:10.1007/s11604-013-0185-9 |
| [9] |
WINKLHOFER S, HINZPETER R, STOCKER D, et al. Combining monoenergetic extrapolations from dual-energy CT with iterative reconstructions: reduction of coil and clip artifacts from intracranial aneurysm therapy[J]. Neuroradiology, 2018, 60(3): 281-291. DOI:10.1007/s00234-018-1981-9 |
| [10] |
周新杰, 周代全, 钟丽娟, 等. 能谱CT血管成像显示甲状腺供血动脉[J]. 中国医学影像技术, 2019, 35(10): 1565-1568. ZHOU X J, ZHOU D Q, ZHONG L J, et al. Dual-energy CT angiography in displaying thyroid feeding artery[J]. Chin J Med Imaging Technol, 2019, 35(10): 1565-1568. DOI:10.13929/j.1003-3289.201904078 |
| [11] |
KUCHENBECKER S, FABY S, SAWALL S, et al. Dual energy CT: How well can pseudo-monochromatic imaging reduce metal artifacts?[J]. Med Phys, 2015, 42(2): 1023-1036. DOI:10.1118/1.4905106 |
| [12] |
董鑫, 吕国士, 刘伟, 等. 能谱CT的MONO成像联合MARs技术在颅内弹簧圈植入物伪影的应用研究[J]. 临床放射学杂志, 2016, 35(5): 794-798. DONG X, LYU G S, LIU W, et al. Application effects of energy spectral CT mono imaging technology united with MARs in removing artifacts of intracranial spring coil implant[J]. J Clin Radiol, 2016, 35(5): 794-798. DOI:10.13437/j.cnki.jcr.2016.05.037 |
| [13] |
张客松, 徐晓麟, 韩青, 等. 骨科去金属伪影技术在人工关节置换术CT检查中的应用[J]. 吉林大学学报(医学版), 2019, 45(1): 179-183, 220. ZHANG K S, XU X L, HAN Q, et al. Application of orthopedic metal artifact reduction technology in CT examination of arthroplasty[J]. J Jilin Univ(Med Ed), 2019, 45(1): 179-183, 220. DOI:10.13481/j.1671-587x.20190134 |
| [14] |
高思喆, 丁长伟, 郭文力, 等. O-MAR技术在颅内动脉瘤栓塞术后CTA中的应用[J]. 中国临床医学影像杂志, 2017, 28(6): 391-393. GAO S Z, DING C W, GUO W L, et al. Application of O-MAR technique in postoperative cTA of intracranial aneurysms embolization[J]. J Chin Clin Med Imaging, 2017, 28(6): 391-393. DOI:10.3969/j.issn.1008-1062.2017.06.003 |
| [15] |
KIDOH M, NAKAURA T, NAKAMURA S, et al. Reduction of dental metallic artefacts in CT: Value of a newly developed algorithm for metal artefact reduction (O-MAR)[J]. Clin Radiol, 2014, 69(1): e11-e16. DOI:10.1016/j.crad.2013.08.008 |



